Toprol Xl 25mg, 50mg, 100mg Metoprolol Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
Qu'est-ce que Toprol XL 100 mg et comment est-il utilisé ?
Toprol XL est un médicament délivré sur ordonnance utilisé pour traiter les symptômes de douleur thoracique (angine de poitrine), d'hypertension artérielle (hypertension) et d'insuffisance rénale. Toprol XL peut être utilisé seul ou avec d'autres médicaments.
Toprol XL appartient à une classe de médicaments appelés Thiazide Combos.
On ne sait pas si Toprol XL 100 mg est sûr et efficace chez les enfants de moins de 18 ans.
Quels sont les effets secondaires possibles de Toprol XL 100 mg ?
Toprol XL peut provoquer des effets secondaires graves, notamment :
- battements de coeur très lents,
- étourdissement,
- essoufflement,
- gonflement,
- prise de poids rapide et
- sensation de froid dans les mains et les pieds
Consultez immédiatement un médecin si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires les plus courants de Toprol XL incluent :
- vertiges,
- sensation de fatigue,
- la dépression,
- confusion,
- problèmes de mémoire,
- cauchemars,
- troubles du sommeil,
- diarrhée, et
- démangeaisons légères ou éruption cutanée
Dites au médecin si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas.
Ce ne sont pas tous les effets secondaires possibles de Toprol XL. Pour plus d'informations, consultez votre médecin ou votre pharmacien.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
ATTENTION
LA CARDIOPATHIE ISCHÉMIQUE
Suite à l'arrêt brutal du traitement par certains agents bêta-bloquants, des exacerbations d'angine de poitrine et, dans certains cas, d'infarctus du myocarde se sont produites. Lors de l'arrêt de TOPROL-XL administré de manière chronique, en particulier chez les patients atteints d'une cardiopathie chimique, la dose doit être progressivement réduite sur une période de 1 à 2 semaines et le patient doit être étroitement surveillé. Si l'angor s'aggrave nettement ou si une insuffisance coronarienne aiguë se développe, l'administration de TOPROL-XL doit être rétablie rapidement, au moins temporairement, et d'autres mesures appropriées pour la prise en charge de l'angor instable doivent être prises. Avertir les patients contre l'interruption ou l'arrêt du traitement sans l'avis du médecin. Étant donné que la maladie coronarienne est courante et peut ne pas être reconnue, il peut être prudent de ne pas interrompre brutalement le traitement par TOPROL-XL, même chez les patients traités uniquement pour l'hypertension (voir AVERTISSEMENTS ET PRECAUTIONS ).
LA DESCRIPTION
TOPROL-XL, succinate de métoprolol, est un bêta1-bloquant sélectif (cardiosélectif) des récepteurs adrénergiques, pour administration orale, disponible sous forme de comprimés à libération prolongée. TOPROL-XL a été formulé pour fournir une libération contrôlée et prévisible de métoprolol pour une administration une fois par jour. Les comprimés comprennent un système à unités multiples contenant du succinate de métoprolol dans une multitude de pastilles à libération contrôlée. Chaque pastille agit comme une unité d'administration de médicament distincte et est conçue pour administrer le métoprolol en continu pendant l'intervalle posologique. Les comprimés contiennent 23,75, 47,5, 95 et 190 mg de succinate de métoprolol équivalent à 25, 50, 100 et 200 mg de tartrate de métoprolol, USP, respectivement. Son nom chimique est le succinate de (±)1-(isopropylamino)-3-[p-(2-méthoxyéthyl)phénoxy]-2-propanol (2:1) (sel). Sa formule structurale est :
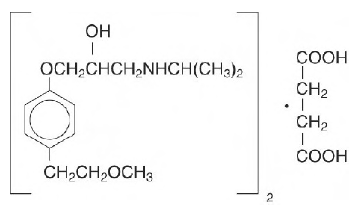
Le succinate de métoprolol est une poudre cristalline blanche d'un poids moléculaire de 652,8. Il est librement soluble dans l'eau; soluble dans le méthanol; peu soluble dans l'éthanol; légèrement soluble dans le dichlorométhane et le 2-propanol; pratiquement insoluble dans l'acétate d'éthyle, l'acétone, l'éther diéthylique et l'heptane. Ingrédients inactifs : dioxyde de silicium, composés de cellulose, fumarate de stéaryle sodique, polyéthylèneglycol, dioxyde de titane, paraffine.
LES INDICATIONS
Hypertension
TOPROL-XL est indiqué pour le traitement de l'hypertension, pour abaisser la tension artérielle. L'abaissement de la pression artérielle réduit le risque d'événements cardiovasculaires mortels et non mortels, principalement des accidents vasculaires cérébraux et des infarctus du myocarde. Ces avantages ont été observés dans des essais contrôlés de médicaments antihypertenseurs appartenant à une grande variété de classes pharmacologiques, y compris le métoprolol.
Le contrôle de l'hypertension artérielle doit faire partie d'une gestion globale des risques cardiovasculaires, y compris, le cas échéant, le contrôle des lipides, la gestion du diabète, la thérapie antithrombotique, l'arrêt du tabac, l'exercice et un apport limité en sodium. De nombreux patients auront besoin de plus d'un médicament pour atteindre leurs objectifs de tension artérielle. Pour des conseils spécifiques sur les objectifs et la gestion, consultez les directives publiées, telles que celles du Comité national mixte sur la prévention, la détection, l'évaluation et le traitement de l'hypertension artérielle (JNC) du National High Blood Pressure Education Program.
De nombreux médicaments antihypertenseurs, appartenant à une variété de classes pharmacologiques et avec différents mécanismes d'action, ont été montrés dans des essais contrôlés randomisés pour réduire la morbidité et la mortalité cardiovasculaires, et on peut conclure qu'il s'agit de la réduction de la pression artérielle, et non d'une autre propriété pharmacologique de les médicaments, qui est en grande partie responsable de ces avantages. Le bénéfice cardiovasculaire le plus important et le plus constant a été une réduction du risque d'accident vasculaire cérébral, mais des réductions de l'infarctus du myocarde et de la mortalité cardiovasculaire ont également été observées régulièrement.
Une pression systolique ou diastolique élevée entraîne un risque cardiovasculaire accru, et l'augmentation du risque absolu par mmHg est plus importante à des pressions artérielles plus élevées, de sorte que même des réductions modestes de l'hypertension sévère peuvent apporter des avantages substantiels. La réduction du risque relatif de la réduction de la pression artérielle est similaire dans les populations avec un risque absolu variable, de sorte que le bénéfice absolu est plus important chez les patients qui présentent un risque plus élevé indépendamment de leur hypertension (par exemple, les patients atteints de diabète ou d'hyperlipidémie), et ces patients seraient attendus bénéficier d'un traitement plus agressif à un objectif de tension artérielle plus basse.
Certains médicaments antihypertenseurs ont des effets plus faibles sur la pression artérielle (en monothérapie) chez les patients noirs, et de nombreux médicaments antihypertenseurs ont des indications et des effets supplémentaires approuvés (p. ex., sur l'angor, l'insuffisance cardiaque ou la néphropathie diabétique). Ces considérations peuvent guider le choix du traitement.
TOPROL-XL peut être administré avec d'autres antihypertenseurs.
Angine de poitrine
TOPROL-XL est indiqué dans le traitement à long terme de l'angine de poitrine, pour réduire les crises d'angine et améliorer la tolérance à l'effort.
Insuffisance cardiaque
TOPROL-XL est indiqué pour réduire le risque de mortalité cardiovasculaire et d'hospitalisation pour insuffisance cardiaque chez les patients souffrant d'insuffisance cardiaque.
DOSAGE ET ADMINISTRATION
Hypertension
Adultes
La posologie initiale habituelle est de 25 à 100 mg par jour en une seule prise. Ajuster la posologie à des intervalles hebdomadaires (ou plus longs) jusqu'à ce qu'une réduction optimale de la pression artérielle soit atteinte. En général, l'effet maximal d'un niveau de dosage donné sera apparent après 1 semaine de traitement. Les doses supérieures à 400 mg par jour n'ont pas été étudiées.
Patients pédiatriques hypertendus âgés de ≥ 6 ans
La dose initiale recommandée de TOPROL-XL est de 1 mg/kg une fois par jour, mais la dose initiale maximale ne doit pas dépasser 50 mg une fois par jour. Ajuster la posologie en fonction de la réponse de la pression artérielle. Les doses supérieures à 2 mg/kg (ou supérieures à 200 mg) une fois par jour n'ont pas été étudiées chez les patients pédiatriques [voir Utilisation dans des populations spécifiques et PHARMACOLOGIE CLINIQUE ].
TOPROL-XL n'a pas été étudié chez les patients pédiatriques de Utilisation dans des populations spécifiques ].
Angine de poitrine
Personnalisez le dosage de TOPROL-XL. La posologie initiale habituelle est de 100 mg par jour, administrée en une seule dose. Augmentez progressivement la posologie toutes les semaines jusqu'à l'obtention d'une réponse clinique optimale ou jusqu'à un ralentissement prononcé du rythme cardiaque. Les doses supérieures à 400 mg par jour n'ont pas été étudiées. Si le traitement doit être interrompu, réduire progressivement la posologie sur une période de 1 à 2 semaines [voir AVERTISSEMENTS ET PRECAUTIONS ].
Insuffisance cardiaque
La posologie doit être individualisée et étroitement surveillée pendant la titration. Avant l'initiation de TOPROL-XL, stabilisez la dose d'autre thérapie de médicament d'insuffisance cardiaque. La dose initiale recommandée de TOPROL-XL est de 25 mg une fois par jour pendant deux semaines chez les patients atteints d'insuffisance cardiaque de classe NYHA II et de 12,5 mg une fois par jour chez les patients atteints d'insuffisance cardiaque plus grave. Doublez la dose toutes les deux semaines jusqu'à la dose la plus élevée tolérée par le patient ou jusqu'à 200 mg de TOPROL-XL. La difficulté initiale avec le titrage ne doit pas empêcher les tentatives ultérieures d'introduction de TOPROL-XL. Si les patients présentent une bradycardie symptomatique, réduisez la dose de TOPROL-XL. En cas d'aggravation transitoire de l'insuffisance cardiaque, envisagez de traiter avec des doses accrues de diurétiques, de réduire la dose de TOPROL-XL ou de l'arrêter temporairement. La dose de TOPROL-XL ne doit pas être augmentée tant que les symptômes d'aggravation de l'insuffisance cardiaque ne se sont pas stabilisés.
Administration
Les comprimés de TOPROL-XL sont sécables et peuvent être divisés ; cependant, ne pas écraser ou mâcher le comprimé entier ou la moitié du comprimé.
COMMENT FOURNIE
Formes posologiques et points forts
Comprimés de 25 mg : Comprimé blanc, ovale, biconvexe, pelliculé, sécable et gravé « A/β ».
Comprimés de 50 mg : Comprimé blanc, rond, biconvexe, pelliculé, sécable et gravé « A/mo ».
Comprimés de 100 mg : Comprimé blanc, rond, biconvexe, pelliculé, sécable et gravé « A/ms ».
Comprimés de 200 mg : Comprimé pelliculé blanc, ovale, biconvexe, sécable et gravé « A/my ».
Stockage et manutention
Les comprimés contenant du succinate de métoprolol équivalent au poids indiqué de tartrate de métoprolol, USP, sont blancs, biconvexes, pelliculés et sécables.
Conserver à 25 °C (77 °F). Excursions autorisées jusqu'à 15-30°C (59-86°F). (Voir USP Température ambiante contrôlée.)
Fabriqué pour : Aralez Pharmaceuticals US Inc. 300 Interpace Parkway, Morris Corporate Center 1, Building C3, Parsippany, NJ 07054. Révisé : avril 2022.
EFFETS SECONDAIRES
Les effets indésirables suivants sont décrits ailleurs dans l'étiquetage :
- Aggravation de l'angor ou de l'infarctus du myocarde [voir AVERTISSEMENTS ET PRECAUTIONS ].
- Aggravation de l'insuffisance cardiaque [voir AVERTISSEMENTS ET PRECAUTIONS ].
- Aggravation du bloc AV [voir CONTRE-INDICATIONS ].
Expérience des essais cliniques
Étant donné que les essais cliniques sont menés dans des conditions très variables, les taux d'effets indésirables observés dans les essais cliniques d'un médicament ne peuvent pas être directement comparés aux taux des essais cliniques d'un autre médicament et peuvent ne pas refléter les taux observés dans la pratique. Les informations sur les effets indésirables issues des essais cliniques fournissent cependant une base pour identifier les événements indésirables qui semblent être liés à l'utilisation de médicaments et pour estimer les taux.
Hypertension et angine
La plupart des effets indésirables ont été légers et transitoires. Les effets indésirables les plus courants (> 2 %) sont la fatigue, les étourdissements, la dépression, la diarrhée, l'essoufflement, la bradycardie et les éruptions cutanées.
Insuffisance cardiaque
Dans l'étude MERIT-HF comparant TOPROL-XL à des doses quotidiennes allant jusqu'à 200 mg (dose moyenne de 159 mg une fois par jour ; n=1 990) à un placebo (n=2 001), 10,3 % des patients recevant TOPROL-XL ont interrompu leur traitement en raison d'effets indésirables contre 12,2 % de patients sous placebo.
Le tableau ci-dessous répertorie les effets indésirables de l'étude MERIT-HF survenus à une incidence ≥ 1 % dans le groupe TOPROLXL et supérieure au placebo de plus de 0,5 %, quelle que soit l'évaluation de la causalité.
Effets indésirables survenus dans l'étude MERIT-HF à une incidence ≥ 1 % dans le groupe TOPROL-XL et supérieure au placebo de plus de 0,5 %
Événements indésirables postopératoires
Dans un essai randomisé, en double aveugle, contrôlé par placebo portant sur 8351 patients atteints ou à risque de maladie athéroscléreuse subissant une chirurgie non vasculaire et qui ne prenaient pas de bêtabloquant, TOPROLXL 100 mg a été débuté 2 à 4 heures avant la chirurgie, puis poursuivi pendant 30 jours à raison de 200 mg par jour. L'utilisation de TOPROL-XL a été associée à une incidence plus élevée de bradycardie (6,6 % contre 2,4 % ; HR, 2,74 ; IC à 95 % 2,19, 3,43), d'hypotension (15 % contre 9,7 % ; HR 1,55 ; IC à 95 % 1,37, 1,74 ), accident vasculaire cérébral (1,0 % contre 0,5 % ; HR 2,17 ; IC à 95 % 1,26, 3,74) et décès (3,1 % contre 2,3 % ; HR 1,33 ; IC à 95 % 1,03, 1,74) par rapport au placebo.
Expérience post-commercialisation
Les effets indésirables suivants ont été identifiés lors de l'utilisation post-approbation de TOPROL-XL ou de métoprolol à libération immédiate. Étant donné que ces réactions sont signalées volontairement par une population de taille incertaine, il n'est pas toujours possible d'estimer de manière fiable leur fréquence ou d'établir une relation causale avec l'exposition au médicament.
Cardiovasculaire: Extrémités froides, insuffisance artérielle (généralement de type Raynaud), palpitations, œdème périphérique, syncope, douleur thoracique et hypotension.
Respiratoire: Respiration sifflante (bronchospasme), dyspnée.
Système nerveux central: Confusion, perte de mémoire à court terme, maux de tête, somnolence, cauchemars, insomnie, anxiété/nervosité, hallucinations, paresthésie.
Gastro-intestinal : Nausées, bouche sèche, constipation, flatulences, brûlures d'estomac, hépatite, vomissements.
Réactions d'hypersensibilité : Prurit.
Divers: Douleur musculo-squelettique, arthralgie, vision floue, diminution de la libido, impuissance masculine, acouphènes, alopécie réversible, agranulocytose, sécheresse oculaire, aggravation du psoriasis, maladie de La Peyronie, transpiration, photosensibilité, troubles du goût.
Effets indésirables potentiels : De plus, il existe des effets indésirables non énumérés ci-dessus qui ont été signalés avec d'autres agents bloquants bêta-adrénergiques et qui doivent être considérés comme des effets indésirables potentiels de TOPROL-XL.
Système nerveux central: Dépression mentale réversible évoluant vers la catatonie ; un syndrome réversible aigu caractérisé par une désorientation temporelle et spatiale, une perte de mémoire à court terme, une labilité émotionnelle, un sensorium obscurci et une diminution des performances en neuropsychométrie.
Hématologique : Agranulocytose, purpura non thrombocytopénique, purpura thrombocytopénique.
Réactions d'hypersensibilité : Laryngospasme, détresse respiratoire.
INTERACTIONS MÉDICAMENTEUSES
Médicaments appauvrissant les catécholamines
Les médicaments déplétant les catécholamines (p. ex., la réserpine, les inhibiteurs de la monoamine oxydase (MAO)) peuvent avoir un effet additif lorsqu'ils sont administrés avec des agents bêta-bloquants. Observer les patients traités par TOPROL-XL plus un dépléteur de catécholamines pour des signes d'hypotension ou de bradycardie marquée, pouvant entraîner des vertiges, une syncope ou une hypotension orthostatique.
Inhibiteurs du CYP2D6
Il a été démontré que les médicaments qui sont de puissants inhibiteurs du CYP2D6 tels que la quinidine, la fluoxétine, la paroxétine et la propafénone doublent les concentrations de métoprolol. Bien qu'il n'y ait aucune information sur les inhibiteurs modérés ou faibles, ceux-ci sont également susceptibles d'augmenter la concentration de métoprolol. Les augmentations de la concentration plasmatique diminuent la cardiosélectivité du métoprolol [voir PHARMACOLOGIE CLINIQUE ]. Surveiller étroitement les patients, lorsque l'association ne peut être évitée.
Digitalis, clonidine et bloqueurs des canaux calciques
Les glycosides digitaliques, la clonidine, le diltiazem et le vérapamil ralentissent la conduction auriculo-ventriculaire et diminuent la fréquence cardiaque. L'utilisation concomitante de bêta-bloquants peut augmenter le risque de bradycardie.
Si la clonidine et un bêta-bloquant, tel que le métoprolol, sont co-administrés, arrêtez le bêta-bloquant plusieurs jours avant l'arrêt progressif de la clonidine car les bêta-bloquants peuvent exacerber l'hypertension rebond qui peut suivre l'arrêt de la clonidine. En cas de remplacement de la clonidine par un traitement bêta-bloquant, retarder l'introduction des bêta-bloquants de plusieurs jours après l'arrêt de l'administration de clonidine.
AVERTISSEMENTS
Inclus dans le cadre du "PRÉCAUTIONS" Section
PRÉCAUTIONS
Arrêt brutal de la thérapie
Suite à l'arrêt brutal du traitement par certains agents bêta-bloquants, des exacerbations d'angine de poitrine et, dans certains cas, d'infarctus du myocarde se sont produites. Lors de l'arrêt de TOPROL-XL administré de manière chronique, en particulier chez les patients atteints de cardiopathie ischémique, réduire progressivement la posologie sur une période de 1 à 2 semaines et surveiller le patient. Si l'angine de poitrine s'aggrave nettement ou si une ischémie coronarienne aiguë se développe, réintroduisez rapidement TOPROL-XL et prenez les mesures appropriées pour la prise en charge de l'angine de poitrine instable. Avertir les patients de ne pas interrompre le traitement sans l'avis de leur médecin. Étant donné que la maladie coronarienne est courante et peut ne pas être reconnue, évitez d'arrêter brusquement TOPROL-XL chez les patients traités uniquement pour l'hypertension.
Insuffisance cardiaque
Une aggravation de l'insuffisance cardiaque peut survenir pendant l'augmentation de la dose de TOPROL-XL. Si de tels symptômes surviennent, augmenter les diurétiques et rétablir la stabilité clinique avant d'augmenter la dose de TOPROL-XL [voir DOSAGE ET ADMINISTRATION ]. Il peut être nécessaire de réduire la dose de TOPROL-XL ou de l'arrêter temporairement. De tels épisodes n'empêchent pas le titrage réussi ultérieur de TOPROL-XL.
Maladie bronchospastique
Les patients atteints de maladies bronchospastiques ne doivent généralement pas recevoir de bêta-bloquants. Cependant, en raison de sa relative cardiosélectivité bêta1, TOPROL-XL peut être utilisé chez les patients atteints de maladie bronchospastique qui ne répondent pas ou ne peuvent tolérer d'autres traitements antihypertenseurs. Étant donné que la sélectivité bêta1 n'est pas absolue, utilisez la dose la plus faible possible de TOPROL-XL. Les bronchodilatateurs, y compris les bêta2-agonistes, doivent être facilement disponibles ou administrés en concomitance [voir DOSAGE ET ADMINISTRATION ].
Bradychardie
Une bradycardie, y compris une pause sinusale, un bloc cardiaque et un arrêt cardiaque, s'est produite avec l'utilisation de TOPROL-XL. Patients présentant un bloc auriculo-ventriculaire du premier degré, un dysfonctionnement du nœud sinusal, des troubles de la conduction (y compris Wolff-Parkinson-White) ou prenant des médicaments concomitants provoquant une bradycardie [voir INTERACTIONS MÉDICAMENTEUSES ], peuvent présenter un risque accru. Surveiller la fréquence cardiaque chez les patients recevant TOPROL-XL. Si une bradycardie sévère se développe, réduisez ou arrêtez TOPROL-XL.
Phéochromocytome
Si TOPROL-XL est utilisé dans le cadre d'un phéochromocytome, il doit être administré en association avec un alpha-bloquant, et seulement après l'initiation de l'alpha-bloquant. L'administration de bêta-bloquants seuls dans le cadre d'un phéochromocytome a été associée à une augmentation paradoxale de la pression artérielle due à l'atténuation de la vasodilatation à médiation bêta dans le muscle squelettique.
Une intervention chirurgicale majeure
Éviter l'initiation d'un régime à forte dose de métoprolol à libération prolongée chez les patients subissant une chirurgie non cardiaque, car une telle utilisation chez les patients présentant des facteurs de risque cardiovasculaire a été associée à la bradycardie, l'hypotension, l'accident vasculaire cérébral et la mort.
La thérapie bêta-bloquante administrée de façon chronique ne doit pas être systématiquement interrompue avant une intervention chirurgicale majeure, cependant, la capacité altérée du cœur à répondre aux stimuli adrénergiques réflexes peut augmenter les risques d'anesthésie générale et d'interventions chirurgicales.
Masquer les symptômes de l'hypoglycémie
Les bêta-bloquants peuvent masquer la tachycardie associée à l'hypoglycémie, mais d'autres manifestations telles que les étourdissements et la transpiration peuvent ne pas être significativement affectées.
Thyrotoxicose
Le blocage bêta-adrénergique peut masquer certains signes cliniques d'hyperthyroïdie, tels que la tachycardie. L'arrêt brutal du bêtabloquant peut déclencher une tempête thyroïdienne.
Une maladie vasculaire périphérique
Les bêta-bloquants peuvent précipiter ou aggraver les symptômes d'insuffisance artérielle chez les patients atteints d'une maladie vasculaire périphérique.
Réaction anaphylactique
Tout en prenant des bêta-bloquants, les patients ayant des antécédents de réactions anaphylactiques graves à divers allergènes peuvent être plus réactifs à des provocations répétées et peuvent ne pas répondre aux doses habituelles d'épinéphrine utilisées pour traiter une réaction allergique.
Toxicologie non clinique
Carcinogenèse, mutagenèse, altération de la fertilité
Des études à long terme chez l'animal ont été menées pour évaluer le potentiel carcinogène du tartrate de métoprolol. Dans des études de 2 ans chez le rat à trois doses orales allant jusqu'à 800 mg/kg/jour (41 fois, sur une base mg/m2, la dose quotidienne de 200 mg pour un patient de 60 kg), il n'y a pas eu d'augmentation dans le développement de néoplasmes bénins ou malins spontanés de tout type. Les seuls changements histologiques qui semblaient être liés au médicament étaient une incidence accrue d'accumulation focale généralement légère de macrophages spumeux dans les alvéoles pulmonaires et une légère augmentation de l'hyperplasie biliaire. Dans une étude de 21 mois chez des souris albinos suisses à trois doses orales allant jusqu'à 750 mg/kg/jour (18 fois, sur une base mg/m2, la dose quotidienne de 200 mg pour un patient de 60 kg), les tumeurs pulmonaires (petits adénomes) sont survenues plus fréquemment chez les souris femelles recevant la dose la plus élevée que chez les animaux témoins non traités. Il n'y a pas eu d'augmentation des tumeurs pulmonaires malignes ou totales (bénignes plus malignes), ni de l'incidence globale des tumeurs ou des tumeurs malignes. Cette étude de 21 mois a été répétée chez des souris CD-1, et aucune différence statistiquement ou biologiquement significative n'a été observée entre les souris traitées et les souris témoins des deux sexes pour tout type de tumeur.
Tous les tests de génotoxicité effectués sur le tartrate de métoprolol (une étude létale dominante chez la souris, des études chromosomiques dans les cellules somatiques, un test de mutagénicité Salmonella/mammifère-microsome et un test d'anomalie du noyau dans les noyaux d'interphase somatique) et le succinate de métoprolol (un test Salmonella/mammifère-microsome test de mutagénicité) étaient négatifs.
Aucun signe d'altération de la fertilité due au tartrate de métoprolol n'a été observé dans une étude réalisée chez le rat à des doses allant jusqu'à 22 fois, sur une base en mg/m2, la dose quotidienne de 200 mg chez un patient de 60 kg.
Utilisation dans des populations spécifiques
Grossesse
Résumé des risques
L'hypertension artérielle et l'insuffisance cardiaque non traitées pendant la grossesse peuvent entraîner des effets indésirables pour la mère et le fœtus (voir Considérations cliniques ). Les données disponibles provenant d'études observationnelles publiées n'ont pas démontré de risque associé au médicament d'anomalies congénitales majeures, de fausse couche ou d'issues maternelles ou fœtales indésirables avec l'utilisation du métoprolol pendant la grossesse. Cependant, il existe des rapports incohérents de retard de croissance intra-utérin, d'accouchement prématuré et de mortalité périnatale avec l'utilisation maternelle de bêta-bloquants, y compris le métoprolol, pendant la grossesse (voir Données ) Dans des études de reproduction animale, il a été démontré que le métoprolol augmente la perte post-implantation et diminue la survie néonatale chez le rat à des doses orales de 500 mg/kg/jour, soit environ 24 fois la dose quotidienne de 200 mg chez un patient de 60 kg sous base mg/m2.
Le risque de fond estimé de malformations congénitales majeures et de fausse couche pour la population indiquée est inconnu. Toutes les grossesses ont un risque de fond de malformation congénitale, de perte ou d'autres résultats indésirables. Dans la population générale des États-Unis, le risque de fond estimé de malformations congénitales majeures et de fausse couche dans les grossesses cliniquement reconnues est de 2 à 4 % et de 15 à 20 %, respectivement.
Considération clinique
Risque maternel et/ou embryonnaire/fœtal associé à la maladie
L'hypertension pendant la grossesse augmente le risque maternel de prééclampsie, de diabète gestationnel, d'accouchement prématuré et de complications à l'accouchement (p. ex., nécessité d'une césarienne et hémorragie post-partum). L'hypertension augmente le risque fœtal de retard de croissance intra-utérin et de mort intra-utérine. Les femmes enceintes souffrant d'hypertension doivent être étroitement surveillées et prises en charge en conséquence.
Le volume systolique et la fréquence cardiaque augmentent pendant la grossesse, ce qui augmente le débit cardiaque, en particulier au cours du premier trimestre. Il existe un risque d'accouchement prématuré chez les femmes enceintes atteintes d'insuffisance cardiaque chronique au 3e trimestre de la grossesse.
Effets indésirables fœtaux/néonatals
Le métoprolol traverse le placenta. Les nouveau-nés nés de mères qui reçoivent du métoprolol pendant la grossesse peuvent présenter un risque d'hypotension, d'hypoglycémie, de bradycardie et de dépression respiratoire. Observez les nouveau-nés et gérez-les en conséquence.
Données
Données humaines
Les données des études observationnelles publiées n'ont pas démontré d'association entre les malformations congénitales majeures et l'utilisation du métoprolol pendant la grossesse. La littérature publiée a rapporté des résultats incohérents de retard de croissance intra-utérin, de naissance prématurée et de mortalité périnatale avec l'utilisation maternelle de métoprolol pendant la grossesse ; cependant, ces études ont des limites méthodologiques qui entravent l'interprétation. Les limites méthodologiques comprennent la conception rétrospective, l'utilisation concomitante d'autres médicaments et d'autres facteurs de confusion non ajustés qui peuvent expliquer les résultats de l'étude, y compris la maladie sous-jacente chez la mère. Ces études observationnelles ne permettent pas d'établir ou d'exclure définitivement tout risque lié au médicament pendant la grossesse.
Données animales
Il a été démontré que le métoprolol augmente la perte post-implantation et diminue la survie néonatale chez le rat à des doses orales de 500 mg/kg/jour, c'est-à-dire 24 fois, en mg/m2, la dose quotidienne de 200 mg chez un rat de 60 kg. patient.
Aucune anomalie fœtale n'a été observée lorsque des rates gravides recevaient du métoprolol par voie orale jusqu'à une dose de 200 mg/kg/jour, soit 10 fois la dose quotidienne de 200 mg chez une patiente de 60 kg.
Lactation
Résumé des risques
Les données disponibles limitées de la littérature publiée indiquent que le métoprolol est présent dans le lait maternel. La dose quotidienne estimée de métoprolol pour le nourrisson reçue du lait maternel varie de 0,05 mg à moins de 1 mg. La dose relative estimée pour le nourrisson était de 0,5 % à 2 % de la dose ajustée en fonction du poids de la mère (voir Données ). Aucun effet indésirable du métoprolol sur le nourrisson allaité n'a été identifié. Il n'existe aucune information concernant les effets du métoprolol sur la production de lait.
Considération clinique
Surveillance des effets indésirables
Surveiller le nourrisson allaité pour déceler une bradycardie et d'autres symptômes de bêta-blocage tels que l'apathie (hypoglycémie).
Données
Sur la base de rapports de cas publiés, la dose quotidienne estimée de métoprolol pour le nourrisson reçue du lait maternel varie de 0,05 mg à moins de 1 mg. La dose relative estimée chez le nourrisson était de 0,5 % à 2 % de la dose ajustée en fonction du poids de la mère.
Chez deux femmes qui prenaient une quantité non précisée de métoprolol, des échantillons de lait ont été prélevés après une dose de métoprolol. La quantité estimée de métoprolol et d'alpha-hydroxy métoprolol dans le lait maternel serait inférieure à 2 % de la dose ajustée au poids de la mère.
Dans une petite étude, le lait maternel a été recueilli toutes les 2 à 3 heures sur un intervalle posologique, chez trois mères (au moins 3 mois après l'accouchement) qui ont pris du métoprolol en quantité non précisée. La quantité moyenne de métoprolol présente dans le lait maternel était de 71,5 mcg/jour (intervalle de 17,0 à 158,7). La dose relative moyenne chez le nourrisson était de 0,5 % de la dose ajustée au poids de la mère.
Femelles et mâles de potentiel reproducteur
Résumé des risques
D'après la littérature publiée, les bêta-bloquants (y compris le métoprolol) peuvent provoquer une dysfonction érectile et inhiber la motilité des spermatozoïdes.
Aucun signe d'altération de la fertilité due au métoprolol n'a été observé chez le rat [voir Toxicologie non clinique ].
Utilisation pédiatrique
Cent quarante-quatre patients pédiatriques hypertendus âgés de 6 à 16 ans ont été randomisés pour recevoir un placebo ou l'un des trois niveaux de dose de TOPROL-XL (0,2, 1,0 ou 2,0 mg/kg une fois par jour) et suivis pendant 4 semaines. L'étude n'a pas atteint son critère d'évaluation principal (dose-réponse pour la réduction de la PAS). Certains critères d'évaluation secondaires prédéfinis ont démontré leur efficacité, notamment :
- Dose-réponse pour la réduction de la DBP,
- 1 mg/kg vs placebo pour le changement de la PAS, et
- 2 mg/kg contre placebo pour la modification de la PAS et de la PAD.
Les réductions moyennes corrigées par placebo de la PAS variaient de 3 à 6 mmHg et de la PAD de 1 à 5 mmHg. La réduction moyenne de la fréquence cardiaque variait de 5 à 7 bpm, mais des réductions considérablement plus importantes ont été observées chez certains individus [voir DOSAGE ET ADMINISTRATION ].
Aucune différence cliniquement pertinente dans le profil des événements indésirables n'a été observée chez les patients pédiatriques âgés de 6 à 16 ans par rapport aux patients adultes.
L'innocuité et l'efficacité de TOPROL-XL n'ont pas été établies chez les patients de
Utilisation gériatrique
Les études cliniques de TOPROL-XL dans l'hypertension n'ont pas inclus un nombre suffisant de sujets âgés de 65 ans et plus pour déterminer s'ils répondent différemment des sujets plus jeunes. D'autres expériences cliniques rapportées chez des patients hypertendus n'ont pas identifié de différences dans les réponses entre les patients âgés et les patients plus jeunes.
Parmi les 1 990 patients atteints d'insuffisance cardiaque randomisés pour recevoir TOPROL-XL dans l'essai MERIT-HF, 50 % (990) étaient âgés de 65 ans et plus et 12 % (238) étaient âgés de 75 ans et plus. Il n'y avait pas de différences notables dans l'efficacité ou le taux d'effets indésirables entre les patients plus âgés et plus jeunes.
En général, utiliser une dose initiale faible chez les patients âgés compte tenu de leur plus grande fréquence de diminution de la fonction hépatique, rénale ou cardiaque et de maladies concomitantes ou d'autres traitements médicamenteux.
Insuffisance hépatique
Aucune étude n'a été réalisée avec TOPROL-XL chez des patients atteints d'insuffisance hépatique. Étant donné que TOPROL-XL est métabolisé par le foie, les taux sanguins de métoprolol sont susceptibles d'augmenter considérablement en cas de fonction hépatique déficiente. Par conséquent, initier le traitement à des doses inférieures à celles recommandées pour une indication donnée ; et augmenter progressivement les doses chez les patients présentant une fonction hépatique altérée.
Insuffisance rénale
La disponibilité systémique et la demi-vie du métoprolol chez les patients insuffisants rénaux ne diffèrent pas de manière cliniquement significative de celles des sujets normaux. Aucune réduction de la posologie n'est nécessaire chez les patients atteints d'insuffisance rénale chronique [voir PHARMACOLOGIE CLINIQUE ].
SURDOSAGE
Signes et symptômes - Un surdosage de TOPROL-XL peut entraîner une bradycardie grave, une hypotension et un choc cardiogénique. La présentation clinique peut également inclure : bloc auriculo-ventriculaire, insuffisance cardiaque, bronchospasme, hypoxie, troubles de la conscience/coma, nausées et vomissements.
Traitement – Envisagez de traiter le patient en soins intensifs. Les patients atteints d'infarctus du myocarde ou d'insuffisance cardiaque peuvent être sujets à une instabilité hémodynamique importante. Un surdosage en bêta-bloquants peut entraîner une résistance significative à la réanimation avec des agents adrénergiques, y compris les bêta-agonistes. Sur la base des actions pharmacologiques du métoprolol, utilisez les mesures suivantes.
Il est peu probable que l'hémodialyse apporte une contribution utile à l'élimination du métoprolol [voir PHARMACOLOGIE CLINIQUE ]. Bradycardie : évaluer le besoin d'atropine, de médicaments stimulant les adrénergiques ou d'un stimulateur cardiaque pour traiter la bradycardie et les troubles de la conduction.
Hypotension : traiter la bradycardie sous-jacente. Envisagez une perfusion intraveineuse de vasopresseurs, tels que la dopamine ou la noradrénaline.
Insuffisance cardiaque et choc : peuvent être traités, le cas échéant, par une expansion volémique appropriée, une injection de glucagon (si nécessaire, suivie d'une perfusion intraveineuse de glucagon), l'administration intraveineuse de médicaments adrénergiques tels que la dobutamine, avec des médicaments agonistes des récepteurs α ajoutés en présence de vasodilatation .
Bronchospasme : Peut généralement être inversé par les bronchodilatateurs.
CONTRE-INDICATIONS
TOPROL-XL est contre-indiqué en cas de bradycardie sévère, de bloc cardiaque du deuxième ou du troisième degré, de choc cardiogénique, d'insuffisance cardiaque décompensée, de maladie des sinus (sauf si un stimulateur cardiaque permanent est en place) et chez les patients hypersensibles à l'un des composants de ce produit.
PHARMACOLOGIE CLINIQUE
Mécanisme d'action
Le métoprolol est un agent bloquant les récepteurs adrénergiques bêta1-sélectif (cardiosélectif). Cet effet préférentiel n'est cependant pas absolu et, à des concentrations plasmatiques plus élevées, le métoprolol inhibe également les récepteurs bêta2-adrénergiques, principalement localisés dans la musculature bronchique et vasculaire.
Le métoprolol n'a pas d'activité sympathomimétique intrinsèque et l'activité de stabilisation de la membrane n'est détectable qu'à des concentrations plasmatiques bien supérieures à celles requises pour le bêta-blocage. Des expériences animales et humaines indiquent que le métoprolol ralentit la fréquence sinusale et diminue la conduction nodale AV.
La sélectivité bêta1 relative du métoprolol a été confirmée par les éléments suivants : (1) Chez les sujets normaux, le métoprolol est incapable d'inverser les effets vasodilatateurs à médiation bêta2 de l'épinéphrine. Cela contraste avec l'effet des bêta-bloquants non sélectifs, qui inversent complètement les effets vasodilatateurs de l'épinéphrine. Chez les patients asthmatiques, le métoprolol réduit significativement moins le VEMS et la CVF qu'un bêta-bloquant non sélectif, le propranolol, à des doses équivalentes de bêtabloquants.
Hypertension: Le mécanisme des effets antihypertenseurs des bêta-bloquants n'a pas été élucidé. Cependant, plusieurs mécanismes possibles ont été proposés : (1) antagonisme compétitif des catécholamines au niveau des sites neuronaux adrénergiques périphériques (en particulier cardiaques), entraînant une diminution du débit cardiaque ; un effet central conduisant à une diminution du flux sympathique vers la périphérie ; et (3) la suppression de l'activité de la rénine.
Angine de poitrine: En bloquant les augmentations induites par les catécholamines de la fréquence cardiaque, de la vitesse et de l'étendue de la contraction myocardique et de la pression artérielle, le métoprolol réduit les besoins en oxygène du cœur à tout niveau d'effort donné, ce qui le rend utile dans la gestion à long terme de l'angine de poitrine. pectoral.
Insuffisance cardiaque: Le mécanisme précis des effets bénéfiques des bêta-bloquants dans l'insuffisance cardiaque n'a pas été élucidé.
Pharmacodynamie
Des études de pharmacologie clinique ont confirmé l'activité bêta-bloquante du métoprolol chez l'homme, comme le montrent (1) la réduction de la fréquence cardiaque et du débit cardiaque au repos et à l'exercice, la réduction de la pression artérielle systolique à l'exercice, (3) l'inhibition de l'absorption induite par l'isoprotérénol. tachycardie et réduction de la tachycardie orthostatique réflexe.
La relation entre les taux plasmatiques de métoprolol et la réduction de la fréquence cardiaque à l'effort est indépendante de la formulation pharmaceutique. Les effets bêta-bloquants dans la plage de 30 à 80 % de l'effet maximal (réduction d'environ 8 à 23 % de la fréquence cardiaque à l'effort) correspondent à des concentrations plasmatiques de métoprolol comprises entre 30 et 540 nmol/L. La sélectivité bêta relative du métoprolol diminue et le blocage des récepteurs bêta2-adrénergiques augmente à une concentration plasmatique supérieure à 300 nmol/L.
Dans cinq études contrôlées chez des sujets sains normaux, le succinate de métoprolol à libération prolongée administré une fois par jour et le métoprolol à libération immédiate administré une à quatre fois par jour ont fourni un bêta-blocage total comparable sur 24 heures (aire sous le bêta-bloquant par rapport au temps courbe) dans la plage de doses de 100 à 400 mg. Dans une autre étude contrôlée, 50 mg une fois par jour pour chaque produit, le succinate de métoprolol à libération prolongée a produit un bêta-blocage total significativement plus élevé sur 24 heures que le métoprolol à libération immédiate. Pour le succinate de métoprolol à libération prolongée, le pourcentage de réduction de la fréquence cardiaque à l'effort était relativement stable tout au long de l'intervalle posologique et le niveau de bêta-blocage augmentait avec l'augmentation des doses de 50 à 300 mg par jour.
Une étude croisée contrôlée chez des patients insuffisants cardiaques a comparé les concentrations plasmatiques et les effets bêta-bloquants de 50 mg de métoprolol à libération immédiate administrés 3 fois par jour, et de 100 mg et 200 mg de succinate de métoprolol à libération prolongée une fois par jour. Le succinate de métoprolol à libération prolongée 200 mg une fois par jour a produit un effet plus important sur la suppression de la fréquence cardiaque induite par l'exercice et surveillée par Holter sur 24 heures par rapport à 50 mg tid de métoprolol à libération immédiate.
Dans d'autres études, le traitement par le succinate de métoprolol a entraîné une amélioration de la fraction d'éjection ventriculaire gauche. Il a également été démontré que le succinate de métoprolol retardait l'augmentation des volumes télésystolique et télédiastolique ventriculaire gauche après 6 mois de traitement.
Bien que le blocage des récepteurs bêta-adrénergiques soit utile dans le traitement de l'angor, de l'hypertension et de l'insuffisance cardiaque, il existe des situations dans lesquelles la stimulation sympathique est vitale. Chez les patients dont le cœur est gravement endommagé, une fonction ventriculaire adéquate peut dépendre de la force sympathique. En présence d'un bloc AV, le bêtabloquant peut empêcher l'effet facilitateur nécessaire de l'activité sympathique sur la conduction. Le blocage bêta2-adrénergique entraîne une constriction bronchique passive en interférant avec l'activité bronchodilatatrice adrénergique endogène chez les patients sujets au bronchospasme et peut également interférer avec les bronchodilatateurs exogènes chez ces patients.
Pharmacocinétique
Absorption
Les concentrations plasmatiques maximales après l'administration une fois par jour de TOPROL-XL représentent en moyenne un quart à la moitié des concentrations plasmatiques maximales obtenues après une dose correspondante de métoprolol conventionnel, administré une fois par jour ou en doses fractionnées. À l'état d'équilibre, la biodisponibilité moyenne du métoprolol après l'administration de TOPROL-XL, dans l'intervalle posologique de 50 à 400 mg une fois par jour, était de 77 % par rapport aux doses uniques ou fractionnées correspondantes de métoprolol conventionnel.
La biodisponibilité du métoprolol montre une augmentation liée à la dose, bien que non directement proportionnelle, avec la dose et n'est pas significativement affectée par la nourriture après l'administration de TOPROL-XL.
Les concentrations plasmatiques maximales après administration orale de comprimés de métoprolol conventionnels, cependant, avoisinent 50 % des niveaux après administration intraveineuse, indiquant un métabolisme de premier passage d'environ 50 %.
Distribution
Le métoprolol traverse la barrière hémato-encéphalique et a été signalé dans le LCR à une concentration de 78 % de la concentration plasmatique simultanée. Seule une petite fraction du médicament (environ 12 %) est liée à l'albumine sérique humaine.
Métabolisme
Le métoprolol est un mélange racémique d'énantiomères R et S et est principalement métabolisé par le CYP2D6. Lorsqu'il est administré par voie orale, il présente un métabolisme stéréosélectif qui dépend du phénotype d'oxydation.
Élimination
L'élimination se fait principalement par biotransformation dans le foie et la demi-vie plasmatique varie d'environ 3 à 7 heures. Moins de 5 % d'une dose orale de métoprolol sont retrouvés sous forme inchangée dans les urines ; le reste est excrété par les reins sous forme de métabolites qui semblent n'avoir aucune activité bêta-bloquante.
Suite à l'administration intraveineuse de métoprolol, la récupération urinaire du médicament inchangé est d'environ 10 %.
Populations spécifiques
Patients atteints d'insuffisance rénale
La disponibilité systémique et la demi-vie du métoprolol chez les patients insuffisants rénaux ne diffèrent pas de manière cliniquement significative de celles des sujets normaux.
Patients pédiatriques
Le profil pharmacocinétique de TOPROL-XL a été étudié chez 120 patients pédiatriques hypertendus (âgés de 6 à 17 ans) recevant des doses allant de 12,5 à 200 mg une fois par jour. La pharmacocinétique du métoprolol était similaire à celles décrites précédemment chez l'adulte. La pharmacocinétique du métoprolol n'a pas été étudiée chez les patients de
Poids corporel, âge et race
La clairance orale apparente du métoprolol (CL/F) a augmenté de façon linéaire avec le poids corporel. L'âge, le sexe et la race n'ont eu aucun effet significatif sur la pharmacocinétique du métoprolol.
Interactions médicamenteuses
CYP2D6
Le métoprolol est principalement métabolisé par le CYP2D6. Chez des sujets sains présentant un phénotype de métaboliseur extensif du CYP2D6, l'administration concomitante de 100 mg de quinidine, un puissant inhibiteur du CYP2D6, et de 200 mg de métoprolol à libération immédiate a triplé la concentration de S-métoprolol et doublé la demi-vie d'élimination du métoprolol. Chez quatre patients atteints de maladie cardiovasculaire, la co-administration de propafénone 150 mg tid avec du métoprolol à libération immédiate 50 mg tid a entraîné une concentration à l'état d'équilibre du métoprolol de 2 à 5 fois celle observée avec le métoprolol seul. Les métaboliseurs rapides qui utilisent simultanément des médicaments inhibiteurs du CYP2D6 auront des taux sanguins de métoprolol augmentés (plusieurs fois), diminuant la cardiosélectivité du métoprolol [voir INTERACTIONS MÉDICAMENTEUSES ].
Pharmacogénomique
Le CYP2D6 est absent chez environ 8 % des Caucasiens (métaboliseurs lents) et environ 2 % de la plupart des autres populations. Le CYP2D6 peut être inhibé par plusieurs médicaments. Les métaboliseurs lents du CYP2D6 auront des taux sanguins de métoprolol augmentés (plusieurs fois), ce qui diminuera la cardiosélectivité du métoprolol.
Etudes cliniques
Hypertension
Dans une étude en double aveugle, 1092 patients souffrant d'hypertension légère à modérée ont été randomisés pour recevoir TOPROLXL une fois par jour (25, 100 ou 400 mg), PLENDIL® (comprimés de félodipine à libération prolongée), l'association ou un placebo. Après 9 semaines, TOPROL-XL seul a diminué la pression artérielle en position assise de 6-8/4-7 mmHg (changement corrigé par rapport au placebo) 24 heures après l'administration. L'association de TOPROL-XL avec PLENDIL a des effets plus importants sur la tension artérielle.
Dans des études cliniques contrôlées, une forme posologique à libération immédiate de métoprolol était un agent antihypertenseur efficace lorsqu'il était utilisé seul ou en traitement concomitant avec des diurétiques de type thiazidique à des doses de 100 à 450 mg par jour. TOPROL-XL, à des doses de 100 à 400 mg une fois par jour, produit un blocage β1 similaire à celui des comprimés de métoprolol conventionnels administrés deux à quatre fois par jour. De plus, TOPROL-XL administré à une dose de 50 mg une fois par jour a abaissé la tension artérielle 24 heures après l'administration dans des études contrôlées par placebo. Dans des études cliniques comparatives contrôlées, le métoprolol à libération immédiate est apparu comme un agent antihypertenseur comparable au propranolol, à la méthyldopa et aux diurétiques de type thiazidique, et a affecté à la fois la tension artérielle en décubitus et en position debout. En raison des taux plasmatiques variables atteints avec une dose donnée et de l'absence de relation cohérente entre l'activité antihypertensive et la concentration plasmatique du médicament, la sélection d'une posologie appropriée nécessite une titration individuelle.
Angine de poitrine
Dans des essais cliniques contrôlés, une formulation à libération immédiate de métoprolol s'est avérée être un agent anti-angineux efficace, réduisant le nombre de crises d'angor et augmentant la tolérance à l'exercice. La posologie utilisée dans ces études variait de 100 à 400 mg par jour. TOPROL-XL, à des doses de 100 à 400 mg une fois par jour, s'est avéré posséder un bêta-bloquant similaire aux comprimés de métoprolol conventionnels administrés deux à quatre fois par jour.
Insuffisance cardiaque
MERIT-HF était une étude randomisée en double aveugle et contrôlée par placebo de TOPROL-XL dans laquelle 3991 patients avec une fraction d'éjection ≤ 0,40 et une insuffisance cardiaque de classe NYHA II-IV attribuable à une ischémie, une hypertension ou une cardiomyopathie ont été randomisés 1: 1 pour TOPROL XL 100 mg ou placebo. Le protocole excluait les patients présentant des contre-indications à l'utilisation de bêtabloquants, ceux devant subir une chirurgie cardiaque et ceux dans les 28 jours suivant un infarctus du myocarde ou une angine instable. Les principaux critères d'évaluation de l'essai étaient (1) la mortalité toutes causes plus l'hospitalisation toutes causes (délai jusqu'au premier événement) et la mortalité toutes causes. Les patients ont été stabilisés avec un traitement concomitant optimal pour l'insuffisance cardiaque, comprenant des diurétiques, des inhibiteurs de l'ECA, des glycosides cardiaques et des nitrates. Lors de la randomisation, 41 % des patients étaient de classe II de la NYHA ; 55 % NYHA Classe III ; 65 % des patients avaient une insuffisance cardiaque attribuée à une cardiopathie ischémique ; 44 % avaient des antécédents d'hypertension ; 25 % souffraient de diabète sucré ; 48 % avaient des antécédents d'infarctus du myocarde. Parmi les patients de l'essai, 90 % étaient sous diurétiques, 89 % sous IEC, 64 % sous digitaliques, 27 % sous hypolipémiant, 37 % sous anticoagulant oral et la fraction d'éjection moyenne était de 0,28. . La durée moyenne de suivi était d'un an. À la fin de l'étude, la dose quotidienne moyenne de TOPROL-XL était de 159 mg.
L'essai a été interrompu prématurément pour une réduction statistiquement significative de la mortalité toutes causes confondues (34 %, p nominal = 0,00009). Le risque de mortalité toutes causes plus hospitalisation toutes causes a été réduit de 19 % (p = 0,00012). L'essai a également montré des améliorations de la mortalité liée à l'insuffisance cardiaque et des hospitalisations liées à l'insuffisance cardiaque, ainsi que de la classe fonctionnelle NYHA.
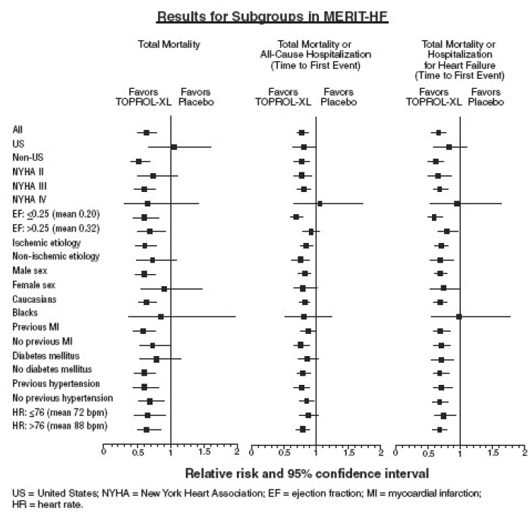
Le tableau ci-dessous présente les principaux résultats pour l'ensemble de la population étudiée. La figure ci-dessous illustre les principaux résultats pour une grande variété de comparaisons de sous-groupes, y compris les populations américaines et non américaines (cette dernière n'étant pas pré-spécifiée). Les critères d'évaluation combinés de la mortalité toutes causes plus l'hospitalisation toutes causes et de la mortalité plus l'hospitalisation pour insuffisance cardiaque ont montré des effets cohérents dans la population globale de l'étude et les sous-groupes, y compris les femmes et la population américaine. Cependant, dans le sous-groupe américain (n=1071) et chez les femmes (n=898), la mortalité globale et la mortalité cardiovasculaire semblaient moins affectées. Des analyses de patientes et de patientes américaines ont été réalisées car elles représentaient chacune environ 25 % de la population globale. Néanmoins, les analyses de sous-groupes peuvent être difficiles à interpréter et on ne sait pas si elles représentent de véritables différences ou des effets de hasard.
Paramètres cliniques de l'étude MERIT-HF
INFORMATIONS PATIENTS
Conseillez aux patients de prendre TOPROL-XL régulièrement et continuellement, comme dirigé, de préférence avec ou immédiatement après les repas. Si une dose est oubliée, le patient ne doit prendre que la prochaine dose prévue (sans la doubler). Les patients ne doivent pas interrompre ou arrêter TOPROL-XL sans consulter le médecin.
Conseillez aux patients (1) d'éviter de faire fonctionner des automobiles et des machines ou de s'engager dans d'autres tâches nécessitant de la vigilance jusqu'à ce que la réponse du patient au traitement par TOPROL-XL ait été déterminée ; contacter le médecin en cas de difficulté respiratoire ; (3) d'informer le médecin ou le dentiste avant tout type de chirurgie qu'il ou elle prend TOPROL-XL.
Les patients atteints d'insuffisance cardiaque doivent être avisés de consulter leur médecin s'ils présentent des signes ou des symptômes d'aggravation de l'insuffisance cardiaque tels qu'une prise de poids ou un essoufflement croissant.
