Sumycin 250mg, 500mg Tetracycline Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
Qu'est-ce que Sumycin et comment est-il utilisé?
La sumycine (chlorhydrate de tétracycline) est un antibiotique utilisé pour traiter de nombreuses infections bactériennes différentes, telles que les infections des voies urinaires, l'acné, la gonorrhée, la chlamydia et autres. Sumycin est disponible sous forme générique.
Quels sont les effets secondaires de Sumycin 250mg ?
Les effets secondaires courants de Sumycin comprennent :
- nausée,
- vomissement,
- diarrhée,
- maux d'estomac,
- perte d'appétit,
- plaques blanches ou plaies dans la bouche ou sur les lèvres,
- langue enflée,
- langue poilue noire,
- mal de gorge,
- difficulté à avaler,
- vertiges,
- mal de tête,
- plaies ou enflure dans la région rectale ou génitale, ou
- démangeaisons ou pertes vaginales.
Pour réduire le développement de bactéries résistantes aux médicaments et maintenir l'efficacité de Sumycin "250" et Sumycine "500" Comprimés (comprimés de chlorhydrate de tétracycline) et autres médicaments antibactériens, Sumycin "250" et Sumycine "500" Les comprimés (comprimés de chlorhydrate de tétracycline) doivent être utilisés uniquement pour traiter ou prévenir les infections dont il est prouvé ou fortement suspecté qu'elles sont causées par des bactéries.
LA DESCRIPTION
Sumycin pour administration orale contient de la tétracycline, un antibiotique isolé de Streptomyces aureofaciens. La tétracycline est décrite chimiquement comme 4-(diméthylamino)-1, 4, 4a, 5, 5a, 6, 11, 12a-octa-hydro-3, 6, 10, 12, 12a-pentahydroxy-6-méthyl-1, 11 -dioxo-2-napthacènecarboxamide; sa formule structurale est :
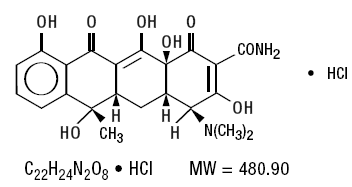
Sumycine "250" et Sumycine "500" Les comprimés (comprimés de chlorhydrate de tétracycline) sont disponibles pour l'administration orale sous forme de comprimés fournissant respectivement 250 mg et 500 mg de chlorhydrate de tétracycline. Ingrédients inactifs : colorants (laque d'aluminium D&C rouge n° 30, dioxyde de titane), hypromellose, lactose anhydre, stéarate de magnésium, cellulose microcristalline, povidone, amidon prégélatinisé, acide stéarique. De plus, 250 mg contiennent du chlorure de méthylène, de l'hydroxypropylcellulose, de la triacétine et 500 mg contiennent du polyéthylèneglycol, du polyparabène, du méthylparabène, du citrate de sodium, du sorbate de potassium, du propylparabène et de la gomme de xanthane.
LES INDICATIONS
Pour réduire le développement de bactéries résistantes aux médicaments et maintenir l'efficacité des comprimés Sumycin '250' et Sumycin '500' (comprimés de chlorhydrate de tétracycline) et d'autres médicaments antibactériens, les comprimés Sumycin '250' et Sumycin '500' (comprimés de chlorhydrate de tétracycline ) ne doit être utilisé que pour traiter ou prévenir les infections dont il est prouvé ou fortement suspecté qu'elles sont causées par des bactéries sensibles. Lorsque des informations sur la culture et la sensibilité sont disponibles, elles doivent être prises en compte lors de la sélection ou de la modification du traitement antibactérien. En l'absence de telles données, l'épidémiologie locale et les schémas de sensibilité peuvent contribuer à la sélection empirique du traitement.
Le chlorhydrate de tétracycline est indiqué pour le traitement des infections suivantes :
La fièvre pourprée des montagnes Rocheuses, la fièvre typhus et le groupe typhus, la fièvre Q, la variole à rickettsies et la fièvre à tiques causées par les rickettsies.
Infections des voies respiratoires causées par Mycoplasma pneumoniae
Lymphogranulome vénérien causé par Chlamydia trachomatis
Psittacose et ornithose à Chlamydia psittaci
Le trachome causé par Chlamydia trachomatis, bien que l'agent infectieux ne soit pas toujours éliminé, à en juger par l'immunofluorescence
Conjonctivite à inclusions causée par Chlamydia trachomatis
Le chlorhydrate de tétracycline est indiqué pour le traitement des infections urétrales, endocervicales ou rectales non compliquées chez l'adulte causées par Chlamydia trachomatis
Urétrite non gonococcique due à Ureaplasma urealyticum Fièvre récurrente due à Borrelia recurrentis
Le chlorhydrate de tétracycline est également indiqué pour le traitement des infections causées par les micro-organismes gram-négatifs suivants :
Chancre mou causé par Haemophilus ducreyi
Peste due à Yersinia pestis (anciennement Pasteurella pestis)
Tularémie due à Francisella tularensis (anciennement Pasteurella tularensis)
Choléra causé par Vibrio cholerae (anciennement Vibrio comma)
Infections à Campylobacter fetus causées par Campylobacter fetus (anciennement Vibrio fetus)
Brucellose due aux espèces de Brucella (en association avec la streptomycine)
Bartonellose à Bartonella bacilliformis
Granulome inguinal causé par Calymmatobacterium granulomatis
Étant donné que de nombreuses souches des groupes de micro-organismes suivants se sont avérées résistantes au chlorhydrate de tétracycline, une culture et des tests de sensibilité sont recommandés.
Le chlorhydrate de tétracycline est indiqué pour le traitement des infections causées par les micro-organismes gram-négatifs suivants, lorsque les tests bactériologiques indiquent une sensibilité appropriée au médicament :
Escherichia coli
Enterobacter aerogenes (anciennement Aerobacter aerogenes)
Espèces de Shigella
Espèces Acinetobacter [anciennement espèces Mima et espèces Herellea]
Infections des voies respiratoires causées par Haemophilus influenzae
Infections des voies respiratoires et des voies urinaires causées par les espèces de Klebsiella
Le chlorhydrate de tétracycline est indiqué pour le traitement des infections causées par les micro-organismes gram-positifs suivants lorsque les tests bactériologiques ont indiqué une sensibilité appropriée au médicament :
Pour les infections des voies respiratoires supérieures causées par Streptococcus pneumoniae (anciennement Diplococcus pneumoniae)
Infections de la peau et des tissus cutanés causées par Staphylococcus aureus. Les tétracyclines ne sont pas les médicaments de choix dans le traitement de tout type d'infections staphylococciques
Lorsque la pénicilline est contre-indiquée, le chlorhydrate de tétracycline est un médicament alternatif dans le traitement des infections suivantes :
Gonorrhée non compliquée causée par Neisseria gonorrhoeae
Syphilis causée par Treponema pallidum
Pian causé par Treponema pertenue
Listériose due à Listeria monocytogenes
Charbon dû à Bacillus anthracis
Infection de Vincent causée par Fusobacterium fusiforme
Actinomycose causée par Actinomyces israelii
Infections causées par les espèces de Clostridia
Dans l'amibiase intestinale aiguë, les chlorhydrates de tétracycline peuvent être une thérapie d'appoint utile aux amibicides.
Dans l'acné sévère, les chlorhydrates de tétracycline peuvent être une thérapie d'appoint utile.
DOSAGE ET ADMINISTRATION
Adultes : la dose quotidienne habituelle est de 1 à 2 g : pour les infections légères à modérées : 500 mg bid ou 250 mg qid ; des doses plus élevées telles que 500 mg qid peuvent être nécessaires pour les infections graves.
Pour les enfants de plus de huit ans : la dose quotidienne habituelle est de 10 à 20 mg/lb (25 à 50 mg/kg) de poids corporel divisée en quatre doses égales.
Le traitement doit être poursuivi pendant au moins 24 à 48 heures après la disparition des symptômes et de la fièvre.
Le traitement de la brucellose, 500 mg de tétracycline quatre fois par jour pendant trois semaines doit être accompagné de streptomycine, 1 g par voie intramusculaire deux fois par jour la première semaine et une fois par jour la deuxième semaine.
Pour le traitement de la gonorrhée non compliquée, 500 mg toutes les six heures pendant sept jours.
Pour le traitement de la syphilis, un total de 30 à 40 g en doses également réparties sur une période de 10 à 15 jours doit être administré. Un suivi étroit, y compris des tests de laboratoire, est recommandé.
Infection urétrale, endocervicale ou rectale non compliquée chez l'adulte causée par Chlamydia trachomatis : 500 mg par voie orale, quatre fois par jour pendant au moins sept jours.
En cas d'acné sévère qui, de l'avis du clinicien, nécessite un traitement à long terme, la posologie initiale recommandée est de 1 g par jour en doses fractionnées. Lorsqu'une amélioration est notée, généralement en une semaine, la posologie doit être progressivement réduite à des niveaux d'entretien allant de 125 à 500 mg par jour. Chez certains patients, il peut être possible de maintenir une rémission adéquate des lésions avec un traitement alterné ou intermittent. Le traitement de l'acné par la tétracycline devrait compléter les autres mesures standard connues pour leur valeur.
Chez les insuffisants rénaux (voir AVERTISSEMENTS la posologie totale doit être diminuée en réduisant les doses individuelles recommandées et/ou en allongeant les intervalles de temps entre les doses.
Dans le traitement des infections streptococciques, une dose thérapeutique de tétracycline doit être administrée pendant au moins 10 jours.
Thérapie concomitante : L'absorption des tétracyclines est altérée par les antiacides contenant de l'aluminium, du calcium ou du magnésium et des préparations contenant du fer.
Les aliments et certains produits laitiers interfèrent également avec l'absorption.
L'administration de quantités adéquates de liquide avec le comprimé et en particulier les gélules de tétracycline est recommandée pour laver le médicament et réduire le risque d'irritation et d'ulcération de l'œsophage (voir EFFETS INDÉSIRABLES )
COMMENT FOURNIE
Comprimés Sumycin® (comprimés de chlorhydrate de tétracycline USP)
Stockage
Conserver les comprimés à température ambiante ; éviter une chaleur excessive. Distribuer dans des récipients étanches et résistants à la lumière.
Fabriqué par : Bristol-Myers Squibb Company, Princeton, NJ 08543 USA. Fabriqué pour : Par Pharmaceutical, Inc. Spring Valley, NY 10977. États-Unis. Révisé le 03/04. Date de révision FDA : 22/07/1997
EFFETS SECONDAIRES
Gastro-intestinal : anorexie, détresse épigastrique, nausées, vomissements, diarrhée, selles molles volumineuses, stomatite, mal de gorge, glossite, langue noire velue, dysphagie, enrouement, entérocolite et lésions inflammatoires (avec prolifération de candidose) dans la région anogénitale, y compris proctite et prurit anal . De rares cas d'oesophagite et d'ulcération de l'oesophage ont été rapportés chez des patients recevant en particulier les formes gélules et comprimés de tétracyclines. La plupart des patients auraient pris des médicaments immédiatement avant d'aller au lit (voir DOSAGE ET ADMINISTRATION ). Ces réactions ont été provoquées à la fois par l'administration orale et parentérale de tétracyclines, mais sont moins fréquentes après l'administration parentérale.
Peau et structures cutanées : éruptions maculopapuleuses et érythémateuses. Une dermatite exfoliative a été rapportée mais est peu fréquente. De rares cas d'onycholyse et de décoloration des ongles ont été rapportés. Une photosensibilité s'est produite. (Voir AVERTISSEMENTS ).
Toxicité rénale : des augmentations du BUN ont été signalées et sont apparemment liées à la dose. (Voir AVERTISSEMENTS. )
Cholestase hépatique : a été rarement signalée et est généralement associée à des doses élevées de tétracycline.

Réactions d'hypersensibilité : Anaphylaxie; réactions de type maladie sérique, telles que fièvre, éruption cutanée et arthralgie ; urticaire, œdème de Quincke, purpura anaphylactoïde, péricardite, exacerbation du lupus érythémateux disséminé.
Hématologique : Sang : anémie, anémie hémolytique, thrombocytopénie, purpura thrombocytopénique, neutropénie et éosinophilie ont été rapportés.
Divers: Des étourdissements et des maux de tête ont été signalés.
Lorsqu'elles sont administrées sur des périodes prolongées, il a été rapporté que les tétracyclines produisaient une décoloration microscopique brun-noir des glandes thyroïdiennes. Aucune anomalie de la fonction thyroïdienne n'est connue. Des fontanelles bombées chez les nourrissons et une hypertension intracrânienne chez les adultes ont été rapportées. (Voir PRÉCAUTIONS-Général. )
INTERACTIONS MÉDICAMENTEUSES
PÉNICILLINE -Étant donné que les médicaments bactériostatiques comme la tétracycline peuvent interférer avec l'action bactéricide de la pénicilline, il est conseillé d'éviter de donner de la tétracycline en association avec de la pénicilline.
ANTICOAGULANTS -Parce qu'il a été démontré que les tétracyclines diminuent l'activité de la prothrombine plasmatique, les patients sous traitement anticoagulant peuvent nécessiter un ajustement à la baisse de leur dose d'anticoagulant.
ANTIACIDES ET PRODUITS CONTENANT DU FER - L'absorption de la tétracycline est altérée par les antiacides contenant de l'aluminium, du calcium ou du magnésium et des préparations contenant du fer.
CONTRACEPTIFS ORAUX L'utilisation concomitante de tétracycline peut rendre les contraceptifs oraux moins efficaces.
MÉTHOXYFLURANE -L'utilisation concomitante de tétracycline et de méthoxyflurane a entraîné une toxicité rénale mortelle.
AVERTISSEMENTS
LES ANTIBIOTIQUES DE LA CLASSE TETRACYCLINE PEUVENT PROVOQUER DES DOMMAGES AU FOETAL LORSQU'ILS SONT ADMINISTRES A UNE FEMME ENCEINTE. SI UNE TÉTRACYCLINE EST UTILISÉE PENDANT LA GROSSESSE, OU SI LA PATIENTE TOMBE ENCEINTE PENDANT CES MÉDICAMENTS, LA PATIENTE DOIT ÊTRE INFORMÉE DU RISQUE POTENTIEL POUR LE FŒTUS.
L'UTILISATION DE MÉDICAMENTS DE LA CLASSE DES TÉTRACYCLINES PENDANT LE DÉVELOPPEMENT DES DENTS (DERNIÈRE MOITIÉ DE LA GROSSESSE, DE LA PETITE ENFANCE ET DE L'ENFANCE À L'ÂGE DE 8 ANS) PEUT PROVOQUER UNE DÉCOLORATION PERMANENTE DES DENTS (JAUNE-GRIS-BRUN).
Cet effet indésirable est plus fréquent lors de l'utilisation à long terme des médicaments, mais a été observé après des traitements répétés à court terme. Une hypoplasie de l'émail a également été rapportée. PAR CONSÉQUENT, LES MÉDICAMENTS À LA TÉTRACYCLINE NE DEVRAIENT PAS ÊTRE UTILISÉS PENDANT LE DÉVELOPPEMENT DES DENTS À MOINS QUE D'AUTRES MÉDICAMENTS NE SONT PROBABLEMENT EFFICACES OU SONT CONTRE-INDIQUÉS.
Toutes les tétracyclines forment un complexe de calcium stable dans tous les tissus osseux. Une diminution du taux de croissance du péroné a été observée chez de jeunes animaux (rats et lapins) ayant reçu de la tétracycline par voie orale à des doses de 25 mg/kg toutes les six heures. Cette réaction s'est avérée réversible lorsque le médicament a été arrêté.
Les résultats d'études animales indiquent que les tétracyclines traversent le placenta, se trouvent dans les tissus fœtaux et peuvent avoir des effets toxiques sur le fœtus en développement (souvent liés à un retard du développement du squelette). Des signes d'embryotoxicité ont également été observés chez des animaux traités en début de gestation.
L'action antianabolique de la tétracycline peut provoquer une augmentation de l'azote uréique. Bien que cela ne soit pas un problème chez les personnes dont la fonction rénale est normale, chez les patients dont la fonction rénale est considérablement altérée, des taux sériques plus élevés de tétracycline peuvent entraîner une azotémie, une hyperphosphatémie et une acidose. En cas d'insuffisance rénale, même la dose orale ou parentérale habituelle peut entraîner une accumulation systémique excessive du médicament et une éventuelle toxicité hépatique. Dans de telles conditions, des doses inférieures aux doses habituelles sont indiquées et, si le traitement est prolongé, des déterminations du taux sérique du médicament peuvent être recommandées.
Une photosensibilité, se manifestant par une réaction exagérée de coup de soleil, a été observée chez certains individus prenant des tétracyclines. Les patients susceptibles d'être exposés à la lumière directe du soleil ou à la lumière ultraviolette doivent être informés que cette réaction peut survenir avec les médicaments à base de tétracycline et le traitement doit être interrompu dès les premiers signes d'érythème cutané.
REMARQUE : Les réactions de photosensibilisation se sont produites le plus fréquemment avec la déméclocycline, moins avec la chlortétracycline et très rarement avec l'oxytétracycline et la tétracycline.
PRÉCAUTIONS
Général
Prescrire Sumycin '250' et Sumycin '500' Tablets (Tetracycline Hydrochloride Tablets) en l'absence d'une infection bactérienne avérée ou fortement suspectée ou d'une indication prophylactique est peu susceptible d'apporter un bénéfice au patient et augmente le risque de développement d'une résistance aux médicaments. bactéries.
Comme avec d'autres antibiotiques, l'utilisation de ce médicament peut entraîner une prolifération d'organismes non sensibles, y compris des champignons. En cas de surinfection, l'antibiotique doit être arrêté et un traitement approprié institué. REMARQUE : La surinfection de l'intestin par les staphylocoques peut mettre la vie en danger.
La pseudotumeur cérébrale (hypertension intracrânienne bénigne) chez l'adulte a été associée à l'utilisation de tétracyclines. Les manifestations cliniques habituelles sont des céphalées et une vision floue. Des fontanelles bombées ont été associées à l'utilisation de tétracyclines chez les nourrissons. Bien que ces deux conditions et les symptômes associés disparaissent généralement après l'arrêt de la tétracycline, la possibilité de séquelles permanentes existe.
Étant donné que les réactions de sensibilité sont plus susceptibles de se produire chez les personnes ayant des antécédents d'allergie, d'asthme, de rhume des foins ou d'urticaire, la préparation doit être utilisée avec prudence chez ces personnes.
La sensibilisation croisée entre les diverses tétracyclines est extrêmement courante.
L'incision et le drainage ou d'autres interventions chirurgicales doivent être effectuées en conjonction avec une antibiothérapie, le cas échéant.
En aucun cas, des tétracyclines périmées ne doivent être administrées, car la dégradation des tétracyclines est hautement néphrotoxique et a parfois provoqué un syndrome de type Fanconi.
Tests de laboratoire
Pendant le traitement à long terme, une évaluation périodique en laboratoire de la fonction des systèmes organiques, y compris les systèmes rénal, hépatique et hématopoïétique, doit être effectuée.
Tous les patients atteints de gonorrhée doivent subir un test sérologique pour la syphilis au moment du diagnostic. Les patients traités par la tétracycline doivent subir un test sérologique de suivi pour la syphilis après 3 mois.
Carcinogenèse, mutagenèse, altération de la fertilité
Des études à long terme menées chez des rats et des souris pour déterminer si le chlorhydrate de tétracycline a un potentiel carcinogène se sont révélées négatives. Certains antibiotiques apparentés (oxytétracycline, minocycline) ont montré des signes d'activité oncogène chez le rat. Dans deux systèmes d'essais in vitro sur cellules de mammifères (lymphome de souris L51784y et cellules pulmonaires de hamster chinois), des signes de mutagénicité ont été observés à des concentrations de chlorhydrate de tétracycline de 60 et 10 µg/mL, respectivement.
Le chlorhydrate de tétracycline n'a eu aucun effet sur la fertilité lorsqu'il a été administré dans l'alimentation de rats mâles et femelles à une dose quotidienne de 25 fois la dose humaine.
Grossesse : Effets tératogènes : Catégorie de grossesse D (voir AVERTISSEMENTS. )
Grossesse : Effets non tératogènes : (voir AVERTISSEMENTS. )
Travail et accouchement
L'effet des tétracyclines sur le travail et l'accouchement est inconnu.
Mères allaitantes
Les tétracyclines sont présentes dans le lait des femmes allaitantes qui prennent un médicament de cette classe. En raison du risque d'effets indésirables graves chez les nourrissons allaités par les tétracyclines, une décision doit être prise soit d'interrompre l'allaitement soit d'arrêter le médicament, en tenant compte de l'importance du médicament pour la mère (voir AVERTISSEMENTS .)
Utilisation pédiatrique
Voir AVERTISSEMENTS et DOSAGE ET ADMINISTRATION.
SURDOSAGE
En cas de surdosage, traiter de manière symptomatique et instituer des mesures de soutien.
CONTRE-INDICATIONS
Ce médicament est contre-indiqué chez les personnes qui ont montré une hypersensibilité à l'une des tétracyclines.
PHARMACOLOGIE CLINIQUE
Les tétracyclines sont adéquatement mais incomplètement absorbées par le tractus gastro-intestinal. Environ 65 % d'une tétracycline à action brève sont liés aux protéines plasmatiques ; la liaison aux protéines plasmatiques pour les analogues à action intermédiaire et prolongée est généralement supérieure.
La pénétration des tétracyclines dans la plupart des fluides et tissus corporels est excellente. Les tétracyclines sont distribuées à des degrés divers dans la bile, le foie, les poumons, les reins, la prostate, l'urine, le liquide céphalo-rachidien, le liquide synovial, la muqueuse du sinus maxillaire, le cerveau, les expectorations et les os. Les tétracyclines traversent le placenta et pénètrent dans la circulation fœtale et le liquide amniotique.
Après une dose orale unique, les concentrations plasmatiques maximales sont atteintes en deux à quatre heures.
Les tétracyclines sont concentrées par le foie dans la bile. Ils sont excrétés dans l'urine et les fèces à des concentrations élevées sous une forme biologiquement active. La clairance rénale des tétracyclines se faisant par filtration glomérulaire, l'excrétion est significativement affectée par l'état de la fonction rénale. (Voir AVERTISSEMENTS. )
Microbiologie
Les tétracyclines sont principalement bactériostatiques et on pense qu'elles exercent leur effet antimicrobien en inhibant la synthèse des protéines. Les tétracyclines ont un spectre d'activité antimicrobien similaire contre une large gamme d'organismes gram-positifs et gram-négatifs. La résistance croisée de ces organismes aux tétracyclines est courante. De plus, les bacilles à Gram négatif rendus résistants à la tétracycline peuvent également présenter une résistance croisée au chloramphénicol.
BACTÉRIES GRAM-NÉGATIVES :
Bartonella bacilliformis Espèce Brucella Calymmatobacterium granulomatis Campylobacter fetus Francisella tularensis Haemophilus ducreyi Haemophilus influenzae Listeria monocytogenes Neisseria gonorrhoeae Vibrio cholerae Yersinia pestis
Étant donné que de nombreuses souches des groupes suivants de micro-organismes gram-négatifs se sont révélées résistantes aux tétracyclines, la culture et les tests de sensibilité sont particulièrement recommandés :
Espèce Acinetobacter Espèce Bacteroides Enterobacter aerogenes Escherichia coli Espèce Klebsiella Espèce Shigella
BACTÉRIES GRAMPOSITIVES :
Groupe Enterococcus [Enterococcus faecalis, (anciennement Streptococcus faecalis) et Enterococcus faecium (anciennement Streptococcus faecium)
Groupe Streptococcus viridans Streptococcus pneumoniae Streptococcus pyogenes
Étant donné que de nombreuses souches de ces micro-organismes gram-positifs se sont révélées résistantes à la tétracycline, il est recommandé de procéder à une culture et à des tests de sensibilité. Jusqu'à 44 % des souches de Streptococcus pyogenes et 74 % d'Enterococcus faecalis (anciennement Streptococcus faecalis) se sont révélées résistantes aux médicaments à base de tétracycline. Par conséquent, les tétracyclines ne doivent pas être utilisées pour le traitement de la maladie streptococcique à moins que l'organisme ne soit connu pour être sensible.
AUTRES MICROORGANISMES :
Espèce Actinomyces Bacillus anthracis Balantidium coli Borrelia recurrentis Chlamydia psittaci Chlamydia trachomatis Espèce Clostridium Espèce Entamoeba Fusobacterium fusiforme Mycoplasma pneumoniae Rickettsiae Propionibacterium acnes Treponema pallidum Treponema pertenue Ureaplasma urealyticum
Test de sensibilité
Techniques de diffusion
Les méthodes quantitatives qui nécessitent la mesure des diamètres de zone donnent l'estimation la plus précise de la sensibilité des bactéries aux agents antimicrobiens.
Une telle procédure standard1 qui a été recommandée pour une utilisation avec des disques pour tester la sensibilité des micro-organismes à la tétracycline utilise le disque de tétracycline de 30 mcg. L'interprétation implique la corrélation des diamètres de zone obtenus dans le test du disque avec la concentration minimale inhibitrice (CMI) pour la tétracycline.
Les rapports du laboratoire donnant les résultats du test de sensibilité standard à disque unique avec un disque de tétracycline de 30 mcg doivent être interprétés selon les critères suivants :
Un rapport "Susceptible" indique que l'agent pathogène est susceptible d'être inhibé par des niveaux sanguins généralement réalisables. Un rapport "intermédiaire" suggère que l'organisme serait sensible si une dose élevée est utilisée ou si l'infection est confinée aux tissus ou aux fluides dans lesquels des niveaux élevés d'antibiotiques (ou antimicrobiens) sont atteints. Un rapport de "résistant" indique que les concentrations réalisables sont peu susceptibles d'être inhibitrices et qu'un autre traitement doit être sélectionné.
Les procédures standardisées nécessitent l'utilisation d'organismes de contrôle de laboratoire. Le disque de tétracycline de 30 mcg doit donner les diamètres de zone suivants :
Techniques de dilution
Utiliser une méthode de dilution standardisée2 (bouillon, gélose, microdilution) ou équivalent avec de la poudre de tétracycline. Les valeurs de CMI obtenues doivent être interprétées selon les critères suivants :
Comme pour les techniques de diffusion standard, les méthodes de dilution nécessitent l'utilisation d'organismes de contrôle de laboratoire. La poudre de tétracycline standard doit fournir les valeurs de CMI suivantes :
Pharmacologie animale et toxicologie animale
Une hyperpigmentation de la thyroïde a été produite par des membres de la classe des tétracyclines chez les espèces suivantes : chez le rat par l'oxytétracycline, la doxycycline, la tétracycline PO4 et la méthacycline ; chez les cochons nains par la doxycycline, la minocycline, la tétracycline PO4 et la méthacycline ; chez le chien par la doxycycline et la minocycline ; chez le singe par la minocycline.
La minocycline, la tétracycline PO4, la méthacycline, la doxycycline, la base de tétracycline, le chlorhydrate d'oxytétracycline et le chlorhydrate de tétracycline étaient goitrigènes chez des rats nourris avec un régime pauvre en iode. Cet effet goitrigène s'accompagnait d'une forte absorption d'iode radioactif. L'administration de minocycline a également produit un gros goitre avec une forte absorption d'iode radioactif chez les rats nourris avec un régime relativement riche en iode.
Le traitement de diverses espèces animales avec cette classe de médicaments a également entraîné l'induction d'une hyperplasie thyroïdienne chez les animaux suivants : chez le rat et le chien (minocycline), chez le poulet (chlortétracycline) et chez le rat et la souris (oxytétracycline). Une hyperplasie des glandes surrénales a été observée chez des chèvres et des rats traités à l'oxytétracycline.
RÉFÉRENCE
1. Comité national des normes de laboratoire clinique, Normes de performance pour les tests de sensibilité aux disques antimicrobiens - Quatrième édition. Norme approuvée NCCLS Document M2-A4, Vol. 10, n° 7 NCCLS, Villanova, Pennsylvanie, avril 1990.
2. National Committee for Clinical Laboratory Standards, Methods for Dilution Antimicrobial Susceptibility Tests for Bacteria that Grow Aerobically-Second Edition. Norme approuvée NCCLS Document M7-A2, Vol. 10, n° 8 NCCLS, Villanova, Pennsylvanie, avril 1990.
INFORMATIONS PATIENTS
Les patients doivent être informés que les médicaments antibactériens, y compris les comprimés Sumycin '250' et Sumycin '500' (comprimés de chlorhydrate de tétracycline), ne doivent être utilisés que pour traiter les infections bactériennes. Ils ne traitent pas les infections virales (par exemple, le rhume). Lorsque les comprimés Sumycin '250' et Sumycin '500' (comprimés de chlorhydrate de tétracycline) sont prescrits pour traiter une infection bactérienne, les patients doivent être informés que, bien qu'il soit courant de se sentir mieux au début du traitement, le médicament doit être pris exactement comme dirigée. Sauter des doses ou ne pas terminer le traitement complet peut (1) diminuer l'efficacité du traitement immédiat et (2) augmenter la probabilité que les bactéries développent une résistance et ne puissent pas être traitées par les comprimés Sumycin '250' et Sumycin '500' ( comprimés de chlorhydrate de tétracycline) ou d'autres médicaments antibactériens à l'avenir.
