Luvox 100mg, 50mg Fluvoxamine Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
Qu'est-ce que Luvox (maléate de fluvoxamine) et comment est-il utilisé ?
Luvox 100 mg est un médicament délivré sur ordonnance utilisé pour traiter les symptômes du trouble obsessionnel-compulsif. Luvox peut être utilisé seul ou avec d'autres médicaments.
Luvox 100 mg appartient à une classe de médicaments appelés antidépresseurs, ISRS.
On ne sait pas si Luvox 100 mg est sûr et efficace chez les enfants de moins de 8 ans.
Quels sont les effets secondaires possibles de Luvox ?
Luvox peut provoquer des effets secondaires graves, notamment :
- anxiété,
- pensées de course,
- comportement à risque,
- troubles du sommeil (insomnie),
- sentiments de bonheur extrême ou d'irritabilité,
- Vision floue,
- vision tunnel,
- douleur ou gonflement des yeux,
- voir des lumières rondes halo,
- convulsions (crises),
- changements de poids ou d'appétit,
- ecchymoses faciles ou saignements inhabituels,
- mal de tête,
- confusion,
- problèmes de mémoire,
- grande faiblesse,
- perte de coordination,
- se sentir instable,
- muscles très raides (rigides),
- forte fièvre,
- transpiration,
- confusion,
- battements cardiaques rapides ou irréguliers,
- tremblements,
- étourdissement,
- agitation,
- hallucinations,
- transpiration,
- frissons
- rythme cardiaque rapide,
- raideur musculaire,
- contractions musculaires,
- nausée,
- des vomissements et
- diarrhée
Consultez immédiatement un médecin si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires les plus courants de Luvox 50 mg incluent :
- somnolence,
- vertiges,
- tremblement,
- se sentir anxieux,
- humeur dépressive,
- troubles du sommeil (insomnie),
- maux d'estomac,
- gaz,
- perte d'appétit,
- nausée,
- vomissement,
- diarrhée,
- bouche sèche,
- bâillement,
- mal de gorge,
- douleur musculaire,
- transpiration,
- éruption,
- menstruations abondantes,
- diminution de la libido,
- éjaculation anormale, et
- difficulté à avoir un orgasme
Dites au médecin si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas.
Ce ne sont pas tous les effets secondaires possibles de Luvox. Pour plus d'informations, consultez votre médecin ou votre pharmacien.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
SUICIDALITÉ ET MÉDICAMENTS ANTIDÉPRESSEURS
Les antidépresseurs ont augmenté le risque par rapport au placebo de pensées et de comportements suicidaires (suicidalité) chez les enfants, les adolescents et les jeunes adultes dans des études à court terme sur le trouble dépressif majeur (TDM) et d'autres troubles psychiatriques. Toute personne envisageant l'utilisation des comprimés de maléate de Fluvox 50mgamine ou de tout autre antidépresseur chez un enfant, un adolescent ou un jeune adulte doit équilibrer ce risque avec le besoin clinique. Les études à court terme n'ont pas montré d'augmentation du risque de suicide avec les antidépresseurs par rapport au placebo chez les adultes au-delà de 24 ans ; il y avait une réduction du risque avec les antidépresseurs par rapport au placebo chez les adultes âgés de 65 ans et plus. La dépression et certains autres troubles psychiatriques sont eux-mêmes associés à une augmentation du risque de suicide. Les patients de tous âges qui commencent un traitement antidépresseur doivent être surveillés de manière appropriée et observés de près pour déceler une aggravation clinique, des tendances suicidaires ou des changements inhabituels de comportement. Les familles et les soignants doivent être informés de la nécessité d'une surveillance étroite et d'une communication avec le prescripteur. Les comprimés de maléate de Fluvox 50 mgamine ne sont pas approuvés pour une utilisation chez les patients pédiatriques, à l'exception des patients souffrant de trouble obsessionnel compulsif (TOC). [Voir AVERTISSEMENTS ET PRECAUTIONS - Aggravation clinique et risque de suicide ].
LA DESCRIPTION
Le maléate de fluvoxamine est un inhibiteur sélectif de la recapture de la sérotonine (5-HT) (ISRS) appartenant à la série chimique des 2-aminoéthyl oximes éthers des aralkylcétones.
Il est chimiquement désigné sous le nom de maléate de 5-méthoxy-4'-(trifluorométhyl)valérophénone-(E)-O-(2-aminoéthyl)oxime (1:1) et a la formule empirique C15H21O2N2F3•C4H4O4. Son poids moléculaire est de 434,41. La formule structurale est :
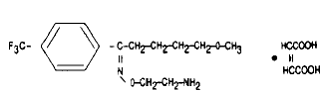
Le maléate d'amine Fluvox 100 mg est une poudre cristalline blanche à blanc cassé, inodore, peu soluble dans l'eau, librement soluble dans l'éthanol et le chloroforme et pratiquement insoluble dans l'éther diéthylique.
Les comprimés de maléate de fluvoxamine sont disponibles en dosages de 25 mg, 50 mg et 100 mg pour administration orale. En plus de l'ingrédient actif, fluvox 100 mg de maléate d'amine, chaque comprimé contient les ingrédients inactifs suivants : cire de carnauba, hypromellose, mannitol, polyéthylèneglycol, polysorbate 80, amidon prégélatinisé (pomme de terre), dioxyde de silicium, stéarylfumarate de sodium, amidon (maïs), et dioxyde de titane. Les comprimés de 50 mg et 100 mg contiennent également des oxydes de fer synthétiques.
LES INDICATIONS
Trouble obsessionnel compulsif
Les comprimés de maléate de fluvoxamine sont indiqués pour le traitement des obsessions et des compulsions chez les patients atteints de trouble obsessionnel-compulsif (TOC), tel que défini dans le DSM-III-R ou le DSM-IV. Les obsessions ou les compulsions provoquent une détresse marquée, prennent du temps ou interfèrent de manière significative avec le fonctionnement social ou professionnel.
Le trouble obsessionnel-compulsif se caractérise par des idées, des pensées, des impulsions ou des images récurrentes et persistantes (obsessions) qui sont des comportements ego-dystoniques et/ou répétitifs, délibérés et intentionnels (compulsions) qui sont reconnus par la personne comme excessifs ou déraisonnables.
L'efficacité des comprimés de maléate de 100 mg de Fluvox a été établie dans quatre essais chez des patients ambulatoires atteints de TOC : deux essais de 10 semaines chez des adultes, un essai de 10 semaines chez des patients pédiatriques (âgés de 8 à 17 ans) et un essai d'entretien chez des adultes [voir Etudes cliniques ].
DOSAGE ET ADMINISTRATION
Adultes
La dose initiale recommandée pour les comprimés de maléate de Fluvox 50 mgamine chez les patients adultes est de 50 mg, administrée en une dose quotidienne unique au coucher. Dans les essais cliniques contrôlés établissant l'efficacité des comprimés de maléate de fluvoxamine dans le TOC, les patients ont été titrés dans une gamme de doses de 100 à 300 mg/jour. Par conséquent, la dose doit être augmentée par paliers de 50 mg tous les 4 à 7 jours, selon la tolérance, jusqu'à ce que le bénéfice thérapeutique maximal soit atteint, sans dépasser 300 mg par jour. Il est conseillé d'administrer une dose quotidienne totale supérieure à 100 mg en deux doses fractionnées. Si les doses ne sont pas égales, la dose la plus élevée doit être administrée au coucher.
Population pédiatrique (enfants et adolescents)
La dose initiale recommandée pour les comprimés de maléate de fluvoxamine dans les populations pédiatriques (âgées de 8 à 17 ans) est de 25 mg, administrée en une dose quotidienne unique au coucher. Dans un essai clinique contrôlé établissant l'efficacité des comprimés de maléate de fluvoxamine dans le TOC, des patients pédiatriques (âgés de 8 à 17 ans) ont été titrés dans une plage de doses de 50 à 200 mg/jour. Les médecins doivent tenir compte des différences d'âge et de sexe lors de l'administration aux patients pédiatriques. La dose maximale chez les enfants jusqu'à l'âge de 11 ans ne doit pas dépasser 200 mg/jour. L'effet thérapeutique chez les filles peut être obtenu avec des doses plus faibles. Un ajustement posologique chez les adolescents (jusqu'à la dose maximale adulte de 300 mg) peut être indiqué pour obtenir un bénéfice thérapeutique. La dose doit être augmentée par paliers de 25 mg tous les 4 à 7 jours, selon la tolérance, jusqu'à ce que le bénéfice thérapeutique maximal soit atteint. Il est conseillé d'administrer une dose quotidienne totale supérieure à 50 mg en deux doses fractionnées. Si les deux doses fractionnées ne sont pas égales, la dose la plus élevée doit être administrée au coucher.
Patients âgés ou atteints d'insuffisance hépatique
Il a été observé que les patients âgés et ceux atteints d'insuffisance hépatique présentaient une diminution de la clairance du maléate de fluvoxamine. Par conséquent, il peut être approprié de modifier la dose initiale et l'ajustement posologique ultérieur pour ces groupes de patients.
Passage d'un patient à ou à partir d'un inhibiteur de la monoamine oxydase (IMAO) destiné à traiter les troubles psychiatriques
Au moins 14 jours doivent s'écouler entre l'arrêt d'un IMAO destiné à traiter les troubles psychiatriques et le début du traitement par les comprimés de maléate de Fluvox 50 mgamine. À l'inverse, il faut attendre au moins 14 jours après l'arrêt de Fluvox 100mgamine Maléate Comprimés avant de commencer un IMAO destiné à traiter les troubles psychiatriques [voir CONTRE-INDICATIONS ].
Utilisation de comprimés de maléate de fluvoxamine avec d'autres IMAO tels que le linézolide ou le bleu de méthylène
Ne pas commencer à prendre des comprimés de maléate de fluvoxamine chez un patient qui est traité avec du linézolide ou du bleu de méthylène par voie intraveineuse car il existe un risque accru de syndrome sérotoninergique. Chez un patient qui nécessite un traitement plus urgent d'une affection psychiatrique, d'autres interventions, y compris l'hospitalisation, doivent être envisagées [voir CONTRE-INDICATIONS ].
Dans certains cas, un patient recevant déjà un traitement par Fluvox 50 mg de maléate d'amine peut nécessiter un traitement urgent avec du linézolide ou du bleu de méthylène par voie intraveineuse. Si des alternatives acceptables au traitement par le linézolide ou le bleu de méthylène par voie intraveineuse ne sont pas disponibles et que les avantages potentiels du traitement par le linézolide ou le bleu de méthylène par voie intraveineuse sont jugés supérieurs aux risques de syndrome sérotoninergique chez un patient particulier, les comprimés de maléate de fluvoxamine doivent être arrêtés rapidement et le linézolide ou le traitement par voie intraveineuse du bleu de méthylène peut être administré. Le patient doit être surveillé pour des symptômes de syndrome sérotoninergique pendant deux semaines ou jusqu'à 24 heures après la dernière dose de linézolide ou de bleu de méthylène par voie intraveineuse, selon la première éventualité. Le traitement par les comprimés de maléate de Fluvox 100 mgamine peut être repris 24 heures après la dernière dose de linézolide ou de bleu de méthylène par voie intraveineuse [voir AVERTISSEMENTS ET PRECAUTIONS ].
Le risque d'administration de bleu de méthylène par des voies non intraveineuses (telles que des comprimés oraux ou par injection locale) ou à des doses intraveineuses bien inférieures à 1 mg/kg avec les comprimés de maléate de Fluvox 100 mgamine n'est pas clair. Le clinicien doit néanmoins être conscient de la possibilité d'apparition de symptômes de syndrome sérotoninergique lors d'une telle utilisation [voir AVERTISSEMENTS ET PRECAUTIONS ].
Traitement prolongé d'entretien/continuation
Il est généralement admis que le trouble obsessionnel compulsif nécessite plusieurs mois ou plus de traitement pharmacologique soutenu. Le bénéfice de maintenir les patients atteints de TOC sous Fluvoxamine Maleate Tablets après avoir obtenu une réponse pendant une durée moyenne d'environ 4 semaines dans une phase à simple insu de 10 semaines au cours de laquelle les patients ont été titrés jusqu'à l'effet a été démontré dans un essai contrôlé [voir Essais cliniques ].
Le médecin qui choisit d'utiliser les comprimés de maléate de fluvoxamine pendant de longues périodes doit réévaluer périodiquement l'utilité à long terme du médicament pour le patient individuel.
Arrêt du traitement par les comprimés de maléate de fluvoxamine
Des symptômes associés à l'arrêt d'autres ISRS ou IRSN ont été signalés [voir AVERTISSEMENTS ET PRECAUTIONS ]. Les patients doivent être surveillés pour ces symptômes lors de l'arrêt du traitement. Une réduction progressive de la dose plutôt qu'un arrêt brutal est recommandée dans la mesure du possible. Si des symptômes intolérables surviennent suite à une diminution de la dose ou à l'arrêt du traitement, la reprise de la dose précédemment prescrite peut être envisagée. Par la suite, le médecin peut continuer à diminuer la dose, mais à un rythme plus graduel.
COMMENT FOURNIE
Formes posologiques et points forts
Les comprimés de maléate de fluvoxamine USP sont disponibles sous les formes suivantes :
Comprimés à 25 mg : non sécables, blancs, elliptiques, pelliculés (avec l'inscription « 1222 » gravée sur une face)
Comprimés 50 mg : sécables, jaunes, elliptiques, pelliculés (marqués « 1225 » d'un côté et sécables de l'autre)
Comprimés 100 mg : sécables, beiges, elliptiques, pelliculés (marqués « 1221 » d'un côté et sécables de l'autre)
Stockage et manutention
Les comprimés de maléate de Fluvox 50mgamine USP sont disponibles dans les concentrations, couleurs, empreintes et présentations suivantes :
non rainuré, blanc, elliptique, pelliculé (gravé « 1222 » sur une face)
Bouteilles de 100 ............. CDN 62559-158-01
sécable, jaune, elliptique, pelliculé (marqué « 1225 » d'un côté et sécable de l'autre)
Bouteilles de 100 ............. CDN 62559-159-01
sécable, beige, elliptique, pelliculé (marqué « 1221 » d'un côté et sécable de l'autre)
Bouteilles de 100 ............. CDN 62559-160-01
Tenir hors de portée des enfants.
Les comprimés de maléate de fluvoxamine doivent être protégés de l'humidité élevée et conservés entre 20 et 25 °C (68 et 77 °F) ; excursions permises jusqu'à 15° à 30°C (59° à 86°F) [voir Température ambiante contrôlée USP ].
Répartir dans des récipients étanches.
Fabriqué par : ANI Pharmaceuticals, Inc., Baudette, MN 56623. Révisé : juillet 2021
EFFETS SECONDAIRES
Étant donné que les essais cliniques sont menés dans des conditions très variables, les taux d'effets indésirables observés dans les essais cliniques d'un médicament ne peuvent pas être directement comparés aux taux des essais cliniques d'un autre médicament et peuvent ne pas refléter les taux observés dans la pratique.
Effets indésirables entraînant l'arrêt du traitement
Sur les 1087 patients TOC et déprimés traités avec du maléate de fluvoxamine dans des essais cliniques contrôlés en Amérique du Nord, 22 % ont arrêté en raison d'un effet indésirable. Les effets indésirables qui ont conduit à l'arrêt du traitement chez au moins 2 % des patients traités par le maléate de fluvoxamine dans ces essais étaient : nausées (9 %), insomnie (4 %), somnolence (4 %), céphalées (3 %) et asthénie, vomissements , nervosité, agitation et étourdissements (2 % chacun).
Incidence dans les essais contrôlés
Effets indésirables couramment observés dans les essais cliniques contrôlés
Les comprimés de maléate de Fluvox 100mgamine ont été étudiés dans des essais contrôlés à court terme de 10 semaines sur le TOC (N=320) et la dépression (N=1350). En général, les taux d'effets indésirables étaient similaires dans les deux ensembles de données ainsi que dans l'étude pédiatrique sur le TOC. Les effets indésirables les plus fréquemment observés associés à l'utilisation des comprimés de maléate de fluvoxamine et susceptibles d'être liés au médicament (incidence de 5 % ou plus et au moins deux fois celle du placebo) d'après le tableau 2 étaient : nausées, somnolence, insomnie, asthénie, nervosité, dyspepsie, éjaculation anormale, transpiration, anorexie, tremblements et vomissements. Dans un pool de deux études portant uniquement sur des patients atteints de TOC, les réactions supplémentaires suivantes ont été identifiées en utilisant la règle ci-dessus : anorgasmie, diminution de la libido, bouche sèche, rhinite, altération du goût et pollakiurie. Dans une étude portant sur des patients pédiatriques atteints de TOC, les réactions supplémentaires suivantes ont été identifiées à l'aide de la règle ci-dessus : agitation, dépression, dysménorrhée, flatulence, hyperkinésie et éruption cutanée.
Effets indésirables survenant à une incidence de 1 %
Le tableau 2 énumère les effets indésirables survenus chez les adultes à une fréquence de 1 % ou plus, et qui étaient plus fréquents que dans le groupe placebo, chez les patients traités avec les comprimés de maléate de fluvoxamine dans deux essais contrôlés par placebo à court terme sur le TOC (10 semaines) et la dépression. essais (6 semaines) dans lesquels les patients recevaient des doses comprises généralement entre 100 et 300 mg/jour. Ce tableau montre le pourcentage de patients dans chaque groupe qui ont eu au moins une occurrence d'une réaction à un moment donné au cours de leur traitement. Les effets indésirables signalés ont été classés à l'aide d'une terminologie standard du dictionnaire basée sur COSTART.
Le prescripteur doit être conscient que ces chiffres ne peuvent pas être utilisés pour prédire l'incidence des effets secondaires dans le cadre de la pratique médicale habituelle lorsque les caractéristiques des patients et d'autres facteurs peuvent différer de ceux qui ont prévalu dans les essais cliniques. De même, les fréquences citées ne peuvent être comparées aux chiffres obtenus à partir d'autres investigations cliniques impliquant différents traitements, utilisations et investigateurs. Les chiffres cités, cependant, fournissent au médecin prescripteur une base pour estimer la contribution relative des facteurs médicamenteux et non médicamenteux au taux d'incidence des effets secondaires dans la population étudiée.
TABLEAU 2 : TAUX D'INCIDENCE DES RÉACTIONS INDÉSIRABLES SURVENUES AU TRAITEMENT PAR SYSTÈME CORPOREL DANS LES POPULATIONS ADULTES DE TOC ET DE DÉPRESSION COMBINÉES1
Effets indésirables dans les études contrôlées par placebo sur le TOC dont le taux est nettement différent (défini comme une différence d'au moins deux fois) par rapport aux taux de réaction regroupés dans les études contrôlées par placebo sur le TOC et la dépression
Les réactions dans les études sur le TOC avec une diminution du taux de deux fois par rapport aux taux de réaction dans les études sur le TOC et la dépression étaient la dysphagie et l'amblyopie (principalement une vision floue). De plus, il y avait une diminution d'environ 25 % des nausées.
Les réactions dans les études sur le TOC dont le taux a été multiplié par deux par rapport aux taux de réaction dans les études sur le TOC et la dépression étaient les suivantes : asthénie, éjaculation anormale (principalement éjaculation retardée), anxiété, rhinite, anorgasmie (chez les hommes), dépression, diminution de la libido, pharyngite , agitation, impuissance, myoclonies/secousses musculaires, soif, perte de poids, crampes dans les jambes, myalgie et rétention urinaire. Ces réactions sont répertoriées par ordre décroissant de taux dans les essais sur le TOC.
Autres effets indésirables dans la population pédiatrique TOC
Chez les patients pédiatriques (N = 57) traités avec les comprimés de maléate de Fluvox 100 mgamine, le profil global des effets indésirables était généralement similaire à celui observé dans les études chez l'adulte, comme indiqué dans le tableau 2. Cependant, les effets indésirables suivants, qui n'apparaissent pas dans le tableau 2, ont été signalés chez au moins deux des patients pédiatriques et étaient plus fréquents avec les comprimés de maléate de fluvoxamine qu'avec le placebo : augmentation de la toux, dysménorrhée, ecchymose, labilité émotionnelle, épistaxis, hyperkinésie, réaction maniaque, éruption cutanée, sinusite et perte de poids.
Dysfonction sexuelle masculine et féminine avec les ISRS
Bien que les modifications du désir sexuel, de la performance sexuelle et de la satisfaction sexuelle se produisent souvent comme des manifestations d'un trouble psychiatrique et avec le vieillissement, elles peuvent également être une conséquence d'un traitement pharmacologique. En particulier, certaines preuves suggèrent que les inhibiteurs sélectifs de la recapture de la sérotonine (ISRS) peuvent provoquer de telles expériences sexuelles fâcheuses.
Des estimations fiables de l'incidence et de la gravité des expériences fâcheuses impliquant le désir sexuel, la performance et la satisfaction sont cependant difficiles à obtenir, en partie parce que les patients et les médecins peuvent être réticents à en discuter. En conséquence, les estimations de l'incidence des expériences et des performances sexuelles indésirables citées dans l'étiquetage des produits sous-estiment probablement leur incidence réelle.
Le tableau 3 présente l'incidence des effets secondaires sexuels signalés par au moins 2 % des patients prenant des comprimés de maléate de 100 mg de Fluvox dans des essais contrôlés par placebo portant sur la dépression et le TOC.
TABLEAU 3 : POURCENTAGE DE PATIENTS SIGNALANT DES RÉACTIONS SEXUELLES INDÉSIRABLES DANS DES ESSAIS CONTRÔLÉS CONTRE PLACEBO POUR ADULTES DANS LE TOC ET LA DÉPRESSION
Il n'y a pas d'études adéquates et bien contrôlées examinant la dysfonction sexuelle avec un traitement à la fluvoxamine.
Le traitement par Fluvox 50mgamine a été associé à plusieurs cas de priapisme. Dans les cas dont l'issue était connue, les patients se sont rétablis sans séquelles et après l'arrêt du fluvox 50 mgamine.
Bien qu'il soit difficile de connaître le risque précis de dysfonctionnement sexuel associé à l'utilisation des ISRS, les médecins doivent régulièrement se renseigner sur ces effets secondaires possibles.
Modifications des signes vitaux
Comparaisons des groupes maléate de fluvoxamine et placebo dans des pools distincts d'essais à court terme sur le TOC et la dépression sur (1) le changement médian par rapport au départ sur diverses variables de signes vitaux et sur (2) l'incidence des patients répondant aux critères de changements potentiellement importants par rapport au départ sur divers signes vitaux signes variables n'ont révélé aucune différence importante entre le maléate de fluvoxamine et le placebo.
Changements de laboratoire
Comparaisons des groupes maléate de fluvoxamine et placebo dans des pools distincts d'essais à court terme sur le TOC et la dépression sur (1) le changement médian par rapport au départ sur diverses variables de chimie sérique, d'hématologie et d'analyse d'urine et sur (2) l'incidence des patients répondant aux critères de changements potentiellement importants à partir de la ligne de base sur diverses variables de chimie sérique, d'hématologie et d'analyse d'urine n'ont révélé aucune différence importante entre le maléate de fluvox 100 mg d'amine et le placebo.
Modifications de l'ECG
Comparaisons des groupes maléate de fluvox 50mgamine et placebo dans des pools séparés d'essais à court terme sur le TOC et la dépression sur (1) le changement moyen par rapport au départ sur diverses variables ECG et sur (2) l'incidence des patients répondant aux critères de changements potentiellement importants par rapport au départ sur divers ECG variables n'ont révélé aucune différence importante entre le maléate de fluvoxamine et le placebo.
Autres réactions observées au cours de l'évaluation préalable à la commercialisation des comprimés de maléate de Fluvox à 100 mg d'amine
Au cours des essais cliniques de précommercialisation menés en Amérique du Nord et en Europe, des doses multiples de maléate de fluvoxamine ont été administrées pour un total combiné de 2 737 patients exposés à des patients souffrant de TOC ou de trouble dépressif majeur. Les réactions indésirables associées à cette exposition ont été enregistrées par les investigateurs cliniques en utilisant la terminologie descriptive de leur choix. Par conséquent, il n'est pas possible de fournir une estimation significative de la proportion d'individus présentant des réactions indésirables sans d'abord regrouper des types similaires de réactions indésirables dans un nombre limité (c'est-à-dire réduit) de catégories de réactions standard.
Dans les tableaux qui suivent, une terminologie standard du dictionnaire basée sur COSTART a été utilisée pour classer les effets indésirables rapportés. Si le terme COSTART pour une réaction était si général qu'il n'était pas informatif, il a été remplacé par un terme plus informatif. Les fréquences présentées représentent donc la proportion des 2 737 patients exposés à des doses multiples de maléate de fluvox 100 mg d'amine qui ont présenté une réaction du type cité à au moins une occasion alors qu'ils recevaient du maléate de fluvoxamine. Toutes les réactions rapportées sont incluses dans la liste ci-dessous, avec les exceptions suivantes : 1) les réactions déjà répertoriées dans le tableau 2, qui présente les taux d'incidence des effets indésirables courants dans les essais cliniques contrôlés par placebo sur le TOC et la dépression, sont exclues ; 2) les réactions pour lesquelles une cause médicamenteuse n'a pas été considérée comme probable sont omises ; 3) réactions pour lesquelles le terme COSTART était trop vague pour être cliniquement significatif et ne pouvait pas être remplacé par un terme plus informatif ; et 4) les réactions signalées chez un seul patient et jugées non potentiellement graves ne sont pas incluses. Il est important de souligner que, bien que les réactions signalées se soient produites pendant le traitement par le maléate de fluvoxamine, une relation causale avec le maléate de fluvoxamine n'a pas été établie.
Les réactions sont en outre classées dans des catégories de systèmes corporels et énumérées par ordre décroissant de fréquence en utilisant les définitions suivantes : les réactions indésirables fréquentes sont définies comme celles qui se produisent en une ou plusieurs occasions chez au moins 1 patient sur 100 ; les effets indésirables peu fréquents sont ceux qui surviennent entre 1/100 et 1/1000 patients ; et les effets indésirables rares sont ceux qui surviennent chez moins de 1/1000 patients.
Corps dans son ensemble - Fréquent : malaise ; Peu fréquent : réaction de photosensibilité et tentative de suicide.
Système cardiovasculaire - Fréquent : syncope.
Système digestif - Peu fréquents : hémorragie gastro-intestinale et méléna ; Rare : hématémèse.
Systèmes sanguin et lymphatique - Peu fréquents : anémie et ecchymoses ; Rares : purpura.
Systèmes métaboliques et nutritionnels - Fréquents : prise de poids et perte de poids.
Système nerveux - Fréquents : hyperkinésie, réaction maniaque et myoclonie ; Peu fréquents : rêves anormaux, akathisie, convulsions, dyskinésie, dystonie, euphorie, syndrome extrapyramidal et contractions musculaires ; Rare : syndrome de sevrage.
Système respiratoire - Peu fréquent : épistaxis. Rare : hémoptysie et laryngisme.
Peau - Peu fréquent : urticaire.
Système urogénital* - Peu fréquents : hématurie, ménorragie et hémorragie vaginale ; Rare : hématospermie.
* Selon le nombre d'hommes ou de femmes, selon le cas.
Rapports post-commercialisation
Les effets indésirables suivants ont été identifiés lors de l'utilisation post-approbation des comprimés de maléate de Fluvox 100mgamine. Étant donné que ces réactions sont signalées volontairement par une population de taille incertaine, il n'est pas toujours possible d'estimer de manière fiable leur fréquence ou d'établir une relation causale avec l'exposition au médicament.
Les rapports volontaires d'effets indésirables chez les patients prenant des comprimés de maléate de Fluvox à 50 mg qui ont été reçus depuis la mise sur le marché et dont la relation causale avec l'utilisation des comprimés de maléate de fluvoxamine est inconnue comprennent : insuffisance rénale aiguë, agranulocytose, aménorrhée, réaction anaphylactique, œdème de Quincke, anémie aplasique, éruption bulleuse , purpura d'Henoch-Schoenlein, hépatite, iléus, pancréatite, porphyrie, syndrome de Stevens-Johnson, nécrolyse épidermique toxique, vascularite et tachycardie ventriculaire (y compris torsades de pointes).
INTERACTIONS MÉDICAMENTEUSES
Interactions potentielles avec des médicaments qui inhibent ou sont métabolisés par les isoenzymes du cytochrome P450
Plusieurs isoenzymes hépatiques du cytochrome P450 sont impliquées dans la biotransformation oxydative d'un grand nombre de médicaments et de composés endogènes structurellement différents. Les connaissances disponibles concernant la relation entre la fluvoxamine et le système isoenzymatique du cytochrome P450 ont été obtenues principalement à partir d'études d'interaction pharmacocinétique menées chez des volontaires sains, mais certaines données préliminaires in vitro sont également disponibles. Sur la base d'une découverte d'interactions substantielles de fluvox 50mgamine avec certains de ces médicaments [voir les parties ultérieures de cette section et aussi AVERTISSEMENTS ET PRECAUTIONS ] et des données in vitro limitées pour le CYP3A4, il semble que le fluvox 100mgamine inhibe plusieurs isoenzymes du cytochrome P450 qui sont connues pour être impliquées dans le métabolisme d'autres médicaments tels que : CYP1A2 (par exemple, warfarine, théophylline, propranolol, tizanidine), CYP2C9 (par exemple , warfarine), CYP3A4 (p. ex., alprazolam) et CYP2C19 (p. ex., oméprazole).
Les données in vitro suggèrent que la fluvoxamine est un inhibiteur relativement faible du CYP2D6.
Environ 7% de la population normale a un code génétique qui conduit à des niveaux réduits d'activité du CYP2D6. Ces personnes ont été qualifiées de «métaboliseurs lents» (MP) de médicaments tels que la débrisoquine, le dextrométhorphane et les antidépresseurs tricycliques. Bien qu'aucun des médicaments étudiés pour les interactions médicamenteuses n'ait affecté de manière significative la pharmacocinétique de la fluvox 50 mgamine, une étude in vivo de la pharmacocinétique d'une dose unique de fluvoxamine chez des sujets de 13 PM a démontré des propriétés pharmacocinétiques altérées par rapport à 16 « métaboliseurs rapides » (EM) : Cmax moyenne, ASC , et la demi-vie ont été augmentées de 52 %, 200 % et 62 %, respectivement, dans le groupe PM par rapport au groupe EM. Cela suggère que la fluvox 100mgamine est métabolisée, au moins en partie, par le CYP2D6. La prudence est recommandée chez les patients connus pour avoir des niveaux réduits d'activité du CYP2D6 et chez ceux recevant des médicaments concomitants connus pour inhiber cette isoenzyme du cytochrome P450 (par exemple, la quinidine).
Le métabolisme de la fluvoxamine n'a pas été entièrement caractérisé et les effets d'une puissante inhibition des isoenzymes du cytochrome P450, comme l'inhibition par le kétoconazole du CYP3A4, sur le métabolisme de la fluvox 100 mgamine n'ont pas été étudiés.
Une interaction fluvoxamine cliniquement significative est possible avec des médicaments ayant un rapport thérapeutique étroit tels que le pimozide, la warfarine, la théophylline, certaines benzodiazépines, l'oméprazole et la phénytoïne. Si les comprimés de maléate de Fluvox 100mgamine doivent être administrés avec un médicament qui est éliminé par métabolisme oxydatif et a une fenêtre thérapeutique étroite, les taux plasmatiques et/ou les effets pharmacodynamiques de ce dernier médicament doivent être surveillés de près, au moins jusqu'à ce que les conditions d'état d'équilibre soient atteintes. atteint [voir CONTRE-INDICATIONS , AVERTISSEMENTS ET PRECAUTIONS ].
Médicaments actifs sur le SNC
Antipsychotiques : Voir AVERTISSEMENTS ET PRECAUTIONS .
Benzodiazépines : Voir AVERTISSEMENTS ET PRECAUTIONS .
Alprazolam : Voir AVERTISSEMENTS ET PRECAUTIONS .
Diazépam : Voir AVERTISSEMENTS ET PRECAUTIONS .
Lorazépam : Une étude de doses multiples de maléate de fluvoxamine (50 mg bid) chez des volontaires sains de sexe masculin (N = 12) et d'une dose unique de lorazépam (dose unique de 4 mg) n'a indiqué aucune interaction pharmacocinétique significative. En moyenne, le lorazépam seul et le lorazépam avec fluvoxamine ont produit des diminutions substantielles du fonctionnement cognitif ; cependant, la co-administration de fluvoxamine et de lorazépam n'a pas produit de diminutions moyennes plus importantes par rapport au lorazépam seul.
De l'alcool: Des études impliquant des doses uniques de 40 g d'éthanol (administration orale dans une étude et intraveineuse dans l'autre) et des doses multiples de maléate d'amine fluvox 100 mg (50 mg bid) n'ont révélé aucun effet de l'un ou l'autre des médicaments sur la pharmacocinétique ou la pharmacodynamique de l'autre. Comme avec d'autres médicaments psychotropes, il faut conseiller aux patients d'éviter l'alcool pendant qu'ils prennent des comprimés de maléate de fluvoxamine.
Carbamazépine : Des taux élevés de carbamazépine et des symptômes de toxicité ont été signalés lors de l'administration concomitante de maléate d'amine fluvox 100 mg et de carbamazépine.
Clozapine : Voir AVERTISSEMENTS ET PRECAUTIONS .
Lithium: Comme avec d'autres médicaments sérotoninergiques, le lithium peut augmenter les effets sérotoninergiques de la fluvoxamine et, par conséquent, l'association doit être utilisée avec prudence. Des convulsions ont été signalées lors de l'administration concomitante de maléate d'amine fluvox 50 mg et de lithium.
Méthadone : Voir AVERTISSEMENTS ET PRECAUTIONS .
Inhibiteurs de la monoamine oxydase : Voir DOSAGE ET ADMINISTRATION , CONTRE-INDICATIONS , AVERTISSEMENTS ET PRECAUTIONS .
Pimozide : Voir CONTRE-INDICATIONS , AVERTISSEMENTS ET PRECAUTIONS .
Rameltéon : Voir AVERTISSEMENTS ET PRECAUTIONS .
Médicaments sérotoninergiques : Voir DOSAGE ET ADMINISTRATION , CONTRE-INDICATIONS , AVERTISSEMENTS ET PRECAUTIONS .
Tacrine : Dans une étude portant sur 13 hommes volontaires sains, une dose unique de 40 mg de tacrine ajoutée à 50 mg de fluvox 100 mg/jour administrés à l'état d'équilibre a été associée à des augmentations de cinq et huit fois de la Cmax et de l'ASC de la tacrine, respectivement, par rapport à l'administration de tacrine seule. Cinq sujets ont présenté des nausées, des vomissements, des sueurs et de la diarrhée après la co-administration, ce qui correspond aux effets cholinergiques de la tacrine.
Thioridazine : Voir CONTRE-INDICATIONS , AVERTISSEMENTS ET PRECAUTIONS .
Tizanidine : Voir CONTRE-INDICATIONS , AVERTISSEMENTS ET PRECAUTIONS .
Antidépresseurs tricycliques (ATC) : Une augmentation significative des taux plasmatiques de TCA a été rapportée lors de l'administration concomitante de maléate de fluvoxamine et d'amitriptyline, de clomipramine ou d'imipramine. La prudence est indiquée lors de l'administration concomitante de comprimés de maléate de fluvoxamine et de TCA ; il peut être nécessaire de surveiller les concentrations plasmatiques de TCA et de réduire la dose de TCA.
Triptans : Il y a eu de rares rapports post-commercialisation de syndrome sérotoninergique avec l'utilisation d'un ISRS et d'un triptan. Si un traitement concomitant par fluvox 50mgamine avec un triptan est cliniquement justifié, une surveillance attentive du patient est conseillée, en particulier lors de l'initiation du traitement et des augmentations de dose [voir AVERTISSEMENTS ET PRECAUTIONS ].
Sumatriptan : Il y a eu de rares rapports post-commercialisation décrivant des patients présentant une faiblesse, une hyperréflexie et une incoordination suite à l'utilisation d'un inhibiteur sélectif de la recapture de la sérotonine (ISRS) et de sumatriptan. Si un traitement concomitant par le sumatriptan et un ISRS (par exemple, la fluoxétine, la fluvoxamine, la paroxétine, la sertraline) est cliniquement justifié, une surveillance appropriée du patient est conseillée.
Tryptophane : Le tryptophane peut augmenter les effets sérotoninergiques de la fluvoxamine et l'association doit donc être utilisée avec prudence. Des vomissements sévères ont été rapportés lors de l'administration concomitante de maléate de fluvoxamine et de tryptophane [voir AVERTISSEMENTS ET PRECAUTIONS ].
Autres drogues
Alosetron : Voir CONTRE-INDICATIONS , AVERTISSEMENTS ET PRECAUTIONS , et la notice Lotronex™ (alosetron).
Digoxine : L'administration de fluvox 100 mg de maléate d'amine 100 mg par jour pendant 18 jours (N = 8) n'a pas affecté de manière significative la pharmacocinétique d'une dose intraveineuse unique de 1,25 mg de digoxine.
Diltiazem : Une bradycardie a été signalée lors de l'administration concomitante de maléate de fluvoxamine et de diltiazem.
Mexilétine : Voir AVERTISSEMENTS ET PRECAUTIONS .
Propranolol et autres bêta-bloquants : L'administration concomitante de maléate de fluvoxamine à raison de 100 mg par jour et de propranolol à raison de 160 mg par jour chez des volontaires sains a entraîné une augmentation moyenne par cinq (intervalle de 2 à 17) des concentrations plasmatiques minimales de propranolol. Dans cette étude, il y avait une légère potentialisation de la réduction de la fréquence cardiaque induite par le propranolol et de la réduction de la pression diastolique à l'effort.
Un cas de bradycardie et d'hypotension et un deuxième cas d'hypotension orthostatique ont été signalés lors de l'administration concomitante de maléate de fluvoxamine et de métoprolol.
Si le propranolol ou le métoprolol est co-administré avec les comprimés de maléate de Fluvox 50 mg, une réduction de la dose initiale de bêta-bloquant et une titration plus prudente de la dose sont recommandées. Aucun ajustement posologique n'est requis pour les comprimés de maléate de fluvoxamine.
L'administration concomitante de maléate de fluvoxamine à 100 mg par jour et d'aténolol à 100 mg par jour (N = 6) n'a pas modifié les concentrations plasmatiques d'aténolol. Contrairement au propranolol et au métoprolol qui subissent un métabolisme hépatique, l'aténolol est principalement éliminé par excrétion rénale.
Théophylline : Voir AVERTISSEMENTS ET PRECAUTIONS .
Warfarine et autres médicaments interférant avec l'hémostase (AINS, aspirine, etc.) : Voir AVERTISSEMENTS ET PRECAUTIONS .
Effets du tabagisme sur le métabolisme de la fluvoxamine
Les fumeurs avaient une augmentation de 25 % du métabolisme de fluvox 100mgamine par rapport aux non-fumeurs.
Thérapie électroconvulsive (ECT)
Il n'y a pas d'études cliniques établissant les bénéfices ou les risques de l'utilisation combinée d'ECT et de maléate de fluvox 100mgamine.
Toxicomanie et dépendance
Substance contrôlée
Les comprimés de maléate de fluvoxamine ne sont pas une substance contrôlée.
Dépendance
Le potentiel d'abus, de tolérance et de dépendance physique avec le maléate d'amine fluvox 100 mg a été étudié dans un modèle de primate non humain. Aucune preuve de phénomènes de dépendance n'a été trouvée. Les effets de l'arrêt des comprimés de maléate de fluvoxamine n'ont pas été systématiquement évalués dans les essais cliniques contrôlés. Les comprimés de maléate de fluvoxamine n'ont pas été systématiquement étudiés dans les essais cliniques pour déterminer le potentiel d'abus, mais il n'y avait aucune indication de comportement de recherche de drogue dans les essais cliniques. Il convient toutefois de noter que les patients à risque de toxicomanie ont été systématiquement exclus des études expérimentales sur le fluvox 100 mg de maléate d'amine. Généralement, il n'est pas possible de prédire sur la base de l'expérience clinique préclinique ou précommercialisation dans quelle mesure un médicament actif sur le SNC sera mal utilisé, détourné et/ou abusé une fois commercialisé. Par conséquent, les médecins doivent soigneusement évaluer les patients pour des antécédents de toxicomanie et suivre ces patients de près, en les observant pour des signes de mésusage ou d'abus de maléate de fluvoxamine (c'est-à-dire, développement d'une tolérance, augmentation de la dose, comportement de recherche de drogue).
AVERTISSEMENTS
Inclus dans le cadre du PRÉCAUTIONS section.
PRÉCAUTIONS
Aggravation clinique et risque de suicide
Les patients atteints de trouble dépressif majeur (TDM), à la fois adultes et pédiatriques, peuvent présenter une aggravation de leur dépression et/ou l'émergence d'idées et de comportements suicidaires (suicidalité) ou des changements de comportement inhabituels, qu'ils prennent ou non des antidépresseurs, et cela le risque peut persister jusqu'à ce qu'une rémission significative se produise. Le suicide est un risque connu de dépression et de certains autres troubles psychiatriques, et ces troubles eux-mêmes sont les meilleurs prédicteurs du suicide. Cependant, on craint depuis longtemps que les antidépresseurs puissent jouer un rôle dans l'aggravation de la dépression et l'émergence de comportements suicidaires chez certains patients au cours des premières phases du traitement. Des analyses groupées d'essais contrôlés par placebo à court terme portant sur des antidépresseurs (ISRS et autres) ont montré que ces médicaments augmentent le risque de pensées et de comportements suicidaires (suicidalité) chez les enfants, les adolescents et les jeunes adultes (âgés de 18 à 24 ans) atteints d'un trouble dépressif majeur ( MDD) et d'autres troubles psychiatriques. Les études à court terme n'ont pas montré d'augmentation du risque de suicide avec les antidépresseurs par rapport au placebo chez les adultes au-delà de 24 ans ; il y avait une réduction avec les antidépresseurs par rapport au placebo chez les adultes âgés de 65 ans et plus.
Les analyses groupées d'essais contrôlés par placebo chez des enfants et des adolescents atteints de TDM, de trouble obsessionnel-compulsif (TOC) ou d'autres troubles psychiatriques comprenaient un total de 24 essais à court terme de 9 antidépresseurs chez plus de 4 400 patients. Les analyses groupées d'essais contrôlés par placebo chez des adultes atteints de TDM ou d'autres troubles psychiatriques comprenaient un total de 295 essais à court terme (durée médiane de 2 mois) de 11 antidépresseurs chez plus de 77 000 patients. Il y avait une variation considérable du risque de suicidalité entre les médicaments, mais une tendance à une augmentation chez les patients plus jeunes pour presque tous les médicaments étudiés. Il y avait des différences dans le risque absolu de suicidalité entre les différentes indications, avec l'incidence la plus élevée dans le TDM. Les différences de risque (médicament vs placebo) étaient cependant relativement stables au sein des tranches d'âge et entre les indications. Ces différences de risque (différence médicament-placebo dans le nombre de cas de suicide pour 1000 patients traités) sont présentées dans le tableau 1.
TABLEAU 1 : DIFFÉRENCES MÉDICAMENT-PLACEBO EN NOMBRE DE CAS DE SUICIDALITÉ POUR 1000 PATIENTS TRAITÉS
Aucun suicide n'est survenu dans aucun des essais pédiatriques. Il y a eu des suicides dans les essais sur les adultes, mais le nombre n'était pas suffisant pour tirer une conclusion sur l'effet du médicament sur le suicide.
On ne sait pas si le risque de suicide s'étend à une utilisation à plus long terme, c'est-à-dire au-delà de plusieurs mois. Cependant, il existe des preuves substantielles provenant d'essais d'entretien contrôlés par placebo chez des adultes souffrant de dépression que l'utilisation d'antidépresseurs peut retarder la récurrence de la dépression.
Tous les patients traités avec des antidépresseurs pour toute indication doivent être surveillés de manière appropriée et observés de près pour déceler une aggravation clinique, des tendances suicidaires et des changements inhabituels de comportement, en particulier au cours des premiers mois d'un traitement médicamenteux, ou lors de changements de dose, soit des augmentations ou diminue.
Les symptômes suivants, anxiété, agitation, attaques de panique, insomnie, irritabilité, hostilité, agressivité, impulsivité, akathisie (agitation psychomotrice), hypomanie et manie, ont été rapportés chez des patients adultes et pédiatriques traités avec des antidépresseurs pour un trouble dépressif majeur ainsi comme pour les autres indications, tant psychiatriques que non psychiatriques. Bien qu'un lien de causalité entre l'apparition de tels symptômes et soit l'aggravation de la dépression et/ou l'émergence d'impulsions suicidaires n'ait pas été établi, on craint que ces symptômes puissent représenter des précurseurs d'une suicidalité émergente.
Il convient d'envisager de modifier le schéma thérapeutique, y compris éventuellement d'arrêter le médicament, chez les patients dont la dépression s'aggrave de manière persistante, ou qui présentent des tendances suicidaires émergentes ou des symptômes qui pourraient être des précurseurs d'une aggravation de la dépression ou des tendances suicidaires, en particulier si ces symptômes sont graves, brusques. au début ou ne faisaient pas partie des symptômes présentés par le patient.
Si la décision a été prise d'arrêter le traitement, la médication doit être réduite, aussi rapidement que possible, mais en reconnaissant qu'un arrêt brutal peut être associé à certains symptômes et risques [voir DOSAGE ET ADMINISTRATION ].
Les familles et les soignants des patients traités avec des antidépresseurs pour un trouble dépressif majeur ou d'autres indications, à la fois psychiatriques et non psychiatriques, doivent être alertés de la nécessité de surveiller les patients pour l'apparition d'agitation, d'irritabilité, de changements inhabituels de comportement et des autres symptômes décrits ci-dessus. , ainsi que l'émergence de tendances suicidaires, et de signaler immédiatement ces symptômes aux professionnels de la santé. Une telle surveillance devrait inclure une observation quotidienne par les familles et les soignants. Les prescriptions de comprimés de maléate de fluvoxamine doivent être rédigées pour la plus petite quantité de comprimés compatible avec une bonne prise en charge du patient, afin de réduire le risque de surdosage.
Dépistage des patients pour le trouble bipolaire
Un épisode dépressif majeur peut être la présentation initiale d'un trouble bipolaire. Il est généralement admis (bien que non établi dans des essais contrôlés) que le traitement d'un tel épisode avec un antidépresseur seul peut augmenter la probabilité de précipitation d'un épisode mixte/maniaque chez les patients à risque de trouble bipolaire. On ne sait pas si l'un des symptômes décrits ci-dessus représente une telle conversion. Cependant, avant d'initier un traitement avec un antidépresseur, les patients présentant des symptômes dépressifs doivent faire l'objet d'un dépistage adéquat pour déterminer s'ils présentent un risque de trouble bipolaire ; un tel dépistage devrait inclure des antécédents psychiatriques détaillés, y compris des antécédents familiaux de suicide, de trouble bipolaire et de dépression. Il convient de noter que les comprimés de maléate de Fluvox 50mgamine ne sont pas approuvés pour une utilisation dans le traitement de la dépression bipolaire.
Syndrome sérotoninergique
Le développement d'un syndrome sérotoninergique potentiellement mortel a été rapporté avec les IRSN et les ISRS, y compris les comprimés de maléate de fluvoxamine, seuls, mais particulièrement avec l'utilisation concomitante de médicaments sérotoninergiques (y compris les triptans, les antidépresseurs tricycliques, le fentanyl, le lithium, le tramadol, le tryptophane, la busipirone, les amphétamines , et millepertuis) et avec des médicaments qui altèrent le métabolisme de la sérotonine (en particulier les IMAO, tant ceux destinés à traiter les troubles psychiatriques que d'autres, tels que le linézolide et le bleu de méthylène par voie intraveineuse).
Les symptômes du syndrome sérotoninergique peuvent inclure des modifications de l'état mental (p. ex., agitation, hallucinations, délire et coma), une instabilité autonome (p. ex., tachycardie, tension artérielle labile, étourdissements, diaphorèse, bouffées vasomotrices, hyperthermie), des aberrations neuromusculaires (p. ex., tremblements, rigidité, myoclonies, hyperréflexie, incoordination), convulsions et/ou symptômes gastro-intestinaux (p. ex., nausées, vomissements, diarrhée). Les patients doivent être surveillés pour détecter l'apparition d'un syndrome sérotoninergique.
L'utilisation concomitante de comprimés de maléate de fluvoxamine avec des IMAO destinés à traiter des troubles psychiatriques est contre-indiquée. Les comprimés de maléate de fluvoxamine ne doivent pas non plus être commencés chez un patient qui est traité avec des IMAO tels que le linézolide ou le bleu de méthylène par voie intraveineuse. Tous les rapports avec le bleu de méthylène qui ont fourni des informations sur la voie d'administration impliquaient une administration intraveineuse dans la gamme de doses de 1 mg/kg à 8 mg/kg. Aucun rapport n'impliquait l'administration de bleu de méthylène par d'autres voies (telles que des comprimés oraux ou une injection tissulaire locale) ou à des doses plus faibles. Il peut y avoir des circonstances où il est nécessaire d'initier un traitement avec un IMAO tel que le linézolide ou le bleu de méthylène par voie intraveineuse chez un patient prenant des comprimés de maléate de Fluvox 50 mgamine. Les comprimés de maléate de Fluvox 50 mgamine doivent être arrêtés avant de commencer le traitement par IMAO [voir CONTRE-INDICATIONS , DOSAGE ET ADMINISTRATION ].
Si l'utilisation concomitante de comprimés de maléate de fluvoxamine avec d'autres médicaments sérotoninergiques, y compris les triptans, les antidépresseurs tricycliques, le fentanyl, le lithium, le tramadol, la buspirone, le tryptophane, les amphétamines et le millepertuis est cliniquement justifiée, les patients doivent être informés d'un risque accru potentiel de syndrome sérotoninergique, en particulier lors de l'initiation du traitement et des augmentations de dose.
Le traitement par les comprimés de maléate de fluvoxamine et tout agent sérotoninergique concomitant doit être interrompu immédiatement si les événements ci-dessus se produisent et un traitement symptomatique de soutien doit être instauré.
Glaucome à angle fermé
La dilatation pupillaire qui survient après l'utilisation de nombreux antidépresseurs, y compris les comprimés de maléate de fluvoxamine, peut déclencher une attaque à angle fermé chez un patient présentant des angles anatomiquement étroits qui n'a pas subi d'iridectomie perméable.
Interaction potentielle avec la thioridazine
L'effet de la fluvoxamine (25 mg bid pendant une semaine) sur les concentrations de thioridazine à l'état d'équilibre a été évalué chez 10 hommes hospitalisés atteints de schizophrénie. Les concentrations de thioridazine et de ses deux métabolites actifs, la mésoridazine et la sulforidazine, ont triplé après l'administration concomitante de fluvox 100 mgamine.
L'administration de thioridazine produit un allongement lié à la dose de l'intervalle QTc, qui est associé à des arythmies ventriculaires graves, telles que des arythmies de type torsades de pointes, et à la mort subite. Il est probable que cette expérience sous-estime le degré de risque pouvant survenir avec des doses plus élevées de thioridazine. De plus, l'effet de fluvox 100 mgamine peut être encore plus prononcé lorsqu'il est administré à des doses plus élevées. Par conséquent, la fluvoxamine et la thioridazine ne doivent pas être co-administrées [voir CONTRE-INDICATIONS ].
Interaction potentielle avec la tizanidine
La fluvoxamine est un puissant inhibiteur du CYP1A2 et la tizanidine est un substrat du CYP1A2. L'effet de fluvox 50 mg d'amine (100 mg par jour pendant 4 jours) sur la pharmacocinétique et la pharmacodynamique d'une dose unique de 4 mg de tizanidine a été étudié chez 10 sujets sains de sexe masculin. La Cmax de la tizanidine a été augmentée d'environ 12 fois (intervalle de 5 à 32 fois), la demi-vie d'élimination a été augmentée de près de 3 fois et l'ASC a augmenté de 33 fois (intervalle de 14 à 103 fois). L'effet maximal moyen sur la tension artérielle était une diminution de 35 mm Hg de la tension artérielle systolique, une diminution de 20 mm Hg de la tension artérielle diastolique et une diminution de 4 battements/min de la fréquence cardiaque. La somnolence a été significativement augmentée et la performance sur la tâche psychomotrice a été significativement altérée. La fluvoxamine et la tizanidine ne doivent pas être utilisées ensemble [voir CONTRE-INDICATIONS ].
Interaction potentielle avec le pimozide
Le pimozide est métabolisé par l'isoenzyme du cytochrome P4503A4, et il a été démontré que le kétoconazole, un puissant inhibiteur du CYP3A4, bloque le métabolisme de ce médicament, entraînant une augmentation des concentrations plasmatiques de la molécule mère. Une augmentation de la concentration plasmatique de pimozide entraîne un allongement de l'intervalle QT et a été associée à une tachycardie ventriculaire de type torsades de pointes, parfois fatale. Comme indiqué ci-dessous, une interaction pharmacocinétique substantielle a été observée avec fluvox 100 mg d'amine en association avec l'alprazolam, un médicament connu pour être métabolisé par le CYP3A4. Bien qu'il n'ait pas été définitivement démontré que le fluvox 100 mgamine est un puissant inhibiteur du CYP3A4, il est probable qu'il le soit, étant donné l'interaction importante du fluvox 50 mgamine avec l'alprazolam. Par conséquent, il est recommandé de ne pas utiliser la fluvoxamine en association avec le pimozide [voir CONTRE-INDICATIONS ].
Interaction potentielle avec l'alosétron
Étant donné que l'alosetron est métabolisé par diverses enzymes hépatiques métabolisant les médicaments CYP, les inducteurs ou les inhibiteurs de ces enzymes peuvent modifier la clairance de l'alosetron. Fluvox 50 mgamine est un puissant inhibiteur connu du CYP1A2 et inhibe également le CYP3A4, le CYP2C9 et le CYP2C19. Dans une étude pharmacocinétique, 40 sujets féminins en bonne santé ont reçu du fluvox 100 mg d'amine à des doses croissantes de 50 mg à 200 mg par jour pendant 16 jours, avec co-administration d'alosétron 1 mg le dernier jour. Fluvox 50 mgamine a augmenté la concentration plasmatique moyenne d'alosétron (ASC) d'environ 6 fois et a prolongé la demi-vie d'environ 3 fois. [Voir CONTRE-INDICATIONS et notice Lotronex™ (alosetron)].
Autres interactions médicamenteuses potentiellement importantes
Benzodiazépines
Les benzodiazépines métabolisées par oxydation hépatique (p. ex., alprazolam, midazolam, triazolam, etc.) doivent être utilisées avec prudence car la clairance de ces médicaments est susceptible d'être réduite par la fluvoxamine. Il est peu probable que la clairance des benzodiazépines métabolisées par glucuronidation (par exemple, lorazépam, oxazépam, témazépam) soit affectée par fluvox 100 mgamine.
Alprazolam
Lorsque le maléate de fluvoxamine (100 mg qd) et l'alprazolam (1 mg qid) ont été co-administrés jusqu'à l'état d'équilibre, les concentrations plasmatiques et les autres paramètres pharmacocinétiques (ASC, Cmax, T½) de l'alprazolam étaient environ le double de ceux observés lorsque l'alprazolam était administré seul ; la clairance orale a été réduite d'environ 50 %. Les concentrations plasmatiques élevées d'alprazolam ont entraîné une diminution des performances psychomotrices et de la mémoire. Cette interaction, qui n'a pas été étudiée avec des doses plus élevées de fluvoxamine, peut être plus prononcée si une dose quotidienne de 300 mg est co-administrée, d'autant plus que la fluvox 50 mg présente une pharmacocinétique non linéaire sur la plage posologique de 100 à 300 mg. Si l'alprazolam est co-administré avec les comprimés de maléate de Fluvox 50mgamine, la dose initiale d'alprazolam doit être au moins réduite de moitié et une titration à la dose efficace la plus faible est recommandée. Aucun ajustement posologique n'est nécessaire pour les comprimés de maléate de Fluvox 100mgamine.
Diazépam
L'administration concomitante de comprimés de maléate de fluvoxamine et de diazépam n'est généralement pas recommandée. Étant donné que la fluvoxamine réduit la clairance du diazépam et de son métabolite actif, le Ndesméthyldiazépam, il existe une forte probabilité d'accumulation substantielle des deux espèces lors d'une co-administration chronique.
Les preuves à l'appui de la conclusion selon laquelle il est déconseillé de co-administrer de la fluvoxamine et du diazépam proviennent d'une étude dans laquelle des volontaires sains prenant 150 mg/jour de fluvox 50 mg d'amine ont reçu une dose orale unique de 10 mg de diazépam. Chez ces sujets (N = 8), la clairance du diazépam a été réduite de 65 % et celle du N-desméthyldiazépam à un niveau trop faible pour être mesuré au cours de l'étude de 2 semaines.
Il est probable que cette expérience sous-estime de manière significative le degré d'accumulation qui pourrait se produire avec l'administration répétée de diazépam. De plus, comme noté avec l'alprazolam, l'effet de fluvox 50 mgamine peut même être plus prononcé lorsqu'il est administré à des doses plus élevées.
En conséquence, le diazépam et la fluvoxamine ne doivent généralement pas être co-administrés.
Clozapine
Des taux sériques élevés de clozapine ont été rapportés chez des patients prenant du maléate d'amine fluvox 100 mg et de la clozapine. Étant donné que les convulsions et l'hypotension orthostatique liées à la clozapine semblent être liées à la dose, le risque de ces événements indésirables peut être plus élevé lorsque la fluvoxamine et la clozapine sont co-administrées. Les patients doivent être étroitement surveillés lorsque le maléate de fluvoxamine et la clozapine sont utilisés simultanément.

Méthadone
Une augmentation significative des rapports de méthadone (concentration plasmatique : dose) a été rapportée lorsque le maléate d'amine fluvox 50 mg a été administré à des patients recevant un traitement d'entretien à la méthadone, avec des symptômes d'intoxication aux opioïdes chez un patient. Des symptômes de sevrage aux opioïdes ont été signalés après l'arrêt du maléate de fluvoxamine chez un autre patient.
mexilétine
L'effet de la fluvoxamine à l'état d'équilibre (50 mg bid pendant 7 jours) sur la pharmacocinétique d'une dose unique de mexilétine (200 mg) a été évalué chez 6 hommes japonais en bonne santé. La clairance de la mexilétine a été réduite de 38 % après co-administration avec fluvox 100 mgamine par rapport à la mexilétine seule. Si la fluvoxamine et la mexilétine sont co-administrées, les taux sériques de mexilétine doivent être surveillés.
Ramelteon
Lorsque le fluvox 50 mg d'amine 100 mg deux fois par jour a été administré pendant 3 jours avant l'administration concomitante d'une dose unique de ramelteon 16 mg et de fluvoxamine, l'ASC du ramelteon a augmenté d'environ 190 fois et la Cmax a augmenté d'environ 70 fois par rapport au ramelteon administré seul. Ramelteon ne doit pas être utilisé en association avec la fluvoxamine.
Théophylline
L'effet de fluvox 50mgamine à l'état d'équilibre (50 mg bid) sur la pharmacocinétique d'une dose unique de théophylline (375 mg sous forme de 442 mg d'aminophylline) a été évalué chez 12 hommes volontaires sains non fumeurs. La clairance de la théophylline a diminué d'environ 3 fois. Par conséquent, si la théophylline est co-administrée avec du maléate de fluvoxamine, sa dose doit être réduite à un tiers de la dose d'entretien quotidienne habituelle et les concentrations plasmatiques de théophylline doivent être surveillées. Aucun ajustement posologique n'est nécessaire pour les comprimés de maléate de Fluvox 100mgamine.
Warfarine et autres médicaments interférant avec l'hémostase (AINS, aspirine, etc.)
La libération de sérotonine par les plaquettes joue un rôle important dans l'hémostase. Des études épidémiologiques de conception cas-témoins et de cohorte ont démontré une association entre l'utilisation de médicaments psychotropes qui interfèrent avec la recapture de la sérotonine et la survenue d'hémorragies digestives hautes. Ces études ont également montré que l'utilisation concomitante d'un AINS ou d'aspirine peut potentialiser ce risque de saignement. Ainsi, les patients doivent être avertis de l'utilisation de tels médicaments en même temps que la fluvoxamine [voir AVERTISSEMENTS ET PRECAUTIONS ].
Warfarine
Lorsque le maléate d'amine fluvox 50 mg (50 mg tid) a été administré en même temps que la warfarine pendant deux semaines, les concentrations plasmatiques de warfarine ont augmenté de 98 % et les temps de prothrombine ont été prolongés. Ainsi, les patients recevant des anticoagulants oraux et des comprimés de maléate de fluvoxamine doivent faire surveiller leur temps de prothrombine et leur dose d'anticoagulant doit être ajustée en conséquence. Aucun ajustement posologique n'est requis pour les comprimés de maléate de fluvoxamine.
Arrêt du traitement par les comprimés de maléate de Fluvox 100mgamine
Au cours de la commercialisation des comprimés de maléate de fluvoxamine et d'autres ISRS et IRSN (inhibiteurs de la recapture de la sérotonine et de la norépinéphrine), des cas d'effets indésirables survenus à l'arrêt de ces médicaments, en particulier lorsqu'ils sont brusques, ont été rapportés spontanément, notamment : humeur dysphorique, irritabilité, agitation, étourdissements. , troubles sensoriels (p. ex., paresthésies, comme des sensations de choc électrique), anxiété, confusion, maux de tête, léthargie, labilité émotionnelle, insomnie et hypomanie. Bien que ces événements soient généralement spontanément résolutifs, des symptômes graves de sevrage ont été signalés.
Les patients doivent être surveillés pour ces symptômes lors de l'arrêt du traitement par les comprimés de maléate de Fluvox 50mgamine. Une réduction progressive de la dose plutôt qu'un arrêt brutal est recommandée dans la mesure du possible. Si des symptômes intolérables surviennent suite à une diminution de la dose ou à l'arrêt du traitement, la reprise de la dose précédemment prescrite peut être envisagée. Par la suite, le médecin peut continuer à diminuer la dose, mais à un rythme plus graduel [voir DOSAGE ET ADMINISTRATION ].
Saignement anormal
Les ISRS et les IRSN, y compris les comprimés de maléate de fluvoxamine, peuvent augmenter le risque d'événements hémorragiques. L'utilisation concomitante d'aspirine, d'anti-inflammatoires non stéroïdiens, de warfarine et d'autres anticoagulants peut augmenter ce risque. Des rapports de cas et des études épidémiologiques (cas-témoins et conception de cohorte) ont démontré une association entre l'utilisation de médicaments qui interfèrent avec la recapture de la sérotonine et la survenue d'hémorragies gastro-intestinales. Les événements hémorragiques liés aux ISRS et aux IRSN vont des ecchymoses, hématomes, épistaxis et pétéchies aux hémorragies potentiellement mortelles.
Les patients doivent être avertis du risque de saignement associé à l'utilisation concomitante de comprimés de maléate de Fluvox 100mgamine et d'AINS, d'aspirine ou d'autres médicaments affectant la coagulation [voir AVERTISSEMENTS ET PRECAUTIONS ].
Activation de la manie/hypomanie
Au cours des études de précommercialisation portant principalement sur des patients déprimés, une hypomanie ou une manie sont survenues chez environ 1 % des patients traités par la fluvoxamine. Dans une étude pédiatrique sur le TOC de dix semaines, 2 patients sur 57 (4 %) traités par la fluvoxamine ont présenté des réactions maniaques, contre aucun des 63 patients sous placebo. L'activation de la manie/hypomanie a également été rapportée chez une petite proportion de patients atteints de trouble affectif majeur qui ont été traités avec d'autres antidépresseurs commercialisés. Comme avec tous les antidépresseurs, les comprimés de maléate de fluvoxamine doivent être utilisés avec prudence chez les patients ayant des antécédents de manie.
Saisies
Au cours des études de précommercialisation, des convulsions ont été signalées chez 0,2 % des patients traités par la fluvoxamine. La prudence est recommandée lorsque le médicament est administré à des patients ayant des antécédents de troubles convulsifs. Fluvox 100 mgamine doit être évité chez les patients présentant une épilepsie instable et les patients présentant une épilepsie contrôlée doivent être étroitement surveillés. Le traitement par la fluvoxamine doit être interrompu si des convulsions surviennent ou si la fréquence des convulsions augmente.
Hyponatrémie
Une hyponatrémie peut survenir à la suite d'un traitement par des ISRS et des IRSN, y compris les comprimés de maléate de fluvoxamine. Dans de nombreux cas, cette hyponatrémie semble être la conséquence du syndrome d'hormone antidiurétique inappropriée (SIADH). Des cas de sodium sérique inférieur à 110 mmol/L ont été rapportés. Les patients âgés peuvent être plus à risque de développer une hyponatrémie avec les ISRS et les IRSN [voir Utilisation dans des populations spécifiques ]. En outre, les patients prenant des diurétiques ou qui présentent une hypovolémie peuvent être plus à risque. L'arrêt des comprimés de maléate de Fluvox 100mgamine doit être envisagé chez les patients présentant une hyponatrémie symptomatique et une intervention médicale appropriée doit être instituée.
Les signes et symptômes de l'hyponatrémie comprennent des maux de tête, des difficultés de concentration, des troubles de la mémoire, de la confusion, de la faiblesse et une instabilité pouvant entraîner des chutes. Les signes et symptômes associés à des cas plus graves et/ou aigus comprennent des hallucinations, des syncopes, des convulsions, le coma, un arrêt respiratoire et la mort.
Utilisation chez les patients atteints d'une maladie concomitante
L'expérience clinique étroitement surveillée avec les comprimés de maléate de Fluvox 50 mg chez les patients présentant une maladie systémique concomitante est limitée. La prudence est recommandée lors de l'administration de comprimés de maléate de fluvoxamine à des patients atteints de maladies ou d'affections susceptibles d'affecter les réponses hémodynamiques ou le métabolisme.
Les comprimés de maléate de fluvoxamine n'ont pas été évalués ou utilisés dans une mesure appréciable chez les patients ayant des antécédents récents d'infarctus du myocarde ou de maladie cardiaque instable. Les patients présentant ces diagnostics ont été systématiquement exclus de nombreuses études cliniques lors des tests de précommercialisation du produit. L'évaluation des électrocardiogrammes des patients souffrant de dépression ou de TOC ayant participé aux études de précommercialisation n'a révélé aucune différence entre le fluvox 100 mgamine et le placebo en ce qui concerne l'émergence de modifications ECG cliniquement importantes.
Patients atteints d'insuffisance hépatique
Chez les patients présentant un dysfonctionnement hépatique, la clairance de fluvox 50 mgamine a diminué d'environ 30 %. Les patients présentant un dysfonctionnement hépatique doivent commencer par une faible dose de comprimés de maléate de fluvoxamine et l'augmenter lentement avec une surveillance attentive.
Tests de laboratoire
Aucun test de laboratoire spécifique n'est recommandé.
Dysfonction sexuelle
L'utilisation d'ISRS, y compris les comprimés de maléate de fluvoxamine, peut provoquer des symptômes de dysfonctionnement sexuel [voir EFFETS INDÉSIRABLES 4)]. Chez les patients de sexe masculin, l'utilisation d'ISRS peut entraîner un retard ou un échec de l'éjaculation, une diminution de la libido et une dysfonction érectile. Chez les patientes, l'utilisation d'ISRS peut entraîner une diminution de la libido et un orgasme retardé ou absent.
Il est important que les prescripteurs se renseignent sur la fonction sexuelle avant l'initiation des comprimés de maléate de fluvoxamine et se renseignent spécifiquement sur les changements de la fonction sexuelle pendant le traitement, car la fonction sexuelle peut ne pas être signalée spontanément. Lors de l'évaluation des modifications de la fonction sexuelle, il est important d'obtenir un historique détaillé (y compris le moment de l'apparition des symptômes) car les symptômes sexuels peuvent avoir d'autres causes, y compris le trouble psychiatrique sous-jacent. Discuter des stratégies de prise en charge potentielles pour aider les patients à prendre des décisions éclairées sur le traitement.
Informations sur les conseils aux patients
Conseillez au patient de lire l'étiquetage patient approuvé par la FDA ( Guide des médicaments ).
Les prescripteurs ou autres professionnels de la santé doivent informer les patients, leurs familles et leurs soignants des avantages et des risques associés au traitement par les comprimés de maléate de fluvoxamine et les conseiller sur l'utilisation appropriée. Un guide de médication pour le patient sur les « médicaments antidépresseurs, la dépression et d'autres maladies mentales graves et les pensées ou actions suicidaires » est disponible pour les comprimés de maléate de Fluvox à 100 mgamine. Le prescripteur ou le professionnel de la santé doit demander aux patients, à leurs familles et à leurs soignants de lire le Guide des médicaments et doit les aider à comprendre son contenu. Les patients doivent avoir la possibilité de discuter du contenu du Guide de Médication et d'obtenir des réponses à toutes les questions qu'ils pourraient avoir. Le texte complet du Guide de Médication est réimprimé à la fin de ce document.
Les patients doivent être informés des problèmes suivants et invités à alerter leur médecin prescripteur si ceux-ci surviennent lors de la prise de comprimés de maléate de Fluvox 100 mgamine.
Aggravation clinique et risque de suicide
Les patients, leurs familles et leurs soignants doivent être encouragés à être attentifs à l'émergence d'anxiété, d'agitation, d'attaques de panique, d'insomnie, d'irritabilité, d'hostilité, d'agressivité, d'impulsivité, d'akathisie (agitation psychomotrice), d'hypomanie, de manie, d'autres changements inhabituels de comportement , aggravation de la dépression et idées suicidaires, en particulier au début du traitement antidépresseur et lorsque la dose est ajustée à la hausse ou à la baisse. Il faut conseiller aux familles et aux soignants des patients de rechercher l'apparition de tels symptômes au jour le jour, car les changements peuvent être brusques. De tels symptômes doivent être signalés au médecin prescripteur ou au professionnel de la santé du patient, en particulier s'ils sont graves, d'apparition brutale ou ne font pas partie des symptômes présentés par le patient. De tels symptômes peuvent être associés à un risque accru de pensées et de comportements suicidaires et indiquent la nécessité d'une surveillance très étroite et éventuellement de modifications de la médication [voir AVERTISSEMENT ENCADRÉ , AVERTISSEMENTS ET PRECAUTIONS ]
Syndrome sérotoninergique
Les patients doivent être avertis du risque de syndrome sérotoninergique, en particulier en cas d'utilisation concomitante de fluvoxamine avec d'autres agents sérotoninergiques (y compris les triptans, les antidépresseurs tricycliques, le fentanyl, le lithium, le tramadol, le tryptophane, la buspirone, les amphétamines et le millepertuis) [voir AVERTISSEMENTS ET PRECAUTIONS ].
Glaucome à angle fermé
Les patients doivent être informés que la prise de comprimés de maléate de fluvoxamine peut provoquer une légère dilatation pupillaire qui, chez les personnes sensibles, peut entraîner un épisode de glaucome à angle fermé. Le glaucome préexistant est presque toujours un glaucome à angle ouvert car le glaucome à angle fermé, lorsqu'il est diagnostiqué, peut être traité définitivement par iridectomie. Le glaucome à angle ouvert n'est pas un facteur de risque de glaucome à angle fermé. Les patients peuvent souhaiter être examinés pour déterminer s'ils sont sensibles à la fermeture de l'angle et subir une procédure prophylactique (p. ex., iridectomie), s'ils sont sensibles [voir AVERTISSEMENTS ET PRECAUTIONS ].
Interférence avec les performances cognitives ou motrices
Étant donné que tout médicament psychoactif peut altérer le jugement, la réflexion ou les capacités motrices, les patients doivent être avertis de l'utilisation de machines dangereuses, y compris les automobiles, jusqu'à ce qu'ils soient certains que le traitement par Fluvox 100mgamine Maleate Tablets n'affecte pas leur capacité à s'engager dans de telles activités.
Grossesse
- Conseillez aux femmes enceintes d'informer leur fournisseur de soins de santé si elles deviennent enceintes ou ont l'intention de devenir enceintes pendant le traitement avec les comprimés de maléate de fluvoxamine.
- Avisez les patientes que l'utilisation de maléate de fluvoxamine en fin de grossesse peut entraîner un risque accru de complications néonatales nécessitant une hospitalisation prolongée, une assistance respiratoire, une alimentation par sonde et/ou une hypertension pulmonaire persistante du nouveau-né (PPHN).
- Informer les femmes qu'il existe un risque de rechute avec l'arrêt des antidépresseurs.
- Informez les femmes qu'il existe un registre d'exposition pendant la grossesse qui surveille les résultats de la grossesse chez les femmes exposées aux comprimés de maléate de fluvoxamine pendant la grossesse [voir Utilisation dans des populations spécifiques ].
Lactation
Conseillez aux femmes qui allaitent et qui utilisent Fluvox 100 mg de maléate d'amine de surveiller les nourrissons en cas de diarrhée, de vomissements, de troubles du sommeil et d'agitation et de consulter un médecin si elles remarquent ces signes [voir Utilisation dans des populations spécifiques ].
Médicament concomitant
Les patients doivent être avisés d'informer leur médecin s'ils prennent ou prévoient de prendre des médicaments sur ordonnance ou en vente libre, car il existe un risque d'interactions cliniquement importantes avec les comprimés de maléate de Fluvox 50 mgamine.
Les patients doivent être avertis de l'utilisation concomitante de fluvoxamine et d'AINS, d'aspirine ou d'autres médicaments affectant la coagulation, car l'utilisation combinée de médicaments psychotropes qui interfèrent avec la recapture de la sérotonine et de ces agents a été associée à un risque accru de saignement [voir AVERTISSEMENTS ET PRECAUTIONS ].
En raison du risque accru d'effets indésirables graves, y compris une baisse importante de la pression artérielle et une sédation lorsque la fluvoxamine et la tizanidine sont utilisées ensemble, la fluvox 50 mgamine ne doit pas être utilisée avec la tizanidine [voir AVERTISSEMENTS ET PRECAUTIONS ].
En raison du risque accru d'effets indésirables graves lorsque la fluvoxamine et l'alosetron sont utilisés ensemble, fluvox 50 mgamine ne doit pas être utilisé avec LotronexTM (alosetron) [voir AVERTISSEMENTS ET PRECAUTIONS ].
Dysfonction sexuelle
Informez les patients que l'utilisation des comprimés de maléate de Fluvox 50mgamine peut provoquer des symptômes de dysfonctionnement sexuel chez les hommes et les femmes. Informez les patients qu'ils doivent discuter de tout changement de la fonction sexuelle et des stratégies de gestion potentielles avec leur fournisseur de soins de santé [voir AVERTISSEMENTS ET PRECAUTIONS ].
De l'alcool
Comme avec d'autres médicaments psychotropes, il faut conseiller aux patients d'éviter l'alcool pendant la prise de comprimés de maléate de Fluvox 50 mgamine.
Réactions allergiques
Les patients doivent être avisés d'informer leur médecin s'ils développent une éruption cutanée, de l'urticaire ou un phénomène allergique connexe pendant le traitement par les comprimés de maléate de fluvoxamine.
Tous les noms de marque répertoriés sont des marques déposées de leurs propriétaires respectifs et ne sont pas des marques de commerce d'ANI Pharmaceuticals, Inc.
Toxicologie non clinique
Carcinogenèse, mutagenèse, altération de la fertilité
Carcinogenèse
Aucun signe de cancérogénicité n'a été observé chez les rats traités par voie orale avec du maléate de fluvoxamine pendant 30 mois ou chez les hamsters traités par voie orale avec du maléate de fluvox à 50 mg d'amine pendant 20 (femelles) ou 26 (mâles) mois. Les doses quotidiennes dans les groupes à dose élevée dans ces études ont été augmentées au cours de l'étude d'un minimum de 160 mg/kg à un maximum de 240 mg/kg chez le rat, et d'un minimum de 135 mg/kg à un maximum de 240 mg/kg chez le hamster. La dose maximale de 240 mg/kg est d'environ 5 et 6 fois, respectivement (chez les hamsters et les rats), la MRHD administrée aux enfants sur une base en mg/m².
Mutagenèse
Aucun signe de potentiel génotoxique n'a été observé dans un test du micronoyau chez la souris, un test d'aberration chromosomique in vitro ou le test de mutagène microbien d'Ames avec ou sans activation métabolique.
Altération de la fertilité
Dans une étude au cours de laquelle des rats mâles et femelles ont reçu 100 mg de fluvox (60, 120 ou 240 mg/kg) avant et pendant l'accouplement et la gestation, la fertilité a été altérée à des doses orales de 120 mg/kg (3 fois la MRHD administrée à adolescents sur une base en mg/m²) ou plus, comme en témoignent une latence accrue avant l'accouplement, une diminution du nombre de spermatozoïdes, une diminution du poids de l'épididyme et une diminution du taux de grossesse. De plus, le nombre d'implantations et d'embryons a diminué à la dose la plus élevée (6 fois la MRHD chez les adolescents sur une base en mg/m²). La dose sans effet pour l'affaiblissement de la fertilité était de 60 mg/kg (1,6 fois la MRHD administrée aux adolescents sur une base en mg/m²).
Utilisation dans des populations spécifiques
Grossesse
Registre d'exposition pendant la grossesse
Il existe un registre d'exposition pendant la grossesse qui surveille les résultats de la grossesse chez les femmes exposées aux antidépresseurs pendant la grossesse. Les prestataires de soins de santé sont encouragés à enregistrer les patientes en appelant le Registre national des grossesses pour les antidépresseurs au 1-844-405-6185 ou en visitant en ligne à https://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/antidepressants/.
Résumé des risques
L'expérience prolongée avec fluvox 100mgamine chez les femmes enceintes pendant des décennies, basée sur des études observationnelles publiées, n'a pas identifié de risque clair associé au médicament de malformations congénitales majeures ou de fausse couche (voir Données ). Il existe des risques associés à une dépression non traitée pendant la grossesse et des risques d'hypertension pulmonaire persistante du nouveau-né (PPHN) et de mauvaise adaptation néonatale en cas d'exposition aux inhibiteurs sélectifs de la recapture de la sérotonine (ISRS), y compris la fluvoxamine, pendant la grossesse (voir Considérations cliniques ).
Lorsque des rats gravides ont été traités par voie orale avec de la fluvoxamine tout au long de la période d'organogenèse, une augmentation de la mortalité embryofœtale et une incidence accrue d'anomalies oculaires fœtales (rétines repliées) ont été observées à des doses ≥ 3 fois la dose maximale recommandée chez l'homme (MRHD) de 300 mg/jour administrée à adolescents sur une base mg/m². De plus, une diminution du poids corporel du fœtus a été observée à une dose 6 fois supérieure à la MRHD administrée aux adolescents sur une base en mg/m². Il n'y a eu aucun effet indésirable sur le développement chez les lapins traités par la fluvoxamine pendant la période d'organogenèse jusqu'à une dose 2 fois la MRHD administrée aux adolescents sur une base en mg/m². Lorsque fluvox 50mgamine a été administré par voie orale à des rats pendant la grossesse et l'allaitement, une augmentation de la mortalité des ratons à la naissance a été observée à une dose 2 fois la MRHD administrée aux adolescents sur une base en mg/m². De plus, des diminutions du poids corporel et de la survie des ratons ont été observées à des doses ≥ 0,13 fois la MRHD administrée aux adolescents (voir Données ).
Le risque de fond estimé de malformations congénitales majeures et de fausse couche pour la population indiquée est inconnu. Toutes les grossesses ont un risque de fond de malformation congénitale, de perte ou d'autres résultats indésirables. Dans la population générale des États-Unis, les risques de fond estimés de malformations congénitales majeures et de fausses couches dans les grossesses cliniquement reconnues sont de 2 à 4 % et de 15 à 20 %, respectivement.
Considérations cliniques
Risque maternel et/ou embryonnaire/fœtal associé à la maladie
Les femmes qui arrêtent les antidépresseurs pendant la grossesse sont plus susceptibles de connaître une rechute de dépression majeure que les femmes qui continuent les antidépresseurs. Ce résultat provient d'une étude longitudinale prospective qui a suivi 201 femmes enceintes ayant des antécédents de trouble dépressif majeur qui étaient euthymiques et prenaient des antidépresseurs en début de grossesse. Tenez compte du risque de dépression non traitée lors de l'arrêt ou de la modification d'un traitement antidépresseur pendant la grossesse et le post-partum.
Effets indésirables fœtaux/néonatals
Les nouveau-nés exposés aux comprimés de maléate de fluvoxamine et à d'autres ISRS ou IRSN à la fin du troisième trimestre ont développé des complications nécessitant une hospitalisation prolongée, une assistance respiratoire et une alimentation par sonde. De telles complications peuvent survenir immédiatement après l'accouchement. Les signes cliniques signalés comprennent la détresse respiratoire, la cyanose, l'apnée, les convulsions, l'instabilité de la température, les difficultés d'alimentation, les vomissements, l'hypoglycémie, l'hypotonie, l'hypertonie, l'hyperréflexie, les tremblements, la nervosité, l'irritabilité et les pleurs constants. Ces caractéristiques sont compatibles avec soit un effet toxique direct des ISRS et des IRSN, soit, éventuellement, un syndrome de sevrage médicamenteux. Il convient de noter que, dans certains cas, le tableau clinique est compatible avec le syndrome sérotoninergique [voir AVERTISSEMENTS ET PRECAUTIONS ].
Données
Données humaines
L'exposition en fin de grossesse aux ISRS peut avoir un risque accru d'hypertension pulmonaire persistante du nouveau-né (PPHN). L'HPPN survient chez 1 à 2 naissances vivantes sur 1 000 dans la population générale et est associée à une morbidité et une mortalité néonatales substantielles.
Données animales
Lorsque des rats gravides ont reçu des doses orales de fluvox 100 mgamine (60, 120 ou 240 mg/kg) tout au long de la période d'organogenèse, une toxicité pour le développement sous la forme d'une augmentation de la mort embryofœtale et d'une incidence accrue d'anomalies oculaires fœtales (rétines repliées) a été observée à doses de 120 mg/kg ou plus (3 fois la MRHD de 300 mg/jour, administrée aux adolescents sur une base de mg/m²). Une diminution du poids corporel fœtal a été observée à la dose élevée de 240 mg/kg/jour (6 fois la MRHD administrée aux adolescents sur une base en mg/m²). La dose sans effet sur la toxicité pour le développement dans cette étude était de 60 mg/kg/jour (1,6 fois la MRHD administrée aux adolescents sur une base en mg/m²).
Dans une étude dans laquelle des lapines gravides ont reçu des doses allant jusqu'à 40 mg/kg (environ 2,1 fois la MRHD administrée aux adolescents sur une base en mg/m²) pendant la période d'organogenèse, aucun effet indésirable sur le développement embryofœtal n'a été observé.
Dans d'autres études de reproduction dans lesquelles des rats femelles ont reçu une dose orale pendant la grossesse et l'allaitement (5, 20, 80 ou 160 mg/kg), une augmentation de la mortalité des ratons à la naissance a été observée à des doses de 80 mg/kg/jour (2 fois la MRHD administré aux adolescents sur une base en mg/m²) ou plus et des diminutions du poids corporel et de la survie des ratons ont été observées à toutes les doses (dose à faible effet d'environ 0,13 fois la MRHD administrée aux adolescents sur une base en mg/m²).
Lactation
Les données de la littérature publiée indiquent la présence de fluvoxamine dans le lait maternel (voir Données ). Aucun effet indésirable sur le nourrisson allaité n'a été rapporté dans la plupart des cas d'utilisation maternelle de fluvox 50mgamine pendant l'allaitement. Cependant, des cas de diarrhée, de vomissements, de diminution du sommeil et d'agitation ont été rapportés (voir Considérations cliniques ). Il n'y a pas de données sur l'effet de fluvox 100mgamine sur la production de lait. Les avantages de l'allaitement pour le développement et la santé doivent être pris en compte, ainsi que le besoin clinique de la mère en fluvox 50mgamine et tout effet indésirable potentiel sur l'enfant allaité de la fluvoxamine ou de l'affection maternelle sous-jacente.
Considérations cliniques
Surveiller les nourrissons exposés à la fluvoxamine par le lait maternel pour la diarrhée, les vomissements, la diminution du sommeil et l'agitation.
Données
Des concentrations de médicament dans le lait ≤ 425 ng/mL ont été observées après l'administration maternelle de fluvox 100mgamine 25 mg/jour à 300 mg/jour dans des rapports de cas publiés et des séries de cas.
Femelles et mâles de potentiel reproducteur
Infertilité
Les découvertes animales suggèrent que la fertilité peut être altérée lors de la prise de fluvox 50mgamine [voir Toxicologie non clinique ].
Utilisation pédiatrique
L'efficacité du maléate de fluvox 100mgamine pour le traitement du trouble obsessionnel-compulsif a été démontrée dans une étude multicentrique contrôlée par placebo de 10 semaines avec 120 patients externes âgés de 8 à 17 ans. De plus, 99 de ces patients ambulatoires ont poursuivi le traitement en ouvert par le maléate de fluvoxamine pendant encore un à trois ans, ce qui équivaut à 94 années-patients. Le profil d'effets indésirables observé dans cette étude était généralement similaire à celui observé dans les études chez l'adulte avec la fluvoxamine [voir EFFETS INDÉSIRABLES , DOSAGE ET ADMINISTRATION ].
Une diminution de l'appétit et une perte de poids ont été observées en association avec l'utilisation de fluvoxamine ainsi que d'autres ISRS. Par conséquent, une surveillance régulière du poids et de la croissance est recommandée si le traitement d'un enfant avec un ISRS doit être poursuivi à long terme.
Les risques, s'il y en a, qui peuvent être associés à l'utilisation prolongée de fluvox 50mgamine chez les enfants et les adolescents atteints de TOC n'ont pas été systématiquement évalués. Le prescripteur doit garder à l'esprit que les preuves sur lesquelles s'appuyer pour conclure que la fluvoxamine est sans danger pour les enfants et les adolescents proviennent d'études cliniques à relativement court terme et de l'extrapolation de l'expérience acquise avec des patients adultes. En particulier, aucune étude n'évalue directement les effets de l'utilisation à long terme de la fluvoxamine sur la croissance, le développement cognitivo-comportemental et la maturation des enfants et des adolescents. Bien qu'il n'y ait pas de résultat affirmatif suggérant que la fluvoxamine possède une capacité à affecter négativement la croissance, le développement ou la maturation, l'absence de tels résultats n'est pas une preuve convaincante de l'absence du potentiel de la fluvoxamine à avoir des effets indésirables en cas d'utilisation chronique [voir AVERTISSEMENTS ET PRECAUTIONS ].
La sécurité et l'efficacité dans la population pédiatrique autre que les patients pédiatriques atteints de TOC n'ont pas été établies [voir AVERTISSEMENT ENCADRÉ ; AVERTISSEMENTS ET PRECAUTIONS ]. Quiconque envisage l'utilisation des comprimés de maléate de Fluvox 100mgamine chez un enfant ou un adolescent doit équilibrer les risques potentiels avec le besoin clinique.
Utilisation gériatrique
Environ 230 patients participant aux études contrôlées de précommercialisation portant sur les comprimés de maléate de fluvoxamine étaient âgés de 65 ans ou plus. Aucune différence globale de sécurité n'a été observée entre ces patients et les patients plus jeunes. D'autres expériences cliniques rapportées n'ont pas identifié de différences de réponse entre les patients âgés et les patients plus jeunes. Cependant, les ISRS et les IRSN, y compris les comprimés de maléate de fluvoxamine, ont été associés à plusieurs cas d'hyponatrémie cliniquement significative chez les patients âgés, qui peuvent être plus à risque de cet effet indésirable [voir AVERTISSEMENTS ET PRECAUTIONS ]. De plus, la clairance de la fluvoxamine est diminuée d'environ 50 % chez les patients âgés par rapport aux patients plus jeunes [voir PHARMACOLOGIE CLINIQUE ], et une plus grande sensibilité de certaines personnes âgées ne peut pas non plus être exclue. Par conséquent, une dose initiale plus faible doit être envisagée chez les patients âgés et les comprimés de maléate de Fluvox 50 mg doivent être titrés lentement au début du traitement.
SURDOSAGE
Les effets suivants ont été signalés lors d'un surdosage de fluvox 100mgamine en comprimés :
- Convulsions, qui peuvent être retardées, et état mental altéré, y compris le coma.
- Toxicité cardiovasculaire, qui peut être retardée, y compris QRS et allongement de l'intervalle QTc. L'hypertension est la plus souvent observée, mais peut rarement voir l'hypotension seule ou avec des co-ingestants, y compris l'alcool.
- Syndrome sérotoninergique (les patients présentant un surdosage médicamenteux multiple avec d'autres médicaments pro-sérotoninergiques peuvent avoir un risque plus élevé).
Une décontamination gastro-intestinale avec du charbon actif doit être envisagée chez les patients qui se présentent tôt après un surdosage de fluvoxamine.
Envisagez de contacter un centre antipoison (1-800-221-2222) ou un toxicologue médical pour obtenir des recommandations sur la gestion du surdosage.
CONTRE-INDICATIONS
Coadministration
L'administration concomitante de tizanidine, de thioridazine, d'alosétron ou de pimozide avec les comprimés de maléate de Fluvox 50 mgamine est contre-indiquée [voir AVERTISSEMENTS ET PRECAUTIONS ].
Syndrome sérotoninergique et inhibiteurs de la monoamine oxydase (IMAO)
L'utilisation d'IMAO destinés à traiter les troubles psychiatriques avec les comprimés de maléate de fluvoxamine ou dans les 14 jours suivant l'arrêt du traitement avec les comprimés de maléate de fluvoxamine est contre-indiquée en raison d'un risque accru de syndrome sérotoninergique. L'utilisation des comprimés de maléate de Fluvox 50mgamine dans les 14 jours suivant l'arrêt d'un IMAO destiné à traiter les troubles psychiatriques est également contre-indiquée [voir DOSAGE ET ADMINISTRATION , AVERTISSEMENTS ET PRECAUTIONS ].
Commencer à prendre des comprimés de maléate de fluvoxamine chez un patient traité par des IMAO tels que le linézolide ou le bleu de méthylène par voie intraveineuse est également contre-indiqué en raison d'un risque accru de syndrome sérotoninergique [voir DOSAGE ET ADMINISTRATION , AVERTISSEMENTS ET PRECAUTIONS ].
PHARMACOLOGIE CLINIQUE
Mécanisme d'action
Le mécanisme d'action du maléate de fluvox 50mgamine dans le trouble obsessionnel compulsif est présumé être lié à son inhibition spécifique de la recapture de la sérotonine dans les neurones cérébraux. Fluvox 100 mgamine s'est avéré être un puissant inhibiteur du transporteur de la recapture de la sérotonine dans des études précliniques, à la fois in vitro et in vivo.
Pharmacodynamie
Dans des études in vitro, le maléate de fluvox 100 mg d'amine n'a pas eu d'affinité significative pour les récepteurs histaminergiques, alpha ou bêta adrénergiques, muscariniques ou dopaminergiques. On pense que l'antagonisme de certains de ces récepteurs est associé à divers effets sédatifs, cardiovasculaires, anticholinergiques et extrapyramidaux de certains médicaments psychotropes.
Pharmacocinétique
Absorption
La biodisponibilité absolue du maléate de fluvoxamine est de 53 %. La biodisponibilité orale n'est pas significativement affectée par les aliments.
Dans une étude de proportionnalité de dose portant sur le maléate de fluvoxamine à 100, 200 et 300 mg/jour pendant 10 jours consécutifs chez 30 volontaires sains, l'état d'équilibre a été atteint après environ une semaine d'administration. Les concentrations plasmatiques maximales à l'état d'équilibre sont survenues dans les 3 à 8 heures suivant l'administration et ont atteint des concentrations moyennes de 88, 283 et 546 ng/mL, respectivement. Ainsi, la fluvoxamine avait une pharmacocinétique non linéaire sur cette plage de doses, c'est-à-dire que des doses plus élevées de maléate de fluvox 100 mgamine produisaient des concentrations disproportionnellement plus élevées que celles prédites à partir de la dose plus faible.
Distribution
Le volume de distribution apparent moyen de la fluvoxamine est d'environ 25 L/kg, suggérant une distribution tissulaire importante.
Environ 80 % de fluvox 100 mgamine est lié aux protéines plasmatiques, principalement l'albumine, sur une plage de concentration de 20 à 2 000 ng/mL.
Métabolisme
Le maléate d'amine Fluvox 100mg est largement métabolisé par le foie; les principales voies métaboliques sont la déméthylation oxydative et la désamination. Neuf métabolites ont été identifiés suite à une dose radiomarquée de 5 mg de maléate d'amine fluvox 100 mg, constituant environ 85 % des produits d'excrétion urinaire de fluvox 100 mg amine. Le principal métabolite humain était l'acide fluvox 100mgamine qui, avec son analogue N-acétylé, représentait environ 60% des produits d'excrétion urinaire. Un troisième métabolite, le fluvoxéthanol, formé par désamination oxydative, représentait environ 10 %. Fluvox 100 mg d'acide aminé et fluvox 100 mg d'éthanol ont été testés dans un test in vitro d'inhibition de la recapture de la sérotonine et de la noradrénaline chez des rats ; ils étaient inactifs à l'exception d'un faible effet de l'ancien métabolite sur l'inhibition de l'absorption de la sérotonine (1 à 2 ordres de grandeur moins puissants que le composé parent). Environ 2 % de fluvox 100 mgamine a été excrété dans l'urine sous forme inchangée [voir INTERACTIONS MÉDICAMENTEUSES ].
Élimination
Après une dose orale marquée au 14C de maléate d'amine fluvox 50mg (5 mg), une moyenne de 94% des produits liés au médicament a été récupérée dans l'urine dans les 71 heures.
La demi-vie plasmatique moyenne de fluvox 100 mg d'amine à l'état d'équilibre après plusieurs doses orales de 100 mg/jour chez de jeunes volontaires sains était de 15,6 heures.
Sujets âgés
Dans une étude sur les comprimés de maléate de fluvoxamine à 50 et 100 mg comparant des personnes âgées (66 à 73 ans) et des sujets jeunes (19 à 35 ans), les concentrations plasmatiques maximales moyennes chez les personnes âgées étaient 40 % plus élevées. La demi-vie d'élimination de doses multiples de fluvox 50mgamine était de 17,4 et 25,9 heures chez les personnes âgées par rapport à 13,6 et 15,6 heures chez les sujets jeunes à l'état d'équilibre pour des doses de 50 et 100 mg, respectivement. Chez les patients âgés, la clairance de fluvox 100 mgamine a été réduite d'environ 50 % et, par conséquent, les comprimés de maléate de fluvox 100 mgamine doivent être titrés lentement au début du traitement [voir DOSAGE ET ADMINISTRATION ].
Sujets pédiatriques
La pharmacocinétique de doses multiples de fluvox 50 mgamine a été déterminée chez des enfants de sexe masculin et féminin (âgés de 6 à 11 ans) et des adolescents (âgés de 12 à 17 ans). Les concentrations plasmatiques à l'état d'équilibre de fluvox 100 mgamine étaient 2 à 3 fois plus élevées chez les enfants que chez les adolescents. L'ASC et la Cmax chez les enfants étaient 1,5 à 2,7 fois plus élevées que chez les adolescents. (Voir le tableau 4.) Comme chez les adultes, les enfants et les adolescents ont présenté une pharmacocinétique non linéaire à doses multiples. Les filles ont montré une ASC (0-12) et une Cmax significativement plus élevées que les garçons et, par conséquent, des doses plus faibles de comprimés de maléate de fluvoxamine peuvent produire un bénéfice thérapeutique. (Voir le tableau 5.) Aucune différence entre les sexes n'a été observée chez les adolescents. Les concentrations plasmatiques de fluvoxamine à l'état d'équilibre étaient similaires chez les adultes et les adolescents à une dose de 300 mg/jour, ce qui indique que l'exposition à la fluvox 100 mgamine était similaire dans ces deux populations. (Voir Tableau 4.) Un ajustement posologique chez les adolescents (jusqu'à la dose maximale adulte de 300 mg) peut être indiqué pour obtenir un bénéfice thérapeutique [voir DOSAGE ET ADMINISTRATION ].
TABLEAU 4 : COMPARAISON DES PARAMÈTRES PHARMACOCINÉTIQUES MOYENS (ET) DU FLUVOX 50 mgAMINE ENTRE LES ENFANTS, LES ADOLESCENTS ET LES ADULTES
TABLEAU 5 : COMPARAISON DES PARAMÈTRES PHARMACOCINÉTIQUES MOYENS (ET) DU FLUVOX 50 mgAMINE ENTRE LES ENFANTS DE GARÇON ET DE FILLE (6 À 11 ANS)
Maladie hépatique et rénale
Une comparaison d'études croisées (sujets sains versus patients atteints de dysfonctionnement hépatique) a suggéré une diminution de 30 % de la clairance de fluvox 50 mgamine en association avec un dysfonctionnement hépatique. Les concentrations plasmatiques minimales moyennes chez les insuffisants rénaux (clairance de la créatinine de 5 à 45 mL/min) après 4 et 6 semaines de traitement (50 mg bid, N=13) étaient comparables entre elles, suggérant l'absence d'accumulation de fluvoxamine chez ces patients [voir AVERTISSEMENTS ET PRECAUTIONS ].
Etudes cliniques
Études sur le TOC chez l'adulte
L'efficacité des comprimés de maléate de fluvoxamine pour le traitement du trouble obsessionnel-compulsif (TOC) a été démontrée dans deux études multicentriques en groupes parallèles de 10 semaines chez des patients externes adultes. Les patients de ces essais ont été titrés à une dose quotidienne totale de maléate de fluvox de 50 mg d'amine de 150 mg/jour au cours des deux premières semaines de l'essai, après quoi la dose a été ajustée dans une fourchette de 100 à 300 mg/jour (selon un calendrier bid) , sur la base de la réponse et de la tolérance. Les patients de ces études souffraient d'un TOC modéré à sévère (DSM-III-R), avec des cotes initiales moyennes sur l'échelle Yale-Brown Obsessive Compulsive Scale (Y-BOCS), score total de 23. Les patients recevant du fluvox 50 mg de maléate d'amine ont présenté des réductions moyennes d'environ 4 à 5 unités sur le score total Y-BOCS, contre une réduction de 2 unités pour les patients sous placebo.
Le tableau 6 fournit la classification des résultats par groupe de traitement sur l'élément d'amélioration globale de l'échelle des impressions cliniques globales (CGI) pour les deux études combinées.
TABLEAU 6 : CLASSIFICATION DES RÉSULTATS (%) SUR L'ITEM D'AMÉLIORATION GLOBALE CGI POUR LES FINISSANTS DANS UN GROUPE DE DEUX ÉTUDES SUR LE TOC POUR ADULTES
Les analyses exploratoires des effets de l'âge et du sexe sur les résultats n'ont suggéré aucune réactivité différentielle sur la base de l'âge ou du sexe.
Étude sur le maintien du TOC chez l'adulte
Dans un essai d'entretien de patients externes adultes atteints de TOC, 114 patients répondant aux critères du DSM-IV pour le TOC et avec un score de l'échelle de Yale-Brown Obsessive Compulsive Scale (Y-BOCS) ≥ 18 ont été titrés à une dose efficace de comprimés de maléate de fluvoxamine de 100 à 300 mg /jour dans le cadre d'une phase initiale de traitement en simple aveugle de 10 semaines. La réponse au traitement au cours de cette phase en simple aveugle a été définie comme des scores Y-BOCS au moins 30 % inférieurs à la valeur initiale à la fin des semaines 8 et 10. Parmi les patients qui ont répondu, leur durée moyenne de réponse était de 4 semaines. Les patients qui ont répondu au cours de cette phase initiale ont été randomisés soit pour continuer les comprimés de maléate de 50 mg de Fluvox (N = 56) soit pour recevoir un placebo (N = 58) dans une phase en double aveugle pour l'observation des rechutes. La rechute au cours de la phase en double aveugle a été définie comme une augmentation du score Y-BOCS d'au moins 30 % par rapport à la valeur initiale pour cette phase ou le refus du patient de poursuivre le traitement en raison d'une augmentation substantielle des symptômes du TOC. Dans la phase à double insu, les patients recevant un traitement continu par les comprimés de maléate de fluvoxamine ont présenté, en moyenne, un taux de rechute significativement plus faible que ceux recevant le placebo.
Un examen des sous-groupes de population de cet essai n'a révélé aucune preuve claire d'un effet d'entretien différentiel sur la base de l'âge ou du sexe.
Étude pédiatrique sur le TOC
L'efficacité des comprimés de maléate de fluvoxamine pour le traitement du TOC a également été démontrée dans une étude multicentrique en groupes parallèles de 10 semaines menée auprès d'une population pédiatrique ambulatoire (enfants et adolescents, âgés de 8 à 17 ans). Les patients de cette étude ont été titrés à une dose quotidienne totale de fluvox 100 mgamine d'environ 100 mg/jour au cours des deux premières semaines de l'essai, après quoi la dose a été ajustée dans une fourchette de 50 à 200 mg/jour (selon un calendrier bid) sur la base de la réponse et de la tolérance. Tous les patients avaient un TOC modéré à sévère (DSM-III-R) avec des notes moyennes de base sur l'échelle CY-BOCS (Children's Yale-Brown Obsessive Compulsive Scale) de 24. Les patients recevant du maléate de fluvox 100 mgamine ont présenté des réductions moyennes de environ six unités sur le score total CY-BOCS, par rapport à une réduction de trois unités pour les patients sous placebo.
Le tableau 7 fournit la classification des résultats par groupe de traitement sur l'élément d'amélioration globale de l'échelle d'impression clinique globale (CGI) pour l'étude pédiatrique.
TABLEAU 7 : CLASSIFICATION DES RÉSULTATS (%) SUR L'ITEM D'AMÉLIORATION GLOBALE CGI POUR LES FINISSANTS EN ÉTUDE PÉDIATRIQUE
Les analyses exploratoires post hoc des effets du genre sur les résultats n'ont pas suggéré de réactivité différentielle sur la base du sexe. D'autres analyses exploratoires ont révélé un effet important du traitement dans le groupe d'âge de 8 à 11 ans et pratiquement aucun effet dans le groupe d'âge de 12 à 17 ans. Bien que la signification de ces résultats ne soit pas claire, les concentrations plasmatiques de fluvoxamine à l'état d'équilibre sont 2 à 3 fois plus élevées chez les enfants que chez les adolescents [voir PHARMACOLOGIE CLINIQUE ] suggère qu'une diminution de l'exposition chez les adolescents peut avoir été un facteur, et un ajustement de la dose chez les adolescents (jusqu'à la dose maximale adulte de 300 mg) peut être indiqué pour obtenir un bénéfice thérapeutique.
INFORMATIONS PATIENTS
Fluvox 100mgamine (Flu VOX ah meen) Comprimés de maléate
Lisez le Guide des médicaments fourni avec les comprimés de maléate de Fluvox 100mgamine avant de commencer à le prendre et chaque fois que vous recevez une recharge. Il peut y avoir de nouvelles informations. Ce Guide de Médication ne prend pas l'endroit de parler à votre pourvoyeur de soins de santé de votre condition médicale ou traitement. Discutez avec votre fournisseur de soins de santé s'il y a quelque chose que vous ne comprenez pas ou si vous voulez en savoir plus.
Quelles sont les informations les plus importantes que je devrais connaître sur les comprimés de maléate de Fluvox 50mgamine ?
La fluvoxamine est le même type de médicament que ceux utilisés pour traiter la dépression et peut provoquer des effets secondaires graves, notamment :
1. Pensées ou actions suicidaires :
- Les comprimés de maléate de fluvoxamine et les médicaments antidépresseurs peuvent augmenter les pensées ou les actions suicidaires. chez certains enfants, adolescents ou jeunes adultes au cours des premiers mois de traitement ou lorsque la dose est modifiée.
- La dépression ou d'autres maladies mentales graves sont les causes les plus importantes de pensées ou d'actions suicidaires.
- Surveillez ces changements et appelez immédiatement votre fournisseur de soins de santé si vous remarquez :
- Changements nouveaux ou soudains d'humeur, de comportement, d'actions, de pensées ou de sentiments, surtout s'ils sont graves.
- Portez une attention particulière à ces changements lorsque Fluvox 100mgamine Maleate Tablets est commencé ou lorsque la dose est modifiée.
Gardez toutes les visites de suivi avec votre fournisseur de soins de santé et appelez entre les visites si vous vous inquiétez des symptômes.
Appelez immédiatement votre fournisseur de soins de santé si vous présentez l'un des symptômes suivants, ou appelez le 911 en cas d'urgence, surtout s'ils sont nouveaux, s'aggravent ou vous inquiètent :
- tentatives de suicide
- agir sur des impulsions dangereuses
- comportement agressif ou violent
- pensées sur le suicide ou la mort
- dépression nouvelle ou pire
- crises d'anxiété ou de panique nouvelles ou pires
- se sentir agité, agité, en colère ou irritable
- troubles du sommeil
- une augmentation de l'activité ou parler plus que ce qui est normal pour vous
- autres changements inhabituels de comportement ou d'humeur
Informez immédiatement votre fournisseur de soins de santé si vous présentez l'un des symptômes suivants ou appelez le 911 en cas d'urgence. Les comprimés de maléate de fluvoxamine peuvent être associés à ces effets secondaires graves :
2. Syndrome sérotoninergique : cette affection peut mettre la vie en danger et peut inclure :
- agitation, hallucinations, coma ou autres changements de l'état mental
- problèmes de coordination ou contractions musculaires (réflexes hyperactifs)
- rythme cardiaque accéléré, pression artérielle élevée ou basse
- transpiration ou fièvre
- nausées, vomissements ou diarrhée
- rigidité musculaire
3. Problèmes visuels
- douleur oculaire
- changements de vision
- gonflement ou rougeur dans ou autour de l'œil
Seules certaines personnes sont à risque pour ces problèmes. Vous voudrez peut-être subir un examen de la vue pour voir si vous êtes à risque et recevoir un traitement préventif si vous l'êtes.
4. Réactions allergiques sévères :
- difficulté à respirer
- gonflement du visage, de la langue, des yeux ou de la bouche
- éruption cutanée, démangeaisons (urticaire) ou cloques, seules ou accompagnées de fièvre ou de douleurs articulaires
5. Saignement anormal : Les comprimés de maléate de Fluvox 100mgamine et les antidépresseurs peuvent augmenter votre risque de saignement ou d'ecchymoses, surtout si vous prenez de la warfarine, un anticoagulant (Coumadin®, Jantoven®), ou un anti-inflammatoire non stéroïdien (AINS, comme l'ibuprofène, le naproxène ou aspirine).
6. Crises ou convulsions
7. Épisodes maniaques :
- énergie considérablement augmentée
- gros troubles du sommeil
- pensées de course
- comportement imprudent
- des idées exceptionnellement grandioses
- bonheur excessif ou irritabilité
- parler plus ou plus vite que d'habitude
8. Changements d'appétit ou de poids. Les enfants et les adolescents doivent faire surveiller leur taille et leur poids pendant le traitement.
9. Faible taux de sel (sodium) dans le sang. Les personnes âgées peuvent être plus à risque pour cela. Les symptômes peuvent inclure :
- mal de tête
- faiblesse ou sensation d'instabilité
- confusion, problèmes de concentration ou de réflexion ou problèmes de mémoire
10. Problèmes sexuels (dysfonctionnement). La prise d'inhibiteurs sélectifs de la recapture de la sérotonine (ISRS), y compris les comprimés de maléate de Fluvox 50mgamine, peut causer des problèmes sexuels.
- Les symptômes chez les hommes peuvent inclure :
- Éjaculation retardée ou incapacité d'avoir une éjaculation
- Diminution de la libido
- Problèmes pour obtenir ou maintenir une érection
- Les symptômes chez les femmes peuvent inclure :
- Diminution de la libido
- Orgasme retardé ou incapacité à avoir un orgasme
Parlez à votre fournisseur de soins de santé si vous développez des changements dans votre fonction sexuelle ou si vous avez des questions ou des préoccupations concernant des problèmes sexuels pendant le traitement avec les comprimés de maléate de Fluvox 50mgamine. Il peut y avoir des traitements que votre fournisseur de soins de santé peut suggérer.
N'arrêtez pas les comprimés de maléate de fluvoxamine sans en parler d'abord à votre fournisseur de soins de santé.
L'arrêt trop rapide des comprimés de maléate de fluvoxamine peut provoquer des symptômes graves, notamment :
- anxiété, irritabilité, humeur haute ou basse, sensation d'agitation ou changements dans les habitudes de sommeil
- maux de tête, sueurs, nausées, étourdissements
- sensations de choc électrique, tremblements, confusion
Que sont les comprimés de maléate de fluvoxamine ?
Les comprimés de maléate de fluvoxamine sont un médicament sur ordonnance utilisé pour traiter le trouble obsessionnel compulsif (TOC). Il est important de parler avec votre fournisseur de soins de santé des risques de traiter le TOC et aussi des risques de ne pas le traiter. Vous devriez discuter de tous les choix de traitement avec votre fournisseur de soins de santé.
Parlez à votre fournisseur de soins de santé si vous pensez que votre état ne s'améliore pas avec le traitement par les comprimés de maléate de Fluvox 100 mgamine.
Qui ne devrait pas prendre les comprimés de maléate de Fluvox 100mgamine ?
Ne prenez jamais les comprimés de maléate de fluvoxamine si vous :
- êtes allergique au maléate de fluvox 50mgamine ou à l'un des ingrédients des comprimés de maléate de fluvoxamine. Voir la fin de ce guide des médicaments pour une liste complète des ingrédients des comprimés de maléate de Fluvox 50mgamine.
- prenez un inhibiteur de la monoamine oxydase (IMAO). Demandez à votre fournisseur de soins de santé ou à votre pharmacien si vous n'êtes pas sûr de prendre un IMAO, y compris l'antibiotique linézolide.
- Ne prenez pas d'IMAO dans les 2 semaines suivant l'arrêt des comprimés de maléate de fluvoxamine, sauf indication contraire de votre médecin.
- Ne commencez pas Fluvox 50mgamine Maleate Tablets si vous avez arrêté de prendre un IMAO au cours des 2 dernières semaines, sauf indication contraire de votre médecin.
Les personnes qui prennent des comprimés de maléate de fluvoxamine peu de temps après un IMAO peuvent avoir des effets secondaires graves, voire mortels. Consultez immédiatement un médecin si vous présentez l'un de ces symptômes :
-
- forte fièvre
- spasmes musculaires incontrôlés
- muscles raides
- changements rapides de la fréquence cardiaque ou de la pression artérielle
- confusion
- perte de connaissance (évanouissement)
- prendre du Mellaril® (thioridazine). Ne prenez pas Mellaril® dans les 2 semaines suivant l'arrêt des comprimés de maléate de Fluvox 50mgamine car cela peut entraîner de graves problèmes de rythme cardiaque ou une mort subite.
- prenez Orap® (pimozide) car la prise de ce médicament avec les comprimés de maléate de Fluvox 50mgamine peut causer de graves problèmes de rythme cardiaque ou une mort subite.
- prendre Zanaflex® (tizanidine). Les comprimés de maléate de fluvoxamine pourraient augmenter la quantité de Zanaflex dans votre corps, ce qui pourrait augmenter ses actions et ses effets secondaires. Cela pourrait inclure de la somnolence et une chute de la pression artérielle et affecter la façon dont vous faites les choses qui nécessitent de la vigilance.
- Prenez Lotronex® (alosétron). Les comprimés de maléate d'amine Fluvox 50mg peuvent augmenter la quantité de Lotronex dans votre corps, ce qui pourrait augmenter ses actions et ses effets secondaires.
Que dois-je dire à mon fournisseur de soins de santé avant de prendre les comprimés de maléate de Fluvox 50mgamine ? Demandez si vous n'êtes pas sûr.
Avant de commencer à prendre des comprimés de maléate de fluvoxamine, informez votre fournisseur de soins de santé si vous :
- Prenez certains médicaments tels que :
- Inhibiteurs de la monoamine oxydase (IMAO) tels que Emsam® (sélégiline), Nardil® (phénelzine) ou Parnate® (tranylcypromine)
- Mellaril® (thioridazine) : utilisé pour traiter les problèmes mentaux ou d'humeur
- Zanaflex® (tizanidine) : utilisé pour traiter la spasticité (une condition dans laquelle les muscles continuent de se contracter et de se cramponner)
- Orap® (pimozide) : utilisé pour traiter le syndrome de Tourette (une affection cérébrale provoquant des tics)
- Lotronex® (alosetron) : utilisé pour traiter une affection caractérisée par la diarrhée, des douleurs abdominales persistantes, des crampes et des ballonnements
- Triptans : utilisés pour traiter les migraines
- Médicaments utilisés pour traiter l'humeur, l'anxiété, les troubles psychotiques ou de la pensée, y compris les tricycliques, le lithium, les ISRS, les IRSN ou les antipsychotiques
- Tramadol : utilisé pour réduire la douleur
- Benzodiazépines : utilisées pour réduire l'anxiété, le stress, les troubles émotionnels ou les convulsions ; vous aide à dormir; aide au sevrage alcoolique; réduit l'agitation; et détend les muscles
- Méthadone : utilisée pour soulager la douleur ou aider à lutter contre la dépendance
- Clozapine : utilisé pour traiter les troubles mentaux
- Mexiletine : utilisé pour traiter les anomalies du rythme cardiaque
- Théophylline : utilisée pour traiter les passages d'air enflés dans vos poumons, pour détendre les muscles de votre poitrine pour soulager l'essoufflement, souvent pour traiter l'asthme
- Warfarine et autres médicaments qui affectent la façon dont votre sang coagule
- Diurétiques pour traiter l'hypertension artérielle, l'insuffisance cardiaque congestive ou l'enflure
- Suppléments en vente libre comme le tryptophane ou le millepertuis
- avoir des problèmes de foie
- avoir des problèmes rénaux
- avoir des problèmes cardiaques
- avez ou avez eu des convulsions ou des convulsions
- souffrez de trouble bipolaire ou de manie
- avez un faible taux de sodium dans le sang
- avoir des antécédents d'accident vasculaire cérébral
- avoir une pression artérielle élevée
- avez ou avez eu des problèmes de saignement
- êtes enceinte ou envisagez de devenir enceinte. Discutez avec votre fournisseur de soins de santé du risque pour votre bébé à naître si vous prenez des comprimés de maléate de Fluvox 50 mgamine.
- Discutez avec votre fournisseur de soins de santé des avantages et des risques du traitement du TOC pendant la grossesse.
- Si vous tombez enceinte pendant le traitement par les comprimés de maléate de Fluvox 50mgamine, parlez à votre fournisseur de soins de santé de l'enregistrement auprès du Registre national des grossesses pour les antidépresseurs. Vous pouvez vous inscrire en composant le 1-844-405-6185.
- allaitez ou envisagez d'allaiter. Les comprimés de maléate de fluvoxamine passent dans votre lait maternel. Discutez avec votre fournisseur de soins de santé de la meilleure façon de nourrir votre bébé pendant que vous prenez les comprimés de maléate de Fluvox 50 mgamine.
Informez votre professionnel de la santé de tous les médicaments que vous prenez, compris les médicaments sur ordonnance et en vente libre, les vitamines et les suppléments à base de plantes. Les comprimés de maléate de fluvoxamine et certains médicaments peuvent interagir les uns avec les autres, peuvent ne pas fonctionner aussi bien ou peuvent provoquer des effets secondaires graves.
Votre fournisseur de soins de santé ou votre pharmacien peut vous dire s'il est sécuritaire de prendre des comprimés de maléate de fluvoxamine avec vos autres médicaments. Ne commencez ni n'arrêtez aucun médicament pendant que vous prenez des comprimés de maléate de fluvoxamine sans en parler d'abord à votre fournisseur de soins de santé.
Si vous prenez des comprimés de maléate de Fluvox 100 mgamine, vous ne devez pas prendre d'autres médicaments contenant de la fluvoxamine, notamment : LUVOX 50 mg CR®
Comment dois-je prendre les comprimés de maléate de fluvoxamine ?
- Prenez les comprimés de maléate de fluvoxamine exactement comme prescrit. Votre fournisseur de soins de santé devra peut-être modifier la dose de comprimés de maléate de Fluvox 100mgamine jusqu'à ce qu'elle soit la bonne dose pour vous.
- Les comprimés de maléate de Fluvox 100mgamine peuvent être pris avec ou sans nourriture.
- Si vous oubliez une dose de comprimés de maléate de fluvoxamine, prenez la dose oubliée dès que vous vous en souvenez. S'il est presque l'heure de la prochaine dose, sautez la dose oubliée et prenez votre prochaine dose à l'heure habituelle. Ne prenez pas deux doses de comprimés de maléate de Fluvox 100mgamine en même temps.
- Si vous avez pris trop de comprimés de maléate de Fluvox 50mgamine, appelez immédiatement votre fournisseur de soins de santé ou un centre antipoison, ou obtenez un traitement d'urgence.
Que dois-je éviter lors de la prise de comprimés de maléate de Fluvox 50mgamine?
Les comprimés de maléate de Fluvox 100mgamine peuvent causer de la somnolence ou affecter votre capacité à prendre des décisions, à penser clairement ou à réagir rapidement. Vous ne devez pas conduire, utiliser de machinerie lourde ou faire d'autres activités dangereuses jusqu'à ce que vous sachiez comment les comprimés de maléate de fluvoxamine vous affectent. Ne buvez pas d'alcool pendant l'utilisation des comprimés de maléate de fluvoxamine.
Quels sont les effets secondaires possibles des comprimés de maléate de Fluvox 100mgamine?
- Les comprimés de maléate de fluvoxamine peuvent provoquer des effets secondaires graves, notamment :
- Voir "Quelles sont les informations les plus importantes que je devrais connaître sur les comprimés de maléate de Fluvox 100mgamine?"
Se sentir anxieux ou avoir du mal à dormir
Les effets secondaires possibles courants chez les personnes qui prennent des comprimés de maléate de Fluvox à 100 mg d'amine comprennent :
- nausée
- envie de dormir
- la faiblesse
- indigestion
- transpiration
- perte d'appétit
- tremblement
- vomissement
- éjaculation retardée
- incapacité à avoir un orgasme
- diminution de la libido
- bouche sèche
- nez encombré
- goût inhabituel
- urination fréquente
Les autres effets indésirables chez les enfants et les adolescents comprennent :
- agitation ou augmentation anormale de l'activité
- se sentir déprimé ou triste
- excès de gaz
- menstruations abondantes
- éruption
- taux de croissance et changement de poids éventuellement ralentis.
Dites à votre fournisseur de soins de santé si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas. Ce ne sont pas tous les effets secondaires possibles des comprimés de maléate de Fluvox 50mgamine. Pour plus d'informations, demandez à votre fournisseur de soins de santé ou votre pharmacien.
APPELER VOTRE MEDECIN POUR OBTENIR DES CONSEILS MEDICAUX SUR LES EFFETS SECONDAIRES. VOUS POUVEZ SIGNALER LES EFFETS SECONDAIRES au 1-800-308-6755 ou à la FDA au 1-800-FDA-1088
Comment dois-je conserver les comprimés de maléate de Fluvox 50mgamine?
Conservez les comprimés de maléate de fluvoxamine à température ambiante entre 59 °F et 86 °F (15 °C et 30 °C).
- Gardez les comprimés de maléate de fluvoxamine à l'abri de l'humidité élevée.
- Gardez le flacon de comprimés de maléate de fluvoxamine fermé hermétiquement.
Gardez les comprimés de maléate de fluvoxamine et tous les médicaments hors de la portée des enfants.
Informations générales sur les comprimés de maléate de Fluvox 100mgamine
Les médicaments sont parfois prescrits à des fins autres que celles énumérées dans un guide des médicaments. N'utilisez pas les comprimés de maléate de fluvoxamine pour une affection pour laquelle il n'a pas été prescrit. Ne donnez pas les comprimés de maléate de Fluvox 100mgamine à d'autres personnes, même si elles ont la même condition. Cela peut leur nuire.
Ce guide de médication résume les informations les plus importantes sur les comprimés de maléate de fluvoxamine. Si vous souhaitez plus d'informations, parlez-en à votre fournisseur de soins de santé. Vous pouvez demander à votre professionnel de la santé ou à votre pharmacien des informations sur les comprimés de maléate de fluvoxamine qui sont destinées aux professionnels de la santé.
Pour plus d'informations sur les comprimés de maléate de Fluvox 50mgamine, appelez sans frais au 1-800-308-6755 ou rendez-vous sur www.anipharmaceuticals.com.
Quels sont les ingrédients des comprimés de maléate de fluvoxamine ?
Ingrédient actif : maléate de fluvoxamine
Ingrédients inactifs:
Les comprimés de 25 mg : cire de carnauba, hypromellose, mannitol, polyéthylèneglycol, polysorbate 80, amidon prégélatinisé (pomme de terre), dioxyde de silicium, stéarylfumarate de sodium, amidon (maïs) et dioxyde de titane.
Les comprimés de 50 mg et 100 mg : En plus des ingrédients inactifs ci-dessus, contiennent des oxydes de fer synthétiques.
Ce guide de médication a été approuvé par la Food and Drug Administration des États-Unis.
