Elavil 10mg, 25mg, 50mg Amitriptyline Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
Qu'est-ce qu'Elavil et comment est-il utilisé ?
Elavil 10mg est un médicament délivré sur ordonnance utilisé pour traiter les symptômes d'anxiété ou d'agitation avec dépression et de schizophrénie avec dépression. Elavil peut être utilisé seul ou avec d'autres médicaments.
Elavil appartient à une classe de médicaments appelés combos psychothérapeutiques.
On ne sait pas si Elavil est sûr et efficace chez les enfants.
Quels sont les effets secondaires possibles d'Elavil 25mg ?
Elavil peut provoquer des effets secondaires graves, notamment :
- ecchymoses ou saignements faciles,
- brûlures d'estomac persistantes,
- tremblement,
- expressions faciales de type masque,
- spasmes musculaires,
- fortes douleurs à l'estomac,
- diminution du désir sexuel,
- seins hypertrophiés ou douloureux,
- tabourets noirs,
- vomi qui ressemble à du marc de café,
- vertiges sévères,
- évanouissement,
- convulsions,
- douleur, rougeur ou gonflement des yeux,
- changements de vision,
- fièvre,
- rigidité musculaire,
- grande confusion,
- la transpiration, et
- rythme cardiaque rapide ou irrégulier
Consultez immédiatement un médecin si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires les plus courants d'Elavil incluent:
- somnolence,
- vertiges,
- bouche sèche,
- Vision floue,
- constipation,
- gain de poids, et
- difficulté à uriner
Dites au médecin si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas.
Ce ne sont pas tous les effets secondaires possibles d'Elavil. Pour plus d'informations, consultez votre médecin ou votre pharmacien.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
Suicidalité et antidépresseurs
Les antidépresseurs ont augmenté le risque par rapport au placebo de pensées et de comportements suicidaires (suicidalité) chez les enfants, les adolescents et les jeunes adultes dans les études à court terme sur le trouble dépressif majeur (TDM) et d'autres troubles psychiatriques. Quiconque envisage l'utilisation de comprimés d'hydrochlorure d'amitriptyline ou de tout autre antidépresseur chez un enfant, un adolescent ou un jeune adulte doit équilibrer ce risque avec le besoin clinique. Les études à court terme n'ont pas montré d'augmentation du risque de suicide avec les antidépresseurs par rapport au placebo chez les adultes au-delà de 24 ans ; il y avait une réduction du risque avec les antidépresseurs par rapport au placebo chez les adultes âgés de 65 ans et plus. La dépression et certains autres troubles psychiatriques sont eux-mêmes associés à une augmentation du risque de suicide. Les patients de tous âges qui commencent un traitement antidépresseur doivent être surveillés de manière appropriée et observés de près pour déceler une aggravation clinique, des tendances suicidaires ou des changements inhabituels de comportement. Les familles et les soignants doivent être informés de la nécessité d'une surveillance étroite et d'une communication avec le prescripteur. Les comprimés d'hydrochlorure d'Amitriptyline ne sont pas approuvés pour l'utilisation dans les patients de pédiatrie (voir des AVERTISSEMENTS : l'aggravation Clinique et le Risque de Suicide, les RENSEIGNEMENTS PATIENT et les PRÉCAUTIONS : l'Utilisation de Pédiatrie.)
LA DESCRIPTION
L'amitriptyline HCl est le chlorhydrate de 3-(10,11-dihydro-5H-dibenzo [a,d] cycloheptène-5-ylidène)-N,N-diméthyl-1-propanamine. Sa formule empirique est C20H23N•HCl et sa formule structurale est :
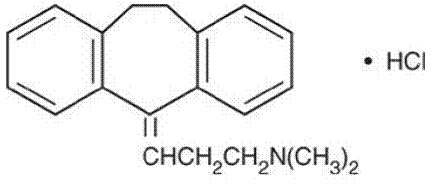
Amitriptyline HCl, un dérivé du dibenzocycloheptadiène, a un poids moléculaire de 313,87. C'est un composé cristallin blanc, inodore, librement soluble dans l'eau.
Amitriptyline HCl est fourni sous forme de comprimés de 10 mg, 25 mg, 50 mg, 75 mg, 100 mg ou 150 mg. Chaque comprimé contient les ingrédients inactifs suivants : dioxyde de silice colloïdale, hypromellose, lactose monohydraté, stéarate de magnésium, cellulose microcristalline, polyéthylèneglycol, polysorbate, glycolate d'amidon sodique et dioxyde de titane. Les comprimés de 10 mg contiennent également le lac FD&C bleu #1. Les comprimés de 25 mg contiennent également du lac D&C jaune #10 et du lac FD&C bleu #2. Les comprimés de 50 mg contiennent également de l'oxyde de fer noir synthétique, de l'oxyde de fer rouge synthétique et de l'oxyde de fer jaune synthétique. Les comprimés de 75 mg contiennent également du lac FD&C jaune #6. Les comprimés de 100 mg contiennent également le lac D&C rouge #33 et le lac FD&C rouge #40. Les comprimés de 150 mg contiennent également le lac FD&C bleu #2 et le lac FD&C jaune #6.
LES INDICATIONS
Pour le soulagement des symptômes de la dépression. La dépression endogène est plus susceptible d'être atténuée que les autres états dépressifs.
DOSAGE ET ADMINISTRATION
La posologie doit être initiée à un niveau bas et augmentée progressivement, en notant attentivement la réponse clinique et tout signe d'intolérance.
Posologie initiale pour les adultes
Pour les patients ambulatoires, 75 mg de chlorhydrate d'amitriptyline par jour en doses fractionnées sont généralement satisfaisants. Si nécessaire, cela peut être augmenté jusqu'à un total de 150 mg par jour. Les augmentations se font de préférence en fin d'après-midi et/ou au coucher. Un effet sédatif peut être apparent avant que l'effet antidépresseur ne soit noté, mais un effet thérapeutique adéquat peut prendre jusqu'à 30 jours pour se développer.
Une autre méthode d'initiation du traitement chez les patients ambulatoires consiste à commencer par 50 à 100 mg de chlorhydrate d'amitriptyline au coucher. Celle-ci peut être augmentée de 25 ou 50 mg selon les besoins dans la dose au coucher jusqu'à un total de 150 mg par jour.
Les patients hospitalisés peuvent avoir besoin de 100 mg par jour au départ. Celle-ci peut être augmentée progressivement jusqu'à 200 mg par jour si nécessaire. Un petit nombre de patients hospitalisés peuvent avoir besoin de 300 mg par jour.
Patients adolescents et âgés
En général, des doses plus faibles sont recommandées pour ces patients. Dix mg 3 fois par jour avec 20 mg au coucher peuvent être satisfaisants chez les patients adolescents et âgés qui ne tolèrent pas des doses plus élevées.
Entretien
La dose d'entretien habituelle d'amitriptyline HCl est de 50 à 100 mg par jour. Chez certains patients, 40 mg par jour suffisent. Pour le traitement d'entretien, la dose quotidienne totale peut être administrée en une seule dose, de préférence au coucher. Lorsqu'une amélioration satisfaisante a été atteinte, la posologie doit être réduite à la quantité la plus faible qui maintiendra le soulagement des symptômes. Il convient de poursuivre le traitement d'entretien pendant 3 mois ou plus pour réduire le risque de rechute.
Utilisation chez les patients pédiatriques
Compte tenu du manque d'expérience sur l'utilisation de ce médicament chez les patients pédiatriques, il n'est pas recommandé à l'heure actuelle chez les patients de moins de 12 ans.
Niveaux plasmatiques
En raison de la grande variation de l'absorption et de la distribution des antidépresseurs tricycliques dans les fluides corporels, il est difficile de corréler directement les taux plasmatiques et l'effet thérapeutique. Cependant, la détermination des taux plasmatiques peut être utile pour identifier les patients qui semblent avoir des effets toxiques et peuvent avoir des taux excessivement élevés, ou ceux chez qui un manque d'absorption ou une non-observance est suspectée. En raison de l'augmentation du temps de transit intestinal et de la diminution du métabolisme hépatique chez les patients âgés, les taux plasmatiques sont généralement plus élevés pour une dose orale donnée de chlorhydrate d'amitriptyline que chez les patients plus jeunes.
Les patients âgés doivent être surveillés attentivement et les taux sériques quantitatifs doivent être mesurés de manière cliniquement appropriée. L'ajustement de la posologie doit être effectué en fonction de la réponse clinique du patient et non en fonction des taux plasmatiques.**
COMMENT FOURNIE
10 mg Les comprimés sont bleus, ronds, non sécables, pelliculés, portant l'inscription « 2101 » gravée sur une face et « V » gravée sur l'autre face. Ils sont fournis comme suit :
Bouteilles de 30 : CDN 0603-2212-16 Bouteilles de 90 : CDN 0603-2212-02 Flacons de 100 : CDN 0603-2212-21 Flacons de 1000 : CDN 0603-2212-32
25mg Les comprimés sont jaunes, ronds, non sécables, pelliculés, portant l'inscription « 2102 » gravée sur une face et « V » gravée sur l'autre face. Ils sont fournis comme suit :
Bouteilles de 90 : CDN 0603-2213-02 Flacons de 100 : CDN 0603-2213-21 Flacons de 1000 : CDN 0603-2213-32 Bouteilles de 2500 : CDN 0603-2213-30
50mg Les comprimés sont beiges, ronds, non sécables, pelliculés, portant l'inscription « 2103 » gravée sur une face et « V » gravée sur l'autre face. Ils sont fournis comme suit :
Bouteilles de 100 : CDN 0603-2214-21 Flacons de 1000 : CDN 0603-2214-32
75mg Les comprimés sont orange, ronds, non sécables, pelliculés, gravés « 2104 » et « V ». Ils sont fournis comme suit :
Bouteilles de 100 : CDN 0603-2215-21 Bouteilles de 300 : CDN 0603-2215-25
100mg Les comprimés sont mauves, ronds, non sécables, pelliculés, gravés « 2105 » et « V ». Ils sont fournis comme suit :
Bouteilles de 100 : CDN 0603-2216-21 Bouteilles de 300 : CDN 0603-2216-25
150mg Les comprimés sont bleus, en forme de capsule, non sécables, pelliculés, portant l'inscription « 2106 » gravée sur une face et « V » gravée sur l'autre face. Ils sont fournis comme suit :
Bouteilles de 100 : CDN 0603-2217-21 Bouteilles de 300 : CDN 0603-2217-25
Stockage et manutention
Stockage
Conserver dans un récipient bien fermé. Conserver à 20°-25°C (68°-77°F) [voir Température ambiante contrôlée USP ]. De plus, les comprimés d'amitriptyline doivent être protégés de la lumière et conservés dans un récipient bien fermé et résistant à la lumière.
RÉFÉRENCES
Ayd FJ Jr : Thérapie à l'amitriptyline pour les réactions dépressives. Psychosomatique 1960;1:320–325.
Diamant S : métaboliseur humain de l'amitriptyline marqué au carbone 14. Curr Ther Res, mars 1965, pp 170–175.
Dorfman W : Expériences cliniques avec l'amitriptyline : Un rapport préliminaire. Psychosomatique 1960 ; 1 : 153– 155.
Fallette JM, Stasney CR, Mintz AA : empoisonnement à l'amitriptyline traité avec de la physostigmine. Sud Med J 1970;63:1492–1493.
Hollister LE, Overall JE, Johnson M, et al : comparaison contrôlée de l'amitriptyline, de l'imipramine et du placebo chez des patients déprimés hospitalisés. J Nerv Ment Dis 1964;139:370–375.
Hordern A, Burt CG, Holt NF : États dépressifs : une étude pharmacothérapeutique, étude de Springfield. Springfield, Ill, Charles C. Thomas, 1965. Jenike MA: Traitement des maladies affectives chez les personnes âgées avec des médicaments et une thérapie électroconvulsive. J Geriatr Psychiatry 1989; 22(1):77–112.
Klerman GL, Cole JO : pharmacologie clinique de l'imipramine et des composés antidépresseurs apparentés. Int J Psychiatry 1976;3:267–304.
Liu B, Anderson G, Mittman N, et al : Utilisation d'inhibiteurs sélectifs de la recapture de la sérotonine ou d'antidépresseurs tricycliques et risque de fractures de la hanche chez les personnes âgées. Lancette 1998 ; 351(9112):1303–1307.
McConaghy N, Joffe AD, Kingston WA, et al : Corrélation des caractéristiques cliniques des patients externes déprimés avec la réponse à l'amitriptyline et à la protriptyline. Br J Psychiatry 1968;114:103–106.
McDonald IM, Perkins M, Marjerrison G, et al : une comparaison contrôlée de l'amitriptyline et de la thérapie électroconvulsive dans le traitement de la dépression. Am J Psychiatry 1966;122:1427–1431.
Slovis T, Ott J, Teitelbaum D, et al : Thérapie à la physostigmine dans l'intoxication aiguë aux antidépresseurs tricycliques. Clin Toxicol 1971;4:451–459.
Symposium sur la dépression avec études particulières d'un nouvel antidépresseur, l'amitriptyline. Dis Nerv Syst, (Section 2) mai 1961, pp 5–56.
*Basé sur une dose maximale recommandée d'amitriptyline de 150 mg/jour ou 3 mg/kg/jour pour un patient de 50 kg.
**Hollister LE : Surveillance des concentrations plasmatiques d'antidépresseurs tricycliques. JAMA 1979; 241(23):2530–2533.
Les comprimés d'Elavil 25 mg sont des comprimés pelliculés jaunes, ronds, non sécables, gravés « 2102 » sur une face et « V » gravé sur l'autre face. Ils sont fournis comme suit : Flacons de 100 : CDN 69874-422-10
Fabriqué par : Qualitest Pharmaceuticals/Vintage Pharmaceuticals, Huntsville, AL 35811. Fabriqué pour : Thompson Medical Solutions, Birmingham, AL 35242. Révisé : avril 2016
EFFETS SECONDAIRES
Aucune information fournieINTERACTIONS MÉDICAMENTEUSES
Médicaments métabolisés par le P450 2D6
L'activité biochimique du médicament métabolisant l'isozyme cytochrome P450 2D6 (débrisoquine hydroxylase) est réduite dans un sous-ensemble de la population caucasienne (environ 7 à 10 % des Caucasiens sont appelés "métaboliseurs lents") ; des estimations fiables de la prévalence de l'activité réduite de l'isoenzyme P450 2D6 parmi les populations asiatiques, africaines et autres ne sont pas encore disponibles. Les métaboliseurs lents ont des concentrations plasmatiques d'antidépresseurs tricycliques (ATC) plus élevées que prévu lorsqu'ils reçoivent des doses habituelles. Selon la fraction de médicament métabolisée par le P450 2D6, l'augmentation de la concentration plasmatique peut être faible ou assez importante (augmentation de 8 fois de l'ASC plasmatique du TCA).
De plus, certains médicaments inhibent l'activité de cette isozyme et font ressembler les métaboliseurs normaux aux métaboliseurs lents. Un individu qui est stable avec une dose donnée de TCA peut devenir brusquement toxique lorsqu'il reçoit l'un de ces médicaments inhibiteurs en traitement concomitant. Les médicaments qui inhibent le cytochrome P450 2D6 comprennent certains qui ne sont pas métabolisés par l'enzyme (quinidine, cimétidine) et beaucoup qui sont des substrats pour P450 2D6 (de nombreux autres antidépresseurs, phénothiazines et les antiarythmiques de type 1C propafénone et flécaïnide). Bien que tous les inhibiteurs sélectifs de la recapture de la sérotonine (ISRS), par exemple la fluoxétine, la sertraline et la paroxétine, inhibent P450 2D6, leur degré d'inhibition peut varier. La mesure dans laquelle les interactions SSRI-TCA peuvent poser des problèmes cliniques dépendra du degré d'inhibition et de la pharmacocinétique du SSRI impliqué. Néanmoins, la prudence est de mise lors de l'administration concomitante d'ATC avec l'un des ISRS et également lors du passage d'une classe à l'autre. Il est particulièrement important de veiller à ce qu'un délai suffisant s'écoule avant d'initier un traitement par TCA chez un patient sevré de la fluoxétine, compte tenu de la longue demi-vie du parent et du métabolite actif (au moins 5 semaines peuvent être nécessaires).
L'utilisation concomitante d'antidépresseurs tricycliques avec des médicaments qui peuvent inhiber le cytochrome P450 2D6 peut nécessiter des doses plus faibles que celles habituellement prescrites pour l'antidépresseur tricyclique ou l'autre médicament. De plus, chaque fois que l'un de ces autres médicaments est retiré de la co-thérapie, une dose accrue d'antidépresseur tricyclique peut être nécessaire. Il est souhaitable de surveiller les taux plasmatiques de TCA chaque fois qu'un TCA va être co-administré avec un autre médicament connu pour être un inhibiteur de P450 2D6.
Inhibiteurs de la monoamine oxydase
Voir CONTRE-INDICATIONS section. la guanéthidine ou des composés agissant de manière similaire ; médicaments pour la thyroïde; alcool, barbituriques et autres dépresseurs du SNC ; et disulfirame – voir AVERTISSEMENTS section. Lorsque le chlorhydrate d'amitriptyline est administré avec des agents anticholinergiques ou des médicaments sympathomimétiques, y compris l'épinéphrine associée à des anesthésiques locaux, une surveillance étroite et un ajustement soigneux des doses sont nécessaires.
L'hyperpyrexie a été signalée lorsque le chlorhydrate d'amitriptyline est administré avec des agents anticholinergiques ou avec des médicaments neuroleptiques, en particulier par temps chaud.
Un iléus paralytique peut survenir chez les patients prenant des antidépresseurs tricycliques en association avec des médicaments de type anticholinergique.
On rapporte que la cimétidine réduit le métabolisme hépatique de certains antidépresseurs tricycliques, retardant ainsi l'élimination et augmentant les concentrations à l'état d'équilibre de ces médicaments. Des effets cliniquement significatifs ont été rapportés avec les antidépresseurs tricycliques lorsqu'ils sont utilisés en concomitance avec la cimétidine. Des augmentations des taux plasmatiques d'antidépresseurs tricycliques, ainsi que de la fréquence et de la gravité des effets secondaires, en particulier anticholinergiques, ont été signalées lorsque la cimétidine a été ajoutée au régime médicamenteux. L'arrêt de la cimétidine chez les patients bien contrôlés recevant des antidépresseurs tricycliques et de la cimétidine peut diminuer les concentrations plasmatiques et l'efficacité des antidépresseurs.
La prudence est recommandée si les patients reçoivent simultanément de fortes doses d'éthchlorvynol. Un délire transitoire a été signalé chez des patients traités par un gramme d'éthchlorvynol et 75 à 150 mg de chlorhydrate d'amitriptyline.
EFFETS SECONDAIRES
Dans chaque catégorie, les effets indésirables suivants sont répertoriés par ordre décroissant de gravité. La liste contient quelques effets indésirables qui n'ont pas été signalés avec ce médicament spécifique. Cependant, les similitudes pharmacologiques entre les antidépresseurs tricycliques exigent que chacune des réactions soit prise en compte lors de l'administration d'amitriptyline.
Cardiovasculaire: Infarctus du myocarde; accident vasculaire cérébral; modifications non spécifiques de l'ECG et modifications de la conduction AV ; bloc cardiaque; arythmies; l'hypotension, en particulier l'hypotension orthostatique ; syncope; hypertension; tachycardie; palpitation.
SNC et neuromusculaire : Coma; convulsions; hallucination; illusion; états confusionnels; désorientation; incoordination; ataxie; tremblements; neuropathie périphérique; engourdissement, picotements et paresthésies des extrémités; des symptômes extrapyramidaux, y compris des mouvements involontaires anormaux et une dyskinésie tardive ; dysarthrie; concentration perturbée; excitation; anxiété; insomnie; agitation; cauchemars; somnolence; vertiges; la faiblesse; fatigue; mal de tête; syndrome de sécrétion inappropriée d'ADH (hormone antidiurétique); acouphène; altération des schémas EEG.
Anticholinergique : Iléus paralytique; hyperpyrexie; rétention urinaire; dilatation des voies urinaires; constipation; vision floue, troubles de l'accommodation, augmentation de la pression oculaire, mydriase ; bouche sèche.
Allergique: Démangeaison de la peau; urticaire; photosensibilisation; œdème du visage et de la langue.
Hématologique : Dépression de la moelle osseuse, y compris agranulocytose, leucopénie, thrombocytopénie ; purpura; éosinophilie.
Gastro-intestinal : Rarement hépatite (y compris altération de la fonction hépatique et ictère) ; nausée; détresse épigastrique; vomissement; anorexie; stomatite; goût particulier; diarrhée; gonflement parotide; langue noire.
Endocrine: Gonflement testiculaire et gynécomastie chez l'homme ; hypertrophie mammaire et galactorrhée chez la femme; augmentation ou diminution de la libido ; impuissance; élévation et abaissement du taux de sucre dans le sang.
Autre: Alopécie; œdème; gain ou perte de poids; fréquence urinaire; augmentation de la transpiration.
Les symptômes de sevrage: Après une administration prolongée, l'arrêt brutal du traitement peut entraîner des nausées, des maux de tête et des malaises. Des réductions progressives de la posologie ont été signalées comme produisant, dans les deux semaines, des symptômes transitoires, notamment de l'irritabilité, de l'agitation et des troubles du rêve et du sommeil.
Ces symptômes ne sont pas révélateurs d'une dépendance. De rares cas de manie ou d'hypomanie survenant dans les 2 à 7 jours suivant l'arrêt d'un traitement chronique par antidépresseurs tricycliques ont été signalés.
Relation causale inconnue : D'autres réactions, signalées dans des circonstances où une relation causale n'a pas pu être établie, sont répertoriées pour servir d'information d'alerte aux médecins.
Corps dans son ensemble : Syndrome de type lupique (arthrite migratrice, ANA et facteur rhumatoïde positifs).
Digestif: Insuffisance hépatique, agueusie.
Événements indésirables post-commercialisation
Un syndrome ressemblant au syndrome malin des neuroleptiques (SMN) a été très rarement rapporté après le début ou l'augmentation de la dose de chlorhydrate d'amitriptyline, avec ou sans médicaments concomitants connus pour provoquer le SMN. Les symptômes ont inclus la rigidité musculaire, la fièvre, les changements de l'état mental, la diaphorèse, la tachycardie et les tremblements.
De très rares cas de syndrome sérotoninergique (SS) ont été signalés avec le chlorhydrate d'amitriptyline en association avec d'autres médicaments qui ont une association reconnue avec le SS.
De très rares cas de cardiomyopathie ont été rapportés avec l'amitriptyline.
AVERTISSEMENTS
Aggravation clinique et risque de suicide
Les patients atteints de trouble dépressif majeur (TDM), à la fois adultes et pédiatriques, peuvent présenter une aggravation de leur dépression et/ou l'émergence d'idées et de comportements suicidaires (suicidalité) ou des changements de comportement inhabituels, qu'ils prennent ou non des antidépresseurs, et cela le risque peut persister jusqu'à ce qu'une rémission significative se produise. Le suicide est un risque connu de dépression et de certains autres troubles psychiatriques, et ces troubles eux-mêmes sont les meilleurs prédicteurs du suicide. Cependant, on craint depuis longtemps que les antidépresseurs puissent jouer un rôle dans l'aggravation de la dépression et l'émergence de comportements suicidaires chez certains patients au cours des premières phases du traitement. Des analyses groupées d'essais contrôlés par placebo à court terme portant sur des antidépresseurs (ISRS et autres) ont montré que ces médicaments augmentent le risque de pensées et de comportements suicidaires (suicidalité) chez les enfants, les adolescents et les jeunes adultes (âgés de 1 824 ans) atteints d'un trouble dépressif majeur ( MDD) et d'autres troubles psychiatriques. Les études à court terme n'ont pas montré d'augmentation du risque de suicide avec les antidépresseurs par rapport au placebo chez les adultes au-delà de 24 ans ; il y avait une réduction avec les antidépresseurs par rapport au placebo chez les adultes âgés de 65 ans et plus.
Les analyses groupées d'essais contrôlés par placebo chez des enfants et des adolescents atteints de TDM, de trouble obsessionnel-compulsif (TOC) ou d'autres troubles psychiatriques comprenaient un total de 24 essais à court terme de 9 antidépresseurs chez plus de 4 400 patients. Les analyses groupées d'essais contrôlés par placebo chez des adultes atteints de TDM ou d'autres troubles psychiatriques comprenaient un total de 295 essais à court terme (durée médiane de 2 mois) de 11 antidépresseurs chez plus de 77 000 patients. Il y avait une variation considérable du risque de suicidalité entre les médicaments, mais une tendance à une augmentation chez les patients plus jeunes pour presque tous les médicaments étudiés. Il y avait des différences dans le risque absolu de suicidalité entre les différentes indications, avec l'incidence la plus élevée dans le TDM. Les différences de risque (médicament vs placebo) étaient cependant relativement stables au sein des tranches d'âge et entre les indications. Ces différences de risque (différence médicament-placebo dans le nombre de cas de suicide pour 1000 patients traités) sont présentées dans le tableau 1.
Aucun suicide n'est survenu dans aucun des essais pédiatriques. Il y a eu des suicides dans les essais sur les adultes, mais le nombre n'était pas suffisant pour tirer une conclusion sur l'effet du médicament sur le suicide.
On ne sait pas si le risque de suicide s'étend à une utilisation à plus long terme, c'est-à-dire au-delà de plusieurs mois. Cependant, il existe des preuves substantielles provenant d'essais d'entretien contrôlés par placebo chez des adultes souffrant de dépression que l'utilisation d'antidépresseurs peut retarder la récurrence de la dépression.
Tous les patients traités avec des antidépresseurs pour toute indication doivent être surveillés de manière appropriée et observés de près pour déceler une aggravation clinique, des tendances suicidaires et des changements inhabituels de comportement, en particulier au cours des premiers mois d'un traitement médicamenteux, ou lors de changements de dose, soit des augmentations ou diminue.
Les symptômes suivants, anxiété, agitation, attaques de panique, insomnie, irritabilité, hostilité, agressivité, impulsivité, akathisie (agitation psychomotrice), hypomanie et manie, ont été rapportés chez des patients adultes et pédiatriques traités avec des antidépresseurs pour un trouble dépressif majeur ainsi comme pour les autres indications, tant psychiatriques que non psychiatriques. Bien qu'un lien de causalité entre l'apparition de tels symptômes et soit l'aggravation de la dépression et/ou l'émergence d'impulsions suicidaires n'ait pas été établi, on craint que ces symptômes puissent représenter des précurseurs d'une suicidalité émergente.
Il convient d'envisager de modifier le schéma thérapeutique, y compris éventuellement d'arrêter le médicament, chez les patients dont la dépression s'aggrave de manière persistante, ou qui présentent des tendances suicidaires émergentes ou des symptômes qui pourraient être des précurseurs d'une aggravation de la dépression ou des tendances suicidaires, en particulier si ces symptômes sont graves, brusques. au début ou ne faisaient pas partie des symptômes présentés par le patient.
Les familles et les soignants des patients traités avec des antidépresseurs pour un trouble dépressif majeur ou d'autres indications, psychiatriques et non psychiatriques, doivent être alertés de la nécessité de surveiller les patients pour l'apparition d'agitation, d'irritabilité, de changements inhabituels de comportement et d'autres symptômes. décrites ci-dessus, ainsi que l'émergence de tendances suicidaires, et de signaler immédiatement ces symptômes aux fournisseurs de soins de santé. Une telle surveillance devrait inclure l'observation quotidienne par les familles et les soignants. Les prescriptions pour les comprimés d'hydrochlorure d'amitriptyline devraient être écrites pour la plus petite quantité de comprimés en harmonie avec la bonne direction patiente, pour réduire le risque d'overdose.
Dépistage des patients pour le trouble bipolaire
Un épisode dépressif majeur peut être la présentation initiale d'un trouble bipolaire. Il est généralement admis (bien que non établi dans des essais contrôlés) que le traitement d'un tel épisode avec un antidépresseur seul peut augmenter la probabilité de précipitation d'un épisode mixte/maniaque chez les patients à risque de trouble bipolaire. On ne sait pas si l'un des symptômes décrits ci-dessus représente une telle conversion. Cependant, avant d'initier un traitement avec un antidépresseur, les patients présentant des symptômes dépressifs doivent faire l'objet d'un dépistage adéquat pour déterminer s'ils présentent un risque de trouble bipolaire ; un tel dépistage devrait inclure des antécédents psychiatriques détaillés, y compris des antécédents familiaux de suicide, de trouble bipolaire et de dépression. Il convient de noter que les comprimés d'hydrochlorure d'amitriptyline ne sont pas approuvés pour une utilisation dans le traitement de la dépression bipolaire.
Le chlorhydrate d'amitriptyline peut bloquer l'action antihypertensive de la guanéthidine ou de composés agissant de manière similaire.
Il doit être utilisé avec prudence chez les patients ayant des antécédents de convulsions et, en raison de son action de type atropine, chez les patients ayant des antécédents de rétention urinaire ou de glaucome à angle fermé. Chez les patients atteints de glaucome à angle fermé, même des doses moyennes peuvent déclencher une crise.
Les patients souffrant de troubles cardiovasculaires doivent être étroitement surveillés. Les médicaments antidépresseurs tricycliques, y compris le chlorhydrate d'amitriptyline, en particulier lorsqu'ils sont administrés à fortes doses, ont été signalés comme provoquant des arythmies, une tachycardie sinusale et un allongement du temps de conduction. Des infarctus du myocarde et des accidents vasculaires cérébraux ont été rapportés avec des médicaments de cette classe.
Une surveillance étroite est nécessaire lorsque le chlorhydrate d'amitriptyline est administré à des patients hyperthyroïdiens ou à ceux qui reçoivent des médicaments pour la thyroïde.
Le chlorhydrate d'amitriptyline peut augmenter la réponse à l'alcool et les effets des barbituriques et d'autres dépresseurs du SNC. Chez les patients susceptibles de consommer de l'alcool de manière excessive, il convient de garder à l'esprit que la potentialisation peut augmenter le danger inhérent à toute tentative de suicide ou à tout surdosage. Des cas de délire ont été signalés lors de l'administration concomitante d'amitriptyline et de disulfirame.
Glaucome à angle fermé
La dilatation pupillaire qui survient après l'utilisation de nombreux antidépresseurs, y compris les comprimés de chlorhydrate d'amitriptyline, peut déclencher une attaque à angle fermé chez un patient présentant des angles anatomiquement étroits qui n'a pas subi d'iridectomie perméable.
Utilisation pendant la grossesse
Catégorie de grossesse C
Aucun effet tératogène n'a été observé chez la souris, le rat ou le lapin lorsque l'amitriptyline a été administrée par voie orale à des doses de 2 à 40 mg/kg/jour (jusqu'à 13 fois la dose maximale recommandée chez l'homme*). Des études dans la littérature ont montré que l'amitriptyline était tératogène chez la souris et le hamster lorsqu'elle était administrée par diverses voies d'administration à des doses de 28 à 100 mg/kg/jour (9 à 33 fois la dose maximale recommandée chez l'homme), produisant de multiples malformations. Une autre étude chez le rat a rapporté qu'une dose orale de 25 mg/kg/jour (8 fois la dose maximale recommandée chez l'homme) provoquait des retards d'ossification des corps vertébraux fœtaux sans autres signes d'embryotoxicité. Chez le lapin, une dose orale de 60 mg/kg/jour (20 fois la dose maximale recommandée chez l'homme) a provoqué une ossification incomplète des os crâniens.
Il a été démontré que l'amitriptyline traverse le placenta. Bien qu'une relation de cause à effet n'ait pas été établie, quelques cas d'effets indésirables, notamment des effets sur le SNC, des déformations des membres ou un retard de développement, ont été signalés chez des nourrissons dont les mères avaient pris de l'amitriptyline pendant la grossesse. Il n'y a pas d'études adéquates et bien contrôlées chez les femmes enceintes. Le chlorhydrate d'amitriptyline ne doit être utilisé pendant la grossesse que si le bénéfice potentiel pour la mère justifie le risque potentiel pour le fœtus.
Mères allaitantes
L'amitriptyline est excrétée dans le lait maternel. Dans un rapport dans lequel un patient a reçu 100 mg/jour d'amitriptyline pendant qu'il allaitait son enfant, des taux de 83 à 141 ng/mL ont été détectés dans le sérum de la mère. Des niveaux de 135 à 151 ng/mL ont été trouvés dans le lait maternel, mais aucune trace du médicament n'a pu être détectée dans le sérum du nourrisson.
En raison du risque d'effets indésirables graves chez les nourrissons allaités à l'amitriptyline, une décision doit être prise d'interrompre l'allaitement ou d'arrêter le médicament, en tenant compte de l'importance du médicament pour la mère.
Utilisation chez les patients pédiatriques
Compte tenu du manque d'expérience sur l'utilisation de ce médicament chez les patients pédiatriques, il n'est pas recommandé à l'heure actuelle chez les patients de moins de 12 ans.
PRÉCAUTIONS
Les patients schizophrènes peuvent développer des symptômes accrus de psychose; les patients présentant une symptomatologie paranoïaque peuvent avoir une exagération de ces symptômes. Les patients déprimés, en particulier ceux qui ont une maladie maniaco-dépressive connue, peuvent connaître un passage à la manie ou à l'hypomanie. Dans ces circonstances, la dose d'amitriptyline peut être réduite ou un tranquillisant majeur tel que la perphénazine peut être administré simultanément.
La possibilité de suicide chez les patients déprimés demeure jusqu'à ce qu'une rémission significative se produise. Les patients potentiellement suicidaires ne doivent pas avoir accès à de grandes quantités de ce médicament. Les ordonnances doivent être écrites pour le plus petit montant possible.
L'administration concomitante de chlorhydrate d'amitriptyline et d'une thérapie par électrochocs peut augmenter les risques associés à une telle thérapie. Un tel traitement doit être limité aux patients pour lesquels il est indispensable.
Lorsque cela est possible, le médicament doit être interrompu plusieurs jours avant une intervention chirurgicale élective.
Des élévations et des baisses de la glycémie ont été rapportées.
Le chlorhydrate d'amitriptyline doit être utilisé avec prudence chez les patients présentant une insuffisance hépatique.
Informations pour les patients
Les prétraçoirs ou d'autres professionnels de la santé devraient informer des patients, leurs familles et leurs caregivers des avantages et des risques associés au traitement avec les comprimés d'hydrochlorure amitriptyline et devraient les conseiller dans son utilisation appropriée. Un patient Guide des médicaments à propos de « Médicaments antidépresseurs, dépression et autres maladies mentales graves et pensées ou actions suicidaires » est disponible pour les comprimés de chlorhydrate d'amitriptyline. Le prescripteur ou le professionnel de la santé doit demander aux patients, à leurs familles et à leurs soignants de lire le Guide des médicaments et devrait les aider à comprendre son contenu. Les patients doivent avoir la possibilité de discuter du contenu du Guide des médicaments et d'obtenir des réponses à leurs éventuelles questions. Le texte complet de la Guide des médicaments est reproduit à la fin de ce document.
Les patients doivent être informés des problèmes suivants et invités à alerter leur médecin traitant si ceux-ci surviennent lors de la prise de comprimés de chlorhydrate d'amitriptyline.
Pendant le traitement par le chlorhydrate d'amitriptyline, les patients doivent être informés de la possibilité d'une altération des capacités mentales et/ou physiques requises pour l'exécution de tâches dangereuses, telles que l'utilisation de machines ou la conduite d'un véhicule à moteur.
Les patients doivent être informés que la prise de comprimés de chlorhydrate d'amitriptyline peut provoquer une légère dilatation papillaire qui, chez les personnes sensibles, peut entraîner un épisode de glaucome à angle fermé. Le glaucome préexistant est presque toujours un glaucome à angle ouvert car le glaucome à angle fermé, lorsqu'il est diagnostiqué, peut être traité définitivement par iridectomie. Le glaucome à angle ouvert n'est pas un facteur de risque de glaucome à angle fermé. Les patients peuvent souhaiter être examinés pour déterminer s'ils sont sensibles à la fermeture de l'angle et subir une intervention prophylactique (p. ex., iridectomie), s'ils y sont sensibles.
Aggravation clinique et risque de suicide
Les patients, leurs familles et leurs soignants doivent être encouragés à être attentifs à l'émergence d'anxiété, d'agitation, d'attaques de panique, d'insomnie, d'irritabilité, d'hostilité, d'agressivité, d'impulsivité, d'akathisie (agitation psychomotrice), d'hypomanie, de manie, d'autres changements inhabituels de comportement , aggravation de la dépression et idées suicidaires, en particulier au début du traitement antidépresseur et lorsque la dose est ajustée à la hausse ou à la baisse. Il faut conseiller aux familles et aux soignants des patients de rechercher l'apparition de tels symptômes au jour le jour, car les changements peuvent être brusques. De tels symptômes doivent être signalés au médecin prescripteur ou au professionnel de la santé du patient, en particulier s'ils sont graves, d'apparition brutale ou ne font pas partie des symptômes présentés par le patient. De tels symptômes peuvent être associés à un risque accru de pensées et de comportements suicidaires et indiquent la nécessité d'une surveillance très étroite et éventuellement de modifications de la médication.
Utilisation pédiatrique
La sécurité et l'efficacité dans la population pédiatrique n'ont pas été établies (voir AVERTISSEMENT DE BOÎTE et AVERTISSEMENTS - Aggravation clinique et risque de suicide ). Quiconque envisage l'utilisation de comprimés d'hydrochlorure d'amitriptyline chez un enfant ou un adolescent doit équilibrer les risques potentiels avec le besoin clinique.
Utilisation gériatrique
L'expérience clinique n'a pas identifié de différences dans les réponses entre les patients âgés et les patients plus jeunes. En général, la sélection de la dose pour un patient âgé doit être prudente, en commençant généralement à l'extrémité inférieure de la plage posologique, reflétant la fréquence plus élevée de diminution de la fonction hépatique, de maladie concomitante et d'autres traitements médicamenteux chez les patients âgés.
Les patients gériatriques sont particulièrement sensibles aux effets secondaires anticholinergiques des antidépresseurs tricycliques, y compris le chlorhydrate d'amitriptyline. Les effets anticholinergiques périphériques comprennent la tachycardie, la rétention urinaire, la constipation, la bouche sèche, la vision floue et l'exacerbation du glaucome à angle fermé. Les effets anticholinergiques du système nerveux central comprennent les troubles cognitifs, le ralentissement psychomoteur, la confusion, la sédation et le délire. Les patients âgés prenant du chlorhydrate d'amitriptyline peuvent présenter un risque accru de chutes. Les patients âgés doivent commencer par de faibles doses de chlorhydrate d'amitriptyline et être étroitement surveillés (voir DOSAGE ET ADMINISTRATION ).
SURDOSAGE
Des décès peuvent survenir à la suite d'un surdosage avec cette classe de médicaments. L'ingestion de plusieurs médicaments (dont l'alcool) est fréquente en cas de surdosage délibéré d'antidépresseurs tricycliques. Comme la prise en charge est complexe et changeante, il est recommandé au médecin de contacter un centre antipoison pour obtenir des informations à jour sur le traitement. Les signes et les symptômes de toxicité se développent rapidement après une surdose d'antidépresseurs tricycliques ; par conséquent, une surveillance hospitalière est requise dès que possible.
manifestations
Les manifestations critiques d'un surdosage comprennent : troubles du rythme cardiaque, hypotension grave, convulsions et dépression du SNC, y compris le coma. Les modifications de l'électrocardiogramme, en particulier de l'axe ou de la largeur du QRS, sont des indicateurs cliniquement significatifs de la toxicité des antidépresseurs tricycliques. De plus, un déplacement de l'axe vers la droite dans le complexe QRS terminal ainsi qu'un intervalle QT prolongé et une tachycardie sinusale sont des indicateurs spécifiques et sensibles d'un surdosage tricyclique de première génération. L'absence de ces résultats n'est pas exclusive. Un intervalle PR prolongé, des modifications de l'onde ST-T, une tachycardie ventriculaire et une fibrillation peuvent également survenir.
D'autres signes de surdosage peuvent inclure : altération de la contractilité du myocarde, confusion, troubles de la concentration, hallucinations visuelles transitoires, pupilles dilatées, troubles de la motilité oculaire, agitation, réflexes hyperactifs, polyradiculonévrite, stupeur, somnolence, rigidité musculaire, vomissements, hypothermie, hyperpyrexie ou tout des symptômes énumérés sous RÉACTIONS INDÉSIRABLES.
La gestion
Général
Obtenir un ECG et commencer immédiatement la surveillance cardiaque. Protégez les voies respiratoires du patient, établissez une ligne intraveineuse et lancez la décontamination gastrique. Un minimum de six heures d'observation avec surveillance cardiaque et observation des signes de dépression du SNC ou respiratoire, d'hypotension, de troubles du rythme cardiaque et/ou de blocs de conduction et de convulsions est nécessaire. Si des signes de toxicité apparaissent à tout moment au cours de la période, une surveillance prolongée est nécessaire. Il existe des rapports de cas de patients succombant à des troubles du rythme mortels tard après un surdosage; ces patients présentaient des signes cliniques d'empoisonnement important avant le décès et la plupart ont reçu une décontamination gastro-intestinale inadéquate. La surveillance des concentrations plasmatiques du médicament ne doit pas guider la prise en charge du patient.
Décontamination gastro-intestinale
Tous les patients suspectés de surdosage d'antidépresseurs tricycliques doivent bénéficier d'une décontamination gastro-intestinale. Cela devrait inclure un lavage gastrique à grand volume suivi de charbon actif. Si la conscience est altérée, les voies respiratoires doivent être sécurisées avant le lavage. EMESIS EST CONTRE-INDIQUÉ.
Cardiovasculaire
Une durée maximale du QRS des dérivations des membres ≥ 0,10 seconde peut être la meilleure indication de la sévérité du surdosage. Le bicarbonate de sodium intraveineux doit être utilisé pour maintenir le pH sérique entre 7,45 et 7,55. Si la réponse du pH est inadéquate, l'hyperventilation peut également être utilisée. L'utilisation concomitante d'hyperventilation et de bicarbonate de sodium doit être effectuée avec une extrême prudence, avec une surveillance fréquente du pH. Un pH > 7,60 ou un pCO2
Dans de rares cas, l'hémoperfusion peut être bénéfique en cas d'instabilité cardiovasculaire réfractaire aiguë chez les patients présentant une toxicité aiguë. Cependant, l'hémodialyse, la dialyse péritonéale, les exsanguinotransfusions et la diurèse forcée ont généralement été signalées comme inefficaces dans l'intoxication aux antidépresseurs tricycliques.
SNC
Chez les patients souffrant de dépression du SNC, une intubation précoce est conseillée en raison du risque de détérioration brutale. Les convulsions doivent être contrôlées avec des benzodiazépines ou, si celles-ci sont inefficaces, avec d'autres anticonvulsivants (p. ex., phénobarbital, phénytoïne).
La physostigmine n'est pas recommandée, sauf pour traiter les symptômes potentiellement mortels qui n'ont pas répondu aux autres thérapies, et uniquement en consultation avec un centre antipoison.
Suivi psychiatrique
Étant donné que le surdosage est souvent délibéré, les patients peuvent tenter de se suicider par d'autres moyens pendant la phase de récupération. Une référence psychiatrique peut être appropriée.
Gestion pédiatrique
Les principes de gestion des surdosages pédiatriques et adultes sont similaires. Il est fortement recommandé que le médecin contacte le centre antipoison local pour un traitement pédiatrique spécifique.
CONTRE-INDICATIONS
Le chlorhydrate d'amitriptyline est contre-indiqué chez les patients qui y ont déjà présenté une hypersensibilité. Il ne doit pas être administré en même temps que des inhibiteurs de la monoamine oxydase. Des crises hyperpyrétiques, des convulsions sévères et des décès sont survenus chez des patients recevant simultanément des antidépresseurs tricycliques et des inhibiteurs de la monoamine oxydase. Lorsqu'on souhaite remplacer un inhibiteur de la monoamine oxydase par du chlorhydrate d'amitriptyline, un minimum de 14 jours doit s'écouler après l'arrêt du premier. L'hydrochlorure d'Amitriptyline devrait alors être lancé prudemment avec une augmentation graduelle dans le dosage jusqu'à ce que la réponse optima soit accomplie.
Le chlorhydrate d'amitriptyline ne doit pas être administré avec le cisapride en raison du potentiel d'allongement de l'intervalle QT et du risque accru d'arythmie.
Ce médicament n'est pas recommandé pour une utilisation pendant la phase de récupération aiguë après un infarctus du myocarde.
PHARMACOLOGIE CLINIQUE
Le chlorhydrate d'amitriptyline est un antidépresseur à effet sédatif. Son mécanisme d'action chez l'homme n'est pas connu. Ce n'est pas un inhibiteur de la monoamine oxydase et il n'agit pas principalement par stimulation du système nerveux central.
L'amitriptyline inhibe le mécanisme de pompe membranaire responsable de l'absorption de noradrénaline et de sérotonine dans les neurones adrénergiques et sérotoninergiques. D'un point de vue pharmacologique, cette action peut potentialiser ou prolonger l'activité neuronale puisque la recapture de ces amines biogènes est physiologiquement importante pour mettre fin à l'activité de transmission. Cette interférence avec la recapture de la norépinéphrine et/ou de la sérotonine est considérée par certains comme étant à la base de l'activité antidépressive de l'amitriptyline.
Métabolisme
Des études chez l'homme suite à l'administration orale d'un médicament marqué au 14C ont indiqué que l'amitriptyline est rapidement absorbée et métabolisée. La radioactivité du plasma était pratiquement négligeable, bien que des quantités importantes de radioactivité soient apparues dans l'urine au bout de 4 à 6 heures et qu'un demi à un tiers du médicament ait été excrété en 24 heures.
L'amitriptyline est métabolisée par N-déméthylation et hydroxylation en pont chez l'homme, le lapin et le rat. La quasi-totalité de la dose est excrétée sous forme de glucuronide ou de sulfate conjugué de métabolites, avec peu de médicament inchangé apparaissant dans l'urine. D'autres voies métaboliques peuvent être impliquées.
INFORMATIONS PATIENTS
Médicaments antidépresseurs, dépression et autres maladies mentales graves, et pensées ou actions suicidaires
Lisez le Guide des médicaments qui accompagne votre médicament antidépresseur ou celui d'un membre de votre famille. Ce guide de médication concerne uniquement le risque de pensées et d'actions suicidaires avec les médicaments antidépresseurs. Parlez à votre fournisseur de soins de santé ou à celui d'un membre de votre famille de :
- tous les risques et avantages du traitement avec des antidépresseurs
- tous les choix de traitement pour la dépression ou d'autres maladies mentales graves
Quelles sont les informations les plus importantes que je devrais connaître sur les médicaments antidépresseurs, la dépression et autres maladies mentales graves, et les pensées ou actions suicidaires ?
- Portez une attention particulière à tout changement, en particulier les changements soudains, d'humeur, de comportement, de pensées ou de sentiments. Ceci est très important lorsqu'un médicament antidépresseur est commencé ou lorsque la dose est modifiée.
- Appelez immédiatement le fournisseur de soins de santé pour signaler des changements nouveaux ou soudains d'humeur, de comportement, de pensées ou de sentiments.
- Gardez toutes les visites de suivi avec le fournisseur de soins de santé comme prévu. Appelez le fournisseur de soins de santé entre les visites au besoin, surtout si vous avez des inquiétudes au sujet des symptômes.
Appelez immédiatement un fournisseur de soins de santé si vous ou un membre de votre famille présentez l'un des symptômes suivants, surtout s'ils sont nouveaux, s'aggravent ou vous inquiètent :
- pensées sur le suicide ou la mort
- tentatives de suicide
- dépression nouvelle ou pire
- anxiété nouvelle ou pire
- se sentir très agité ou agité
- crises de panique
- troubles du sommeil (insomnie)
- irritabilité nouvelle ou pire
- agir de manière agressive, être en colère ou violent
- agir sur des impulsions dangereuses
- une augmentation extrême de l'activité et de la conversation (manie)
- autres changements inhabituels de comportement ou d'humeur
- Problèmes visuels : douleur oculaire, changements dans la vision, gonflement ou rougeur dans ou autour de l'œil
Que dois-je savoir d'autre sur les antidépresseurs ?
- N'arrêtez jamais un médicament antidépresseur sans en parler d'abord à un fournisseur de soins de santé. L'arrêt soudain d'un médicament antidépresseur peut provoquer d'autres symptômes.
- Problèmes visuels. Seules certaines personnes sont à risque pour ces problèmes. Vous voudrez peut-être subir un examen de la vue pour voir si vous êtes à risque et recevoir un traitement préventif si vous l'êtes.
- Les antidépresseurs sont des médicaments utilisés pour traiter la dépression et d'autres maladies. Il est important de discuter de tous les risques de traiter la dépression et aussi des risques de ne pas la traiter. Les patients et leurs familles ou autres soignants doivent discuter de tous les choix de traitement avec le fournisseur de soins de santé, et pas seulement de l'utilisation d'antidépresseurs.
- Les antidépresseurs ont d'autres effets secondaires. Parlez au fournisseur de soins de santé des effets secondaires du médicament prescrit pour vous ou un membre de votre famille.
- Les médicaments antidépresseurs peuvent interagir avec d'autres médicaments . Connaissez tous les médicaments que vous ou un membre de votre famille prenez. Gardez une liste de tous les médicaments à montrer au professionnel de la santé. Ne commencez pas de nouveaux médicaments sans d'abord consulter votre fournisseur de soins de santé.
- Tous les médicaments antidépresseurs prescrits aux enfants ne sont pas approuvés par la FDA pour une utilisation chez les enfants. Parlez au fournisseur de soins de santé de votre enfant pour plus d'informations.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
Ce guide de médication a été approuvé par la Food and Drug Administration des États-Unis pour tous les antidépresseurs.
