Eskalith 300mg Lithium carbonate Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
Qu'est-ce qu'Eskalith et comment est-il utilisé ?
Eskalith 300 mg est un médicament sur ordonnance utilisé pour traiter les symptômes du trouble bipolaire. Eskalith 300 mg peut être utilisé seul ou avec d'autres médicaments.
Eskalith 300 mg appartient à une classe de médicaments appelés agents des troubles bipolaires.
On ne sait pas si Eskalith est sûr et efficace chez les enfants de moins de 7 ans.
Quels sont les effets secondaires possibles d'Eskalith ?
Eskalith 300 mg peut provoquer des effets secondaires graves, notamment :
- urticaire,
- difficulté à respirer,
- gonflement du visage, des lèvres, de la langue ou de la gorge,
- faiblesse musculaire,
- contractions musculaires,
- somnolence,
- étourdissement,
- des changements d'humeur,
- Vision floue,
- résonne dans tes oreilles,
- battements cardiaques irréguliers,
- confusion,
- troubles de l'élocution,
- maladresse,
- difficulté à respirer,
- convulsions,
- essoufflement,
- fièvre,
- augmentation de la soif ou de la miction,
- la faiblesse,
- vertiges,
- sensation de rotation,
- problèmes de mémoire,
- hallucinations,
- problèmes d'équilibre ou de mouvement musculaire,
- perte de contrôle des intestins ou de la vessie,
- saisie,
- avoir très soif ou chaud,
- incapacité à uriner,
- transpiration abondante,
- peau chaude et sèche,
- maux de tête intenses,
- résonne dans tes oreilles,
- nausée,
- problèmes de vue,
- douleur derrière les yeux,
- agitation,
- fièvre
- ,
- frissons,
- rythme cardiaque rapide,
- rigidité musculaire,
- contractions musculaires,
- perte de coordination et
- diarrhée
Consultez immédiatement un médecin si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires les plus courants d'Eskalith 300 mg incluent :
- vertiges,
- somnolence,
- des tremblements dans tes mains,
- difficulté à marcher,
- bouche sèche,
- augmentation de la soif ou de la miction,
- nausée,
- vomissement,
- perte d'appétit,
- Douleur d'estomac,
- sensation de froid,
- décoloration des doigts ou des orteils,
- éruption cutanée, et
- Vision floue
Dites au médecin si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas.
Ce ne sont pas tous les effets secondaires possibles d'Eskalith. Pour plus d'informations, consultez votre médecin ou votre pharmacien.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
ATTENTION
La toxicité du lithium est étroitement liée aux niveaux de lithium sérique et peut survenir à des doses proches des niveaux thérapeutiques. Des installations permettant des déterminations rapides et précises du lithium sérique doivent être disponibles avant de commencer le traitement (voir DOSAGE ET ADMINISTRATION ).
LA DESCRIPTION
ESKALITH contient du carbonate de lithium, une poudre blanche alcaline légère de formule moléculaire Li2CO3 et de poids moléculaire 73,89. Le lithium est un élément du groupe des métaux alcalins de numéro atomique 3, de poids atomique 6,94 et d'une raie d'émission à 671 nm sur le photomètre à flamme.
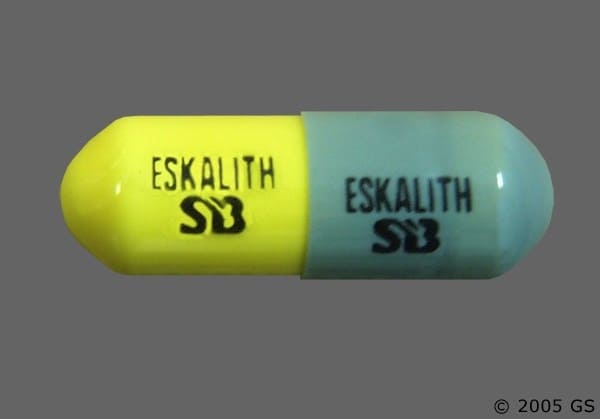
Gélules ESKALITH (carbonate de lithium) : Chaque capsule, avec un capuchon gris opaque et un corps jaune opaque, porte le nom du produit ESKALITH (carbonate de lithium) et SB et contient 300 mg de carbonate de lithium. Les ingrédients inactifs consistent en alcool benzylique, chlorure de cétylpyridinium, D&C jaune n° 10, FD&C vert n° 3, FD&C rouge n° 40, FD&C jaune n° 6, gélatine, lactose, stéarate de magnésium, povidone, laurylsulfate de sodium, dioxyde de titane, et des traces d'autres ingrédients inactifs.
Comprimés à libération contrôlée ESKALITH (carbonate de lithium) CR : Chaque comprimé rond, jaune, biconvexe, portant les inscriptions en creux SKF et J10 sur une face et sécable sur l'autre, contient 450 mg de carbonate de lithium. Les ingrédients inactifs sont l'acide alginique, la gélatine, l'oxyde de fer, le stéarate de magnésium et le glycolate d'amidon sodique.
Les comprimés ESKALITH (carbonate de lithium) CR à 450 mg sont conçus pour libérer une partie de la dose initialement et le reste progressivement ; le schéma de libération des comprimés à libération contrôlée réduit la variabilité des taux sanguins de lithium observée avec les formes posologiques à libération immédiate.
LES INDICATIONS
ESKALITH (carbonate de lithium) est indiqué dans le traitement des épisodes maniaques de la maladie maniaco-dépressive. Le traitement d'entretien prévient ou diminue l'intensité des épisodes ultérieurs chez les patients maniaco-dépressifs ayant des antécédents de manie.
Les symptômes typiques de la manie comprennent la pression de la parole, l'hyperactivité motrice, le besoin réduit de sommeil, la fuite des idées, la grandiosité, l'exaltation, le manque de jugement, l'agressivité et éventuellement l'hostilité. Lorsqu'il est administré à un patient souffrant d'un épisode maniaque, ESKALITH (carbonate de lithium) peut produire une normalisation de la symptomatologie en 1 à 3 semaines.
DOSAGE ET ADMINISTRATION
Les gélules à libération immédiate sont généralement administrées tid ou qid. Les doses de comprimés à libération contrôlée sont généralement administrées bid (intervalles d'environ 12 heures). Lors de l'initiation d'un traitement avec du lithium à libération immédiate ou à libération contrôlée, la posologie doit être individualisée en fonction des taux sériques et de la réponse clinique.
Lors du passage d'un patient de capsules à libération immédiate à des comprimés à libération contrôlée ESKALITH (carbonate de lithium) CR, donner la même dose quotidienne totale lorsque cela est possible. La plupart des patients sous traitement d'entretien sont stabilisés avec 900 mg par jour, p. ex., ESKALITH (carbonate de lithium) CR 450 mg bid Lorsque la dose précédente de lithium à libération immédiate n'est pas un multiple de 450 mg, p. ) RC au multiple de 450 mg le plus proche de la dose quotidienne d'origine, mais inférieur à celle-ci, c'est-à-dire 1 350 mg. Lorsque les 2 doses sont inégales, donner la dose la plus importante le soir. Dans l'exemple ci-dessus, avec une dose quotidienne totale de 1 350 mg, il faut généralement administrer 450 mg d'ESKALITH (carbonate de lithium) CR le matin et 900 mg d'ESKALITH (carbonate de lithium) CR le soir. Si vous le souhaitez, la dose quotidienne totale de 1 350 mg peut être administrée en 3 doses égales de 450 mg d'ESKALITH (carbonate de lithium) CR. Ces patients doivent être surveillés à des intervalles de 1 à 2 semaines, et la posologie doit être ajustée si nécessaire, jusqu'à ce que des taux sériques et un état clinique stables et satisfaisants soient atteints.
Lorsque les patients nécessitent une titration plus étroite que celle disponible avec des doses d'ESKALITH (carbonate de lithium) CR par paliers de 450 mg, des gélules à libération immédiate doivent être utilisées.
Manie aiguë : La réponse optimale du patient à ESKALITH (carbonate de lithium) peut généralement être établie et maintenue avec 1 800 mg par jour en doses fractionnées. De telles doses produiront normalement le niveau de lithium sérique souhaité compris entre 1,0 et 1,5 mEq/L.
La posologie doit être individualisée en fonction des taux sériques et de la réponse clinique. Une surveillance régulière de l'état clinique du patient et des taux sériques de lithium est nécessaire. Les concentrations sériques doivent être déterminées deux fois par semaine pendant la phase aiguë et jusqu'à ce que la concentration sérique et l'état clinique du patient soient stabilisés.
Contrôle à long terme : Les niveaux de lithium sérique souhaitables sont de 0,6 à 1,2 mEq/L. La posologie variera d'un individu à l'autre, mais généralement 900 mg à 1 200 mg par jour en doses fractionnées maintiendront ce niveau. Les taux sériques de lithium dans les cas non compliqués recevant un traitement d'entretien pendant la rémission doivent être surveillés au moins tous les deux mois.
Les patients exceptionnellement sensibles au lithium peuvent présenter des signes de toxicité à des taux sériques inférieurs à 1,0 mEq/L.
N.-B. : Les échantillons de sang pour les déterminations de lithium sérique doivent être prélevés immédiatement avant la dose suivante lorsque les concentrations de lithium sont relativement stables (c'est-à-dire 8 à 12 heures après la dose précédente). Une confiance totale ne doit pas être placée uniquement sur les taux sériques. Une évaluation précise du patient nécessite à la fois une analyse clinique et une analyse de laboratoire.
Les patients âgés répondent souvent à une posologie réduite et peuvent présenter des signes de toxicité à des taux sériques habituellement tolérés par les patients plus jeunes.
COMMENT FOURNIE
ESKALITH (carbonate de lithium) Gélules 300 mg sont des capsules grises et jaunes imprimées avec "ESKALITH (carbonate de lithium)" et "SB" sur un côté de chaque moitié de la capsule, dans des bouteilles de 100 (NDC 0007-4007-20).
Comprimés ESKALITH (carbonate de lithium) CR 450 mg sont ronds, jaunes, biconvexes, comprimés à libération contrôlée, gravés avec "SKF" et "J10" sur un côté et marqués sur l'autre côté, en flacons de 100 (NDC 0007-4010-20).
CONDITIONS DE STOCKAGE : Le magasin à 25°C (77°F), les excursions permises à 15-30°C (59-86°F) [voient USP la Température de Pièce Contrôlée].
Fabriqué par : Cardinal Health., Winchester, KY 40391 pour GlaxoSmithKline., Research Triangle Park, NC 27709. Septembre 2003 Date de révision FDA : 03/11/2004
EFFETS SECONDAIRES
La survenue et la sévérité des effets indésirables sont généralement directement liées aux concentrations sériques de lithium ainsi qu'à la sensibilité individuelle des patients au lithium, et se produisent généralement plus fréquemment et avec une plus grande sévérité à des concentrations plus élevées.
Des réactions indésirables peuvent survenir à des taux sériques de lithium inférieurs à 1,5 mEq/L. Des réactions indésirables légères à modérées peuvent survenir à des niveaux de 1,5 à 2,5 mEq/L, et des réactions modérées à sévères peuvent être observées à des niveaux de 2,0 mEq/L et plus.
De légers tremblements des mains, une polyurie et une légère soif peuvent survenir pendant le traitement initial de la phase maniaque aiguë et peuvent persister tout au long du traitement. Des nausées transitoires et légères et une gêne générale peuvent également apparaître au cours des premiers jours d'administration de lithium.
Ces effets secondaires disparaissent généralement avec la poursuite du traitement ou une réduction temporaire ou l'arrêt de la posologie. En cas de persistance, l'arrêt de la thérapie au lithium peut être nécessaire.
La diarrhée, les vomissements, la somnolence, la faiblesse musculaire et le manque de coordination peuvent être des signes précoces d'intoxication au lithium et peuvent survenir à des niveaux de lithium inférieurs à 2,0 mEq/L. À des niveaux plus élevés, une ataxie, des vertiges, des acouphènes, une vision floue et une grande quantité d'urine diluée peuvent être observés. Des taux sériques de lithium supérieurs à 3,0 mEq/L peuvent produire un tableau clinique complexe, impliquant plusieurs organes et systèmes d'organes. Les taux sériques de lithium ne doivent pas dépasser 2,0 mEq/L pendant la phase aiguë du traitement.
Les réactions suivantes ont été signalées et semblent être liées aux taux sériques de lithium, y compris des taux se situant dans l'intervalle thérapeutique :
Système neuromusculaire/nerveux central Tremblements, hyperirritabilité musculaire (fasciculations, contractions musculaires, mouvements cloniques de membres entiers), hypertonie, ataxie, mouvements choréo-athétotiques, réflexe tendineux profond hyperactif, symptômes extrapyramidaux dont dystonie aiguë, rigidité de la roue dentée, accès de perte de connaissance, crises épileptiformes, troubles de l'élocution, étourdissements , vertiges, nystagmus déprimé, incontinence d'urine ou de matières fécales, somnolence, retard psychomoteur, agitation, confusion, stupeur, coma, mouvements de la langue, tics, acouphènes, hallucinations, mauvaise mémoire, fonctionnement intellectuel ralenti, réponse surprise, aggravation de syndromes cérébraux organiques, myasthénie grave (rarement).
Cardiovasculaire : Arythmie cardiaque, hypotension, collapsus circulatoire périphérique, bradycardie, dysfonctionnement du nœud sinusal avec bradycardie sévère (pouvant entraîner une syncope).
Gastro-intestinal : Anorexie, nausées, vomissements, diarrhée, gastrite, gonflement des glandes salivaires, douleurs abdominales, salivation excessive, flatulences, indigestion.
Génito-urinaire Glycosurie, diminution de la clairance de la créatinine, albuminurie, oligurie et symptômes de diabète insipide néphrogénique incluant polyurie, soif et polydipsie.
Dermatologique : Sécheresse et amincissement des cheveux, alopécie, anesthésie de la peau, acné, folliculite chronique, xérose cutanée, psoriasis ou son exacerbation, prurit généralisé avec ou sans éruption cutanée, ulcères cutanés, œdème de Quincke.
Autonome : Vision floue, bouche sèche, impuissance/dysfonctionnement sexuel.
Anomalies thyroïdiennes : Goitre euthyroïdien et/ou hypothyroïdie (dont myxœdème) accompagnés de baisse de T3 et T4. L'absorption d'I131 peut être élevée. (Voir PRÉCAUTIONS .) Paradoxalement, de rares cas d'hyperthyroïdie ont été rapportés.
Changements EEG : Ralentissement diffus, élargissement du spectre fréquentiel, potentialisation et désorganisation du rythme de fond.
Modifications ECG : Aplatissement réversible, isoélectricité ou inversion des ondes T. Divers : Fatigue, léthargie, scotomes transitoires, exophtalmie, déshydratation, perte de poids, leucocytose, céphalées, hyperglycémie transitoire, hypercalcémie, hyperparathyroïdie, prise de poids excessive, gonflement œdémateux des chevilles ou des poignets, goût métallique, dysgueusie/altération du goût, goût salé, soif , lèvres enflées, oppression thoracique, articulations enflées et/ou douloureuses, fièvre, polyarthralgie, caries dentaires.
Certains cas de diabète insipide néphrogénique, d'hyperparathyroïdie et d'hypothyroïdie persistant après l'arrêt du lithium ont été signalés.
Quelques rapports ont été reçus concernant le développement d'une décoloration douloureuse des doigts et des orteils et une sensation de froid aux extrémités dans la journée suivant le début du traitement au lithium. Le mécanisme par lequel ces symptômes (ressemblant au syndrome de Raynaud) se sont développés n'est pas connu. La récupération a suivi l'arrêt.
Des cas de pseudotumeur cérébrale (augmentation de la pression intracrânienne et œdème papillaire) ont été signalés avec l'utilisation du lithium. Si elle n'est pas détectée, cette condition peut entraîner un élargissement de la tache aveugle, une constriction des champs visuels et éventuellement une cécité due à une atrophie optique. Le lithium doit être arrêté, si cliniquement possible, si ce syndrome survient.
INTERACTIONS MÉDICAMENTEUSES
La prudence s'impose lorsque le lithium et les diurétiques sont utilisés en concomitance, car la perte de sodium induite par les diurétiques peut réduire la clairance rénale du lithium et augmenter les taux sériques de lithium avec un risque de toxicité au lithium. Les patients recevant un tel traitement combiné doivent faire surveiller étroitement les taux sériques de lithium et ajuster la dose de lithium si nécessaire.
Les taux de lithium doivent être étroitement surveillés lorsque les patients commencent ou arrêtent l'utilisation d'AINS. Dans certains cas, la toxicité du lithium résulte d'interactions entre un AINS et le lithium. Il a été rapporté que l'indométhacine et le piroxicam augmentent de manière significative les concentrations plasmatiques de lithium à l'état d'équilibre. Il existe également des preuves que d'autres agents anti-inflammatoires non stéroïdiens, y compris les inhibiteurs sélectifs de la cyclooxygénase-2 (COX-2), ont le même effet. Dans une étude menée chez des sujets sains, les taux plasmatiques moyens de lithium à l'état d'équilibre ont augmenté d'environ 17 % chez les sujets recevant du lithium 450 mg bid avec du célécoxib 200 mg bid par rapport aux sujets recevant du lithium seul.
L'utilisation concomitante de métronidazole et de lithium peut provoquer une toxicité au lithium en raison d'une diminution de la clairance rénale. Les patients recevant un tel traitement combiné doivent être étroitement surveillés.
Il existe des preuves que les inhibiteurs de l'enzyme de conversion de l'angiotensine, tels que l'énalapril et le captopril, et les antagonistes des récepteurs de l'angiotensine II, tels que le losartan, peuvent augmenter considérablement les taux plasmatiques de lithium à l'état d'équilibre, entraînant parfois une toxicité du lithium. Lorsque de telles combinaisons sont utilisées, la dose de lithium peut devoir être diminuée et les taux plasmatiques de lithium doivent être mesurés plus souvent.
L'utilisation concomitante d'agents bloquant les canaux calciques avec du lithium peut augmenter le risque de neurotoxicité sous forme d'ataxie, de tremblements, de nausées, de vomissements, de diarrhée et/ou d'acouphènes. La prudence est recommandée.
L'administration concomitante de lithium avec des inhibiteurs sélectifs de la recapture de la sérotonine doit être entreprise avec prudence car il a été rapporté que cette association entraîne des symptômes tels que diarrhée, confusion, tremblements, étourdissements et agitation.
Les médicaments suivants peuvent réduire les concentrations sériques de lithium en augmentant l'excrétion urinaire de lithium : acétazolamide, urée, préparations de xanthine et agents alcalinisants tels que le bicarbonate de sodium.
Il a également été démontré que les éléments suivants interagissent avec le lithium : méthyldopa, phénytoïne et carbamazépine.
AVERTISSEMENTS
Le lithium ne doit généralement pas être administré aux patients souffrant d'une maladie rénale ou cardiovasculaire importante, d'un affaiblissement ou d'une déshydratation sévère ou d'une déplétion sodée, car le risque de toxicité du lithium est très élevé chez ces patients. Si l'indication psychiatrique met la vie en danger et si un tel patient ne répond pas aux autres mesures, un traitement au lithium peut être entrepris avec une extrême prudence, y compris des déterminations quotidiennes du lithium sérique et un ajustement aux doses généralement faibles habituellement tolérées par ces personnes. Dans de tels cas, l'hospitalisation est une nécessité.
La thérapie chronique au lithium peut être associée à une diminution de la capacité de concentration rénale, se présentant parfois comme un diabète insipide néphrogénique, avec polyurie et polydipsie. Ces patients doivent être soigneusement pris en charge pour éviter la déshydratation avec la rétention de lithium et la toxicité qui en résultent. Cette condition est généralement réversible lorsque le lithium est arrêté.
Des changements morphologiques avec une fibrose glomérulaire et interstitielle et une atrophie des néphrons ont été rapportés chez des patients sous traitement chronique au lithium. Des modifications morphologiques ont également été observées chez des patients maniaco-dépressifs jamais exposés au lithium. La relation entre les changements fonctionnels et morphologiques rénaux et leur association avec la thérapie au lithium n'a pas été établie.
Lorsque la fonction rénale est évaluée, pour les données de base avant le début de la thérapie au lithium ou par la suite, une analyse d'urine de routine et d'autres tests peuvent être utilisés pour évaluer la fonction tubulaire (p. ) et la fonction glomérulaire (p. ex., créatinine sérique ou clairance de la créatinine). Au cours de la thérapie au lithium, des modifications progressives ou soudaines de la fonction rénale, même dans les limites de la normale, indiquent la nécessité de réévaluer le traitement.
Un syndrome encéphalopathique (caractérisé par une faiblesse, une léthargie, de la fièvre, des tremblements et de la confusion, des symptômes extrapyramidaux, une leucocytose, une élévation des enzymes sériques, de l'azote uréique et du FBS) est survenu chez quelques patients traités au lithium plus un neuroleptique. Dans certains cas, le syndrome a été suivi de lésions cérébrales irréversibles. En raison d'un lien de causalité possible entre ces événements et l'administration concomitante de lithium et de neuroleptiques, les patients recevant un tel traitement combiné doivent être étroitement surveillés afin de détecter tout signe précoce de toxicité neurologique et le traitement doit être interrompu rapidement si de tels signes apparaissent. Ce syndrome encéphalopathique peut être similaire ou identique au syndrome malin des neuroleptiques (SMN).
La toxicité du lithium est étroitement liée aux taux sériques de lithium et peut survenir à des doses proches des taux thérapeutiques (voir DOSAGE ET ADMINISTRATION ).
Les patients ambulatoires et leurs familles doivent être avertis que le patient doit interrompre le traitement au carbonate de lithium et contacter son médecin si des signes cliniques de toxicité au lithium tels que diarrhée, vomissements, tremblements, ataxie légère, somnolence ou faiblesse musculaire surviennent.
Le carbonate de lithium peut altérer les capacités mentales et/ou physiques. Avertir les patients des activités nécessitant de la vigilance (par exemple, faire fonctionner des véhicules ou des machines).
Le lithium peut prolonger les effets des agents bloquants neuromusculaires. Par conséquent, les agents bloquants neuromusculaires doivent être administrés avec prudence aux patients recevant du lithium.
PRÉCAUTIONS
Utilisation pendant la grossesse : Des effets indésirables sur l'implantation chez le rat, la viabilité des embryons chez la souris et le métabolisme in vitro des testicules de rat et des spermatozoïdes humains ont été attribués au lithium, de même que la tératogénicité chez les espèces sous-mammifères et la fente palatine chez la souris.
Chez l'homme, le carbonate de lithium peut nuire au fœtus lorsqu'il est administré à une femme enceinte. Les données des registres des naissances au lithium suggèrent une augmentation des anomalies cardiaques et autres, en particulier l'anomalie d'Ebstein. Si ce médicament est utilisé chez des femmes en âge de procréer, ou pendant la grossesse, ou si une patiente tombe enceinte pendant qu'elle prend ce médicament, la patiente doit être informée du risque potentiel pour le fœtus.
Utilisation chez les mères allaitantes : Le lithium est excrété dans le lait maternel. L'allaitement ne doit pas être entrepris pendant la thérapie au lithium, sauf dans des circonstances rares et inhabituelles où, de l'avis du médecin, les avantages potentiels pour la mère l'emportent sur les risques possibles pour l'enfant.
Utilisation chez les patients pédiatriques : Étant donné que les informations concernant la sécurité et l'efficacité du carbonate de lithium chez les enfants de moins de 12 ans ne sont pas disponibles, son utilisation chez ces patients n'est pas recommandée.
On a signalé un syndrome transitoire de dystonie aiguë et d'hyperréflexie chez un enfant de 15 kg ayant ingéré 300 mg de carbonate de lithium.
Utilisation chez les personnes âgées : Les patients âgés ont souvent besoin de doses de lithium plus faibles pour atteindre des taux sériques thérapeutiques. Ils peuvent également présenter des effets indésirables à des taux sériques habituellement tolérés par les patients plus jeunes.
Général : La capacité à tolérer le lithium est plus grande pendant la phase maniaque aiguë et diminue lorsque les symptômes maniaques s'atténuent (Voir DOSAGE ET ADMINISTRATION ).
L'espace de distribution du lithium se rapproche de celui de l'eau corporelle totale. Le lithium est principalement excrété dans l'urine avec une excrétion insignifiante dans les fèces. L'excrétion rénale du lithium est proportionnelle à sa concentration plasmatique. La demi-vie d'élimination du lithium est d'environ 24 heures. Le lithium diminue la réabsorption du sodium par les tubules rénaux, ce qui pourrait entraîner une déplétion sodée. Par conséquent, il est essentiel que le patient maintienne une alimentation normale, y compris en sel, et un apport hydrique adéquat (2 500 à 3 000 mL) au moins pendant la période de stabilisation initiale. Une diminution de la tolérance au lithium a été rapportée comme résultant d'une transpiration prolongée ou d'une diarrhée et, si cela se produit, un supplément de liquide et de sel doit être administré sous surveillance médicale attentive et l'apport de lithium doit être réduit ou suspendu jusqu'à ce que la condition soit résolue.
En plus de la transpiration et de la diarrhée, une infection concomitante avec des températures élevées peut également nécessiter une réduction temporaire ou l'arrêt de la médication.
Les troubles thyroïdiens sous-jacents préexistants ne constituent pas nécessairement une contre-indication au traitement au lithium ; en cas d'hypothyroïdie, une surveillance attentive de la fonction thyroïdienne pendant la stabilisation au lithium et l'entretien permet de corriger les paramètres thyroïdiens changeants, le cas échéant ; en cas d'hypothyroïdie pendant la stabilisation au lithium et l'entretien, un traitement thyroïdien supplémentaire peut être utilisé.
SURDOSAGE
Les niveaux toxiques pour le lithium sont proches des niveaux thérapeutiques. Il est donc important que les patients et leurs familles soient avertis de surveiller les premiers symptômes toxiques, d'arrêter le médicament et d'informer le médecin s'ils surviennent. Les symptômes toxiques sont énumérés en détail sous RÉACTIONS INDÉSIRABLES.
Traitement : Aucun antidote spécifique pour l'empoisonnement au lithium n'est connu. Les premiers symptômes de la toxicité du lithium peuvent généralement être traités en réduisant ou en arrêtant la posologie du médicament et en reprenant le traitement à une dose plus faible après 24 à 48 heures. Dans les cas graves d'empoisonnement au lithium, l'objectif premier du traitement consiste à éliminer cet ion du patient. Le traitement est essentiellement le même que celui utilisé dans l'empoisonnement aux barbituriques : 1) lavage gastrique, 2) correction du déséquilibre hydrique et électrolytique et 3) régulation de la fonction rénale. L'urée, le mannitol et l'aminophylline produisent tous des augmentations significatives de l'excrétion de lithium. L'hémodialyse est un moyen efficace et rapide d'éliminer l'ion du patient gravement toxique. La prophylaxie des infections, des radiographies pulmonaires régulières et le maintien d'une respiration adéquate sont essentiels.
CONTRE-INDICATIONS
Aucune information fournie.
PHARMACOLOGIE CLINIQUE
ACTIONS
Des études précliniques ont montré que le lithium modifie le transport du sodium dans les cellules nerveuses et musculaires et entraîne un déplacement vers le métabolisme intraneuronal des catécholamines, mais le mécanisme biochimique spécifique de l'action du lithium dans la manie est inconnu.
INFORMATIONS PATIENTS
Aucune information fournie. Veuillez vous référer au AVERTISSEMENTS et PRÉCAUTIONS sections.
