Ditropan 2.5mg, 5mg Oxybutynin Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
Qu'est-ce que Ditropan et comment est-il utilisé ?
Ditropan est un médicament d'ordonnance utilisé pour traiter les symptômes d'une vessie hyperactive. Ditropan 5 mg peut être utilisé seul ou avec d'autres médicaments.
Ditropan appartient à une classe de médicaments appelés agents antispasmodiques urinaires.
On ne sait pas si Ditropan est sûr et efficace chez les enfants de moins de 5 ans.
Quels sont les effets secondaires possibles de Ditropan ?
Ditropan peut provoquer des effets secondaires graves, notamment :
- fortes douleurs à l'estomac,
- constipation,
- Vision floue,
- vision tunnel,
- douleur oculaire,
- voir des halos autour des lumières,
- peu ou pas de miction,
- miction douloureuse ou difficile,
- sensation de soif ou de chaleur,
- être incapable d'uriner,
- transpiration abondante, et
- peau chaude et sèche
Consultez immédiatement un médecin si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires les plus courants de Ditropan incluent :
- vertiges,
- somnolence,
- Vision floue,
- bouche sèche,
- diarrhée, et
- constipation
Dites au médecin si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas.
Ce ne sont pas tous les effets secondaires possibles de Ditropan. Pour plus d'informations, consultez votre médecin ou votre pharmacien.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
LA DESCRIPTION
Chaque comprimé DITROPAN® (chlorure d'oxybutynine) sécable, biconvexe et bleu gravé contient 5 mg de chlorure d'oxybutynine. Chimiquement, le chlorure d'oxybutynine est le chlorhydrate de d,l (racémique) 4-diéthylamino-2-butynyl phénylcyclohexylglycolate. La
La formule empirique du chlorure d'oxybutynine est C22H31NO3•HCl. La formule structurelle apparaît ci-dessous :
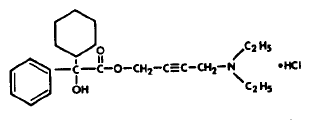
Le chlorure d'oxybutynine est un solide cristallin blanc d'un poids moléculaire de 393,9. Il est facilement soluble dans l'eau et les acides, mais relativement insoluble dans les alcalis.
Les comprimés DITROPAN contiennent également du stéarate de calcium, de la laque FD&C Blue #1, du lactose et de la cellulose microcristalline.
Les comprimés DITROPAN doivent être administrés par voie orale.
Catégorie thérapeutique : Antispasmodique, anticholinergique.
LES INDICATIONS
DITROPAN 2,5 mg XL® (chlorure d'oxybutynine) est un antagoniste muscarinique indiqué pour le traitement de la vessie hyperactive avec des symptômes d'incontinence urinaire par impériosité, d'urgence et de fréquence.
DITROPAN XL® est également indiqué pour le traitement des patients pédiatriques âgés de 6 ans et plus présentant des symptômes d'hyperactivité du détrusor associés à une affection neurologique (par exemple, le spina bifida).
DOSAGE ET ADMINISTRATION
DITROPAN 2,5 mg XL® doit être avalé entier à l'aide de liquides et ne doit pas être mâché, divisé ou écrasé.
DITROPAN XL® peut être administré avec ou sans nourriture.
Adultes
La dose initiale recommandée de DITROPAN 5mg XL® est de 5 ou 10 mg une fois par jour à peu près à la même heure chaque jour. La posologie peut être ajustée par paliers de 5 mg pour atteindre un équilibre entre efficacité et tolérabilité (jusqu'à un maximum de 30 mg/jour). En général, l'adaptation de la posologie peut être effectuée à des intervalles d'environ une semaine.
Patients pédiatriques âgés de 6 ans et plus
La dose initiale recommandée de DITROPAN 5 mg XL® est de 5 mg une fois par jour à peu près à la même heure chaque jour. La posologie peut être ajustée par paliers de 5 mg pour atteindre un équilibre entre efficacité et tolérabilité (jusqu'à un maximum de 20 mg/jour).
COMMENT FOURNIE
Formes posologiques et points forts
Les comprimés à libération prolongée DITROPAN 5 mg XL® sont disponibles sous forme de comprimés de 5 et 10 mg à usage oral :
5mg : Comprimé jaune pâle, rond, avec « 5 XL » imprimé sur une face à l'encre noire.
10 mg Comprimé rose, rond, avec « 10 XL » imprimé sur une face à l'encre noire.
Stockage et manutention
DITROPAN XL® comprimés à libération prolongée sont disponibles en deux dosages, 5 mg (jaune pâle) et 10 mg (rose) et sont imprimés sur un côté avec « 5 XL » ou « 10 XL » à l'encre noire. Les comprimés à libération prolongée DITROPAN XL® sont offerts en flacons de 100 comprimés.
Stockage
Conserver à 25 °C (77 °F); excursions autorisées jusqu'à 15-30 °C (59-86 °F) [voir Température ambiante contrôlée USP ]. Protéger de l'humidité et de l'humidité.
Tenir hors de portée des enfants.
Fabriqué par : ALZA Corporation, Vacaville, CA 95688, un produit technologique ALZA OROS. Fabriqué pour : Janssen Pharmaceuticals, Inc., Titusville, NJ 08560. Révisé : septembre 2019
EFFETS SECONDAIRES
Expérience des essais cliniques
Étant donné que les essais cliniques sont menés dans des conditions très variables, les taux d'effets indésirables observés dans les essais cliniques d'un médicament ne peuvent pas être directement comparés aux taux des essais cliniques d'un autre médicament et peuvent ne pas refléter les taux observés dans la pratique clinique.
L'innocuité et l'efficacité de DITROPAN 2,5 mg XL® (5 à 30 mg/jour) ont été évaluées chez 774 sujets adultes qui ont participé à cinq essais cliniques contrôlés en double aveugle. Dans quatre des cinq études, Ditropan 5 mg IR (5 à 20 mg/jour chez 199 sujets) était un comparateur actif. Les effets indésirables signalés par ≥ 1 % des sujets sont présentés dans le tableau 1.
Le taux d'abandon en raison d'effets indésirables était de 4,4 % avec DITROPAN XL® comparativement à 0 % avec Ditropan IR. L'effet indésirable le plus fréquent entraînant l'arrêt du médicament à l'étude était la bouche sèche (0,7 %).
Les effets indésirables suivants ont été rapportés par Troubles du métabolisme et de la nutrition : anorexie, rétention d'eau; Affections vasculaires : bouffée de chaleur; Troubles respiratoires, thoraciques et médiastinaux : dysphonie; Problèmes gastro-intestinaux: dysphagie, selles fréquentes; Troubles généraux et anomalies au site d'administration : gêne thoracique, soif.
Expérience post-commercialisation
Les effets indésirables supplémentaires suivants ont été signalés dans le monde après la commercialisation de DITROPAN 5 mg XL®. Étant donné que les réactions post-commercialisation sont signalées volontairement par une population de taille incertaine, il n'est pas toujours possible d'estimer de manière fiable leur fréquence ou d'établir une relation causale avec l'exposition au médicament.
Infections et infestations : Infection urinaire; Troubles psychiatriques: trouble psychotique, agitation, état confusionnel, hallucinations, troubles de la mémoire, comportement anormal ; Troubles du système nerveux : convulsions; Troubles oculaires : glaucome; Troubles respiratoires, thoraciques et médiastinaux : congestion nasale; Troubles cardiaques : arythmie, tachycardie, palpitations, allongement de l'intervalle QT ; Troubles vasculaires : bouffées vasomotrices, hypertension; Troubles de la peau et du tissu sous-cutané : éruption; Troubles rénaux et urinaires : impuissance; Troubles généraux et conditions au site d'administration : réactions d'hypersensibilité, y compris œdème de Quincke avec obstruction des voies respiratoires, urticaire et œdème du visage ; réactions anaphylactiques nécessitant une hospitalisation pour un traitement d'urgence ; Blessure, empoisonnement et complications procédurales : chute.
Les événements indésirables supplémentaires signalés avec certaines autres formulations de chlorure d'oxybutynine comprennent : cycloplégie, mydriase et suppression de la lactation. Dans un cas rapporté, l'utilisation concomitante d'oxybutynine avec de la carbamazépine et du dantrolène a été associée à des effets indésirables tels que vomissements, somnolence, confusion, instabilité, troubles de l'élocution et nystagmus, suggérant une toxicité de la carbamazépine.
INTERACTIONS MÉDICAMENTEUSES
L'utilisation concomitante d'oxybutynine avec d'autres médicaments anticholinergiques ou avec d'autres agents provoquant une sécheresse de la bouche, de la constipation, de la somnolence (somnolence) et/ou d'autres effets de type anticholinergique peut augmenter la fréquence et/ou la sévérité de ces effets.
Les agents anticholinergiques peuvent potentiellement altérer l'absorption de certains médicaments administrés de manière concomitante en raison des effets anticholinergiques sur la motilité gastro-intestinale. Cela peut être préoccupant pour les médicaments à index thérapeutique étroit. Les agents anticholinergiques peuvent également antagoniser les effets des agents procinétiques, tels que le métoclopramide.
Les concentrations plasmatiques moyennes d'oxybutynine étaient environ 2 fois plus élevées lorsque DITROPAN 5 mg XL® était administré avec du kétoconazole, un puissant inhibiteur du CYP3A4. D'autres inhibiteurs du système enzymatique du cytochrome P450 3A4, tels que les agents antimycosiques (p. ex., itraconazole et miconazole) ou les antibiotiques macrolides (p. ex., érythromycine et clarithromycine), peuvent modifier les paramètres pharmacocinétiques moyens de l'oxybutynine (c.-à-d. Cmax et ASC). La pertinence clinique de ces interactions potentielles n'est pas connue. La prudence s'impose lorsque de tels médicaments sont co-administrés.
AVERTISSEMENTS
Inclus dans le cadre du PRÉCAUTIONS section.
PRÉCAUTIONS
Angiœdème
Des œdèmes de Quincke du visage, des lèvres, de la langue et/ou du larynx ont été rapportés avec l'oxybutynine. Dans certains cas, un œdème de Quincke est survenu après la première dose. L'œdème de Quincke associé à un gonflement des voies respiratoires supérieures peut mettre la vie en danger. En cas d'atteinte de la langue, de l'hypopharynx ou du larynx, l'oxybutynine doit être rapidement interrompue et un traitement approprié et/ou les mesures nécessaires pour garantir une voie aérienne dégagée doivent être rapidement mises en place.
Effets sur le système nerveux central
L'oxybutynine est associée à des effets anticholinergiques sur le système nerveux central (SNC) [voir EFFETS INDÉSIRABLES ]. Divers effets anticholinergiques sur le SNC ont été signalés, notamment des hallucinations, de l'agitation, de la confusion et de la somnolence. Les patients doivent être surveillés pour des signes d'effets anticholinergiques sur le SNC, en particulier au cours des premiers mois suivant le début du traitement ou l'augmentation de la dose. Conseillez aux patients de ne pas conduire ou utiliser de machinerie lourde jusqu'à ce qu'ils sachent comment DITROPAN XL® les affecte. Si un patient présente des effets anticholinergiques sur le SNC, une réduction de la dose ou l'arrêt du médicament doit être envisagé.
DITROPAN XL® doit être utilisé avec prudence chez les patients atteints de démence préexistante traités avec des inhibiteurs de la cholinestérase en raison du risque d'aggravation des symptômes.
DITROPAN XL® doit être utilisé avec prudence chez les patients atteints de la maladie de Parkinson en raison du risque d'aggravation des symptômes.
Aggravation des symptômes de la myasthénie grave
DITROPAN XL® doit être utilisé avec prudence chez les patients atteints de myasthénie grave en raison du risque d'aggravation des symptômes.
Aggravation des symptômes de diminution de la motilité gastro-intestinale chez les patients atteints de neuropathie autonome
DITROPAN 2,5 mg XL® doit être utilisé avec prudence chez les patients atteints de neuropathie autonome en raison du risque d'aggravation des symptômes de diminution de la motilité gastro-intestinale.
Rétention urinaire
DITROPAN 5 mg XL® doit être administré avec prudence chez les patients présentant une obstruction cliniquement significative de l'évacuation de la vessie en raison du risque de rétention urinaire [voir CONTRE-INDICATIONS ].
Effets indésirables gastro-intestinaux
DITROPAN 2,5 mg XL® doit être administré avec prudence chez les patients présentant des troubles gastro-intestinaux obstructifs en raison du risque de rétention gastrique [voir CONTRE-INDICATIONS ].
DITROPAN XL®, comme d'autres médicaments anticholinergiques, peut diminuer la motilité gastro-intestinale et doit être utilisé avec prudence chez les patients atteints d'affections telles que la colite ulcéreuse et l'atonie intestinale.
DITROPAN 2,5 mg XL® doit être utilisé avec prudence chez les patients souffrant de reflux gastro-œsophagien et/ou prenant simultanément des médicaments (tels que des bisphosphonates) pouvant provoquer ou aggraver une œsophagite.
Comme avec tout autre matériau indéformable, il convient d'être prudent lors de l'administration de DITROPAN XL® à des patients présentant un rétrécissement gastro-intestinal sévère préexistant (pathologique ou iatrogène). De rares cas de symptômes obstructifs ont été rapportés chez des patients présentant des sténoses connues en association avec l'ingestion d'autres médicaments dans des formulations à libération contrôlée indéformables.

Toxicologie non clinique
Carcinogenèse, mutagenèse, altération de la fertilité
Une étude de 24 mois chez le rat à des doses de chlorure d'oxybutynine de 20, 80 et 160 mg/kg/jour n'a montré aucun signe de cancérogénicité. Ces doses sont environ 6, 25 et 50 fois l'exposition humaine maximale, sur la base d'une dose équivalente humaine tenant compte de la normalisation de la surface corporelle.
Le chlorure d'oxybutynine n'a montré aucune augmentation de l'activité mutagène lorsqu'il a été testé dans les systèmes de test Schizosaccharomyces pompholiciformis, Saccharomyces cerevisiae et Salmonella typhimurium.
Les études de reproduction avec le chlorure d'oxybutynine chez la souris, le rat, le hamster et le lapin n'ont montré aucun signe d'altération de la fertilité.
Utilisation dans des populations spécifiques
Grossesse
Catégorie de grossesse B
Il n'y a pas d'études adéquates et bien contrôlées utilisant DITROPAN 5mg XL® chez les femmes enceintes. DITROPAN XL® ne doit être utilisé pendant la grossesse que si les avantages potentiels pour la patiente l'emportent sur les risques pour la patiente et le fœtus. Les femmes qui tombent enceintes pendant le traitement par DITROPAN XL® sont encouragées à contacter leur médecin.
Résumé des risques
Sur la base de données animales, l'oxybutynine devrait avoir une faible probabilité d'augmenter le risque d'effets indésirables sur le développement au-dessus du risque de fond.
Données animales
Les études de reproduction avec le chlorure d'oxybutynine chez la souris, le rat, le hamster et le lapin n'ont montré aucun signe d'altération de la fertilité ou de mal au fœtus de l'animal.
Mères allaitantes
On ne sait pas si l'oxybutynine est excrétée dans le lait maternel. Étant donné que de nombreux médicaments sont excrétés dans le lait maternel, la prudence s'impose lorsque DITROPAN 5 mg XL® est administré à une femme qui allaite.
Utilisation pédiatrique
L'innocuité et l'efficacité de DITROPAN XL® ont été étudiées chez 60 enfants dans le cadre d'un essai ouvert non randomisé de 24 semaines. Les patients étaient âgés de 6 à 15 ans, tous présentaient des symptômes d'hyperactivité du détrusor en association avec une affection neurologique (p. ex., spina bifida), tous utilisaient un cathétérisme intermittent propre et tous étaient des utilisateurs actuels de chlorure d'oxybutynine. Les résultats de l'étude ont démontré que l'administration de DITROPAN 2,5 mg XL® 5 à 20 mg/jour était associée à une augmentation par rapport au départ du volume moyen d'urine par sondage de 108 ml à 136 ml, une augmentation par rapport au départ du volume moyen d'urine après le réveil matinal de 148 mL à 189 mL, et une augmentation par rapport au départ du pourcentage moyen de cathétérismes sans épisode de fuite de 34 % à 51 %.
Les résultats urodynamiques étaient cohérents avec les résultats cliniques. L'administration de DITROPAN XL® a entraîné une augmentation par rapport au départ de la capacité cystométrique maximale moyenne de 185 ml à 254 ml, une diminution par rapport au départ de la pression moyenne du détrusor à la capacité cystométrique maximale de 44 cm H2O à 33 cm H2O et une réduction du pourcentage des patients démontrant des contractions non inhibées du détrusor (d'au moins 15 cm HO) de 60 % à 28 %.
La pharmacocinétique de DITROPAN 5 mg XL® chez ces patients correspondait à celle rapportée chez les adultes [voir PHARMACOLOGIE CLINIQUE ].
DITROPAN 5mg XL® n'est pas recommandé chez les patients pédiatriques qui ne peuvent pas avaler le comprimé entier sans mâcher, diviser ou écraser, ou chez les enfants de moins de 6 ans.
Utilisation gériatrique
Le taux et la sévérité des effets anticholinergiques rapportés par les patients de moins de 65 ans et ceux de 65 ans et plus étaient similaires. La pharmacocinétique de DITROPAN XL® était similaire chez tous les patients étudiés (jusqu'à 78 ans).
Insuffisance rénale
Aucune étude n'a été menée avec DITROPAN XL® chez des patients atteints d'insuffisance rénale.
Insuffisance hépatique
Aucune étude n'a été menée avec DITROPAN 2,5 mg XL® chez des patients atteints d'insuffisance hépatique.
SURDOSAGE
La libération continue d'oxybutynine de DITROPAN 5 mg XL® doit être envisagée dans le traitement d'un surdosage. Les patients doivent être surveillés pendant au moins 24 heures. Le traitement doit être symptomatique et de soutien. Un cathartique peut être administré.
Le surdosage de chlorure d'oxybutynine a été associé à des effets anticholinergiques, notamment une excitation du système nerveux central, des bouffées vasomotrices, de la fièvre, une déshydratation, une arythmie cardiaque, des vomissements et une rétention urinaire.
L'ingestion de 100 mg de chlorure d'oxybutynine en association avec de l'alcool a été rapportée chez un garçon de 13 ans qui a perdu la mémoire et chez une femme de 34 ans qui a développé une stupeur, suivie d'une désorientation et d'une agitation au réveil, des pupilles dilatées, une sécheresse peau, arythmie cardiaque et rétention d'urine. Les deux patients se sont complètement rétablis avec un traitement symptomatique.
CONTRE-INDICATIONS
DITROPAN 2,5 mg XL® est contre-indiqué chez les patients souffrant de rétention urinaire, de rétention gastrique et d'autres troubles sévères de la motilité gastro-intestinale diminuée, de glaucome à angle fermé non contrôlé.
DITROPAN 2,5 mg XL® est également contre-indiqué chez les patients qui ont démontré une hypersensibilité à la substance médicamenteuse ou à d'autres composants du produit. Des cas de réactions d'hypersensibilité, notamment d'anaphylaxie et d'œdème de Quincke, ont été signalés.
PHARMACOLOGIE CLINIQUE
Mécanisme d'action
L'oxybutynine détend le muscle lisse de la vessie. Le chlorure d'oxybutynine exerce un effet antispasmodique direct sur les muscles lisses et inhibe l'action muscarinique de l'acétylcholine sur les muscles lisses. Aucun effet bloquant ne se produit au niveau des jonctions neuromusculaires squelettiques ou des ganglions autonomes (effets antinicotiniques).
L'activité antimuscarinique réside principalement dans l'isomère R. Un métabolite, la déséthyloxybutynine, a une activité pharmacologique similaire à celle de l'oxybutynine dans les études in vitro.
Pharmacodynamie
Chez les patients atteints d'affections caractérisées par des contractions involontaires de la vessie, des études cystométriques ont démontré que l'oxybutynine augmente la capacité de la vessie (vésicale), diminue la fréquence des contractions non inhibées du muscle détrusor et retarde le désir initial d'uriner.
Pharmacocinétique
Absorption
Après la première dose de DITROPAN XL®, les concentrations plasmatiques d'oxybutynine augmentent pendant 4 à 6 heures; par la suite, des concentrations stables sont maintenues jusqu'à 24 heures, minimisant les fluctuations entre les concentrations maximales et minimales associées à l'oxybutynine.
Les biodisponibilités relatives de la R- et S-oxybutynine de DITROPAN XL® sont de 156 % et 187 %, respectivement, par rapport à l'oxybutynine. Les paramètres pharmacocinétiques moyens pour la R- et la S-oxybutynine sont résumés dans le tableau 2. Les profils de concentration plasmatique en fonction du temps pour la R- et la S-oxybutynine sont de forme similaire ; La figure 1 montre le profil de la R-oxybutynine.
Figure 1 : Concentrations plasmatiques moyennes de R-oxybutynine suite à une dose unique de DITROPAN XL® 10 mg et d'oxybutynine 5 mg administrée toutes les 8 heures (n = 23 pour chaque traitement).
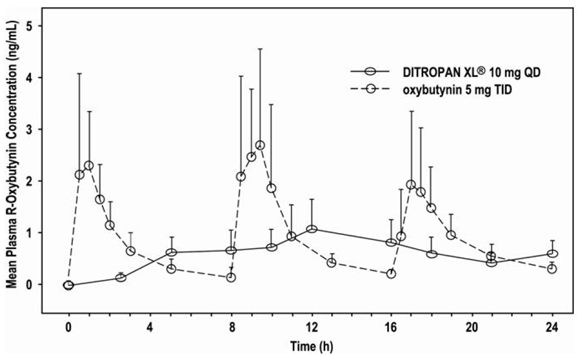
Les concentrations plasmatiques d'oxybutynine à l'état d'équilibre sont atteintes au jour 3 d'administrations répétées de DITROPAN XL®, sans accumulation de médicament observée ni modification des paramètres pharmacocinétiques de l'oxybutynine et de la déséthyloxybutynine.
La pharmacocinétique à l'état d'équilibre de DITROPAN 5 mg XL® a été étudiée chez 19 enfants âgés de 5 à 15 ans présentant une hyperactivité du détrusor associée à une affection neurologique (par exemple, le spina bifida). Les enfants recevaient DITROPAN 2,5 mg XL® à une dose quotidienne totale allant de 5 à 20 mg (0,10 à 0,77 mg/kg). Une technique d'échantillonnage clairsemé a été utilisée pour obtenir des échantillons de sérum. Lorsque toutes les données disponibles sont normalisées à un équivalent de 5 mg par jour de DITROPAN XL®, les paramètres pharmacocinétiques moyens dérivés pour la R- et S-oxybutynine et la R- et S-déséthyloxybutynine sont résumés dans le tableau 3. Les profils de concentration plasmatique-temps pour R- et S-oxybutynine sont de forme similaire; La figure 2 montre le profil de la R-oxybutynine lorsque toutes les données disponibles sont normalisées à un équivalent de 5 mg par jour.
Figure 2 : Concentrations plasmatiques moyennes de R-oxybutynine à l'état d'équilibre (± ET) après administration de 5 à 20 mg de DITROPAN 5 mg XL® une fois par jour chez les enfants âgés de 5 à 15 ans. Le graphique représente toutes les données disponibles normalisées à un équivalent de DITROPAN XL® 5 mg une fois par jour.
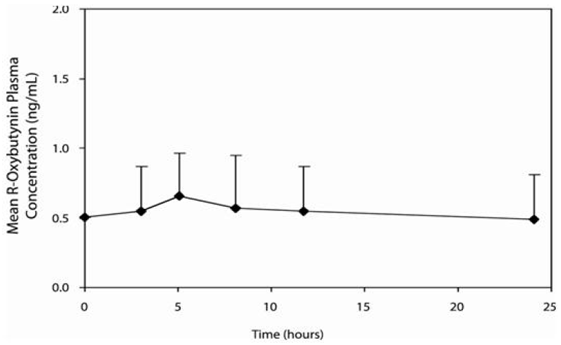
Effets alimentaires
Le taux et l'étendue de l'absorption et du métabolisme de l'oxybutynine sont similaires à jeun et à jeun.
Distribution
L'oxybutynine est largement distribuée dans les tissus de l'organisme après absorption systémique. Le volume de distribution est de 193 L après administration intraveineuse de 5 mg de chlorure d'oxybutynine. Les deux énantiomères de l'oxybutynine sont fortement liés (> 99 %) aux protéines plasmatiques. Les deux énantiomères de la N-déséthyloxybutynine sont également fortement liés (> 97 %) aux protéines plasmatiques. La principale protéine de liaison est la glycoprotéine acide alpha-1.
Métabolisme
L'oxybutynine est métabolisée principalement par les systèmes enzymatiques du cytochrome P450, en particulier le CYP3A4 que l'on trouve principalement dans le foie et la paroi intestinale. Ses produits métaboliques comprennent l'acide phénylcyclohexylglycolique, qui est pharmacologiquement inactif, et la déséthyloxybutynine, qui est pharmacologiquement active. Suite à l'administration de DITROPAN 2,5 mg XL®, les concentrations plasmatiques de R- et S-déséthyloxybutynine sont respectivement de 73 % et 92 % des concentrations observées avec l'oxybutynine.
Excrétion
L'oxybutynine est largement métabolisée par le foie, moins de 0,1 % de la dose administrée étant excrétée sous forme inchangée dans l'urine. De plus, moins de 0,1 % de la dose administrée est excrétée sous forme de métabolite déséthyloxybutynine.
Proportionnalité des doses
Les paramètres pharmacocinétiques de l'oxybutynine et de la déséthyloxybutynine (Cmax et ASC) après l'administration de 5 à 20 mg de DITROPAN 5 mg XL® sont proportionnels à la dose.
Utilisation dans des populations spécifiques
Pédiatrique
La pharmacocinétique de DITROPAN 2,5 mg XL® a été évaluée chez 19 enfants âgés de 5 à 15 ans présentant une hyperactivité du détrusor associée à une affection neurologique (par exemple, le spina bifida). La pharmacocinétique de DITROPAN 2,5 mg XL® chez ces patients pédiatriques correspondait à celle rapportée chez les adultes (voir les tableaux 2 et 3 et les figures 1 et 2 ci-dessus).
Le genre
Il n'y a pas de différences significatives dans la pharmacocinétique de l'oxybutynine chez des volontaires sains de sexe masculin et féminin après l'administration de DITROPAN 2,5 mg XL®.
Course
Les données disponibles suggèrent qu'il n'y a pas de différences significatives dans la pharmacocinétique de l'oxybutynine basée sur la race chez les volontaires sains après l'administration de DITROPAN 2,5 mg XL®.
Etudes cliniques
DITROPAN 5 mg XL® a été évalué pour le traitement des patients atteints d'hyperactivité vésicale présentant des symptômes d'incontinence urinaire par impériosité, d'urgence et de fréquence dans trois études d'efficacité contrôlées. La majorité des patients étaient de race blanche (89,0 %) et de sexe féminin (91,9 %) avec un âge moyen de 59 ans (extrêmes, 18 à 98 ans). Les critères d'entrée exigeaient que les patients aient une incontinence par impériosité ou mixte (avec une prédominance d'incontinence par impériosité) comme en témoignent ≥ 6 épisodes d'incontinence par impériosité par semaine et ≥ 10 mictions par jour. L'étude 1 était un plan d'augmentation de dose fixe, tandis que les deux autres études utilisaient un plan d'ajustement de dose dans lequel la dose finale de chaque patient était ajustée en fonction d'un équilibre entre l'amélioration des symptômes d'incontinence et la tolérabilité des effets secondaires. Les trois études incluaient des patients connus pour être réactifs à l'oxybutynine ou à d'autres médicaments anticholinergiques, et ces patients ont été maintenus sur une dose finale jusqu'à 2 semaines.
Les résultats d'efficacité pour les trois essais contrôlés sont présentés dans les tableaux 4, 5 et 6 suivants et les figures 3, 4 et 5.
Figure 3 : Changement moyen (±ET) des épisodes d'incontinence urinaire par impériosité par semaine depuis le départ (étude 1)
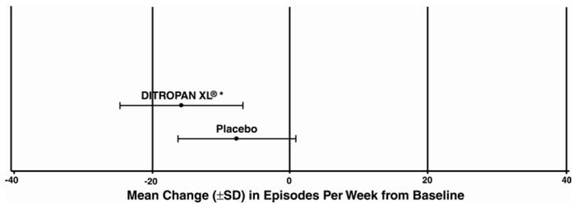
Figure 4 : Changement moyen (± ET) des épisodes d'incontinence urinaire par impériosité par semaine depuis le départ (étude 2)
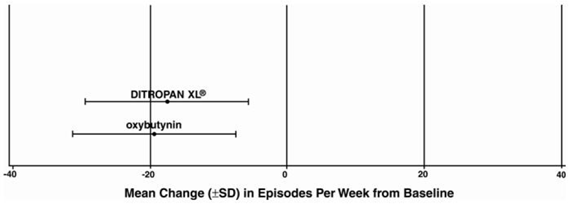
Figure 5 : Changement moyen (±ET) des épisodes d'incontinence urinaire par impériosité par semaine depuis le départ (étude 3)
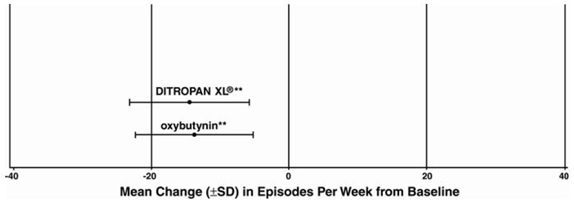
INFORMATIONS PATIENTS
- Les patients doivent être informés que l'oxybutynine peut provoquer un œdème de Quincke susceptible d'entraîner une obstruction des voies respiratoires potentiellement mortelle. Les patients doivent être avisés d'arrêter rapidement le traitement par l'oxybutynine et de consulter immédiatement un médecin s'ils présentent un gonflement de la langue, un œdème du laryngopharynx ou des difficultés respiratoires.
- Les patients doivent être informés que les agents anticholinergiques (antimuscariniques) tels que DITROPAN XL® peuvent produire des effets indésirables cliniquement significatifs liés à l'activité anticholinergique tels que :
- Rétention urinaire et constipation
- Chaleur prostration due à une diminution de la transpiration. Une prostration par la chaleur peut survenir lorsque des médicaments anticholinergiques sont administrés en présence d'une température ambiante élevée.
- Les patients doivent être informés que les médicaments anticholinergiques tels que DITROPAN 5 mg XL® peuvent entraîner une somnolence (somnolence), des étourdissements ou une vision floue. Les patients doivent être avisés de faire preuve de prudence lorsqu'ils décident de s'engager dans des activités potentiellement dangereuses jusqu'à ce que les effets de DITROPAN XL® aient été déterminés.
- Les patients doivent être informés que l'alcool peut augmenter la somnolence causée par les agents anticholinergiques tels que DITROPAN XL®.
- Les patients doivent être informés que DITROPAN 5 mg XL® doit être avalé entier à l'aide de liquides. Les patients ne doivent pas mâcher, diviser ou écraser les comprimés. Le médicament est contenu dans une enveloppe non résorbable conçue pour libérer le médicament à une vitesse contrôlée. La coque du comprimé est éliminée du corps ; les patients ne doivent pas s'inquiéter s'ils remarquent occasionnellement dans leurs selles quelque chose qui ressemble à un comprimé.
- DITROPAN 5 mg XL® doit être pris à peu près à la même heure chaque jour.
