Ponstel 250mg, 500mg Mefenamic Acid Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
PONSTEL® (acide méfénamique) Capsules, USP 250 mg
Risque cardiovasculaire
- Les AINS peuvent entraîner un risque accru d'événements thrombotiques cardiovasculaires graves, d'infarctus du myocarde et d'accident vasculaire cérébral, qui peuvent être mortels. Ce risque peut augmenter avec la durée d'utilisation. Les patients atteints de maladies cardiovasculaires ou présentant des facteurs de risque de maladies cardiovasculaires peuvent être plus à risque (voir AVERTISSEMENTS ).
- PONSTEL® (acide méfénamique) est contre-indiqué pour le traitement de la douleur périopératoire dans le cadre d'un pontage coronarien (PAC) (voir AVERTISSEMENTS ).
Risque gastro-intestinal
- Les AINS entraînent un risque accru d'événements indésirables gastro-intestinaux graves, notamment des saignements, des ulcérations et des perforations de l'estomac ou des intestins, qui peuvent être fatals. Ces événements peuvent survenir à tout moment pendant l'utilisation et sans symptômes d'avertissement. Les patients âgés sont plus à risque d'événements gastro-intestinaux graves (voir AVERTISSEMENTS ).
LA DESCRIPTION
Ponstel® (acide méfénamique) fait partie du groupe fénamate des anti-inflammatoires non stéroïdiens (AINS). Chaque capsule ivoire à bandes bleues contient 250 mg d'acide méfénamique pour administration orale. L'acide méfénamique est une poudre microcristalline blanche à blanc grisâtre, inodore, avec un point de fusion de 230°-231°C et une solubilité dans l'eau de 0,004 % à pH 7,1. Le nom chimique est l'acide N-2,3-xylylanthranilique. Le poids moléculaire est de 241,29. Sa formule moléculaire est C15H15NO2 et la formule structurale de l'acide méfénamique est :
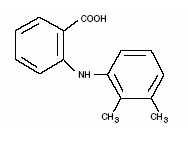
Chaque gélule contient également du lactose, NF. L'enveloppe et/ou la bande de la gélule contient de l'acide citrique, USP ; D&C jaune n° 10 ; FD&C bleu n° 1 ; FD&C rouge n° 3 ; FD&C jaune n° 6 ; gélatine, NF; monooléate de glycérol; dioxyde de silicium, NF; benzoate de sodium, NF; le laurylsulfate de sodium, NF; dioxyde de titane, USP.
LES INDICATIONS
Examinez attentivement les avantages et les risques potentiels de PONSTEL (acide méfénamique) et des autres options de traitement avant de décider d'utiliser PONSTEL (acide méfénamique) . Utiliser la dose efficace la plus faible pendant la durée la plus courte compatible avec les objectifs de traitement individuels du patient (voir AVERTISSEMENTS ).
PONSTEL (acide méfénamique) est indiqué :
- Pour le soulagement de la douleur légère à modérée chez les patients âgés de 14 ans et plus, lorsque le traitement ne dépassera pas une semaine (7 jours).
- Pour le traitement de la dysménorrhée primaire.
DOSAGE ET ADMINISTRATION
Examinez attentivement les avantages et les risques potentiels de PONSTEL (acide méfénamique) et des autres options de traitement avant de décider d'utiliser PONSTEL (acide méfénamique) . Utiliser la dose efficace la plus faible pendant la durée la plus courte compatible avec les objectifs de traitement individuels du patient (voir AVERTISSEMENTS ).
Après avoir observé la réponse au traitement initial par PONSTEL (acide méfénamique), la dose et la fréquence doivent être ajustées en fonction des besoins de chaque patient.
Pour le soulagement de la douleur aiguë chez les adultes et les adolescents de 14 ans et plus, la dose recommandée est de 500 mg comme dose initiale suivie de 250 mg toutes les 6 heures au besoin, ne dépassant généralement pas une semaine.4
Pour le traitement de la dysménorrhée primaire, la dose recommandée est de 500 mg en dose initiale suivie de 250 mg toutes les 6 heures, administrés par voie orale, en commençant par l'apparition des saignements et des symptômes associés. Des études cliniques indiquent qu'un traitement efficace peut être initié dès le début des règles et ne devrait pas être nécessaire pendant plus de 2 à 3 jours.5
COMMENT FOURNIE
Ponstel (acide méfénamique) est disponible sous forme de capsules ivoire à bandes bleues de 250 mg, portant les inscriptions « FHPC 400 » et « PONSTEL® (acide méfénamique) ».
EFFETS SECONDAIRES
Chez les patients prenant du Ponstel (acide méfénamique) ou d'autres AINS, les effets indésirables les plus fréquemment rapportés survenant chez environ 1 à 10 % des patients sont :
Expériences gastro-intestinales, y compris - douleurs abdominales, constipation, diarrhée, dyspepsie, flatulences, saignements/perforations importants, brûlures d'estomac, nausées, ulcères gastro-intestinaux (gastriques/duodénaux), vomissements, fonction rénale anormale, anémie, étourdissements, œdème, élévation des enzymes hépatiques, maux de tête, augmentation du temps de saignement, prurit, éruptions cutanées, acouphènes
Les effets indésirables supplémentaires rapportés occasionnellement et répertoriés ici par système corporel incluent :
Corps dans son ensemble - fièvre, infection, septicémie
Système cardiovasculaire - insuffisance cardiaque congestive, hypertension, tachycardie, syncope
Système digestif - bouche sèche, œsophagite, ulcères gastriques/peptiques, gastrite, saignement gastro-intestinal, glossite, hématémèse, hépatite, ictère
Système sanguin et lymphatique - ecchymoses, éosinophilie, leucopénie, méléna, purpura, saignement rectal, stomatite, thrombocytopénie
Métabolique et nutritionnel - changements de poids
Système nerveux anxiété, asthénie, confusion, dépression, troubles des rêves, somnolence ; insomnie, malaise, nervosité, paresthésie, somnolence, tremblements, vertige
Système respiratoire - asthme, dyspnée
Peau et phanères - alopécie, photosensibilité, prurit, sudation
Sens spéciaux - Vision floue
Système urogénital - cystite, dysurie, hématurie, néphrite interstitielle, oligurie/polyurie, protéinurie, insuffisance rénale
Les autres effets indésirables, qui surviennent rarement, sont :
Corps dans son ensemble - réactions anaphylactoïdes, changements d'appétit, mort
Système cardiovasculaire - arythmie, hypotension, infarctus du myocarde, palpitations, vascularite
Système digestif - éructation, insuffisance hépatique, pancréatite
Système sanguin et lymphatique - agranulocytose, anémie hémolytique, anémie aplasique, lymphadénopathie, pancytopénie
Métabolique et nutritionnel - hyperglycémie
Système nerveux - convulsions, coma, hallucinations, méningite.
Respiratoire dépression respiratoire, pneumonie
Peau et phanères - œdème de Quincke, nécrose épidermique toxique, érythème polymorphe, dermatite exfoliative, syndrome de Stevens-Johnson, urticaire
Sens spéciaux - conjonctivite, déficience auditive
INTERACTIONS MÉDICAMENTEUSES
Un certain nombre de composés sont des inhibiteurs du CYP2C9. Aucune étude sur les interactions médicamenteuses de l'acide méfénamique et de ces composés n'a été menée. La possibilité d'une sécurité et d'une efficacité altérées doit être envisagée lorsque Ponstel (acide méfénamique) est utilisé en concomitance avec ces médicaments.
Inhibiteurs de l'ECA
Des rapports suggèrent que les AINS pourraient diminuer l'effet antihypertenseur des inhibiteurs de l'ECA. Cette interaction doit être prise en compte chez les patients prenant des AINS en même temps que des inhibiteurs de l'ECA.
Aspirine
Lorsque PONSTEL (acide méfénamique) est administré avec de l'aspirine, sa liaison aux protéines est réduite, bien que la clairance de PONSTEL (acide méfénamique) libre ne soit pas altérée. La signification clinique de cette interaction n'est pas connue ; cependant, comme avec d'autres AINS, l'administration concomitante d'ACIDE MEFÉNAMIQUE et d'aspirine n'est généralement pas recommandée en raison du risque d'effets indésirables accrus.
Diurétiques
Des études cliniques, ainsi que des observations post-commercialisation, ont montré que PONSTEL (acide méfénamique) peut réduire l'effet natriurétique du furosémide et des thiazides chez certains patients. Cette réponse a été attribuée à l'inhibition de la synthèse rénale des prostaglandines. Lors d'un traitement concomitant par AINS, le patient doit être étroitement surveillé afin de détecter tout signe d'insuffisance rénale (voir PRÉCAUTIONS, Effets rénaux ), ainsi que pour assurer l'efficacité diurétique.
Lithium
Les AINS ont entraîné une élévation des taux plasmatiques de lithium et une réduction de la clairance rénale du lithium. La concentration minimale moyenne de lithium a augmenté de 15 % et la clairance rénale a diminué d'environ 20 %. Ces effets ont été attribués à l'inhibition de la synthèse rénale des prostaglandines par les AINS. Ainsi, lorsque des AINS et du lithium sont administrés simultanément, les sujets doivent être surveillés attentivement pour détecter des signes de toxicité au lithium.
Méthotrexate
Il a été rapporté que les AINS inhibent de manière compétitive l'accumulation de méthotrexate dans les tranches de rein de lapin. Cela peut indiquer qu'ils pourraient augmenter la toxicité du méthotrexate. La prudence s'impose lorsque des AINS sont administrés en concomitance avec le méthotrexate.
Warfarine
Les effets de la warfarine et des AINS sur les saignements gastro-intestinaux sont synergiques, de sorte que les utilisateurs des deux médicaments ensemble ont un risque de saignements gastro-intestinaux graves plus élevé que les utilisateurs de l'un ou l'autre médicament seul.
Antiacides
Dans une étude à dose unique (n=6), l'ingestion d'un antiacide contenant 1,7 gramme d'hydroxyde de magnésium avec 500 mg d'acide méfénamique a augmenté la Cmax et l'ASC de l'acide méfénamique de 125 % et 36 %, respectivement.1
Interactions médicament/test de laboratoire
Ponstel (acide méfénamique) peut prolonger le temps de prothrombine.4 Par conséquent, lorsque le médicament est administré à des patients recevant des anticoagulants oraux, une surveillance fréquente du temps de prothrombine est nécessaire.
Une réaction faussement positive pour la bile urinaire, en utilisant le test du comprimé diazoïque, peut survenir après l'administration d'acide méfénamique. Si une biliurie est suspectée, d'autres procédures de diagnostic, telles que le test ponctuel de Harrison, doivent être effectuées.
RÉFÉRENCES
4. Glazko AJ : Observations expérimentales des acides flufénamique, méfénamique et méclofénamique. Partie III. Disposition métabolique, dans Fenamates in Medicine. A Symposium, Londres, 1966. Annals of Physical Medicine, Supplément, pp 23-36, 1967.
AVERTISSEMENTS
Effets cardiovasculaires
Événements thrombotiques cardiovasculaires
Des essais cliniques de plusieurs AINS sélectifs et non sélectifs de la COX-2 d'une durée allant jusqu'à trois ans ont montré un risque accru d'événements thrombotiques cardiovasculaires (CV) graves, d'infarctus du myocarde et d'accident vasculaire cérébral, qui peuvent être mortels. Tous les AINS, à la fois sélectifs et non sélectifs de la COX-2, peuvent avoir un risque similaire. Les patients présentant une maladie CV connue ou des facteurs de risque de maladie CV peuvent être plus à risque. Afin de minimiser le risque potentiel d'événement CV indésirable chez les patients traités par un AINS, la dose efficace la plus faible doit être utilisée pendant la durée la plus courte possible. Les médecins et les patients doivent rester attentifs à l'apparition de tels événements, même en l'absence de symptômes CV antérieurs. Les patients doivent être informés des signes et/ou symptômes d'événements CV graves et des mesures à prendre s'ils surviennent.
Il n'existe aucune preuve cohérente que l'utilisation concomitante d'aspirine atténue le risque accru d'événements thrombotiques CV graves associés à l'utilisation d'AINS. L'utilisation concomitante d'aspirine et d'un AINS augmente le risque d'événements gastro-intestinaux graves (voir MISES EN GARDE GI ).
Deux grands essais cliniques contrôlés portant sur un AINS sélectif de la COX-2 pour le traitement de la douleur au cours des 10 à 14 premiers jours suivant un PAC ont révélé une incidence accrue d'infarctus du myocarde et d'accident vasculaire cérébral (voir CONTRE-INDICATIONS ).
Hypertension
Les AINS, y compris PONSTEL (acide méfénamique), peuvent entraîner l'apparition d'une nouvelle hypertension ou l'aggravation d'une hypertension préexistante, l'un ou l'autre pouvant contribuer à l'augmentation de l'incidence des événements CV. Les patients prenant des thiazidiques ou des diurétiques de l'anse peuvent présenter une réponse altérée à ces traitements lorsqu'ils prennent des AINS. Les AINS, y compris PONSTEL (acide méfénamique), doivent être utilisés avec prudence chez les patients hypertendus. La tension artérielle (TA) doit être étroitement surveillée au début du traitement par AINS et tout au long du traitement.
Insuffisance cardiaque congestive et œdème
Une rétention hydrique et un œdème ont été observés chez certains patients prenant des AINS. PONSTEL (acide méfénamique) doit être utilisé avec prudence chez les patients souffrant de rétention hydrique ou d'insuffisance cardiaque.
Effets gastro-intestinaux - Risque d'ulcération, de saignement et de perforation
Les AINS, y compris PONSTEL (acide méfénamique), peuvent provoquer des effets indésirables gastro-intestinaux (GI) graves, notamment une inflammation, des saignements, une ulcération et une perforation de l'estomac, de l'intestin grêle ou du gros intestin, qui peuvent être fatals. Ces événements indésirables graves peuvent survenir à tout moment, avec ou sans symptômes précurseurs, chez les patients traités par AINS. Seul un patient sur cinq, qui développe un événement indésirable gastro-intestinal supérieur grave sous traitement par AINS, est symptomatique. Des ulcères gastro-intestinaux supérieurs, des saignements macroscopiques ou des perforations causés par les AINS surviennent chez environ 1 % des patients traités pendant 3 à 6 mois et chez environ 2 à 4 % des patients traités pendant un an. Ces tendances se poursuivent avec une durée d'utilisation plus longue, augmentant la probabilité de développer un événement gastro-intestinal grave à un moment donné au cours du traitement. Cependant, même une thérapie à court terme n'est pas sans risque.
Les AINS doivent être prescrits avec une extrême prudence chez les personnes ayant des antécédents d'ulcère ou d'hémorragie gastro-intestinale. Les patients ayant des antécédents d'ulcère peptique et/ou d'hémorragie gastro-intestinale qui utilisent des AINS ont un risque plus de 10 fois plus élevé de développer une hémorragie gastro-intestinale par rapport aux patients ne présentant aucun de ces facteurs de risque. D'autres facteurs qui augmentent le risque d'hémorragie gastro-intestinale chez les patients traités par AINS comprennent l'utilisation concomitante de corticostéroïdes oraux ou d'anticoagulants, une durée plus longue du traitement par AINS, le tabagisme, la consommation d'alcool, l'âge avancé et un mauvais état de santé général. La plupart des rapports spontanés d'événements gastro-intestinaux mortels concernent des patients âgés ou affaiblis et, par conséquent, des précautions particulières doivent être prises lors du traitement de cette population.
Afin de minimiser le risque potentiel d'événement GI indésirable chez les patients traités par un AINS, la dose efficace la plus faible doit être utilisée pendant la durée la plus courte possible. Les patients et les médecins doivent rester attentifs aux signes et symptômes d'ulcération et de saignement gastro-intestinaux pendant le traitement par AINS et initier rapidement une évaluation et un traitement supplémentaires si un événement indésirable gastro-intestinal grave est suspecté. Cela devrait inclure l'arrêt de l'AINS jusqu'à ce qu'un événement indésirable gastro-intestinal grave soit exclu. Pour les patients à haut risque, des thérapies alternatives qui n'impliquent pas d'AINS doivent être envisagées.
Effets rénaux
L'administration à long terme d'AINS a entraîné une nécrose papillaire rénale et d'autres lésions rénales. Une toxicité rénale a également été observée chez des patients chez qui les prostaglandines rénales ont un rôle compensateur dans le maintien de la perfusion rénale. Chez ces patients, l'administration d'un anti-inflammatoire non stéroïdien peut entraîner une réduction dose-dépendante de la formation des prostaglandines et, accessoirement, du débit sanguin rénal, ce qui peut précipiter une décompensation rénale manifeste. Les patients les plus à risque de cette réaction sont ceux qui présentent une fonction rénale altérée, une insuffisance cardiaque, un dysfonctionnement hépatique, ceux qui prennent des diurétiques et des inhibiteurs de l'ECA et les personnes âgées. L'arrêt du traitement par AINS est généralement suivi d'un retour à l'état antérieur au traitement.
Maladie rénale avancée
Aucune information n'est disponible pour des études contrôlées concernant l'utilisation de PONSTEL (acide méfénamique) chez les patients atteints d'insuffisance rénale avancée. Par conséquent, le traitement par PONSTEL (acide méfénamique) n'est pas recommandé chez ces patients atteints d'insuffisance rénale avancée (voir CONTRE-INDICATIONS ).
Réactions anaphylactoïdes
Comme avec d'autres AINS, des réactions anaphylactoïdes peuvent survenir chez des patients n'ayant jamais été exposés à PONSTEL (acide méfénamique) . PONSTEL (acide méfénamique) ne doit pas être administré aux patients atteints de la triade de l'aspirine. Ce complexe de symptômes survient généralement chez les patients asthmatiques qui présentent une rhinite avec ou sans polypes nasaux, ou qui présentent un bronchospasme sévère, potentiellement mortel, après avoir pris de l'aspirine ou d'autres AINS (voir CONTRE-INDICATIONS et PRÉCAUTIONS - Asthme préexistant ). Une aide d'urgence doit être recherchée dans les cas où une réaction anaphylactoïde se produit.
Réactions cutanées
Les AINS, y compris PONSTEL (acide méfénamique), peuvent provoquer des effets indésirables cutanés graves tels que la dermatite exfoliative, le syndrome de Stevens-Johnson (SJS) et la nécrolyse épidermique toxique (TEN), qui peuvent être fatals. Ces événements graves peuvent survenir sans avertissement. Les patients doivent être informés des signes et symptômes des manifestations cutanées graves et l'utilisation du médicament doit être interrompue dès la première apparition d'une éruption cutanée ou de tout autre signe d'hypersensibilité.
Grossesse
En fin de grossesse, comme avec les autres AINS, PONSTEL (acide méfénamique) doit être évité car il peut provoquer une fermeture prématurée du canal artériel.
PRÉCAUTIONS
Général
On ne peut pas s'attendre à ce que PONSTEL (acide méfénamique) se substitue aux corticostéroïdes ou traite l'insuffisance de corticostéroïdes. L'arrêt brutal des corticostéroïdes peut entraîner une exacerbation de la maladie. Les patients sous corticothérapie prolongée doivent voir leur traitement diminuer lentement si une décision est prise d'arrêter les corticoïdes.
L'activité pharmacologique de PONSTEL (acide méfénamique) dans la réduction de la fièvre et de l'inflammation peut diminuer l'utilité de ces signes diagnostiques dans la détection des complications d'affections douloureuses présumées non infectieuses.
Effets hépatiques
Des élévations limites d'un ou de plusieurs tests hépatiques peuvent survenir chez jusqu'à 15 % des patients prenant des AINS, y compris PONSTEL (acide méfénamique) . Ces anomalies biologiques peuvent progresser, rester inchangées ou être transitoires avec la poursuite du traitement. Des élévations notables de l'ALT ou de l'AST (environ trois fois ou plus la limite supérieure de la normale) ont été signalées chez environ 1 % des patients dans les essais cliniques avec des AINS. De plus, de rares cas de réactions hépatiques sévères, incluant ictère et hépatite fulminante mortelle, nécrose hépatique et insuffisance hépatique, dont certaines avec issue fatale, ont été rapportés.
Un patient présentant des symptômes et/ou des signes évoquant un dysfonctionnement hépatique, ou chez qui un test hépatique anormal s'est produit, doit être évalué à la recherche de signes de développement d'une réaction hépatique plus grave pendant le traitement par PONSTEL (acide méfénamique) . Si des signes cliniques et des symptômes compatibles avec une maladie du foie se développent ou si des manifestations systémiques surviennent (p. ex., éosinophilie, éruption cutanée, etc.), PONSTEL (acide méfénamique) doit être interrompu.
Effets hématologiques
L'anémie est parfois observée chez les patients recevant des AINS, y compris PONSTEL (acide méfénamique) . Cela peut être dû à une rétention hydrique, à une perte de sang gastro-intestinal ou à un effet incomplètement décrit sur l'érythropoïèse. Les patients sous traitement à long terme avec des AINS, y compris PONSTEL (acide méfénamique), doivent faire vérifier leur hémoglobine ou leur hématocrite s'ils présentent des signes ou des symptômes d'anémie. Les AINS inhibent l'agrégation plaquettaire et il a été démontré qu'ils prolongent le temps de saignement chez certains patients. Contrairement à l'aspirine, leur effet sur la fonction plaquettaire est quantitativement moindre, de plus courte durée et réversible. Les patients recevant PONSTEL (acide méfénamique) susceptibles d'être affectés par des altérations de la fonction plaquettaire, tels que ceux présentant des troubles de la coagulation ou les patients recevant des anticoagulants, doivent être étroitement surveillés.
Asthme préexistant
Les patients asthmatiques peuvent avoir un asthme sensible à l'aspirine. L'utilisation d'aspirine chez les patients souffrant d'asthme sensible à l'aspirine a été associée à un bronchospasme sévère qui peut être fatal. Étant donné qu'une réactivité croisée, y compris un bronchospasme, entre l'aspirine et d'autres anti-inflammatoires non stéroïdiens a été signalée chez ces patients sensibles à l'aspirine, PONSTEL (acide méfénamique) ne doit pas être administré aux patients présentant cette forme de sensibilité à l'aspirine et doit être utilisé avec prudence chez patients ayant un asthme préexistant.
Informations pour les patients
Les patients doivent être informés des informations suivantes avant de commencer un traitement par un AINS et périodiquement au cours du traitement en cours. Les patients doivent également être encouragés à lire les AINS Guide des médicaments qui accompagne chaque ordonnance délivrée.
Tests de laboratoire
Étant donné que des ulcérations et des saignements graves du tractus gastro-intestinal peuvent survenir sans symptômes d'avertissement, les médecins doivent surveiller les signes ou les symptômes de saignement gastro-intestinal. Les patients sous traitement à long terme avec des AINS doivent faire vérifier périodiquement leur CBC et un profil chimique. Si des signes cliniques et des symptômes compatibles avec une maladie hépatique ou rénale se développent, des manifestations systémiques surviennent (par exemple, éosinophilie, éruption cutanée, etc.) ou si des tests hépatiques anormaux persistent ou s'aggravent, Ponstel (acide méfénamique) doit être arrêté.
Grossesse
Effets tératogènes
Catégorie de grossesse C
Les études de reproduction menées chez le rat et le lapin n'ont pas mis en évidence de signes d'anomalies du développement. Cependant, les études de reproduction animale ne sont pas toujours prédictives de la réponse humaine. Il n'y a pas d'études adéquates ou bien contrôlées chez les femmes enceintes. Postel ne doit être utilisé pendant la grossesse que si le bénéfice potentiel justifie le risque potentiel pour le fœtus.
Effets non tératogènes
En raison des effets connus des anti-inflammatoires non stéroïdiens sur le système cardiovasculaire fœtal (fermeture du canal artériel), l'utilisation pendant la grossesse (en particulier en fin de grossesse) doit être évitée.
Travail et accouchement
Dans les études chez le rat avec des AINS, comme avec d'autres médicaments connus pour inhiber la synthèse des prostaglandines, une incidence accrue de dystocie, un retard de parturition et une diminution de la survie des ratons se sont produits. Les effets de Ponstel (acide méfénamique) sur le travail et l'accouchement chez les femmes enceintes sont inconnus.
Mères allaitantes
Des traces de PONSTEL (acide méfénamique) peuvent être présentes dans le lait maternel et transmises au nourrisson.7 En raison du risque d'effets indésirables graves chez les nourrissons allaités par PONSTEL (acide méfénamique), il convient de décider s'il faut interrompre l'allaitement ou d'arrêter le médicament, en tenant compte de l'importance du médicament pour la mère.
Utilisation pédiatrique
L'innocuité et l'efficacité chez les patients pédiatriques de moins de 14 ans n'ont pas été établies.
Utilisation gériatrique
Les études cliniques de Ponstel (acide méfénamique) n'ont pas inclus un nombre suffisant de sujets âgés de 65 ans et plus pour déterminer s'ils réagissent différemment des sujets plus jeunes. Comme pour tout AINS, la prudence s'impose chez les personnes âgées (65 ans et plus).
Ce médicament est connu pour être en grande partie excrété par les reins et le risque de réactions toxiques à ce médicament peut être plus élevé chez les patients présentant une insuffisance rénale. Étant donné que les patients âgés sont plus susceptibles d'avoir une fonction rénale diminuée, une attention particulière doit être portée au choix de la dose et il peut être utile de surveiller la fonction rénale (voir PHARMACOLOGIE CLINIQUE et ÉVÉNEMENTS INDÉSIRABLES).
RÉFÉRENCES
7. Buchanan RA, et al. L'excrétion de l'acide méfénamique dans le lait maternel. Curr The Res. 10:592, 1968.
SURDOSAGE
Les symptômes consécutifs à un surdosage aigu d'AINS se limitent généralement à une léthargie, une somnolence, des nausées, des vomissements et des douleurs épigastriques, qui sont généralement réversibles avec des soins de soutien. Gastro-intestinal Une hypertension, une insuffisance rénale aiguë, une dépression respiratoire et un coma peuvent survenir, mais sont rares. Des réactions anaphylactoïdes ont été rapportées lors de l'ingestion thérapeutique d'AINS et peuvent survenir à la suite d'un surdosage.
Les patients doivent être pris en charge par des soins symptomatiques et de soutien suite à un surdosage d'AINS. Il n'y a pas d'antidote spécifique. Des vomissements et/ou du charbon actif (60 à 100 g chez l'adulte, 1 à 2 g/kg chez l'enfant) et/ou cathartique osmotique peuvent être indiqués chez les patients vus dans les 4 heures suivant une ingestion avec symptômes ou suite à un surdosage important (5 à 10 fois la dose habituelle). La diurèse forcée, l'alcalinisation de l'urine, l'hémodialyse ou l'hémoperfusion peuvent ne pas être utiles en raison d'une forte liaison aux protéines.
CONTRE-INDICATIONS
PONSTEL (acide méfénamique) est contre-indiqué chez les patients présentant une hypersensibilité connue à l'acide méfénamique.
PONSTEL (acide méfénamique) ne doit pas être administré aux patients qui ont présenté de l'asthme, de l'urticaire ou des réactions de type allergique après avoir pris de l'aspirine ou d'autres AINS. Des réactions sévères, rarement fatales, de type anaphylactique aux AINS ont été rapportées chez ces patients (voir MISES EN GARDE - Réactions anaphylactoïdes et PRÉCAUTIONS - Asthme préexistant ).
PONSTEL (acide méfénamique) est contre-indiqué pour le traitement de la douleur périopératoire dans le cadre d'un pontage coronarien (PAC) (voir AVERTISSEMENTS ).
Ponstel (acide méfénamique) est contre-indiqué chez les patients présentant une ulcération active aiguë ou une inflammation chronique du tractus gastro-intestinal supérieur ou inférieur.
Ponstel (acide méfénamique) ne doit pas être utilisé chez les patients atteints d'insuffisance rénale préexistante.
PHARMACOLOGIE CLINIQUE
Pharmacodynamie
Ponstel (acide méfénamique) est un anti-inflammatoire non stéroïdien (AINS) qui présente des activités anti-inflammatoires, analgésiques et antipyrétiques chez les modèles animaux. Le mécanisme d'action de Ponstel (acide méfénamique), comme celui des autres AINS, n'est pas complètement élucidé mais peut être lié à l'inhibition de la prostaglandine synthétase.
Pharmacocinétique
Absorption
L'acide méfénamique est rapidement absorbé après administration orale. Dans deux études à dose orale unique de 500 mg, l'étendue moyenne de l'absorption était de 30,5 mcg/h/mL (CV de 17 %).1,2 La biodisponibilité de la capsule par rapport à une dose IV ou à une solution buvable n'a pas été étudiée.
Après une dose orale unique de 1 gramme, des concentrations plasmatiques maximales moyennes comprises entre 10 et 20 mcg/mL3 ont été rapportées. Les concentrations plasmatiques maximales sont atteintes en 2 à 4 heures et la demi-vie d'élimination est d'environ 2 heures. Après plusieurs doses, les concentrations plasmatiques sont proportionnelles à la dose sans signe d'accumulation de médicament. Dans un essai à doses multiples chez des sujets adultes normaux (n = 6) recevant des doses de 1 gramme d'acide méfénamique quatre fois par jour, des concentrations à l'état d'équilibre de 20 mcg/mL ont été atteintes le deuxième jour d'administration, ce qui correspond à la courte demi- la vie.
L'effet de la nourriture sur le taux et le degré d'absorption de l'acide méfénamique n'a pas été étudié. Il a été démontré que l'ingestion concomitante d'antiacides contenant de l'hydroxyde de magnésium augmente significativement le taux et l'étendue de l'absorption de l'acide méfénamique (voir PRÉCAUTIONS : INTERACTIONS MÉDICAMENTEUSES ).1
Distribution
L'acide méfénamique a été signalé comme étant lié à plus de 90 % à l'albumine.9 La relation entre la fraction non liée et la concentration du médicament n'a pas été étudiée. Le volume de distribution apparent (Vzss/F) estimé après une dose orale de 500 mg d'acide méfénamique était de 1,06 L/kg.2
D'après ses propriétés physiques et chimiques, Ponstel (acide méfénamique) devrait être excrété dans le lait maternel humain.
Métabolisme
L'acide méfénamique est métabolisé par l'enzyme CYP2C9 du cytochrome P450 en acide 3-hydroxyméthyl méfénamique (métabolite I). Une oxydation supplémentaire en acide 3-carboxyméfénamique (métabolite II) peut se produire10. L'activité de ces métabolites n'a pas été étudiée. Les métabolites peuvent subir une glucuronidation et l'acide méfénamique est également glucuronidé directement. Un niveau plasmatique maximal avoisinant 20 mcg/mL a été observé à 3 heures pour le métabolite hydroxy et son glucuronide (n = 6) après une dose unique de 1 gramme. De même, un pic plasmatique de 8 mcg/mL a été observé à 6-8 heures pour le métabolite carboxy et son glucuronide.3
Excrétion
Environ cinquante-deux pour cent d'une dose d'acide méfénamique sont excrétés dans l'urine principalement sous forme de glucuronides d'acide méfénamique (6 %), d'acide 3-hydroxyméfénamique (25 %) et d'acide 3-carboxyméfénamique (21 %). La voie d'élimination fécale représente jusqu'à 20 % de la dose, principalement sous forme d'acide 3-carboxyméfénamique non conjugué.3
La demi-vie d'élimination de l'acide méfénamique est d'environ deux heures. Les demi-vies des métabolites I et II n'ont pas été rapportées avec précision, mais semblent être plus longues que celles du composé d'origine.3 Les métabolites peuvent s'accumuler chez les patients souffrant d'insuffisance rénale ou hépatique. Le glucuronide d'acide méfénamique peut se lier de manière irréversible aux protéines plasmatiques. Étant donné que l'excrétion rénale et hépatique sont des voies d'élimination importantes, des ajustements posologiques chez les patients présentant un dysfonctionnement rénal ou hépatique peuvent être nécessaires. Ponstel (acide méfénamique) ne doit pas être administré aux patients présentant une maladie rénale préexistante ou aux patients présentant une insuffisance rénale significative.
TABLEAU 1 : Estimations des paramètres pharmacocinétiques pour l'acide méfénamique
Populations particulières
Pédiatrique
Ponstel (acide méfénamique) n'a pas été suffisamment étudié chez les patients pédiatriques de moins de 14 ans. Une étude chez 17 nourrissons prématurés ayant reçu 2 mg/kg a indiqué que la demi-vie était environ cinq fois plus longue que celle des adultes, ce qui correspond à la faible activité des enzymes métaboliques chez les nouveau-nés. La Cmax moyenne dans cette étude était de 4 mcg/mL (plage de 2,9 à 6,1). Le temps moyen jusqu'à la concentration maximale (Tmax) était de 8 heures (plage de 2 à 18 heures).11
Course
Les différences pharmacocinétiques dues à la race n'ont pas été identifiées.
Insuffisance hépatique
La pharmacocinétique de l'acide méfénamique n'a pas été étudiée chez les patients présentant un dysfonctionnement hépatique. Comme le métabolisme hépatique est une voie importante d'élimination de l'acide méfénamique, les patients atteints d'une maladie hépatique aiguë et chronique peuvent nécessiter des doses réduites de Ponstel (acide méfénamique) par rapport aux patients ayant une fonction hépatique normale.
Insuffisance rénale
La pharmacocinétique de l'acide méfénamique n'a pas été étudiée chez les insuffisants rénaux. Étant donné que l'acide méfénamique, ses métabolites et ses conjugués sont principalement excrétés par les reins, il est possible que les métabolites de l'acide méfénamique s'accumulent. Ponstel (acide méfénamique) ne doit pas être administré aux patients présentant une maladie rénale préexistante ou aux patients présentant une insuffisance rénale significative.
Etudes cliniques
Dans des essais cliniques contrôlés à double insu, Ponstel (acide méfénamique) a été évalué pour le traitement de la dysménorrhée spasmodique primaire. Les paramètres utilisés pour déterminer l'efficacité comprenaient l'évaluation de la douleur par le patient et l'investigateur ; le besoin de médicaments analgésiques concomitants ; et l'évaluation du changement dans la fréquence et la sévérité des symptômes caractéristiques de la dysménorrhée spasmodique. Les patients ont reçu soit Ponstel (acide méfénamique), 500 mg (2 gélules) à une dose initiale de 250 mg toutes les 6 heures, soit un placebo dès l'apparition des saignements ou des douleurs, selon la première éventualité. Après trois cycles menstruels, les patientes ont été transférées vers le traitement alternatif pendant trois cycles supplémentaires. Ponstel (acide méfénamique) était significativement supérieur au placebo dans tous les paramètres, et les deux traitements (médicament et placebo) étaient également tolérés.
RÉFÉRENCES
1. Neuvonen PJ, Kivisto KT : Amélioration de l'absorption des médicaments par les antiacides. Une interaction médicamenteuse non reconnue. Clin Pharmacokinet. 27:120-8, août 1994.
2. Tall AR, Mistilits SP : Études sur Ponstan (acide méfénamique) : I. Perte de sang gastro-intestinale ; II. Absorption et excrétion d'une nouvelle formulation. J Int Med Res (Royaume-Uni). 1975, 3 (3) p176-82.
3. Winder CV, Kaump DH, Glazko et al : Observations expérimentales des acides flufénamique, méfénamique et méclofénamique. AnnPhys Med (Eng), Suppl p7-49.1967.
9. Champion GD, Graham GG : Pharmacocinétique des agents anti-inflammatoires non stéroïdiens. Aust NZ J Méd. 8 (Supp 1): 94-100, juin 1978.
10. McGurk KA, Remmel RP, Hosagrahara VP, Tosh D, Burchell B : Réactivité de l'acide méfénamique 1-o-acyl glucuronide avec des protéines in vitro et ex vivo. Médicament Metab Dispos. Août 1996, 24 (8) p842-9.
11. Ito K, Niida Y, Sato J et al : Pharmacocinétique de l'acide méfénamique chez les prématurés présentant une persistance du canal artériel. Acta Paediatr JPN. 36 (4): 387-91, 1994.
INFORMATIONS PATIENTS
Guide des médicaments pour les anti-inflammatoires non stéroïdiens (AINS)
(Voir la fin de ce guide de médication pour une liste de médecines de prescription NSAID.)
Quelles sont les informations les plus importantes que je devrais connaître sur les médicaments appelés anti-inflammatoires non stéroïdiens (AINS) ?
Les médicaments AINS peuvent augmenter le risque de crise cardiaque ou d'accident vasculaire cérébral pouvant entraîner la mort. Cette chance augmente :
- avec une utilisation prolongée de médicaments AINS
- chez les personnes qui ont une maladie cardiaque
Les médicaments AINS ne doivent jamais être utilisés juste avant ou après une chirurgie cardiaque appelée "greffe de pontage coronarien (PAC)".
Les médicaments AINS peuvent provoquer des ulcères et des saignements dans l'estomac et les intestins à tout moment pendant le traitement.
Ulcères et saignements :
- peut arriver sans symptômes d'avertissement
- peut causer la mort
Le risque qu'une personne développe un ulcère ou saigne augmente avec :
- prendre des médicaments appelés « corticostéroïdes » et « anticoagulants »
- utilisation plus longue
- fumeur
- buvant de l'alcool
- âge avancé
- avoir une mauvaise santé
Les médicaments AINS ne doivent être utilisés que :
- exactement comme prescrit
- à la dose la plus faible possible pour votre traitement
- pour le temps le plus court nécessaire
Que sont les anti-inflammatoires non stéroïdiens (AINS) ?
Les médicaments AINS sont utilisés pour traiter la douleur et la rougeur, l'enflure et la chaleur (inflammation) causées par des conditions médicales telles que :
- différents types d'arthrite
- crampes menstruelles et autres types de douleurs à court terme
Qui ne devrait pas prendre d'anti-inflammatoire non stéroïdien (AINS) ?
Ne prenez pas de médicament AINS :
- si vous avez eu une crise d'asthme, de l'urticaire ou une autre réaction allergique à l'aspirine ou à tout autre médicament AINS
- pour la douleur juste avant ou après un pontage cardiaque
Dites à votre fournisseur de soins de santé :
- sur toutes vos conditions médicales.
- sur tous les médicaments que vous prenez. Les AINS et certains autres médicaments peuvent interagir entre eux et provoquer des effets secondaires graves. Conservez une liste de vos médicaments à montrer à votre fournisseur de soins de santé et à votre pharmacien.
- si vous êtes enceinte. Les médicaments AINS ne doivent pas être utilisés par les femmes enceintes en fin de grossesse.
- si vous allaitez. Parlez-en à votre médecin.
Quels sont les effets secondaires possibles des anti-inflammatoires non stéroïdiens (AINS) ?
Obtenez immédiatement de l'aide d'urgence si vous présentez l'un des symptômes suivants :
- essoufflement ou difficulté à respirer
- douleur thoracique
- faiblesse dans une partie ou un côté de votre corps
- troubles de l'élocution
- gonflement du visage ou de la gorge
Arrêtez votre médicament AINS et appelez immédiatement votre fournisseur de soins de santé si vous présentez l'un des symptômes suivants :
Ce ne sont pas tous les effets secondaires des médicaments AINS. Parlez à votre fournisseur de soins de santé ou à votre pharmacien pour plus d'informations sur les médicaments AINS.
Autres informations sur les anti-inflammatoires non stéroïdiens (AINS)
- L'aspirine est un médicament AINS, mais il n'augmente pas le risque de crise cardiaque. L'aspirine peut provoquer des saignements dans le cerveau, l'estomac et les intestins. L'aspirine peut également provoquer des ulcères dans l'estomac et les intestins.
- Certains de ces médicaments AINS sont vendus à des doses plus faibles sans ordonnance (en vente libre). Parlez à votre fournisseur de soins de santé avant d'utiliser des AINS en vente libre pendant plus de 10 jours.
Médicaments AINS nécessitant une ordonnance
Ce guide de médicaments a été approuvé par la Food and Drug Administration des États-Unis. Date d'entrée en vigueur : 19/02/2008
