Danazol 50mg, 100mg, 200mg Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
Qu'est-ce que le Danazol 100 mg et comment est-il utilisé ?
Le danazol 50 mg est un médicament sur ordonnance utilisé pour traiter les symptômes de l'endométriose, de l'œdème de Quincke héréditaire et de la maladie fibrokystique du sein. Le danazol peut être utilisé seul ou avec d'autres médicaments.
Le danazol appartient à une classe de médicaments appelés androgènes.
On ne sait pas si Danazol est sûr et efficace chez les enfants.
Quels sont les effets secondaires possibles du Danazol ?
Le danazol 100 mg peut provoquer des effets secondaires graves, notamment :
- gonflement des mains et des pieds,
- changements menstruels (spottings, règles manquées),
- des changements d'humeur,
- nervosité,
- sautes d'humeur,
- éruption,
- démangeaison,
- gonflement du visage, de la langue ou de la gorge,
- étourdissements sévères et
- difficulté à respirer
Consultez immédiatement un médecin si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires les plus courants de Danazol 200 mg incluent :
- gain de poids,
- acné,
- peau ou cheveux gras,
- rinçage,
- transpiration,
- chute de cheveux,
- changements de voix (enrouement, changements de hauteur),
- mal de gorge,
- croissance anormale des poils du corps (chez les femmes),
- sécheresse vaginale, irritation, brûlure ou démangeaison,
- diminution de la taille des seins,
- rétention d'eau,
- la dépression,
- ballonnements,
- irritabilité,
- modifications du cycle menstruel (spottings, saignements irréguliers, règles manquées),
- nervosité et
- des changements d'humeur
Dites au médecin si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas.
Ce ne sont pas tous les effets secondaires possibles du Danazol. Pour plus d'informations, consultez votre médecin ou votre pharmacien.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
LA DESCRIPTION
Danazol 50 mg est un stéroïde synthétique dérivé de l'éthistérone. C'est une poudre cristalline blanche à jaune pâle, pratiquement insoluble ou insoluble dans l'eau, et peu soluble dans l'alcool. Chimiquement, le danazol 100 mg est du 17α-Pregna-2,4-dien-20-yno [2,3-d]-isoxazol-17-ol. La formule moléculaire est C22H27NO2. Il a un poids moléculaire de 337,46 et la formule développée suivante :
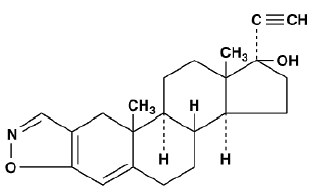
Les gélules de danazol pour administration orale contiennent 50 mg, 100 mg ou 200 mg de danazol.
ingrédients inactifs
lactose anhydre, lactose monohydraté, stéarate de magnésium, amidon prégélatinisé, laurylsulfate de sodium, talc. Les enveloppes des gélules pour 200 mg de danazol contiennent du D&C Yellow #10, du FD&C Red #40, du D&C Red #28, de la gélatine et du dioxyde de titane. Les enveloppes des gélules pour 50 mg et 100 mg de danazol 50 mg contiennent du D&C jaune n° 10, du FD&C rouge n° 40, de la gélatine et du dioxyde de titane. L'encre d'impression de la capsule contient : glaçage gomme laque dans l'éthanol, oxyde de fer noir, alcool n-butylique, propylène glycol, éthanol, méthanol, laque d'aluminium FD&C bleu n° 2, laque d'aluminium FD&C rouge n° 40, laque d'aluminium FD&C bleu n° 1 , et laque d'aluminium D&C jaune n° 10.
LES INDICATIONS
Endométriose
Les gélules de Danazol 100mg sont indiquées pour le traitement de l'endométriose justiciable d'une prise en charge hormonale.
Angiœdème héréditaire
Les gélules de danazol sont indiquées pour la prévention des crises d'œdème de Quincke de tous types (cutané, abdominal, laryngé) chez l'homme et la femme.
DOSAGE ET ADMINISTRATION
Endométriose
En cas de maladie modérée à sévère, ou chez les patients infertiles en raison de l'endométriose, une dose initiale de 800 mg administrée en deux doses fractionnées est recommandée. L'aménorrhée et la réponse rapide aux symptômes douloureux sont mieux obtenues à ce niveau de dosage. Une titration progressive à la baisse jusqu'à une dose suffisante pour maintenir l'aménorrhée peut être envisagée en fonction de la réponse du patient. Pour les cas bénins, une dose quotidienne initiale de 200 mg à 400 mg administrée en deux doses fractionnées est recommandée et peut être ajustée en fonction de la réponse du patient. La thérapie doit commencer pendant la menstruation. Sinon, des tests appropriés doivent être effectués pour s'assurer que la patiente n'est pas enceinte pendant le traitement par les gélules de danazol 50 mg (voir CONTRE-INDICATIONS et AVERTISSEMENTS ). Il est essentiel que le traitement se poursuive sans interruption pendant 3 à 6 mois mais peut être prolongé jusqu'à 9 mois si nécessaire. Après l'arrêt du traitement, si les symptômes réapparaissent, le traitement peut être réinstitué .
Angiœdème héréditaire
Les exigences de dosage pour le traitement continu d'angioedema héréditaire avec les capsules danazol devraient être individualisées sur la base de la réponse clinique du patient. Il est recommandé de commencer le patient avec 200 mg, deux ou trois fois par jour. Après l'obtention d'une réponse initiale favorable en termes de prévention des épisodes de crises oedémateuses, la posologie continue appropriée doit être déterminée en diminuant la posologie de 50 % ou moins à des intervalles de un à trois mois ou plus si la fréquence des crises avant le traitement l'exige. . En cas de crise, la posologie quotidienne peut être augmentée jusqu'à 200 mg. Pendant la phase d'ajustement de la dose, une surveillance étroite de la réponse du patient est indiquée, en particulier si le patient a des antécédents d'atteinte des voies respiratoires.
COMMENT FOURNIE
Gélules de danazol 50 mg USP, 50 mg sont disponibles sous forme de capsules opaques de maïs/opaques blanches portant le logo « LANNETT » sur le capuchon et « 1392 » sur le corps et sont fournies en :
Flacons de 100 ( CDN 0527-1392-01)
Gélules de danazol USP, 100 mg sont disponibles sous forme de capsules opaques au maïs/opaques au maïs portant le logo « LANNETT » sur le capuchon et « 1368 » sur le corps et sont fournies en :
Flacons de 100 ( CDN 0527-1368-01)
Gélules de danazol USP, 200 mg sont disponibles sous forme de capsules orange opaque/orange opaque portant le logo « LANNETT » sur le capuchon et « 1369 » sur le corps et sont fournies en :
Bouteilles de 60 ( CDN 0527-1369-06) Flacons de 100 ( CDN 0527-1369-01)
Le magasin à 20 ° à 25°C (68 ° à 77°F) [voit USP la Température de Pièce Contrôlée].
Dispenser dans un récipient bien fermé avec une fermeture à l'épreuve des enfants comme défini dans l'USP.
Distribué par : Lannett Company, Inc. Philadelphie, PA 19154. Révisé : Mai 2018
EFFETS SECONDAIRES
Les événements suivants ont été rapportés en association avec l'utilisation de gélules de danazol 100 mg :
Les effets semblables aux androgènes comprennent la prise de poids, l'acné et la séborrhée. Un léger hirsutisme, un œdème, une perte de cheveux, une modification de la voix, pouvant prendre la forme d'un enrouement, d'un mal de gorge ou d'une instabilité ou d'une aggravation de la tonalité, peuvent survenir et peuvent persister après l'arrêt du traitement. L'hypertrophie du clitoris est rare.
D'autres effets endocriniens possibles sont les troubles menstruels, notamment les saignotements, l'altération du rythme du cycle et l'aménorrhée. Bien que les saignements cycliques et l'ovulation reviennent généralement dans les 60 à 90 jours suivant l'arrêt du traitement par les gélules de danazol, une aménorrhée persistante a parfois été signalée.
Les bouffées vasomotrices, la transpiration, la sécheresse et l'irritation vaginales et la réduction de la taille des seins peuvent refléter une diminution des œstrogènes. Nervosité et labilité émotionnelle ont été rapportées. Chez l'homme, une légère réduction de la spermatogenèse peut être évidente pendant le traitement. Des anomalies du volume, de la viscosité, du nombre de spermatozoïdes et de la motilité du sperme peuvent survenir chez les patients recevant un traitement à long terme.
Un dysfonctionnement hépatique, mis en évidence par une élévation réversible des enzymes sériques et/ou un ictère, a été rapporté chez des patients recevant une dose quotidienne de gélules de danazol de 400 mg ou plus. Il est recommandé que les patients recevant des gélules de danazol soient surveillés pour un dysfonctionnement hépatique par des tests de laboratoire et une observation clinique. Une toxicité hépatique grave, y compris ictère cholestatique, péliose hépatique, adénome hépatique, lésion hépatocellulaire, ictère hépatocellulaire et insuffisance hépatique, a été rapportée (voir AVERTISSEMENTS et PRÉCAUTIONS ).
Des anomalies dans les tests de laboratoire peuvent survenir pendant le traitement par les gélules de danazol 50 mg, y compris CPK, tolérance au glucose, glucagon, globuline de liaison à la thyroïde, globuline de liaison aux hormones sexuelles, autres protéines plasmatiques, lipides et lipoprotéines.
Les réactions suivantes ont été rapportées, une relation de cause à effet avec l'administration de gélules de danazol n'a été ni confirmée ni infirmée ;
Allergique: urticaire, prurit et rarement, congestion nasale ;
Effets sur le SNC : maux de tête, nervosité et labilité émotionnelle, étourdissements et évanouissements, dépression, fatigue, troubles du sommeil, tremblements, paresthésies, faiblesse, troubles visuels et rarement, hypertension intracrânienne bénigne, anxiété, modifications de l'appétit, frissons et rarement convulsions, syndrome de Guillain-Barré ;
Gastro-intestinal : gastro-entérite, nausées, vomissements, constipation et, rarement, pancréatite et péliose splénique ;
Musculo-squelettique : crampes ou spasmes musculaires, ou douleurs, douleurs articulaires, blocage articulaire, gonflement articulaire, douleur dans le dos, le cou ou les extrémités, et rarement, syndrome du canal carpien pouvant être secondaire à une rétention hydrique ;
Génito-urinaire : hématurie, aménorrhée post-thérapeutique prolongée ;
Hématologique : une augmentation du nombre de globules rouges et de plaquettes. Une érythrocytose, une leucocytose ou une polycythémie réversibles peuvent être provoquées. Une éosinophilie, une leucopénie et une thrombocytopénie ont également été notées.
Peau: éruptions cutanées (maculopapuleuses, vésiculaires, papuleuses, purpuriques, pétéchiales) et rarement, sensibilité au soleil, syndrome de Stevens-Johnson et érythème polymorphe ;
Autre: augmentation des besoins en insuline chez les patients diabétiques, modification de la libido, infarctus du myocarde, palpitations, tachycardie, élévation de la pression artérielle, pneumonite interstitielle et, rarement, cataractes, saignement des gencives, fièvre, douleurs pelviennes, écoulement mamelonnaire. Des tumeurs malignes du foie ont été signalées dans de rares cas, après une utilisation à long terme.
INTERACTIONS MÉDICAMENTEUSES
L'allongement du temps de prothrombine survient chez les patients stabilisés sous warfarine.
Le traitement par le danazol 50 mg peut entraîner une augmentation des taux de carbamazépine chez les patients prenant les deux médicaments.

Le danazol 50 mg peut provoquer une résistance à l'insuline. La prudence s'impose en cas d'utilisation avec des médicaments antidiabétiques.
Le danazol 100 mg peut augmenter les taux plasmatiques de cyclosporine et de tacrolimus, entraînant une augmentation de la toxicité rénale de ces médicaments. Une surveillance des concentrations systémiques de ces médicaments et des ajustements posologiques appropriés peuvent être nécessaires en cas d'utilisation concomitante avec le danazol.
Le danazol 100 mg peut augmenter la réponse calcémique aux analogues synthétiques de la vitamine D dans l'hypoparathyroïdie primaire.
Le risque de myopathie et de rhabdomyolyse est augmenté par l'administration concomitante de danazol 50 mg avec des statines telles que la simvastatine, l'atorvastatine et la lovastatine. La prudence s'impose en cas d'utilisation concomitante. Consultez l'étiquetage du produit pour les statines pour des informations spécifiques sur les restrictions de dose en présence de danazol.
AVERTISSEMENTS
L'utilisation de danazol 100 mg pendant la grossesse est contre-indiquée. Un test sensible (p. ex., test de la sous-unité bêta si disponible) capable de déterminer une grossesse précoce est recommandé immédiatement avant le début du traitement. De plus, une méthode de contraception non hormonale doit être utilisée pendant le traitement. Si une patiente tombe enceinte alors qu'elle prend du danazol 200 mg, l'administration du médicament doit être interrompue et la patiente doit être informée du risque potentiel pour le fœtus. L'exposition au danazol 200 mg in utero peut entraîner des effets androgènes sur le fœtus féminin; des cas d'hypertrophie clitoridienne, de fusion labiale, d'anomalie du sinus urogénital, d'atrésie vaginale et d'organes génitaux ambigus ont été signalés (voir PRÉCAUTIONS : Grossesse, Effets tératogènes ).
Des événements thromboemboliques, thrombotiques et thrombophlébitiques, y compris une thrombose du sinus sagittal et des accidents vasculaires cérébraux potentiellement mortels ou mortels, ont été rapportés.
L'expérience du traitement à long terme avec le danazol 100 mg est limitée. Une péliose hépatique et un adénome hépatique bénin ont été observés lors d'une utilisation à long terme. La péliose hépatique et l'adénome hépatique peuvent être silencieux jusqu'à ce qu'ils soient compliqués par une hémorragie intra-abdominale aiguë potentiellement mortelle. Le médecin doit donc être attentif à cette possibilité. Des tentatives doivent être faites pour déterminer la dose la plus faible qui fournira une protection adéquate. Si le médicament a été commencé à un moment d'exacerbation d'un œdème angioneurotique héréditaire dû à un traumatisme, au stress ou à une autre cause, des tentatives périodiques de diminution ou d'arrêt du traitement doivent être envisagées.
Le danazol 100 mg a été associé à plusieurs cas d'hypertension intracrânienne bénigne également connue sous le nom de pseudotumeur cérébrale. Les premiers signes et symptômes de l'hypertension intracrânienne bénigne comprennent un œdème papillaire, des maux de tête, des nausées et des vomissements et des troubles visuels. Les patients présentant ces symptômes doivent subir un dépistage de l'œdème papillaire et, le cas échéant, les patients doivent être informés d'arrêter immédiatement le danazol 100 mg et d'être référés à un neurologue pour un diagnostic et des soins plus approfondis.
Une altération temporaire des lipoprotéines sous la forme d'une diminution des lipoprotéines de haute densité et éventuellement d'une augmentation des lipoprotéines de basse densité a été rapportée pendant le traitement par le danazol. Ces altérations peuvent être importantes et les prescripteurs doivent tenir compte de l'impact potentiel sur le risque d'athérosclérose et de maladie coronarienne en fonction du bénéfice potentiel du traitement pour le patient.
Les patients doivent être étroitement surveillés afin de détecter tout signe d'effets androgéniques dont certains peuvent ne pas être réversibles même lorsque l'administration du médicament est arrêtée.
PRÉCAUTIONS
Étant donné que les gélules de danazol peuvent provoquer une certaine rétention d'eau, les affections susceptibles d'être influencées par ce facteur, telles que l'épilepsie, la migraine ou un dysfonctionnement cardiaque ou rénal, la polycythémie et l'hypertension, nécessitent une observation attentive. Utiliser avec prudence chez les patients atteints de diabète sucré.
Étant donné qu'un dysfonctionnement hépatique se manifestant par de modestes augmentations des taux sériques de transaminases a été rapporté chez des patients traités par des gélules de danazol, des tests périodiques de la fonction hépatique doivent être effectués (voir AVERTISSEMENTS et EFFETS INDÉSIRABLES ).
Il a été rapporté que l'administration de danazol 50 mg provoque une exacerbation des manifestations de la porphyrie aiguë intermittente (voir CONTRE-INDICATIONS ).
La surveillance en laboratoire de l'état hématologique doit être envisagée.
Tests de laboratoire
Le traitement au danazol peut interférer avec les déterminations en laboratoire de la testostérone, de l'androstènedione et de la déhydroépiandrostérone. D'autres événements métaboliques comprennent une réduction de la globuline de liaison à la thyroïde et de la T4 avec une absorption accrue de T3, mais sans perturbation de l'hormone stimulant la thyroïde ou de l'indice de thyroxine libre.
Carcinogenèse, mutagenèse, altération de la fertilité
Les données actuelles sont insuffisantes pour évaluer la cancérogénicité du danazol.
Grossesse Effets tératogènes
(voir CONTRE-INDICATIONS .) Le danazol 50 mg administré par voie orale à des rates gravides du 6e au 15e jour de gestation à des doses allant jusqu'à 250 mg/kg/jour (7 à 15 fois la dose humaine) n'a pas entraîné d'embryotoxicité ou de tératogénicité induite par le médicament, ni de différence dans la portée la taille, la viabilité ou le poids de la progéniture par rapport aux témoins. Chez le lapin, l'administration de danazol 200 mg les jours 6 à 18 de la gestation à des doses de 60 mg/kg/jour et plus (2 à 4 fois la dose humaine) a entraîné une inhibition du développement fœtal.
Mères allaitantes
(voir CONTRE-INDICATIONS .)
Utilisation pédiatrique
L'innocuité et l'efficacité chez les patients pédiatriques n'ont pas été établies.
Utilisation gériatrique
Les études cliniques sur les gélules de danazol n'ont pas inclus un nombre suffisant de sujets âgés de 65 ans et plus pour déterminer l'innocuité et l'efficacité de Danocrine chez les patients âgés.
SURDOSAGE
Aucune information fournie
CONTRE-INDICATIONS
Les gélules de Danazol 50 mg ne doivent pas être administrées aux patients présentant :
PHARMACOLOGIE CLINIQUE
Danazol supprime l'axe pituitaire-ovarien. Cette suppression est probablement une combinaison d'une réponse hypothalamo-hypophysaire déprimée à une production d'œstrogène réduite, de l'altération du métabolisme des stéroïdes sexuels et de l'interaction du danazol avec les récepteurs des hormones sexuelles. Le seul autre effet hormonal démontrable est une faible activité androgénique. Le danazol 50 mg diminue la production de l'hormone folliculo-stimulante (FSH) et de l'hormone lutéinisante (LH).
Des preuves récentes suggèrent un effet inhibiteur direct au niveau des sites gonadiques et une liaison du danazol aux récepteurs des stéroïdes gonadiques au niveau des organes cibles. En outre, il a été démontré que le danazol 50 mg diminue de manière significative les taux d'IgG, d'IgM et d'IgA, ainsi que les auto-anticorps anti-phospholipides et isotopes IgG chez les patientes atteintes d'endométriose et les élévations associées des auto-anticorps, ce qui suggère que cela pourrait être un autre mécanisme par lequel il facilite la régression de la maladie. .
Dans le traitement de l'endométriose, le danazol modifie le tissu endométrial normal et ectopique afin qu'il devienne inactif et atrophique. La résolution complète des lésions de l'endomètre se produit dans la majorité des cas.
Les modifications de la cytologie vaginale et de la glaire cervicale reflètent l'effet suppresseur du danazol sur l'axe hypophyso-ovarien.
Des changements dans le cycle menstruel peuvent survenir.
Généralement, l'action hypophyso-suppressive du danazol 200 mg est réversible. L'ovulation et les saignements cycliques reviennent généralement dans les 60 à 90 jours après l'arrêt du traitement par danazol 100 mg.
Dans le traitement de l'angio-œdème héréditaire, le danazol à doses efficaces prévient les crises de la maladie caractérisées par un œdème épisodique des viscères abdominaux, des extrémités, du visage et des voies respiratoires qui peut être invalidant et, si les voies respiratoires sont atteintes, mortel. De plus, le danazol 100 mg corrige partiellement ou complètement l'anomalie biochimique primaire de l'angio-œdème héréditaire en augmentant les taux de l'inhibiteur déficient de la C1 estérase (C1El). À la suite de cette action, les taux sériques du composant C4 du système du complément sont également augmentés.
Pharmacocinétique
Absorption
Après administration orale d'une dose de 400 mg à des volontaires sains de sexe masculin, les concentrations plasmatiques maximales de danazol sont atteintes entre 2 et 8 heures, avec un Tmax médian de 4 heures. Des conditions d'état d'équilibre sont observées après 6 jours d'administration biquotidienne de gélules de danazol 100 mg.
Les paramètres pharmacocinétiques des gélules de danazol 100 mg après administration d'une dose orale de 400 mg à des hommes en bonne santé sont résumés dans le tableau suivant :
Les paramètres pharmacocinétiques des gélules de danazol après administration orale de doses uniques de 100, 200 et 400 mg à des femmes volontaires en bonne santé sont résumés dans le tableau suivant :
Proportionnalité des doses
Les études de biodisponibilité indiquent que les concentrations sanguines n'augmentent pas proportionnellement à l'augmentation de la dose administrée.
L'administration d'une dose unique de gélules de danazol chez des femmes volontaires en bonne santé a révélé qu'une augmentation de 4 fois de la dose ne produisait qu'une augmentation de 1,6 et 2,5 fois de l'ASC et une augmentation de 1,3 et 2,2 fois de la Cmax à jeun et à jeun, respectivement. Un degré similaire de non-proportionnalité à la dose a été observé à l'état d'équilibre.
Effet alimentaire
L'administration d'une dose unique de gélules de 100 mg et 200 mg de danazol à des femmes volontaires a montré que l'étendue de la disponibilité et la concentration plasmatique maximale augmentaient de 3 à 4 fois, respectivement, après un repas (> 30 grammes de matières grasses), par rapport à l'état de jeûne. De plus, la nourriture a également retardé le temps moyen jusqu'à la concentration maximale de danazol d'environ 30 minutes. Même après plusieurs dosages dans des conditions d'alimentation/de jeûne moins extrêmes, il subsistait une différence de biodisponibilité d'environ 2 à 2,5 fois entre les états nourri et à jeun.
Distribution
Le danazol 100 mg est lipophile et peut se répartir dans les membranes cellulaires, indiquant la probabilité de distribution dans les compartiments des tissus profonds.
Métabolisme et excrétion
Le danazol 200 mg semble être métabolisé et les métabolites sont éliminés par les voies rénales et fécales. Les deux principaux métabolites excrétés dans l'urine sont le 2-hydroxyméthyl danazol 50 mg et l'éthistérone. Au moins dix produits différents ont été identifiés dans les matières fécales.
La demi-vie d'élimination rapportée du danazol 100 mg est variable d'une étude à l'autre. La demi-vie moyenne du danazol chez les hommes sains est de 9,7 h. Après 6 mois d'administration de 200 mg trois fois par jour chez des patientes atteintes d'endométriose, la demi-vie du danazol était de 23,7 heures.
INFORMATIONS PATIENTS
Aucune information fournie. Veuillez vous référer au AVERTISSEMENTS et PRÉCAUTIONS sections.
