Mellaril 10mg, 25mg, 50mg, 100mg Thioridazine Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
Qu'est-ce que Mellaril Topper et comment est-il utilisé ?
Mellaril Topper est un médicament d'ordonnance utilisé pour traiter les symptômes de la schizophrénie et des troubles dépressifs. Mellaril 25mg Topper peut être utilisé seul ou avec d'autres médicaments.
- Mellaril 50 mg Topper appartient à une classe de médicaments appelés antipsychotiques, phénothiazine.
- On ne sait pas si Mellaril Topper est sûr et efficace chez les enfants de moins de 2 ans.
Quels sont les effets secondaires possibles de Mellaril Topper ?
Mellaril 100 mg Topper peut provoquer des effets secondaires graves, notamment :
- urticaire,
- difficulté à respirer,
- gonflement du visage, des lèvres, de la langue ou de la gorge,
- mouvements musculaires incontrôlés dans les bras, les jambes ou le visage (mâcher, claquer des lèvres, froncer les sourcils, cligner des yeux ou bouger les yeux),
- battements de cœur rapides ou battants,
- flottant dans ta poitrine,
- essoufflement,
- vertiges soudains,
- agitation,
- confusion,
- saisie,
- diminution de la vision nocturne,
- vision tunnel,
- larmoiement,
- sensibilité accrue à la lumière,
- peu ou pas d'urine,
- fièvre,
- des frissons,
- plaies buccales,
- plaies cutanées,
- mal de gorge,
- toux,
- étourdissement,
- muscles très raides (rigides),
- forte fièvre,
- la transpiration, et
- tremblements
Consultez immédiatement un médecin si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires les plus courants de Mellaril Topper incluent :
- somnolence,
- bouche sèche,
- Vision floue,
- nausée,
- vomissement,
- constipation,
- diarrhée,
- gonflement ou écoulement des seins,
- changements dans vos menstruations, et
- gonflement des mains ou des pieds
Dites au médecin si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas.
Ce ne sont pas tous les effets secondaires possibles de Mellaril 10mg Topper. Pour plus d'informations, consultez votre médecin ou votre pharmacien.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
ATTENTION
Il a été démontré que MELLARIL® (THIORIDAZINE HCl) PROLONGE L'INTERVALLE QTc D'UNE MANIÈRE LIÉE À LA DOSE, ET LES MÉDICAMENTS AYANT CE POTENTIEL, Y COMPRIS MELLARIL (thioridazine hcl), ONT ÉTÉ ASSOCIÉS À DES ARYTHMIES DE TYPE TORSADE DE POINTES ET À LA MORT SUBITE. EN RAISON DE SON POTENTIEL D'EFFETS PROARRYTHMIQUES SIGNIFICATIFS, POSSIBLEMENT MORTELS, MELLARIL (chlorhydrate de thioridazine) DOIT ÊTRE RÉSERVÉ POUR LE TRAITEMENT DES PATIENTS SCHIZOPHRÉNIQUES QUI NE RÉAGISSENT PAS À DES TRAITEMENTS ADÉQUATS AVEC D'AUTRES MÉDICAMENTS ANTIPSYCHOTIQUES, SOIT PARCE QUE D'UNE EFFICACITÉ INSUFFISANTE OU DE L'INCAPACITÉ À ATTEINDRE UNE DOSE EFFICACE EN RAISON DES EFFETS INDÉSIRABLES INTOLÉRABLES DE CES MÉDICAMENTS. (VOIR MISES EN GARDE, CONTRE-INDICATIONS, ET LES INDICATIONS ).
LA DESCRIPTION
Mellaril® (chlorhydrate de thioridazine) est la 2-méthylmercapto-10-[2-(N-méthyl-2-pipéridyl)éthyl]phénothiazine.
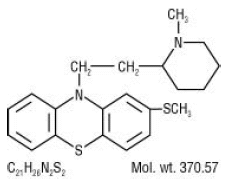
Comprimés de 10 mg, 15 mg, 25 mg, 50 mg, 100 mg, 150 mg et 200 mg
Ingrédient actif: Chlorhydrate de thioridazine, USP
Comprimés de 10 mg
Ingrédients inactifs: acacia, sulfate de calcium dihydraté, cire de carnauba, jaune D&C #10, bleu FD&C #1, jaune FD&C #6, gélatine, lactose, méthylparabène, povidone, propylparabène, benzoate de sodium, amidon, acide stéarique, saccharose, oxyde de fer noir synthétique, talc , dioxyde de titane et autres ingrédients.
Comprimés de 15 mg
Ingrédients inactifs: acacia, sulfate de calcium dihydraté, cire de carnauba, D&C Red #7, gélatine, lactose, méthylparabène, povidone, propylparabène, amidon, acide stéarique, saccharose, oxyde de fer noir synthétique, talc, dioxyde de titane et autres ingrédients.
Comprimés de 25 mg
Ingrédients inactifs: acacia, sulfate de calcium dihydraté, cire de carnauba, gélatine, lactose, méthylparabène, povidone, propylparabène, benzoate de sodium, amidon, acide stéarique, saccharose, oxyde de fer noir synthétique, oxyde de fer synthétique, talc, dioxyde de titane et autres ingrédients.
Comprimés de 50 mg
Ingrédients inactifs: acacia, sulfate de calcium dihydraté, cire de carnauba, gélatine, lactose, benzoate de sodium, amidon, acide stéarique, saccharose, oxyde de fer noir synthétique, talc, dioxyde de titane et autres ingrédients.
Comprimés de 100 mg
Ingrédients inactifs: acacia, sulfate de calcium dihydraté, cire de carnauba, jaune D&C #10, bleu FD&C #1, bleu FD&C #2, jaune FD&C #6, lactose, méthylparabène, povidone, propylparabène, benzoate de sodium, sorbitol, amidon, acide stéarique, saccharose, synthétique oxyde de fer noir, talc, dioxyde de titane et autres ingrédients.
Comprimés de 150 mg
Ingrédients inactifs: acacia, sulfate de calcium dihydraté, cire de carnauba, jaune D&C #10, vert FD&C #3, jaune FD&C #6, lactose, méthylparabène, povidone, propylparabène, benzoate de sodium, amidon, acide stéarique, saccharose, oxyde de fer noir synthétique, talc, titane dioxyde et d'autres ingrédients.
Comprimés de 200 mg
Ingrédients inactifs: acacia, alginate d'ammonium et de calcium, sulfate de calcium dihydraté, cire de carnauba, dioxyde de silicium colloïdal, D&C Red #7, lactose, stéarate de magnésium, méthylparabène, povidone, propylparabène, benzoate de sodium, amidon, acide stéarique, saccharose, oxyde de fer noir synthétique, talc, dioxyde de titane et d'autres ingrédients.
Solution buvable à 30 mg/mL et 100 mg/mL (concentrée)
Ingrédient actif: Chlorhydrate de thioridazine, USP
Solution buvable à 30 mg/mL (concentré)
Ingrédients inactifs: alcool, 3,0 %, arôme, méthylparabène, propylparabène, eau purifiée et solution de sorbitol. Peut contenir de l'hydroxyde de sodium ou de l'acide chlorhydrique pour ajuster le pH.
Solution buvable à 100 mg/mL (concentré)
Ingrédients inactifs: alcool, 4,2 %, arôme, glycérine, méthylparabène, propylparabène, eau purifiée, solution de sorbitol et saccharose. Peut contenir de l'hydroxyde de sodium ou de l'acide chlorhydrique pour ajuster le pH.
Suspension orale à 5 mg/mL et 20 mg/mL
Ingrédient actif: chaque mL contient de la thioridazine, USP, équivalente à 5 mg et 20 mg de chlorhydrate de thioridazine, USP, respectivement.
Suspension orale à 5 mg/mL
Ingrédients inactifs: carbomère 934, arôme, polysorbate 80, eau purifiée, hydroxyde de sodium et saccharose.
Suspension orale à 20 mg/mL
Ingrédients inactifs: carbomère 934, jaune D&C #10, jaune FD&C #6, arôme, polysorbate 80, eau purifiée, hydroxyde de sodium et saccharose.
LES INDICATIONS
Mellaril® (chlorhydrate de thioridazine) est indiqué pour la prise en charge des patients schizophrènes qui ne répondent pas de manière adéquate au traitement par d'autres médicaments antipsychotiques. En raison du risque d'effets proarythmiques importants, potentiellement mortels, associés au traitement par Mellaril (chlorhydrate de thioridazine), Mellaril (chlorhydrate de thioridazine) ne doit être utilisé que chez les patients qui n'ont pas répondu de manière adéquate au traitement par des cycles appropriés d'autres médicaments antipsychotiques, soit en raison d'une efficacité insuffisante ou
l'incapacité d'atteindre une dose efficace en raison des effets indésirables intolérables de ces médicaments. Par conséquent, avant d'initier un traitement par Mellaril (chlorhydrate de thioridazine), il est fortement recommandé qu'un patient reçoive au moins 2 essais, chacun avec un médicament antipsychotique différent, à une dose adéquate et pendant une durée adéquate (voir AVERTISSEMENTS et CONTRE-INDICATIONS ).
Cependant, le prescripteur doit être conscient que Mellaril (chlorhydrate de thioridazine) n'a pas été systématiquement évalué dans des essais contrôlés chez des patients schizophrènes réfractaires au traitement et que son efficacité chez ces patients est inconnue.
DOSAGE ET ADMINISTRATION
Étant donné que Mellaril (chlorhydrate de thioridazine) est associé à un allongement lié à la dose de l'intervalle QTc, qui est un événement potentiellement mortel, son utilisation doit être réservée aux patients schizophrènes qui ne répondent pas de manière adéquate au traitement par d'autres médicaments antipsychotiques. La posologie doit être individualisée et la plus petite dose efficace doit être déterminée pour chaque patient (voir LES INDICATIONS et AVERTISSEMENTS ).
Adultes
La dose initiale habituelle pour les patients schizophrènes adultes est de 50 à 100 mg trois fois par jour, avec une augmentation progressive jusqu'à un maximum de 800 mg par jour si nécessaire. Une fois le contrôle efficace des symptômes atteint, la posologie peut être réduite progressivement pour déterminer la dose d'entretien minimale. La posologie quotidienne totale varie de 200 à 800 mg, divisée en deux à quatre doses.
Patients pédiatriques
Pour les patients pédiatriques atteints de schizophrénie qui ne répondent pas aux autres agents, la dose initiale recommandée est de 0,5 mg/kg/jour administrée en doses fractionnées. La posologie peut être augmentée progressivement jusqu'à l'obtention d'un effet thérapeutique optimal ou jusqu'à ce que la dose maximale de 3 mg/kg/jour soit atteinte.
COMMENT FOURNIE
Comprimés Mellaril® (chlorhydrate de thioridazine)
10 mg
Chartreuse brillante, comprimés enrobés ; "S" imprimé d'un côté, "78-2'' imprimé de l'autre côté, en noir.
Flacon de 100.................................................. CDN 0078-0002-05 Flacon de 1000................................................ CDN 0078-0002-09 Dosage unitaire de 100 ............ CDN 0078-0002-06
15mg
Comprimés enrobés roses ; "S" imprimé d'un côté, "78-8'' imprimé de l'autre côté, en noir.
Flacon de 100.................................................. CDN 0078-0008-05
25mg
Comprimés enrobés brun clair; "S" imprimé d'un côté, "MELLARIL (thioridazine hcl) 25'' imprimé de l'autre côté, en noir.
Flacon de 100.................................................. CDN 0078-0003-05 Flacon de 1000................................................ CDN 0078-0003-09 Conditionnement unitaire de 100 ............ CDN 0078-0003-06
50mg
Comprimés blancs enrobés ; "S" imprimé d'un côté, "MELLARIL (thioridazine hcl) 50'' imprimé de l'autre côté, en noir.
Flacon de 100.................................................. CDN 0078-0004-05 Flacon de 1000................................................ CDN 0078-0004-09 Paquet de dose unitaire de 100............ CDN 0078-0004-06
100mg
Comprimés enrobés vert clair ; " ^4&" imprimé d'un côté, "MELLARIL (thioridazine hcl) 100'' imprimé de l'autre côté, en noir.
Flacon de 100.................................................. CDN 0078-0005-05 Flacon de 1000................................................ CDN 0078-0005-09 Dosage unitaire de 100 ............ CDN 0078-0005-06
150mg
Comprimés enrobés jaunes ; "S" imprimé d'un côté, "MELLARIL (thioridazine hcl) 150'' imprimé de l'autre côté, en noir.
Flacon de 100.................................................. CDN 0078-0006-05
200mg
Comprimés enrobés roses, " ^4& " imprimé sur un côté, " MELLARIL (thioridazine hcl) 200'' imprimé sur l'autre côté, en noir.
Flacon de 100.................................................. CDN 0078-0007-05 Conditionnement unitaire de 100 ............ CDN 0078-0007-06
Stocker et distribuer
En dessous de 86 °F (30 °C) ; récipient étanche.
Solution orale de Mellaril® (chlorhydrate de thioridazine) (concentré)
30 mg/mL
Un liquide clair, jaune paille avec une odeur de cerise. Chaque mL contient 30 mg de chlorhydrate de thioridazine, USP, alcool à 3,0 % en volume. Contenant immédiat : bouteilles en verre ambré de 4 fl. oz. (118 mL) comme suit : 4 fl. oz. flacons, dans des cartons de 12 flacons, accompagnés d'un compte-gouttes gradué pour délivrer 10 mg, 25 mg et 50 mg de chlorhydrate de thioridazine, USP ( CDN 0078-0001-31).
100 mg/mL
Un liquide clair, jaune clair avec une odeur de fraise. Chaque mL contient 100 mg de chlorhydrate de thioridazine, USP, alcool, 4,2 % en volume. Contenant immédiat : bouteilles en verre ambré de 4 fl. oz. (118 mL), en cartons de 12 flacons, accompagnés d'un compte-gouttes gradué pour délivrer 100 mg, 150 mg et 200 mg de chlorhydrate de thioridazine, USP ( CDN 0078-0009-31).
Stocker et distribuer
En dessous de 86 °F (30 °C) ; flacon en verre ambré étanche.
La solution buvable (concentré) peut être diluée avec de l'eau distillée, de l'eau du robinet acidifiée ou des jus appropriés. Chaque dose doit être ainsi diluée juste avant l'administration - la préparation et la conservation des dilutions en vrac ne sont pas recommandées.
Mellaril (chlorhydrate de thioridazine) -S® (thioridazine) suspension orale
5 mg/mL
Une suspension blanc cassé au goût de menthe poivrée et à l'odeur de menthe poivrée. Chaque mL contient de la thioridazine, USP, équivalente à 5 mg de chlorhydrate de thioridazine, USP. Aromatisé à la menthe dans des bouteilles de pinte (NDC 0078-0068-33).
20 mg/mL
Une suspension jaune au goût de menthe poivrée et à l'odeur de menthe poivrée. Chaque mL contient de la thioridazine, USP, équivalente à 20 mg de chlorhydrate de thioridazine, USP. Aromatisé à la menthe dans des bouteilles de pinte (NDC 0078-0069-33).
Stocker et distribuer
En dessous de 77 °F (25 °C) ; flacon en verre ambré étanche.
Informations supplémentaires disponibles pour les médecins. Novartis Pharmaceuticals Corporation, East Hanover, New Jersey 07936. Révisé : juin 2000.
EFFETS SECONDAIRES
Dans les plages posologiques recommandées avec Mellaril® (chlorhydrate de thioridazine), la plupart des effets secondaires sont légers et transitoires.
Système nerveux central: Une somnolence peut survenir à l'occasion, en particulier lorsque de fortes doses sont administrées au début du traitement. Généralement, cet effet a tendance à s'atténuer avec la poursuite du traitement ou une réduction de la posologie. Un pseudoparkinsonisme et d'autres symptômes extrapyramidaux peuvent survenir mais sont peu fréquents. Une confusion nocturne, une hyperactivité, une léthargie, des réactions psychotiques, une agitation et des maux de tête ont été rapportés mais sont extrêmement rares.
Système nerveux autonome: Sécheresse de la bouche, vision floue, constipation, nausées, vomissements, diarrhée, congestion nasale et pâleur ont été observés.
Système endocrinien: Une galactorrhée, un engorgement mammaire, une aménorrhée, une inhibition de l'éjaculation et un œdème périphérique ont été décrits.
Peau: Des dermatites et des éruptions cutanées de type urticarienne ont été rarement observées. La photosensibilité est extrêmement rare.
Système cardiovasculaire: Mellaril (chlorhydrate de thioridazine) produit un allongement lié à la dose de l'intervalle QTc, qui est associé à la capacité de provoquer des arythmies de type torsade de pointes, une tachycardie ventriculaire polymorphe potentiellement mortelle et une mort subite (voir AVERTISSEMENTS ). Des arythmies de type torsade de pointes et des morts subites ont été signalées en association avec Mellaril (chlorhydrate de thioridazine) . Une relation causale entre ces événements et le traitement par Mellaril (chlorhydrate de thioridazine) n'a pas été établie mais, étant donné la capacité de Mellaril (chlorhydrate de thioridazine) à prolonger l'intervalle QTc, une telle relation est possible. D'autres modifications de l'ECG ont été signalées (voir Dérivés de la phénothiazine : effets cardiovasculaires ).

Autre: De rares cas décrits comme un gonflement de la parotide ont été rapportés après l'administration de Mellaril (chlorhydrate de thioridazine).
Rapports post-introduction
Il s'agit de rapports volontaires d'événements indésirables temporairement associés à Mellaril (chlorhydrate de thioridazine) qui ont été reçus depuis la commercialisation, et il peut n'y avoir aucun lien de causalité entre l'utilisation de Mellaril (chlorhydrate de thioridazine) et ces événements : le priapisme.
Dérivés de la phénothiazine
Il convient de noter que l'efficacité, les indications et les effets indésirables ont varié avec les différentes phénothiazines. Il a été rapporté que la vieillesse diminue la tolérance aux phéno-thiazines. Les effets secondaires neurologiques les plus fréquents chez ces patients sont le parkinsonisme et l'acathisie. Il semble y avoir un risque accru d'agranulocytose et de leucopénie dans la population gériatrique. Le médecin doit être conscient que les événements suivants se sont produits avec une ou plusieurs phénothiazines et doivent être pris en compte chaque fois que l'un de ces médicaments est utilisé :
Réactions autonomes : Myosis, obstipation, anorexie, iléus paralytique.
Réactions cutanées : Érythème, dermatite exfoliative, dermatite de contact.
Dyscrasies sanguines : Agranulocytose, leucopénie, éosinophilie, thrombocytopénie, anémie, anémie aplasique, pancytopénie.
Réactions allergiques : Fièvre, œdème laryngé, œdème de Quincke, asthme.
Hépatotoxicité : Jaunisse, stase biliaire.
Effets cardiovasculaires : Des modifications de la partie terminale de l'électrocardiogramme, notamment un allongement de l'intervalle QT, une dépression et une inversion de l'onde T, ainsi que l'apparition d'une onde provisoirement identifiée comme une onde T bifide ou une onde U, ont été observées chez des patients recevant des phénothiazines, notamment Mellaril (chlorhydrate de thioridazine) . À ce jour, ceux-ci semblent être dus à une repolarisation altérée, non liée à des lésions myocardiques et réversibles. Néanmoins, un allongement significatif de l'intervalle QT a été associé à des arythmies ventriculaires graves et à la mort subite (voir AVERTISSEMENTS ). Une hypotension, entraînant rarement un arrêt cardiaque, a été rapportée.
Symptômes extrapyramidaux : Akathisie, agitation, agitation motrice, réactions dystoniques, trismus, torticolis, opisthotonos, crises oculogyres, tremblements, rigidité musculaire, akinésie.
Dyskinésie tardive: L'utilisation chronique de neuroleptiques peut être associée au développement d'une dyskinésie tardive. Les principales caractéristiques de ce syndrome sont décrites dans le AVERTISSEMENTS section et par la suite.
Le syndrome est caractérisé par des mouvements choréoathétoïdes involontaires qui impliquent de manière variable la langue, le visage, la bouche, les lèvres ou la mâchoire (p. ex., protrusion de la langue, gonflement des joues, plissement de la bouche, mouvements de mastication), le tronc et les extrémités. La gravité du syndrome et le degré de déficience produit varient considérablement.
Le syndrome peut devenir cliniquement reconnaissable soit pendant le traitement, soit lors de la réduction de la posologie, soit à l'arrêt du traitement. Les mouvements peuvent diminuer en intensité et peuvent disparaître complètement si un traitement ultérieur par neuroleptiques est suspendu. On pense généralement que la réversibilité est plus probable après une exposition aux neuroleptiques à court plutôt qu'à long terme. Par conséquent, la détection précoce de la dyskinésie tardive est importante. Pour augmenter la probabilité de détecter le syndrome le plus tôt possible, la posologie du médicament neuroleptique doit être réduite périodiquement (si possible sur le plan clinique) et le patient doit être surveillé pour déceler les signes de la maladie. Cette manœuvre est essentielle, car les médicaments neuroleptiques peuvent masquer les signes du syndrome.
Syndrome malin des neuroleptiques (SMN) : L'utilisation chronique de neuroleptiques peut être associée au développement du syndrome malin des neuroleptiques. Les principales caractéristiques de ce syndrome sont décrites dans le AVERTISSEMENTS section et par la suite. Les manifestations cliniques du SMN sont l'hyperpyrexie, la rigidité musculaire, l'altération de l'état mental et des signes d'instabilité autonome (pouls ou tension artérielle irréguliers, tachycardie, diaphorèse et troubles du rythme cardiaque).
Perturbations endocriniennes : Irrégularités menstruelles, altération de la libido, gynécomastie, lactation, prise de poids, œdème. Des tests de grossesse faussement positifs ont été rapportés.
Troubles urinaires : Rétention, incontinence.
Les autres: Hyperpyrexie. Des effets comportementaux évoquant une réaction paradoxale ont été rapportés. Ceux-ci incluent l'excitation, les rêves bizarres, l'aggravation des psychoses et les états confusionnels toxiques. Plus récemment, un syndrome peau-œil particulier a été reconnu comme un effet secondaire après un traitement à long terme avec des phénothiazines. Cette réaction est marquée par une pigmentation progressive des zones de la peau ou de la conjonctive et/ou accompagnée d'une décoloration de la sclérotique et de la cornée exposées. Des opacités du cristallin antérieur et de la cornée décrites comme étant de forme irrégulière ou étoilée ont également été rapportées. Syndrome de type lupus érythémateux disséminé.
INTERACTIONS MÉDICAMENTEUSES
L'activité réduite de l'isoenzyme 2D6 du cytochrome P450, les médicaments qui inhibent cette isozyme (p. ex., la fluoxétine et la paroxétine) et certains autres médicaments (p. ex., la fluvoxamine, le propranolol et le pindolol) semblent inhiber sensiblement le métabolisme de la thioridazine. On s'attendrait à ce que les niveaux élevés de thioridazine qui en résultent augmentent l'allongement de l'intervalle QTc associé au Mellaril (chlorhydrate de thioridazine) et puissent augmenter le risque d'arythmies cardiaques graves, potentiellement mortelles, telles que les arythmies de type torsade de pointes. Un tel risque accru peut également résulter de l'effet additif de la co-administration de Mellaril (chlorhydrate de thioridazine) avec d'autres agents qui allongent l'intervalle QTc. Par conséquent, Mellaril (chlorhydrate de thioridazine) est contre-indiqué avec ces médicaments ainsi que chez les patients, représentant environ 7 % de la population normale, qui sont connus pour avoir une anomalie génétique entraînant une réduction des niveaux d'activité de P450 2D6 (voir AVERTISSEMENTS et CONTRE-INDICATIONS ).
Médicaments qui inhibent le cytochrome P450 2D6
Dans une étude portant sur 19 sujets masculins en bonne santé, comprenant 6 hydroxylateurs lents et 13 rapides de la débrisoquine, une dose orale unique de 25 mg de thioridazine a produit une Cmax 2,4 fois plus élevée et une ASC 4,5 fois plus élevée pour la thioridazine dans les hydroxylateurs lents par rapport à hydroxylateurs rapides. Le taux d'hydroxylation de la débrisoquine semble dépendre du niveau d'activité de l'isoenzyme 2D6 du cytochrome P450. Ainsi, cette étude suggère que les médicaments qui inhibent P450 2D6 ou la présence de niveaux d'activité réduits de cette isozyme produiront des niveaux plasmatiques élevés de thioridazine. Par conséquent, la co-administration de médicaments qui inhibent P450 2D6 avec Mellaril (chlorhydrate de thioridazine) et l'utilisation de Mellaril (chlorhydrate de thioridazine) chez les patients connus pour avoir une activité réduite de P450 2D6 sont contre-indiquées.
Médicaments qui réduisent la clairance de Mellaril® (chlorhydrate de thioridazine) par d'autres mécanismes
Fluvoxamine : L'effet de la fluvoxamine (25 mg bid pendant une semaine) sur la concentration de thioridazine à l'état d'équilibre a été évalué chez 10 hommes hospitalisés atteints de schizophrénie. Les concentrations de thioridazine et de ses deux métabolites actifs, la mésoridazine et la sulforidazine, ont triplé suite à la co-administration de fluvoxamine. Fluvoxamine et Mellaril (chlorhydrate de thioridazine) ne doivent pas être co-administrés.
Propranolol : Il a été rapporté que l'administration concomitante de propranolol (100 à 800 mg par jour) produisait des augmentations des taux plasmatiques de thioridazine (environ 50 % à 400 %) et de ses métabolites (environ 80 % à 300 %). Le propranolol et le Mellaril (chlorhydrate de thioridazine) ne doivent pas être co-administrés.
Pindolol : L'administration concomitante de pindolol et de thioridazine a entraîné des augmentations modérées et liées à la dose des taux sériques de thioridazine et de deux de ses métabolites, ainsi que des taux sériques de pindolol plus élevés que prévu. Pindolol et Mellaril (chlorhydrate de thioridazine) ne doivent pas être co-administrés.
Médicaments qui allongent l'intervalle QTc
Il n'y a pas d'études sur la co-administration de Mellaril (chlorhydrate de thioridazine) et d'autres médicaments qui allongent l'intervalle QTc. Cependant, on s'attend à ce qu'une telle co-administration produise un allongement additif de l'intervalle QTc et, par conséquent, une telle utilisation est contre-indiquée.
AVERTISSEMENTS
Potentiel d'effets proarythmiques
EN RAISON DU POTENTIEL D'EFFETS PROARRYTHMIQUES SIGNIFICATIFS, POSSIBLEMENT MORTELS AVEC LE TRAITEMENT MELLARIL® (THIORIDAZINE HCl), MELLARIL (thioridazine hcl) DOIT ÊTRE RÉSERVÉ POUR LE TRAITEMENT DES PATIENTS SCHIZOPHRÉNIQUES QUI NE MONTRENT PAS UNE RÉPONSE ACCEPTABLE À DES TRAITEMENTS ADÉQUATS. TRAITEMENT AVEC D'AUTRES MÉDICAMENTS ANTIPSYCHOTIQUES, SOIT EN RAISON D'UNE EFFICACITÉ INSUFFISANTE, SOIT DE L'IMPOSSIBILITÉ D'ATTEINDRE UNE DOSE EFFICACE EN RAISON DES EFFETS INDÉSIRABLES INTOLÉRABLES DE CES MÉDICAMENTS. PAR CONSÉQUENT, AVANT DE COMMENCER UN TRAITEMENT AVEC MELLARIL (thioridazine hcl), IL EST FORTEMENT RECOMMANDÉ QU'UN PATIENT REÇOIT AU MOINS DEUX ESSAIS, CHACUN AVEC UN PRODUIT MÉDICAMENTANT ANTIPSYCHOTIQUE DIFFÉRENT, À UNE DOSE ADÉQUATE ET POUR UNE DURÉE ADÉQUATE. MELLARIL (thioridazine hcl) N'A PAS ÉTÉ ÉVALUÉ SYSTÉMATIQUEMENT DANS DES ESSAIS CONTRÔLÉS DANS LE TRAITEMENT DE PATIENTS SCHIZOPHRÉNIQUES RÉFRACTAIRES ET SON EFFICACITÉ CHEZ CES PATIENTS EST INCONNUE.
Une étude croisée chez neuf hommes en bonne santé comparant des doses uniques de thioridazine 10 mg et 50 mg avec un placebo a démontré un allongement lié à la dose de l'intervalle QTc. L'augmentation maximale moyenne de l'intervalle QTc après la dose de 50 mg était d'environ 23 msec ; un allongement plus important peut être observé dans le traitement clinique des patients non dépistés.
L'allongement de l'intervalle QTc a été associé à la capacité de provoquer des arythmies de type torsade de pointes, une tachycardie ventriculaire polymorphe potentiellement mortelle et une mort subite. Il existe plusieurs rapports de cas publiés de torsade de pointes et de mort subite associés au traitement par la thioridazine. Une relation causale entre ces événements et le traitement par Mellaril (chlorhydrate de thioridazine) n'a pas été établie mais, étant donné la capacité de Mellaril (chlorhydrate de thioridazine) à prolonger l'intervalle QTc, une telle relation est possible.
Certaines circonstances peuvent augmenter le risque de torsade de pointes et/ou de mort subite en association avec l'utilisation de médicaments qui allongent l'intervalle QTc, notamment 1) la bradycardie, 2) l'hypokaliémie, 3) l'utilisation concomitante d'autres médicaments qui allongent l'intervalle QTc, 4) présence d'un allongement congénital de l'intervalle QT, et 5) pour la thioridazine en particulier, son utilisation chez les patients présentant une activité réduite de P450 2D6 ou sa co-administration avec des médicaments pouvant inhiber P450 2D6 ou par un autre mécanisme interférer avec la clairance de thioridazine (voir CONTRE-INDICATIONS et PRÉCAUTIONS ).
Il est recommandé que les patients envisagés pour un traitement par Mellaril (chlorhydrate de thioridazine) subissent un ECG de base et mesurent les taux de potassium sérique. Le potassium sérique doit être normalisé avant d'initier le traitement et les patients présentant un intervalle QTc supérieur à 450 msec ne doivent pas recevoir de traitement par Mellaril (chlorhydrate de thioridazine). Il peut également être utile de surveiller périodiquement les ECG et le potassium sérique pendant le traitement par Mellaril (chlorhydrate de thioridazine), en particulier pendant une période d'ajustement de la dose. Mellaril (chlorhydrate de thioridazine) doit être arrêté chez les patients présentant un intervalle QTc supérieur à 500 msec.
Les patients prenant Mellaril (chlorhydrate de thioridazine) qui présentent des symptômes pouvant être associés à l'apparition de torsades de pointes (par exemple, étourdissements, palpitations ou syncope) peuvent justifier une évaluation cardiaque plus approfondie ; en particulier, la surveillance Holter doit être envisagée.
Dyskinésie tardive
La dyskinésie tardive, un syndrome consistant en des mouvements dyskinétiques involontaires potentiellement irréversibles, peut se développer chez les patients traités avec des médicaments neuroleptiques (antipsychotiques). Bien que la prévalence du syndrome semble être la plus élevée chez les personnes âgées, en particulier les femmes âgées, il est impossible de se fier aux estimations de prévalence pour prédire, au début du traitement neuroleptique, quels patients sont susceptibles de développer le syndrome. On ne sait pas si les médicaments neuroleptiques diffèrent dans leur potentiel de provoquer une dyskinésie tardive.
On pense que le risque de développer le syndrome et la probabilité qu'il devienne irréversible augmentent à mesure que la durée du traitement et la dose cumulée totale de médicaments neuroleptiques administrés au patient augmentent. Cependant, le syndrome peut se développer, bien que beaucoup moins fréquemment, après des périodes de traitement relativement brèves à faibles doses.
Il n'existe aucun traitement connu pour les cas établis de dyskinésie tardive, bien que le syndrome puisse disparaître, partiellement ou complètement, si le traitement neuroleptique est arrêté. Cependant, le traitement neuroleptique lui-même peut supprimer (ou supprimer partiellement) les signes et les symptômes du syndrome et peut ainsi masquer le processus pathologique sous-jacent. L'effet de la suppression symptomatique sur l'évolution à long terme du syndrome est inconnu.
Compte tenu de ces considérations, les neuroleptiques doivent être prescrits de la manière la plus susceptible de minimiser la survenue d'une dyskinésie tardive. Le traitement neuroleptique chronique doit généralement être réservé aux patients qui souffrent d'une maladie chronique qui, 1) est connue pour répondre aux médicaments neuroleptiques, et, 2) pour qui des traitements alternatifs, tout aussi efficaces, mais potentiellement moins nocifs, ne sont pas disponibles ou appropriés. Chez les patients nécessitant un traitement chronique, la dose la plus faible et la durée de traitement la plus courte produisant une réponse clinique satisfaisante doivent être recherchées. La nécessité de poursuivre le traitement doit être réévaluée périodiquement.
Si des signes et symptômes de dyskinésie tardive apparaissent chez un patient sous neuroleptiques, l'arrêt du médicament doit être envisagé. Cependant, certains patients peuvent nécessiter un traitement malgré la présence du syndrome.
(Pour plus d'informations sur la description de la dyskinésie tardive et sa détection clinique, veuillez vous référer aux sections Information pour les patients et EFFETS INDÉSIRABLES. )
Il a été suggéré, en ce qui concerne les phénothiazines en général, que les personnes qui ont manifesté une réaction d'hypersensibilité (p. ex., dyscrasie sanguine, jaunisse) à l'une peuvent être plus enclines à manifester une réaction à d'autres. Il convient de prêter attention au fait que les phénothiazines sont capables de potentialiser les dépresseurs du système nerveux central (par exemple, les anesthésiques, les opiacés, l'alcool, etc.) ainsi que les insecticides à base d'atropine et de phosphore. Les médecins doivent soigneusement évaluer les avantages par rapport aux risques lorsqu'ils traitent des troubles moins graves.
Les études de reproduction chez l'animal et l'expérience clinique à ce jour n'ont pas montré d'effet tératogène avec Mellaril (chlorhydrate de thioridazine) . Cependant, étant donné qu'il est souhaitable de réduire au minimum l'administration de tous les médicaments pendant la grossesse, Mellaril (chlorhydrate de thioridazine) ne doit être administré que lorsque les bénéfices tirés du traitement dépassent les risques éventuels pour la mère et le fœtus.
Syndrome malin des neuroleptiques (SMN)
Un complexe de symptômes potentiellement mortel parfois appelé syndrome malin des neuroleptiques (SMN) a été rapporté en association avec des médicaments antipsychotiques. Les manifestations cliniques du SMN sont l'hyperpyrexie, la rigidité musculaire, l'altération de l'état mental et des signes d'instabilité autonome (pouls ou tension artérielle irréguliers, tachycardie, diaphorèse et troubles du rythme cardiaque).
L'évaluation diagnostique des patients atteints de ce syndrome est compliquée. Pour arriver à un diagnostic, il est important d'identifier les cas où la présentation clinique comprend à la fois une maladie médicale grave (p. ex., pneumonie, infection systémique, etc.) et des signes et symptômes extrapyramidaux non traités ou insuffisamment traités. D'autres considérations importantes dans le diagnostic différentiel comprennent la toxicité anticholinergique centrale, le coup de chaleur, la fièvre médicamenteuse et la pathologie primaire du système nerveux central (SNC).
La prise en charge du SMN doit inclure 1) l'arrêt immédiat des médicaments antipsychotiques et d'autres médicaments non essentiels au traitement concomitant, 2) un traitement symptomatique intensif et une surveillance médicale, et 3) le traitement de tout problème médical grave concomitant pour lequel des traitements spécifiques sont disponibles. Il n'y a pas d'accord général sur les schémas thérapeutiques pharmacologiques spécifiques pour le SMN non compliqué.
Si un patient nécessite un traitement médicamenteux antipsychotique après avoir récupéré d'un SMN, la réintroduction potentielle d'un traitement médicamenteux doit être soigneusement envisagée. Le patient doit être étroitement surveillé, car des récidives de SMN ont été rapportées.
Dépresseurs du système nerveux central
Comme dans le cas des autres phénothiazines, Mellaril (thioridazine hcl) est capable de potentialiser les dépresseurs du système nerveux central (par exemple, l'alcool, les anesthésiques, les barbituriques, les narcotiques, les opiacés, d'autres médicaments psychoactifs, etc.) ainsi que les insecticides à base d'atropine et de phosphore. Une dépression respiratoire sévère et un arrêt respiratoire ont été rapportés lorsqu'un patient a reçu une phénothiazine et une forte dose concomitante d'un barbiturique.
PRÉCAUTIONS
Une leucopénie et/ou une agranulocytose et des convulsions ont été rapportées mais sont peu fréquentes. Mellaril® (chlorhydrate de thioridazine) s'est avéré utile dans le traitement des troubles du comportement chez les patients épileptiques, mais les médicaments anticonvulsivants doivent également être maintenus. La rétinopathie pigmentaire, qui a été observée principalement chez les patients prenant des doses supérieures aux doses recommandées, se caractérise par une diminution de l'acuité visuelle, une coloration brunâtre de la vision et une altération de la vision nocturne ; l'examen du fond d'œil révèle des dépôts de pigment. La possibilité de cette complication peut être réduite en restant dans les limites de dosage recommandées.
Lorsque les patients participent à des activités nécessitant une vigilance mentale complète (par exemple, la conduite), il est conseillé d'administrer les phénothiazines avec prudence et d'augmenter progressivement la posologie. Les patientes semblent avoir une plus grande tendance à l'hypotension orthostatique que les patients masculins. L'administration d'épinéphrine doit être évitée dans le traitement de l'hypotension d'origine médicamenteuse compte tenu du fait que les phénothiazines peuvent parfois induire un effet inverse de l'épinéphrine. Si un vasoconstricteur est nécessaire, les plus appropriés sont le lévartérénol et la phényléphrine.
Les médicaments neuroleptiques élèvent les niveaux de prolactine; l'élévation persiste pendant l'administration chronique. Des expériences de culture de tissus indiquent qu'environ un tiers des cancers du sein humains sont dépendants de la prolactine in vitro, un facteur d'importance potentielle si la prescription de ces médicaments est envisagée chez une patiente atteinte d'un cancer du sein déjà détecté. Bien que des troubles tels que la galactorrhée, l'aménorrhée, la gynécomastie et l'impuissance aient été rapportés, la signification clinique des taux sériques élevés de prolactine est inconnue pour la plupart des patients. Une augmentation des néoplasmes mammaires a été constatée chez les rongeurs après administration chronique de médicaments neuroleptiques. Cependant, ni les études cliniques ni les études épidémiologiques menées à ce jour n'ont montré d'association entre l'administration chronique de ces médicaments et la tumorigenèse mammaire ; les preuves disponibles sont considérées comme trop limitées pour être concluantes à l'heure actuelle.
Utilisation pédiatrique
Voir DOSAGE section Patients pédiatriques .
SURDOSAGE
Bon nombre des symptômes observés sont des prolongements des effets secondaires décrits sous EFFETS INDÉSIRABLES. Mellaril® (chlorhydrate de thioridazine) (chlorhydrate de thioridazine) peut être toxique en cas de surdosage, la toxicité cardiaque étant particulièrement préoccupante. Une surveillance fréquente de l'ECG et des signes vitaux des patients en surdosage est recommandée. Une observation de plusieurs jours peut être nécessaire en raison du risque d'effets différés.
Signes et symptômes
Les effets et les complications cliniques d'un surdosage aigu impliquant des phénothiazines peuvent inclure :
Cardiovasculaire: Arythmies cardiaques, hypotension, choc, modifications de l'ECG, allongement des intervalles QT et PR, modifications non spécifiques des ondes ST et T, bradycardie, tachycardie sinusale, bloc auriculo-ventriculaire, tachycardie ventriculaire, fibrillation ventriculaire, torsades de pointes, dépression myocardique.
Système nerveux central: Sédation, effets extrapyramidaux, confusion, agitation, hypothermie, hyperthermie, agitation, convulsions, aréflexie, coma.
Système nerveux autonome: Mydriase, myosis, peau sèche, bouche sèche, congestion nasale, rétention urinaire, vision floue.
Respiratoire: Dépression respiratoire, apnée, œdème pulmonaire.
Gastro-intestinal : Hypomotilité, constipation, iléus.
Rénal: Oligurie, urémie.
Les plages de dose toxique et de concentration sanguine des phénothiazines n'ont pas été fermement établies. Il a été suggéré que la plage de concentration sanguine toxique pour la thioridazine commence à 1,0 mg/dL, et 2-8 mg/dL est la plage de concentration létale.
Traitement
Une voie aérienne doit être établie et entretenue. Une oxygénation et une ventilation adéquates doivent être assurées.
La surveillance cardiovasculaire doit commencer immédiatement et doit inclure une surveillance électrocardiographique continue pour détecter d'éventuelles arythmies. Le traitement peut inclure une ou plusieurs des interventions thérapeutiques suivantes : correction des anomalies électrolytiques et de l'équilibre acido-basique, lidocaïne, phénytoïne, isoprotérénol, stimulation ventriculaire et défibrillation. Le disopyramide, le procaïnamide et la quinidine peuvent produire des effets additifs d'allongement de l'intervalle QT lorsqu'ils sont administrés à des patients présentant un surdosage aigu de Mellaril et doivent être évités (voir AVERTISSEMENTS et CONTRE-INDICATIONS ). La prudence s'impose lors de l'administration de lidocaïne, car elle peut augmenter le risque de développer des convulsions.
Le traitement de l'hypotension peut nécessiter des fluides intraveineux et des vasopresseurs. La phényléphrine, le lévartérénol ou le métaraminol sont les agents vasopresseurs appropriés à utiliser dans la prise en charge de l'hypotension réfractaire. Les puissantes propriétés bloquantes α-adrénergiques des phénothiazines rendent inappropriée l'utilisation de vasopresseurs ayant des propriétés agonistes mixtes α et β-adrénergiques, notamment l'épinéphrine et la dopamine. Une vasodilatation paradoxale peut en résulter. De plus, il est raisonnable de s'attendre à ce que les propriétés de blocage α-adrénergique du brétylium puissent s'ajouter à celles du Mellaril (thioridazine hcl), entraînant une hypotension problématique.
Lors de la prise en charge d'un surdosage, le médecin doit toujours envisager la possibilité d'une implication de plusieurs médicaments. Un lavage gastrique et des doses répétées de charbon actif doivent être envisagés. L'induction de vomissements est moins préférable au lavage gastrique en raison du risque de dystonie et du potentiel d'aspiration de vomissures. Les vomissements ne doivent pas être provoqués chez les patients susceptibles de se détériorer rapidement ou chez ceux dont la conscience est altérée.
Les symptômes extrapyramidaux aigus peuvent être traités avec du chlorhydrate de diphénhydramine ou du mésylate de benztropine.
Évitez l'utilisation de barbituriques lors du traitement des convulsions, car ils peuvent potentialiser la dépression respiratoire induite par la phénothiazine.
La diurèse forcée, l'hémoperfusion, l'hémodialyse et la manipulation du pH de l'urine sont d'un bénéfice peu probable dans le traitement d'un surdosage de phénothiazine en raison de leur grand volume de distribution et de leur forte liaison aux protéines plasmatiques.
Des informations à jour sur le traitement d'un surdosage peuvent souvent être obtenues auprès d'un centre antipoison régional certifié. Les numéros de téléphone des centres antipoison régionaux certifiés sont répertoriés dans le Physicians' Desk Reference®**.
CONTRE-INDICATIONS
L'utilisation de Mellaril® (chlorhydrate de thioridazine) doit être évitée en association avec d'autres médicaments connus pour allonger l'intervalle QTc et chez les patients présentant un syndrome du QT long congénital ou des antécédents d'arythmies cardiaques.
Réduction de l'activité de l'isoenzyme 2D6 du cytochrome P450 Les médicaments qui inhibent cette isozyme (p. ex., fluoxétine et paroxétine) et certains autres médicaments (p. ex., fluvoxamine, propranolol et pindolol) semblent inhiber sensiblement le métabolisme de la thioridazine. On s'attendrait à ce que les niveaux élevés de thioridazine qui en résultent augmentent l'allongement de l'intervalle QTc associé au Mellaril (chlorhydrate de thioridazine) et puissent augmenter le risque d'arythmies cardiaques graves, potentiellement mortelles, telles que les arythmies de type torsade de pointes. Un tel risque accru peut également résulter de l'effet additif de la co-administration de Mellaril (chlorhydrate de thioridazine) avec d'autres agents qui allongent l'intervalle QTc. Par conséquent, Mellaril (chlorhydrate de thioridazine) est contre-indiqué avec ces médicaments ainsi que chez les patients, représentant environ 7 % de la population normale, qui sont connus pour avoir une anomalie génétique entraînant une réduction des niveaux d'activité de P450 2D6 (voir AVERTISSEMENTS et PRÉCAUTIONS ).
Comme d'autres phénothiazines, Mellaril (chlorhydrate de thioridazine) est contre-indiqué en cas de dépression sévère du système nerveux central ou d'états comateux quelle qu'en soit la cause, y compris la dépression du système nerveux central d'origine médicamenteuse (voir AVERTISSEMENTS ). Il convient également de noter qu'une cardiopathie hypertensive ou hypotensive de degré extrême est une contre-indication à l'administration de phénothiazine.
PHARMACOLOGIE CLINIQUE
L'activité pharmacologique de base du Mellaril® (chlorhydrate de thioridazine) est similaire à celle des autres phénothiazines, mais est associée à une stimulation extrapyramidale minimale.
Cependant, il a été démontré que la thioridazine prolonge l'intervalle QTc de manière dose-dépendante. Cet effet peut augmenter le risque d'arythmies ventriculaires graves, potentiellement mortelles, telles que les arythmies de type torsade de pointes. En raison de ce risque, Mellaril (chlorhydrate de thioridazine) est indiqué uniquement chez les patients schizophrènes qui n'ont pas répondu ou ne peuvent pas tolérer d'autres agents antipsychotiques (voir AVERTISSEMENTS et CONTRE-INDICATIONS ). Cependant, le prescripteur doit être conscient que Mellaril (chlorhydrate de thioridazine) n'a pas été systématiquement évalué dans des essais contrôlés chez des patients schizophrènes réfractaires au traitement et que son efficacité chez ces patients est inconnue.
INFORMATIONS PATIENTS
Les patients doivent être informés que Mellaril (chlorhydrate de thioridazine) a été associé à des troubles du rythme cardiaque potentiellement mortels. Le risque de tels événements peut être augmenté lorsque certains médicaments sont administrés avec Mellaril (chlorhydrate de thioridazine). Par conséquent, les patients doivent informer le prescripteur qu'ils reçoivent un traitement par Mellaril (chlorhydrate de thioridazine) avant de prendre tout nouveau médicament.
Compte tenu de la probabilité que certains patients exposés de façon chronique aux neuroleptiques développent une dyskinésie tardive, il est conseillé que tous les patients chez qui une utilisation chronique est envisagée reçoivent, si possible, une information complète sur ce risque. La décision d'informer les patients et/ou leurs tuteurs doit évidemment tenir compte des circonstances cliniques et de la capacité du patient à comprendre les informations fournies.
