Reglan 10mg Metoclopramide Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
Qu'est-ce que Reglan 10 mg et comment est-il utilisé ?
Reglan 10 mg est un médicament délivré sur ordonnance utilisé pour traiter les symptômes du reflux gastro-oesophagien (RGO), des nausées et des vomissements causés par la chimiothérapie, la gastroparésie diabétique et lors de la radiologie du tractus gastro-intestinal supérieur. Reglan 10 mg peut être utilisé seul ou avec d'autres médicaments.
Reglan 10 mg appartient à une classe de médicaments appelés agents antiémétiques ; Agents procinétiques.
Quels sont les effets secondaires possibles de Reglan 10mg ?
Reglan peut provoquer des effets secondaires graves, notamment :
- tremblements ou secousses dans les bras ou les jambes,
- confusion,
- la dépression,
- pensées suicidaires ou de vous faire du mal,
- mouvements musculaires lents ou saccadés de votre visage,
- convulsions (convulsions),
- anxiété,
- agitation,
- sensation de nervosité,
- difficulté à rester immobile,
- troubles du sommeil (insomnie),
- gonflement,
- essoufflement,
- prise de poids rapide,
- muscles très raides ou rigides,
- forte fièvre,
- transpiration,
- confusion,
- battements cardiaques rapides ou irréguliers, et
- étourdissement
Consultez immédiatement un médecin si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires les plus courants de Reglan 10 mg incluent :
- agitation,
- somnolence,
- manque d'énergie,
- nausée,
- vomissement,
- mal de tête,
- confusion, et
- troubles du sommeil (insomnie)
Dites au médecin si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas.
Ce ne sont pas tous les effets secondaires possibles de Reglan. Pour plus d'informations, consultez votre médecin ou votre pharmacien.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
ATTENTION
DYSKINÉSIE TARDIVE
Le traitement par le métoclopramide peut provoquer une dyskinésie tardive, un trouble du mouvement grave souvent irréversible. Le risque de développer une dyskinésie tardive augmente avec la durée du traitement et la dose cumulée totale.
Le traitement par métoclopramide doit être interrompu chez les patients qui développent des signes ou des symptômes de dyskinésie tardive. Il n'existe aucun traitement connu pour la dyskinésie tardive. Chez certains patients, les symptômes peuvent s'atténuer ou disparaître après l'arrêt du traitement par le métoclopramide.
Le traitement par métoclopramide pendant plus de 12 semaines doit être évité dans tous les cas, sauf rares, où l'on pense que le bénéfice thérapeutique l'emporte sur le risque de développer une dyskinésie tardive.
Voir les AVERTISSEMENTS
LA DESCRIPTION
Pour l'administration orale, les comprimés de reglan® (comprimés de métoclopramide, USP) 10 mg sont des comprimés blancs, sécables, en forme de capsule gravés « REGLAN » sur un côté et « ANI 10 » sur le côté opposé.
Chaque tablette contient:
Métoclopramide base 10 mg (sous forme de monochlorhydrate monohydraté)
ingrédients inactifs
Stéarate de magnésium, mannitol, cellulose microcristalline, acide stéarique.
Les comprimés reglan® (comprimés de métoclopramide, USP) à 5 mg sont des comprimés verts de forme elliptique gravés « REGLAN » sur « 5 » sur un côté et « ANI » sur le côté opposé.
Chaque tablette contient:
Métoclopramide base 5 mg (sous forme de monochlorhydrate monohydraté)
ingrédients inactifs
Amidon de maïs, laque d'aluminium D&C jaune 10, laque d'aluminium FD&C bleu 1, lactose, cellulose microcristalline, dioxyde de silicium, acide stéarique.
Le chlorhydrate de métoclopramide est une substance blanche cristalline, inodore, librement soluble dans l'eau. Chimiquement, il s'agit du monochlorhydrate monohydraté de 4-amino-5-chloro-N-[2-(diéthylamino)éthyl]-2-méthoxy benzamide. Sa formule moléculaire est C14H22ClN3O2 • HCl • H2O. Son poids moléculaire est de 354,3.
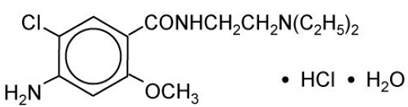
LES INDICATIONS
L'utilisation des comprimés de reglan® est recommandée pour les adultes uniquement. La durée du traitement ne doit pas dépasser 12 semaines.
Reflux gastro-oesophagien symptomatique
Les comprimés reglan® sont indiqués comme traitement à court terme (4 à 12 semaines) pour les adultes souffrant de reflux gastro-œsophagien symptomatique et documenté qui ne répondent pas au traitement conventionnel.
Le principal effet du métoclopramide est sur les symptômes de brûlures d'estomac postprandiales et diurnes avec un effet moins observé sur les symptômes nocturnes. Si les symptômes se limitent à des situations particulières, comme après le repas du soir, l'utilisation de métoclopramide en doses uniques avant la situation provocatrice doit être envisagée, plutôt que d'utiliser le médicament tout au long de la journée. La guérison des ulcères et des érosions de l'œsophage a été démontrée par endoscopie à la fin d'un essai de 12 semaines utilisant des doses de 15 mg qid Comme il n'y a pas de corrélation documentée entre les symptômes et la guérison des lésions de l'œsophage, les patients présentant des lésions documentées doivent être surveillés par endoscopie.
Gastroparésie diabétique (stase gastrique diabétique)
Les comprimés reglan® (comprimés de métoclopramide, USP) sont indiqués pour le soulagement des symptômes associés à la stase gastrique diabétique aiguë et récurrente. Les manifestations habituelles de la vidange gastrique retardée (p. ex., nausées, vomissements, brûlures d'estomac, plénitude persistante après les repas et anorexie) semblent répondre au reglan® dans des intervalles de temps différents. Un soulagement significatif des nausées survient tôt et continue de s'améliorer sur une période de trois semaines. Le soulagement des vomissements et de l'anorexie peut précéder le soulagement de la plénitude abdominale d'une semaine ou plus.
DOSAGE ET ADMINISTRATION
Le traitement avec les comprimés reglan® ne doit pas dépasser 12 semaines.
Pour le soulagement du reflux gastro-oesophagien symptomatique
Administrer de 10 mg à 15 mg de reglan® (chlorhydrate de métoclopramide, USP) par voie orale jusqu'à qid 30 minutes avant chaque repas et au coucher, selon les symptômes à traiter et la réponse clinique (voir PHARMACOLOGIE CLINIQUE et INDICATIONS ET USAGE ). Si les symptômes ne surviennent que par intermittence ou à des moments précis de la journée, l'utilisation de métoclopramide en doses uniques jusqu'à 20 mg avant la situation provoquante peut être préférée à un traitement continu. Parfois, les patients (tels que les patients âgés) qui sont plus sensibles aux effets thérapeutiques ou indésirables du métoclopramide n'auront besoin que de 5 mg par dose.
L'expérience avec les érosions et les ulcérations oesophagiennes est limitée, mais la guérison a jusqu'à présent été documentée dans un essai contrôlé utilisant un traitement qid à 15 mg/dose, et ce schéma thérapeutique doit être utilisé lorsque des lésions sont présentes, tant qu'il est toléré (voir EFFETS INDÉSIRABLES ). En raison de la faible corrélation entre les symptômes et l'aspect endoscopique de l'œsophage, le traitement dirigé contre les lésions œsophagiennes est mieux guidé par une évaluation endoscopique.
Un traitement de plus de 12 semaines n'a pas été évalué et ne peut être recommandé.
Pour le soulagement des symptômes As s ociated with Diabetic Gas tropares is (Diabetic Gas tric Stas is ) Administrer 10 mg de métoclopramide 30 minutes avant chaque repas et au coucher pendant deux à huit semaines, selon la réponse et la probabilité de bien-être continu à l'arrêt du médicament.
La voie d'administration initiale doit être déterminée par la sévérité des symptômes présentés. Si seules les premières manifestations de la stase gastrique diabétique sont présentes, l'administration orale de reglan® peut être initiée. Cependant, si des symptômes graves sont présents, le traitement doit commencer par une injection de métoclopramide (consulter l'étiquetage de l'injection avant de commencer l'administration parentérale).
L'administration d'une injection de métoclopramide jusqu'à 10 jours peut être nécessaire avant que les symptômes ne disparaissent, moment auquel une administration orale peut être instituée. Étant donné que la stase gastrique diabétique est fréquemment récurrente, le traitement par reglan® doit être réinstauré dès la première manifestation.
Utilisation chez les patients atteints d'insuffisance rénale ou hépatique
Étant donné que le métoclopramide est principalement excrété par les reins, chez les patients dont la clairance de la créatinine est inférieure à 40 mL/min, le traitement doit être instauré à environ la moitié de la dose recommandée. Selon les considérations d'efficacité et de sécurité cliniques, la posologie peut être augmentée ou diminuée selon le cas.
Voir SURDOSAGE section pour plus d'informations sur la dialyse.
Le métoclopramide subit un métabolisme hépatique minimal, à l'exception d'une simple conjugaison. Son utilisation sûre a été décrite chez des patients atteints d'une maladie hépatique avancée dont la fonction rénale était normale.
COMMENT FOURNIE
Chaque comprimé reglan® blanc, en forme de capsule et sécable (comprimés de métoclopramide, USP) contient 10 mg de métoclopramide base (sous forme de monochlorhydrate monohydraté). Disponible en:
Flacons de 100 comprimés ( CDN 62559-166-01)
Chaque comprimé reglan® vert de forme elliptique (comprimés de métoclopramide, USP) contient 5 mg de métoclopramide base (sous forme de monochlorhydrate monohydraté). Disponible en:
Flacons de 100 comprimés ( CDN 62559-165-01)
Distribuer les comprimés dans un récipient étanche et résistant à la lumière.
Les comprimés doivent être conservés à température ambiante contrôlée, entre 20°C et 25°C (68°F et 77°F).
Fabriqué par : ANI Pharmaceuticals, Inc. Baudette, MN 56623. Révisé : décembre 2014
EFFETS SECONDAIRES
En général, l'incidence des effets indésirables est corrélée à la dose et à la durée d'administration du métoclopramide. Les réactions suivantes ont été signalées, bien que dans la plupart des cas, les données ne permettent pas d'en estimer la fréquence :
Effets sur le SNC
L'agitation, la somnolence, la fatigue et la lassitude surviennent chez environ 10 % des patients recevant la dose la plus couramment prescrite de 10 mg qid (voir PRÉCAUTIONS ). Insomnie, maux de tête, confusion, étourdissements ou dépression mentale avec idées suicidaires (voir AVERTISSEMENTS surviennent moins fréquemment. L'incidence de la somnolence est plus élevée à des doses plus élevées. Il existe des rapports isolés de crises convulsives sans relation claire avec le métoclopramide. Rarement, des hallucinations ont été rapportées.
Réactions extrapyramidales (EPS)
Les réactions dystoniques aiguës, le type le plus courant d'EPS associé au métoclopramide, surviennent chez environ 0,2 % des patients (1 sur 500) traités par 30 à 40 mg de métoclopramide par jour. Les symptômes comprennent des mouvements involontaires des membres, des grimaces faciales, un torticolis, une crise oculogyre, une saillie rythmique de la langue, un discours de type bulbaire, un trismus, un opisthotonus (réactions de type tétanique) et, rarement, un stridor et une dyspnée éventuellement dus à un laryngospasme ; habituellement, ces symptômes sont facilement inversés par la diphenhydramine (voir AVERTISSEMENTS ).
Les symptômes de type parkinsonien peuvent inclure une bradykinésie, des tremblements, une rigidité de la roue dentée, un faciès semblable à un masque (voir AVERTISSEMENTS ).
La dyskinésie tardive est le plus souvent caractérisée par des mouvements involontaires de la langue, du visage, de la bouche ou de la mâchoire, et parfois par des mouvements involontaires du tronc et/ou des extrémités ; les mouvements peuvent être d'apparence choréo-athétotique (voir AVERTISSEMENTS ).
L'agitation motrice (akathisie) peut consister en des sentiments d'anxiété, d'agitation, de nervosité et d'insomnie, ainsi qu'une incapacité à rester assis, à faire les cent pas, à taper du pied. Ces symptômes peuvent disparaître spontanément ou répondre à une réduction de la posologie.
Syndrome malin des neuroleptiques
De rares cas de syndrome malin des neuroleptiques (SMN) ont été rapportés. Ce syndrome potentiellement mortel comprend le complexe de symptômes d'hyperthermie, d'altération de la conscience, de rigidité musculaire et de dysfonctionnement autonome (voir AVERTISSEMENTS ).
Perturbations endocriniennes
Galactorrhée, aménorrhée, gynécomastie, impuissance secondaire à une hyperprolactinémie (voir PRÉCAUTIONS ). Rétention hydrique secondaire à une élévation transitoire de l'aldostérone (voir PHARMACOLOGIE CLINIQUE ).
Cardiovasculaire
Hypotension, hypertension, tachycardie supraventriculaire, bradycardie, rétention hydrique, insuffisance cardiaque congestive aiguë et bloc AV possible (voir CONTRE-INDICATIONS et PRÉCAUTIONS ).
Gastro-intestinal
Nausées et troubles intestinaux, principalement diarrhée.
Hépatique
Rarement, cas d'hépatotoxicité, caractérisée par des signes tels qu'un ictère et une altération des tests de la fonction hépatique, lorsque le métoclopramide a été administré avec d'autres médicaments ayant un potentiel hépatotoxique connu.
Rénal
Fréquence urinaire et incontinence.
Hématologique
Quelques cas de neutropénie, de leucopénie ou d'agranulocytose, généralement sans lien clair avec le métoclopramide. Méthémoglobinémie, chez l'adulte et surtout en cas de surdosage chez le nouveau-né (voir SURDOSAGE ). Sulfhémoglobinémie chez l'adulte.
Réactions allergiques
Quelques cas d'éruption cutanée, d'urticaire ou de bronchospasme, en particulier chez les patients ayant des antécédents d'asthme. Rarement, œdème angioneurotique, y compris œdème glossal ou laryngé.
Divers
Troubles visuels. Porphyrie.
INTERACTIONS MÉDICAMENTEUSES
Les effets du métoclopramide sur la motilité gastro-intestinale sont contrecarrés par les médicaments anticholinergiques et les analgésiques narcotiques. Des effets sédatifs additifs peuvent survenir lorsque le métoclopramide est administré avec de l'alcool, des sédatifs, des hypnotiques, des narcotiques ou des tranquillisants.
La découverte que le métoclopramide libère des catécholamines chez les patients souffrant d'hypertension essentielle suggère qu'il doit être utilisé avec prudence, voire pas du tout, chez les patients recevant des inhibiteurs de la monoamine oxydase.
L'absorption de médicaments par l'estomac peut être diminuée (p. ex., digoxine) par le métoclopramide, tandis que la vitesse et/ou l'étendue de l'absorption de médicaments par l'intestin grêle peuvent être augmentées (p. ex., acétaminophène, tétracycline, lévodopa, éthanol, cyclosporine).
La gastroparésie (stase gastrique) peut être responsable d'un mauvais contrôle du diabète chez certains patients. L'insuline administrée de manière exogène peut commencer à agir avant que les aliments aient quitté l'estomac et entraîner une hypoglycémie. Étant donné que l'action du métoclopramide influencera l'apport de nourriture dans les intestins et donc le taux d'absorption, la posologie de l'insuline ou le moment de l'administration peuvent nécessiter un ajustement.
AVERTISSEMENTS
La dépression mentale est survenue chez des patients avec et sans antécédent de dépression. Les symptômes allaient de légers à graves et comprenaient des idées suicidaires et le suicide. Le métoclopramide ne doit être administré aux patients ayant des antécédents de dépression que si les bénéfices attendus l'emportent sur les risques potentiels.
Des symptômes extrapyramidaux, se manifestant principalement par des réactions dystoniques aiguës, surviennent chez environ 1 patient sur 500 traités avec les doses adultes habituelles de 30 à 40 mg/jour de métoclopramide. Ceux-ci sont généralement observés au cours des 24 à 48 premières heures de traitement par le métoclopramide, surviennent plus fréquemment chez les patients pédiatriques et les patients adultes de moins de 30 ans et sont encore plus fréquents à des doses plus élevées. Ces symptômes peuvent inclure des mouvements involontaires des membres et des grimaces faciales, un torticolis, une crise oculogyre, une protrusion rythmique de la langue, un discours de type bulbaire, un trismus ou des réactions dystoniques ressemblant au tétanos. Rarement, des réactions dystoniques peuvent se présenter sous forme de stridor et de dyspnée, probablement dues à un laryngospasme. Si ces symptômes devaient apparaître, injectez 50 mg de chlorhydrate de diphenhydramine par voie intramusculaire et ils disparaîtront généralement. Le mésylate de benztropine, 1 à 2 mg par voie intramusculaire, peut également être utilisé pour inverser ces réactions.
Des symptômes de type parkinsonien sont apparus, plus fréquemment au cours des 6 premiers mois après le début du traitement par le métoclopramide, mais parfois après des périodes plus longues. Ces symptômes disparaissent généralement dans les 2 à 3 mois suivant l'arrêt du métoclopramide. Les patients atteints de la maladie de Parkinson préexistante doivent recevoir du métoclopramide avec prudence, voire pas du tout, car ces patients peuvent présenter une exacerbation des symptômes parkinsoniens lors de la prise de métoclopramide.
Dyskinésie tardive
(Voir BOX AVERTISSEMENT)
Le traitement par le métoclopramide peut provoquer une dyskinésie tardive (TD), un trouble potentiellement irréversible et défigurant caractérisé par des mouvements involontaires du visage, de la langue ou des extrémités. Le risque de développer une dyskinésie tardive augmente avec la durée du traitement et la dose cumulée totale. Une analyse des schémas d'utilisation a montré qu'environ 20 % des patients qui prenaient du métoclopramide le prenaient pendant plus de 12 semaines. Le traitement par métoclopramide pendant plus longtemps que les 12 semaines recommandées doit être évité dans tous les cas, sauf rares, où l'on pense que le bénéfice thérapeutique l'emporte sur le risque de développer une DT.
Bien que le risque de développer une TD dans la population générale puisse être accru chez les personnes âgées, les femmes et les diabétiques, il n'est pas possible de prédire quels patients développeront une DT induite par le métoclopramide. Le risque de développer la DT et la probabilité que la DT devienne irréversible augmentent avec la durée du traitement et la dose cumulée totale.
Le métoclopramide doit être arrêté chez les patients qui développent des signes ou des symptômes de TD. Il n'existe aucun traitement efficace connu pour les cas établis de DT, bien que chez certains patients, la DT puisse disparaître, partiellement ou complètement, quelques semaines à plusieurs mois après l'arrêt du métoclopramide.
Le métoclopramide lui-même peut supprimer, ou supprimer partiellement, les signes de TD, masquant ainsi le processus pathologique sous-jacent. L'effet de cette suppression symptomatique sur l'évolution à long terme de la DT est inconnu. Par conséquent, le métoclopramide ne doit pas être utilisé pour le contrôle symptomatique de la TD.
Syndrome malin des neuroleptiques (SMN)
De rares cas ont été rapportés d'un complexe de symptômes peu fréquent mais potentiellement mortel, parfois appelé syndrome malin des neuroleptiques (SMN) associé au métoclopramide. Les manifestations cliniques du SMN comprennent l'hyperthermie, la rigidité musculaire, une altération de la conscience et des signes d'instabilité autonome (pouls ou tension artérielle irréguliers, tachycardie, diaphorèse et arythmies cardiaques).
L'évaluation diagnostique des patients atteints de ce syndrome est compliquée. Pour arriver à un diagnostic, il est important d'identifier les cas où la présentation clinique comprend à la fois une maladie médicale grave (p. ex., pneumonie, infection systémique, etc.) et des signes et symptômes extrapyramidaux non traités ou insuffisamment traités. D'autres considérations importantes dans le diagnostic différentiel comprennent la toxicité anticholinergique centrale, le coup de chaleur, l'hyperthermie maligne, la fièvre médicamenteuse et la pathologie primaire du système nerveux central (SNC).
La prise en charge du SMN doit inclure 1) l'arrêt immédiat du métoclopramide et d'autres médicaments non essentiels au traitement concomitant, 2) un traitement symptomatique intensif et une surveillance médicale, et 3) le traitement de tout problème médical concomitant grave pour lequel des traitements spécifiques sont disponibles. La bromocriptine et le dantrolène sodique ont été utilisés dans le traitement du SMN, mais leur efficacité n'a pas été établie (voir EFFETS INDÉSIRABLES ).
PRÉCAUTIONS
Général
Dans une étude menée chez des patients hypertendus, il a été démontré que le métoclopramide administré par voie intraveineuse libère des catécholamines ; par conséquent, la prudence s'impose lorsque le métoclopramide est utilisé chez des patients souffrant d'hypertension.
Étant donné que le métoclopramide produit une augmentation transitoire de l'aldostérone plasmatique, certains patients, en particulier ceux atteints de cirrhose ou d'insuffisance cardiaque congestive, peuvent être à risque de développer une rétention hydrique et une surcharge volémique. Si ces effets indésirables surviennent à tout moment pendant le traitement par le métoclopramide, le médicament doit être arrêté.
Des effets indésirables, en particulier ceux impliquant le système nerveux, peuvent survenir après l'arrêt de l'utilisation de reglan®. Un petit nombre de patients peuvent connaître une période de sevrage après l'arrêt de reglan® qui peut inclure des étourdissements, de la nervosité et/ou des maux de tête.
Informations pour les patients
L'utilisation de reglan® est recommandée pour les adultes uniquement. Le métoclopramide peut altérer les capacités mentales et/ou physiques nécessaires à l'exécution de tâches dangereuses telles que l'utilisation de machines ou la conduite d'un véhicule à moteur. Le patient ambulatoire doit être averti en conséquence.
Pour plus d'informations, les patients doivent être invités à consulter le Guide des médicaments pour les comprimés reglan®.

Carcinogenèse, mutagenèse, altération de la fertilité
Une étude de 77 semaines a été menée chez des rats avec des doses orales allant jusqu'à environ 40 fois la dose quotidienne maximale recommandée chez l'homme. Le métoclopramide élève les taux de prolactine et l'élévation persiste pendant l'administration chronique. Des expériences de culture de tissus indiquent qu'environ un tiers des cancers du sein humains sont prolactine-dépendants in vitro, un facteur d'importance potentielle si la prescription de métoclopramide est envisagée chez une patiente atteinte d'un cancer du sein préalablement détecté. Bien que des troubles tels que la galactorrhée, l'aménorrhée, la gynécomastie et l'impuissance aient été rapportés avec les médicaments élevant la prolactine, la signification clinique des taux sériques élevés de prolactine est inconnue pour la plupart des patients. Une augmentation des néoplasmes mammaires a été constatée chez les rongeurs après administration chronique de neuroleptiques stimulant la prolactine et de métoclopramide. Cependant, ni les études cliniques ni les études épidémiologiques menées à ce jour n'ont montré d'association entre l'administration chronique de ces médicaments et la tumorigenèse mammaire ; les preuves disponibles sont trop limitées pour être concluantes à l'heure actuelle.
Un test de mutagénicité d'Ames réalisé sur le métoclopramide s'est révélé négatif.
Catégorie de grossesse B
Des études de reproduction réalisées chez des rats, des souris et des lapins par les voies IV, IM, SC et orale à des doses maximales allant de 12 à 250 fois la dose humaine n'ont démontré aucune altération de la fertilité ni aucun effet nocif important pour le fœtus dû au métoclopramide. Il n'y a cependant pas d'études adéquates et bien contrôlées chez les femmes enceintes. Étant donné que les études sur la reproduction chez l'animal ne sont pas toujours prédictives de la réponse humaine, ce médicament ne doit être utilisé pendant la grossesse qu'en cas de nécessité absolue.
Mères allaitantes
Le métoclopramide est excrété dans le lait maternel. La prudence s'impose lorsque le métoclopramide est administré à une mère qui allaite.
Utilisation pédiatrique
La sécurité et l'efficacité chez les patients pédiatriques n'ont pas été établies (voir SURDOSAGE ).
Des précautions doivent être prises lors de l'administration de métoclopramide aux nouveau-nés car une clairance prolongée peut produire des concentrations sériques excessives (voir PHARMACOLOGIE CLINIQUE - Pharmacocinétique ). De plus, les nouveau-nés ont des taux réduits de NADH-cytochrome b5 réductase qui, en combinaison avec les facteurs pharmacocinétiques susmentionnés, rendent les nouveau-nés plus sensibles à la méthémoglobinémie (voir SURDOSAGE ).
Le profil de sécurité du métoclopramide chez l'adulte ne peut pas être extrapolé aux patients pédiatriques. Les dystonies et autres réactions extrapyramidales associées au métoclopramide sont plus fréquentes dans la population pédiatrique que chez les adultes. (Voir AVERTISSEMENTS et EFFETS INDÉSIRABLES - Réactions extrapyramidales. )
Utilisation gériatrique
Les études cliniques de reglan® n'ont pas inclus un nombre suffisant de sujets âgés de 65 ans et plus pour déterminer si les sujets âgés réagissent différemment des sujets plus jeunes.
Le risque de développer des effets secondaires de type parkinsonien augmente avec l'augmentation de la dose. Les patients gériatriques doivent recevoir la dose la plus faible de reglan® efficace. Si des symptômes de type parkinsonien se développent chez un patient gériatrique recevant reglan®, reglan® doit généralement être interrompu avant de commencer tout agent anti-parkinsonien spécifique (voir AVERTISSEMENTS et DOSAGE ET ADMINISTRATION – Pour le soulagement des reflux gastro-ophagiens symptomatiques ).
Les personnes âgées peuvent être plus à risque de dyskinésie tardive (voir AVERTISSEMENTS - Dyskinésie tardive ).
La sédation a été rapportée chez les utilisateurs de reglan®. La sédation peut être source de confusion et se manifester par une sursédation chez les personnes âgées (voir PHARMACOLOGIE CLINIQUE , PRÉCAUTIONS – Informations pour les patients et EFFETS INDÉSIRABLES – Effets sur le SNC ).
reglan® est connu pour être en grande partie excrété par les reins, et le risque de réactions toxiques à ce médicament peut être plus élevé chez les patients présentant une insuffisance rénale (voir DOSAGE ET ADMINISTRATION – Utilisation chez les patients atteints d'insuffisance rénale ou hépatique ).
Pour ces raisons, la sélection de la dose pour un patient âgé doit être prudente, en commençant généralement par le bas de la plage posologique, reflétant la fréquence plus élevée de diminution de la fonction rénale, de maladie concomitante ou d'autre traitement médicamenteux chez les personnes âgées (voir DOSAGE ET ADMINISTRATION – Pour le soulagement du reflux gastro-oesophagien symptomatique et l'utilisation chez les patients atteints d'insuffisance rénale ou hépatique ).
Autres populations particulières
Les patients présentant un déficit en NADH-cytochrome b5 réductase présentent un risque accru de développer une méthémoglobinémie et/ou une sulfhémoglobinémie lorsque le métoclopramide est administré. Chez les patients présentant un déficit en G6PD qui présentent une méthémoglobinémie induite par le métoclopramide, le traitement au bleu de méthylène n'est pas recommandé (voir SURDOSAGE ).
SURDOSAGE
Les symptômes de surdosage peuvent inclure somnolence, désorientation et réactions extrapyramidales. Les médicaments anticholinergiques ou antiparkinsoniens ou les antihistaminiques aux propriétés anticholinergiques peuvent être utiles pour contrôler les réactions extrapyramidales. Les symptômes sont spontanément résolutifs et disparaissent généralement dans les 24 heures.
L'hémodialyse élimine relativement peu de métoclopramide, probablement en raison de la faible quantité de médicament dans le sang par rapport aux tissus. De même, la dialyse péritonéale continue ambulatoire n'élimine pas de quantités significatives de médicament. Il est peu probable que la posologie doive être ajustée pour compenser les pertes par dialyse. La dialyse n'est probablement pas une méthode efficace d'élimination du médicament dans les situations de surdosage.
Un surdosage accidentel dû à une mauvaise administration a été rapporté chez des nourrissons et des enfants utilisant la solution buvable de métoclopramide. Bien qu'il n'y ait pas de tendance cohérente dans les rapports associés à ces surdoses, les événements comprenaient des convulsions, des réactions extrapyramidales et de la léthargie.
Une méthémoglobinémie est survenue chez des nouveau-nés prématurés et nés à terme ayant reçu des surdoses de métoclopramide (1 à 4 mg/kg/jour par voie orale, intramusculaire ou intraveineuse pendant 1 à 3 jours ou plus). La méthémoglobinémie peut être inversée par l'administration intraveineuse de bleu de méthylène. Cependant, le bleu de méthylène peut provoquer une anémie hémolytique chez les patients présentant un déficit en G6PD, qui peut être fatale (voir PRÉCAUTIONS – Autres populations particulières ).
CONTRE-INDICATIONS
Le métoclopramide ne doit pas être utilisé chaque fois que la stimulation de la motilité gastro-intestinale peut être dangereuse, par exemple en présence d'une hémorragie gastro-intestinale, d'une obstruction mécanique ou d'une perforation.
Le métoclopramide est contre-indiqué chez les patients atteints de phéochromocytome car le médicament peut provoquer une crise hypertensive, probablement due à la libération de catécholamines de la tumeur. De telles crises hypertensives peuvent être contrôlées par la phentolamine.
Le métoclopramide est contre-indiqué chez les patients présentant une sensibilité ou une intolérance connue au médicament. Le métoclopramide ne doit pas être utilisé chez les épileptiques ou les patients recevant d'autres médicaments susceptibles de provoquer des réactions extrapyramidales, car la fréquence et la gravité des crises ou des réactions extrapyramidales peuvent être augmentées.
PHARMACOLOGIE CLINIQUE
Le métoclopramide stimule la motilité du tractus gastro-intestinal supérieur sans stimuler les sécrétions gastriques, biliaires ou pancréatiques. Son mode d'action n'est pas clair. Il semble sensibiliser les tissus à l'action de l'acétylcholine. L'effet du métoclopramide sur la motilité ne dépend pas d'une innervation vagale intacte, mais il peut être aboli par des médicaments anticholinergiques.
Le métoclopramide augmente le tonus et l'amplitude des contractions gastriques (en particulier antrales), détend le sphincter pylorique et le bulbe duodénal et augmente le péristaltisme du duodénum et du jéjunum, ce qui accélère la vidange gastrique et le transit intestinal. Il augmente le tonus au repos du sphincter inférieur de l'œsophage. Il a peu ou pas d'effet sur la motilité du côlon ou de la vésicule biliaire.
Chez les patients souffrant de reflux gastro-oesophagien et d'une LESP basse (pression du sphincter oesophagien inférieur), des doses orales uniques de métoclopramide produisent des augmentations liées à la dose de la LESP. Les effets commencent à environ 5 mg et augmentent jusqu'à 20 mg (la plus grande dose testée). L'augmentation des LESP à partir d'une dose de 5 mg dure environ 45 minutes et celle de 20 mg dure entre 2 et 3 heures. Une augmentation du taux de vidange de l'estomac a été observée avec des doses orales uniques de 10 mg.
Les propriétés antiémétiques du métoclopramide semblent être le résultat de son antagonisme des récepteurs dopaminergiques centraux et périphériques. La dopamine produit des nausées et des vomissements par stimulation de la zone de déclenchement des chimiorécepteurs médullaires (CTZ), et le métoclopramide bloque la stimulation de la CTZ par des agents comme ldopa ou l'apomorphine qui sont connus pour augmenter les niveaux de dopamine ou pour posséder des effets de type dopamine. Le métoclopramide supprime également le ralentissement de la vidange gastrique provoqué par l'apomorphine.
Comme les phénothiazines et les médicaments apparentés, qui sont également des antagonistes de la dopamine, le métoclopramide produit une sédation et peut entraîner des réactions extrapyramidales, bien que celles-ci soient relativement rares (voir AVERTISSEMENTS ). Le métoclopramide inhibe les effets centraux et périphériques de l'apomorphine, induit la libération de prolactine et provoque une augmentation transitoire des taux circulants d'aldostérone, qui peut être associée à une rétention hydrique transitoire.
Le début de l'action pharmacologique du métoclopramide est de 1 à 3 minutes après une dose intraveineuse, de 10 à 15 minutes après une administration intramusculaire et de 30 à 60 minutes après une dose orale. les effets pharmacologiques persistent pendant 1 à 2 heures.
Pharmacocinétique
Le métoclopramide est rapidement et bien absorbé. Par rapport à une dose intraveineuse de 20 mg, la biodisponibilité orale absolue du métoclopramide est de 80 % ± 15,5 % comme démontré dans une étude croisée de 18 sujets. Les concentrations plasmatiques maximales surviennent environ 1 à 2 heures après une dose orale unique. Un temps similaire jusqu'au pic est observé après des doses individuelles à l'état d'équilibre.
Dans une étude à dose unique sur 12 sujets, l'aire sous la courbe concentration-temps du médicament augmente de façon linéaire avec des doses de 20 à 100 mg. Les concentrations maximales augmentent linéairement avec la dose ; le temps pour atteindre les concentrations maximales reste le même ; la clairance de tout le corps est inchangée ; et le taux d'élimination reste le même. La demi-vie d'élimination moyenne chez les personnes ayant une fonction rénale normale est de 5 à 6 heures. Les processus cinétiques linéaires décrivent adéquatement l'absorption et l'élimination du métoclopramide.
Environ 85 % de la radioactivité d'une dose administrée par voie orale apparaît dans l'urine dans les 72 heures. Sur les 85 % éliminés dans les urines, environ la moitié est présente sous forme de métoclopramide libre ou conjugué.
Le médicament n'est pas fortement lié aux protéines plasmatiques (environ 30%). Le volume de distribution corporel total est élevé (environ 3,5 L/kg), ce qui suggère une distribution importante du médicament dans les tissus.
L'insuffisance rénale affecte la clairance du métoclopramide. Dans une étude portant sur des patients présentant divers degrés d'insuffisance rénale, une réduction de la clairance de la créatinine a été corrélée à une réduction de la clairance plasmatique, de la clairance rénale, de la clairance non rénale et à une augmentation de la demi-vie d'élimination. La cinétique du métoclopramide en présence d'insuffisance rénale reste cependant linéaire. La réduction de la clairance résultant d'une insuffisance rénale suggère qu'un ajustement à la baisse de la posologie d'entretien doit être effectué pour éviter l'accumulation de médicament.
Données pharmacocinétiques adultes
Chez les patients pédiatriques, la pharmacodynamique du métoclopramide après administration orale et intraveineuse est très variable et une relation concentration-effet n'a pas été établie.
Il n'y a pas suffisamment de données fiables pour conclure si la pharmacocinétique du métoclopramide chez l'adulte et la population pédiatrique sont similaires. Bien qu'il n'y ait pas suffisamment de données pour étayer l'efficacité du métoclopramide chez les patients pédiatriques souffrant de reflux gastro-œsophagien (RGO) symptomatique ou de nausées et de vomissements liés à la chimiothérapie anticancéreuse, sa pharmacocinétique a été étudiée dans ces populations de patients.
Dans une étude en ouvert, six patients pédiatriques (tranche d'âge, 3,5 semaines à 5,4 mois) atteints de RGO ont reçu du métoclopramide 0,15 mg/kg solution buvable toutes les 6 heures pour 10 doses. La concentration plasmatique maximale moyenne de métoclopramide après la dixième dose était 2 fois plus élevée (56,8 μg/L) que celle observée après la première dose (29 μg/L), ce qui indique une accumulation de médicament lors d'administrations répétées. Après la dixième dose, le temps moyen pour atteindre les concentrations maximales (2,2 heures), la demi-vie (4,1 heures), la clairance (0,67 L/h/kg) et le volume de distribution (4,4 L/kg) du métoclopramide étaient similaires à celles observées après la première dose. Chez le patient le plus jeune (âge, 3,5 semaines), la demi-vie du métoclopramide après la première et la dixième dose (23,1 et 10,3 h, respectivement) était significativement plus longue par rapport aux autres nourrissons en raison d'une clairance réduite. Cela peut être attribué à des systèmes hépatique et rénal immatures à la naissance.
Des doses intraveineuses uniques de métoclopramide de 0,22 à 0,46 mg/kg (moyenne, 0,35 mg/kg) ont été administrées en 5 minutes à 9 patients pédiatriques atteints d'un cancer recevant une chimiothérapie (âge moyen, 11,7 ans ; intervalle, 7 à 14 ans) pour la prophylaxie des cytotoxiques. vomissements provoqués. Les concentrations plasmatiques de métoclopramide extrapolées au temps zéro variaient de 65 à 395 μg/L (moyenne, 152 μg/L). La demi-vie d'élimination moyenne, la clairance et le volume de distribution du métoclopramide étaient de 4,4 heures (intervalle de 1,7 à 8,3 heures), de 0,56 L/h/kg (intervalle de 0,12 à 1,20 L/h/kg) et de 3,0 L/ kg (plage, 1,0 à 4,8 L/kg), respectivement.
Dans une autre étude, neuf patients cancéreux pédiatriques (tranche d'âge, 1 à 9 ans) ont reçu 4 à 5 perfusions intraveineuses (sur 30 minutes) de métoclopramide à une dose de 2 mg/kg pour contrôler les vomissements. Après la dernière dose, les concentrations sériques maximales de métoclopramide variaient de 1060 à 5680 μg/L. La demi-vie d'élimination moyenne, la clairance et le volume de distribution du métoclopramide étaient de 4,5 heures (intervalle de 2,0 à 12,5 heures), de 0,37 L/h/kg (intervalle de 0,10 à 1,24 L/h/kg) et de 1,93 L/ kg (plage, 0,95 à 5,50 L/kg), respectivement.
INFORMATIONS PATIENTS
REGLAN (REG-lan) (comprimés de métoclopramide) Comprimés
Lisez l'Indicateur de Médication qui vient avec REGLAN avant que vous commenciez à le prendre et chaque fois que vous recevez une recharge. Il peut y avoir de nouvelles informations. Si vous prenez un autre produit contenant du métoclopramide (tel que REGLAN 10 mg injectable, REGLAN ODT ou une solution orale de métoclopramide), vous devez lire le Guide des médicaments fourni avec ce produit. Certaines informations peuvent être différentes. Ce Guide de Médication ne prend pas l'endroit de parler avec votre docteur de votre état médical ou de votre traitement.
Quelle est l'information la plus importante que je devrais connaître sur REGLAN ?
REGLAN peut provoquer des effets secondaires graves, notamment :
Dyskinésie tardive (mouvements musculaires anormaux). Ces mouvements se produisent principalement dans les muscles du visage. Vous ne pouvez pas contrôler ces mouvements. Ils peuvent ne pas disparaître même après l'arrêt de REGLAN. Il n'existe aucun traitement pour la dyskinésie tardive, mais les symptômes peuvent s'atténuer ou disparaître avec le temps après l'arrêt de la prise de REGLAN.
Vos chances de contracter une dyskinésie tardive augmentent :
- plus vous prenez REGLAN 10 mg et plus vous prenez REGLAN 10 mg. Vous ne devez pas prendre REGLAN 10 mg pendant plus de 12 semaines.
- si vous êtes plus âgé, surtout si vous êtes une femme
- si vous êtes diabétique
Il n'est pas possible pour votre médecin de savoir si vous développerez une dyskinésie tardive si vous prenez REGLAN.
Appelez immédiatement votre médecin si vous ressentez des mouvements que vous ne pouvez pas arrêter ou contrôler, tels que :
- claquer des lèvres, mâcher ou plisser la bouche
- froncer les sourcils ou froncer les sourcils
- tirer la langue
- cligner des yeux et bouger les yeux
- tremblement des bras et des jambes
Voir la rubrique "Quels sont les effets secondaires possibles de REGLAN 10mg ?" pour plus d'informations sur les effets secondaires.
Qu'est-ce que REGLAN 10mg ?
REGLAN 10mg est un médicament délivré sur ordonnance utilisé :
- chez l'adulte pendant 4 à 12 semaines pour soulager les symptômes de brûlures d'estomac avec reflux gastro-oesophagien (RGO) lorsque certains autres traitements ne fonctionnent pas. REGLAN soulage les brûlures d'estomac pendant la journée et les brûlures d'estomac après les repas. Il aide également les ulcères de l'œsophage à guérir.
- pour soulager les symptômes de la lenteur de la vidange de l'estomac chez les personnes atteintes de diabète. REGLAN aide à traiter les symptômes tels que les nausées, les vomissements, les brûlures d'estomac, la sensation de satiété longtemps après un repas et la perte d'appétit. Tous ces symptômes ne s'améliorent pas en même temps.
On ne sait pas si REGLAN est sûr et fonctionne chez les enfants.
Qui ne devrait pas prendre REGLAN 10mg ?
Ne prenez pas REGLAN si vous :
- avez des problèmes d'estomac ou d'intestin qui pourraient s'aggraver avec REGLAN, tels que des saignements, un blocage ou une déchirure de la paroi de l'estomac ou de l'intestin
- avez une tumeur de la glande surrénale appelée phéochromocytome
- êtes allergique à REGLAN 10mg ou à quoi que ce soit dedans. Voir la fin de ce Guide de Médication pour une liste d'ingrédients dans REGLAN.
- prendre des médicaments qui peuvent provoquer des mouvements incontrôlés, tels que des médicaments pour les maladies mentales avoir des convulsions
Que dois-je dire à mon médecin avant de prendre REGLAN ?
Informez votre médecin de toutes vos conditions médicales, y compris si vous avez :
- la dépression
- la maladie de Parkinson
- hypertension artérielle
- problèmes rénaux. Votre médecin peut commencer avec une dose plus faible.
- problèmes de foie ou insuffisance cardiaque. REGLAN peut amener votre corps à retenir les liquides.
- Diabète. Votre dose d'insuline devra peut-être être modifiée.
- cancer du sein
- vous êtes enceinte ou envisagez de devenir enceinte. On ne sait pas si REGLAN 10 mg nuira à votre bébé à naître.
- vous allaitez. REGLAN 10mg peut passer dans le lait maternel et peut nuire à votre bébé. Discutez avec votre médecin de la meilleure façon de nourrir votre bébé si vous prenez REGLAN.
Informez votre médecin de tous les médicaments que vous prenez, y compris les médicaments sur ordonnance et en vente libre, les vitamines et les suppléments à base de plantes. REGLAN et certains autres médicaments peuvent interagir les uns avec les autres et peuvent ne pas fonctionner aussi bien ou provoquer des effets secondaires possibles. Ne commencez pas de nouveaux médicaments pendant que vous prenez REGLAN 10 mg jusqu'à ce que vous en parliez avec votre médecin.
Prévenez surtout votre médecin si vous prenez :
- un autre médicament contenant du métoclopramide, tel que REGLAN 10 mg ODT ou une solution buvable de métoclopramide
- un médicament contre l'hypertension
- un médicament contre la dépression, en particulier un inhibiteur de la monoamine oxydase (IMAO)
- insuline
- un médicament qui peut vous rendre somnolent, comme les anxiolytiques, les somnifères et les narcotiques.
Si vous ne savez pas si votre médicament fait partie de la liste ci-dessus, demandez à votre médecin ou à votre pharmacien.
Connaissez les médicaments que vous prenez. Conservez-en une liste et montrez-la à votre médecin et à votre pharmacien lorsque vous recevez un nouveau médicament.
Comment dois-je prendre REGLAN ?
- REGLAN 10 mg se présente sous la forme d'un comprimé que vous prenez par voie orale.
- Prenez REGLAN exactement comme votre médecin vous l'a indiqué. Ne modifiez pas votre dose à moins que votre médecin ne vous le dise.
- Vous ne devriez pas prendre REGLAN pendant plus de 12 semaines.
- Si vous avez pris trop de REGLAN 10 mg, appelez immédiatement votre médecin ou votre centre antipoison.
Que devrais-je éviter en prenant REGLAN?
- Ne buvez pas d'alcool en prenant REGLAN. L'alcool peut aggraver certains effets secondaires de REGLAN 10 mg, comme la somnolence.
- Ne conduisez pas, ne travaillez pas avec des machines ou n'effectuez pas de tâches dangereuses jusqu'à ce que vous sachiez comment REGLAN vous affecte. REGLAN peut causer de la somnolence.
Quels sont les effets secondaires possibles de REGLAN ?
Reglan peut provoquer des effets secondaires graves, notamment :
- Dyskinésie tardive (mouvements musculaires anormaux). Voir "Quelles sont les informations les plus importantes que je dois connaître sur REGLAN ?"
- Spasmes incontrôlés des muscles du visage et du cou, ou des muscles du corps, des bras et des jambes (dystonie). Ces spasmes musculaires peuvent provoquer des mouvements et des positions corporelles anormaux. Ces spasmes commencent généralement dans les 2 premiers jours de traitement. Ces spasmes surviennent plus souvent chez les enfants et les adultes de moins de 30 ans.
- Dépression, pensées suicidaires et suicide. Certaines personnes qui prennent REGLAN deviennent déprimées. Vous pouvez penser à vous faire du mal ou à vous suicider. Certaines personnes qui prennent Reglan ont mis fin à leurs jours (suicide).
- Syndrome malin des neuroleptiques (SMN). Le SMN est une affection très rare mais très grave qui peut survenir avec Reglan. Le SMN peut entraîner la mort et doit être traité à l'hôpital. Les symptômes du SMN comprennent : une forte fièvre, des muscles raides, des problèmes de réflexion, un rythme cardiaque très rapide ou irrégulier et une transpiration accrue.
- Parkinsonisme. Les symptômes comprennent de légers tremblements, une raideur corporelle, des difficultés à bouger ou à garder l'équilibre. Si vous avez déjà la maladie de Parkinson, vos symptômes peuvent s'aggraver pendant que vous recevez REGLAN.
Appelez votre médecin et obtenez une aide médicale immédiatement si vous :
- se sentir déprimé ou penser à se faire du mal ou à se suicider
- avoir une forte fièvre, des muscles raides, des problèmes de réflexion, un rythme cardiaque très rapide ou irrégulier et une transpiration accrue
- avez des mouvements musculaires que vous ne pouvez pas arrêter ou contrôler
- avoir des mouvements musculaires nouveaux ou inhabituels
Les effets secondaires courants de Reglan 10mg incluent:
- se sentir agité, somnolent, fatigué, étourdi ou épuisé
- mal de tête
- confusion
- troubles du sommeil
Vous pouvez avoir plus d'effets secondaires plus longtemps vous prenez REGLAN et plus vous prenez REGLAN.
Vous pouvez toujours avoir des effets secondaires après avoir arrêté REGLAN. Vous pouvez avoir des symptômes d'arrêt (sevrage) de REGLAN 10mg tels que des maux de tête et une sensation de vertige ou de nervosité.
Informez votre médecin de tout effet secondaire qui vous dérange ou qui ne disparaît pas. Ce ne sont pas tous les effets secondaires possibles de REGLAN.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
Comment dois-je conserver REGLAN ?
- Gardez REGLAN à la température ambiante entre 68°F à 77°F (20°C à 25°C).
- Conservez REGLAN 10 mg dans le flacon dans lequel il se trouve. Gardez le flacon bien fermé.
Gardez REGLAN 10 mg et tous les médicaments hors de la portée des enfants.
Informations générales sur REGLAN
Les médicaments sont parfois prescrits à des fins autres que celles énumérées dans un guide des médicaments. Ne pas utiliser REGLAN pour une condition pour laquelle il n'a pas été prescrit. Ne donnez pas REGLAN 10 mg à d'autres personnes, même si elles présentent les mêmes symptômes que vous. Cela peut leur nuire.
Ce Guide de Médication résume les informations les plus importantes sur REGLAN. Si vous souhaitez plus d'informations, parlez-en à votre médecin. Vous pouvez demander à votre médecin ou à votre pharmacien des informations sur REGLAN 10 mg destinées aux professionnels de la santé. Pour plus d'informations, rendez-vous sur www.anipharmaceuticals.com ou appelez sans frais au 1-800-308-6755.
Quels sont les ingrédients de REGLAN ?
Ingrédient actif: métoclopramide
Ingrédients inactifs :
REGLAN 10 mg comprimés : stéarate de magnésium, mannitol, cellulose microcristalline, acide stéarique
REGLAN 5 mg comprimés : amidon de maïs, laque d'aluminium D&C jaune 10, laque d'aluminium FD&C bleu 1, lactose, cellulose microcristalline, dioxyde de silicium, acide stéarique
