Traitement du diabète: Glucophage 500mg, 850mg, 1000mg Metformin Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
Qu'est-ce que Glucophage et comment est-il utilisé ?
Glucophage est un médicament délivré sur ordonnance utilisé pour améliorer le contrôle de la glycémie chez les adultes atteints de diabète sucré de type 2. Glucophage peut être utilisé seul ou avec d'autres médicaments.
Glucophage 850 mg appartient à une classe de médicaments appelés antidiabétiques.
On ne sait pas si Glucophage est sûr et efficace chez les enfants de moins de 10 ans.
Quels sont les effets secondaires possibles de Glucophage ?
- douleurs musculaires inhabituelles,
- avoir froid,
- difficulté à respirer,
- se sentir étourdi ou étourdi,
- fatigue,
- la faiblesse,
- Douleur d'estomac,
- des vomissements et
- rythme cardiaque lent ou irrégulier
Consultez immédiatement un médecin si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires les plus courants de Glucophage comprennent :
- hypoglycémie,
- nausée,
- maux d'estomac, et
- diarrhée
Dites au médecin si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas.
Ce ne sont pas tous les effets secondaires possibles de Glucophage. Pour plus d'informations, consultez votre médecin ou votre pharmacien.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
ATTENTION
ACIDOSE LACTIQUE
Des cas post-commercialisation d'acidose lactique associée à la metformine ont entraîné la mort, l'hypothermie, l'hypotension et des bradyarythmies résistantes. Le début de l'acidose lactique associée à la metformine est souvent discret, accompagné uniquement de symptômes non spécifiques tels que malaise, myalgies, détresse respiratoire, somnolence et douleurs abdominales. L'acidose lactique associée à la metformine était caractérisée par des taux sanguins élevés de lactate (> 5 mmol/litre), une acidose à trou anionique (sans signe de cétonurie ou de cétonémie), une augmentation du rapport lactate/pyruvate ; et taux plasmatiques de metformine généralement > 5 mcg/mL [voir MISES EN GARDE ET PRÉCAUTIONS].
Les facteurs de risque d'acidose lactique associée à la metformine comprennent l'insuffisance rénale, l'utilisation concomitante de certains médicaments (par exemple, les inhibiteurs de l'anhydrase carbonique tels que le topiramate), l'âge de 65 ans ou plus, la réalisation d'un examen radiologique avec contraste, la chirurgie et d'autres procédures, les états hypoxiques (par exemple, , insuffisance cardiaque congestive aiguë), consommation excessive d'alcool et insuffisance hépatique.
Des mesures pour réduire le risque d'acidose lactique associée à la metformine et la gérer dans ces groupes à haut risque sont fournies [voir POSOLOGIE ET ADMINISTRATION, CONTRE-INDICATIONS, MISES EN GARDE ET PRÉCAUTIONS].
Si une acidose lactique associée à la metformine est suspectée, arrêtez immédiatement GLUCOPHAGE ou GLUCOPHAGE XR et mettez en place des mesures générales de soutien en milieu hospitalier. Une hémodialyse rapide est recommandée [voir MISES EN GARDE ET PRÉCAUTIONS].
LA DESCRIPTION
GLUCOPHAGE/GLUCOPHAGE 500 mg XR contiennent l'agent antihyperglycémiant metformine, qui est un biguanide, sous forme de monochlorhydrate. Le nom chimique du chlorhydrate de metformine est le chlorhydrate de diamide N,N-diméthylimidodicarbonimidique. La formule structurelle est comme indiqué ci-dessous:
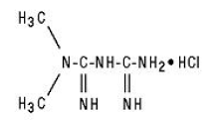
Le chlorhydrate de metformine est un composé cristallin blanc à blanc cassé avec une formule moléculaire de C4H11N5 • HCl et un poids moléculaire de 165,63. Il est facilement soluble dans l'eau et pratiquement insoluble dans l'acétone, l'éther et le chloroforme. Le pKa de la metformine est de 12,4. Le pH d'une solution aqueuse à 1 % de chlorhydrate de metformine est de 6,68.
Les comprimés GLUCOPHAGE contiennent 500 mg, 850 mg ou 1000 mg de chlorhydrate de metformine, ce qui équivaut à 389,93 mg, 662,88 mg, 779,86 mg de metformine base, respectivement. Chaque comprimé contient les ingrédients inactifs povidone et stéarate de magnésium. De plus, l'enrobage des comprimés de 500 mg et 850 mg contient de l'hypromellose et l'enrobage du comprimé de 1000 mg contient de l'hypromellose et du polyéthylène glycol.
GLUCOPHAGE 500 mg XR contient 500 mg ou 750 mg de chlorhydrate de metformine, ce qui équivaut respectivement à 389,93 mg et 584,90 mg de metformine base.
Les comprimés de GLUCOPHAGE XR à 500 mg contiennent les ingrédients inactifs hypromellose, cellulose microcristalline, carboxyméthylcellulose sodique et stéarate de magnésium.
Les comprimés de GLUCOPHAGE 850 mg XR 750 mg contiennent les ingrédients inactifs hypromellose, carboxyméthylcellulose sodique, stéarate de magnésium et pigment rouge d'oxyde de fer.
LES INDICATIONS
GLUCOPHAGE 850 mg est indiqué en complément d'un régime alimentaire et d'exercices physiques pour améliorer le contrôle glycémique chez les adultes et les patients pédiatriques de 10 ans et plus atteints de diabète sucré de type 2.
GLUCOPHAGE XR est indiqué comme complément au régime alimentaire et à l'exercice physique pour améliorer le contrôle glycémique chez les adultes atteints de diabète sucré de type 2.
DOSAGE ET ADMINISTRATION
Posologie adulte
Glucophage
- La dose initiale recommandée de GLUCOPHAGE 850 mg est de 500 mg par voie orale 2 fois/jour ou 850 mg 1 fois/jour, administrée avec les repas.
- Augmentez la dose par paliers de 500 mg par semaine ou de 850 mg toutes les 2 semaines en fonction du contrôle glycémique et de la tolérance, jusqu'à une dose maximale de 2550 mg par jour, administrée en doses fractionnées.
- Des doses supérieures à 2000 mg peuvent être mieux tolérées administrées 3 fois par jour avec les repas.
Glucophage XR
- Avalez les comprimés de GLUCOPHAGE XR entiers et ne les écrasez jamais, ne les coupez pas et ne les mâchez pas.
- La dose initiale recommandée de GLUCOPHAGE XR est de 500 mg par voie orale une fois par jour avec le repas du soir.
- Augmentez la dose par paliers de 500 mg par semaine en fonction du contrôle glycémique et de la tolérance, jusqu'à un maximum de 2 000 mg une fois par jour avec le repas du soir.
- Si le contrôle glycémique n'est pas atteint avec GLUCOPHAGE XR 2000 mg une fois par jour, envisager un essai de GLUCOPHAGE 850 mg XR 1000 mg deux fois par jour. Si des doses plus élevées sont nécessaires, passer à GLUCOPHAGE 500 mg à des doses quotidiennes totales allant jusqu'à 2550 mg administrées en doses quotidiennes fractionnées, comme décrit ci-dessus.
- Les patients recevant GLUCOPHAGE 1000 mg peuvent être remplacés par GLUCOPHAGE 850 mg XR une fois par jour à la même dose quotidienne totale, jusqu'à 2000 mg une fois par jour.
Dosage pédiatrique pour Glucophage
- La dose initiale recommandée de GLUCOPHAGE 850 mg pour les patients pédiatriques de 10 ans et plus est de 500 mg par voie orale deux fois par jour, administrée avec les repas.
- Augmenter la posologie par paliers de 500 mg par semaine en fonction du contrôle glycémique et de la tolérance, jusqu'à un maximum de 2 000 mg par jour, administrés en doses fractionnées deux fois par jour.
Recommandations d'utilisation en cas d'insuffisance rénale
- Évaluer la fonction rénale avant le début de GLUCOPHAGE/GLUCOPHAGE 500 mg XR et périodiquement par la suite.
- GLUCOPHAGE/GLUCOPHAGE 500 mg XR est contre-indiqué chez les patients dont le débit de filtration glomérulaire estimé (DFGe) est inférieur à 30 mL/minute/1,73 m2.
- L'initiation de GLUCOPHAGE/GLUCOPHAGE 850mg XR chez les patients avec un DFGe compris entre 30 et 45 mL/minute/1,73 m2 n'est pas recommandée.
- Chez les patients prenant GLUCOPHAGE/GLUCOPHAGE 1000 mg XR dont le DFGe tombe ultérieurement en dessous de 45 ml/min/1,73 m2, évaluer le bénéfice-risque de la poursuite du traitement.
- Arrêtez GLUCOPHAGE/GLUCOPHAGE 1000 mg XR si le DFGe du patient tombe ultérieurement en dessous de 30 mL/minute/1,73 m2 [voir AVERTISSEMENTS ET PRECAUTIONS ].
Interruption des procédures d'imagerie par contraste iodé
Interrompre GLUCOPHAGE/GLUCOPHAGE XR au moment ou avant une procédure d'imagerie par contraste iodé chez les patients avec un DFGe compris entre 30 et 60 mL/min/1,73 m2 ; chez les patients ayant des antécédents de maladie du foie, d'alcoolisme ou d'insuffisance cardiaque ; ou chez les patients qui recevront un produit de contraste iodé intra-artériel. Réévaluer l'eGFR 48 heures après la procédure d'imagerie ; recommencer GLUCOPHAGE/GLUCOPHAGE XR si la fonction rénale est stable.
COMMENT FOURNIE
Formes posologiques et points forts
GLUCOPHAGE 850 mg est disponible en :
- Comprimés : 500 mg ronds, blancs à blanc cassé, pelliculés, portant l'inscription « BMS 6060 » gravée sur la périphérie d'un côté et « 500 » gravée sur la face de l'autre côté.
- Comprimés : 850 mg ronds, blancs à blanc cassé, pelliculés portant l'inscription « BMS 6070 » gravée sur la périphérie d'un côté et « 850 » gravée sur la face de l'autre côté.
- Comprimés : 1 000 mg blancs, ovales, biconvexes, pelliculés portant l'inscription « BMS 6071 » gravée sur un côté et « 1000 » gravée sur le côté opposé et avec une ligne bissectrice des deux côtés.
GLUCOPHAGE XR est disponible en :
- Comprimés à libération prolongée : 500 mg blancs à blanc cassé, en forme de gélule, biconvexes, portant l'inscription « BMS 6063 » gravée sur une face et « 500 » gravée sur l'autre face.
- Comprimés à libération prolongée : 750 mg rouge pâle et pouvant avoir un aspect tacheté, en forme de gélule, biconvexe, portant l'inscription « BMS 6064 » gravée sur une face et « 750 » gravée sur l'autre face.
Stockage et manutention
Stockage
Conserver à 20°–25°C (68°–77°F); excursions autorisées jusqu'à 15°–30°C (59°–86°F). [Voir USP Température ambiante contrôlée.]
Répartir dans des récipients résistants à la lumière.
Distribué par : Bristol-Myers Squibb Company Princeton, NJ 08543 USA. Révisé : mai 2018.
EFFETS SECONDAIRES
Les effets indésirables suivants sont également discutés ailleurs dans l'étiquetage :
- Acidose lactique [voir AVERTISSEMENT DE BOÎTE et AVERTISSEMENTS ET PRECAUTIONS ]
- Carence en vitamine B12 [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Hypoglycémie [voir AVERTISSEMENTS ET PRECAUTIONS ]
Expérience des études cliniques
Étant donné que les essais cliniques sont menés dans des conditions très variables, les taux d'effets indésirables observés dans les essais cliniques d'un médicament ne peuvent pas être directement comparés aux taux des essais cliniques d'un autre médicament et peuvent ne pas refléter les taux observés dans la pratique.
Glucophage
Dans un essai clinique américain de GLUCOPHAGE 850 mg chez des patients atteints de diabète sucré de type 2, un total de 141 patients ont reçu GLUCOPHAGE 1 000 mg jusqu'à 2 550 mg par jour. Les effets indésirables rapportés chez plus de 5 % des patients traités par GLUCOPHAGE 500 mg et qui étaient plus fréquents que chez les patients traités par placebo sont listés dans le tableau 1.
La diarrhée a conduit à l'arrêt de GLUCOPHAGE 500mg chez 6% des patients. De plus, les effets indésirables suivants ont été signalés chez ≥ 1 % à ≤ 5 % des patients traités par GLUCOPHAGE et ont été plus fréquemment signalés avec GLUCOPHAGE qu'avec le placebo : selles anormales, hypoglycémie, myalgie, étourdissements, dyspnée, trouble des ongles, éruption cutanée, augmentation de la transpiration, goût troubles thoraciques, frissons, syndrome grippal, bouffées vasomotrices, palpitations.
Dans les essais cliniques sur GLUCOPHAGE 500 mg d'une durée de 29 semaines, une diminution à des niveaux inférieurs à la normale des taux sériques de vitamine B12 précédemment normaux a été observée chez environ 7 % des patients.
Patients pédiatriques
Dans les essais cliniques avec GLUCOPHAGE chez des patients pédiatriques atteints de diabète sucré de type 2, le profil des effets indésirables était similaire à celui observé chez les adultes.
Glucopage XR
Dans des essais contrôlés par placebo, 781 patients ont reçu GLUCOPHAGE 1000 mg XR. Les effets indésirables rapportés chez plus de 5 % des patients traités par GLUCOPHAGE XR à 850 mg, et qui étaient plus fréquents chez les patients traités par GLUCOPHAGE XR que sous placebo, sont répertoriés dans le tableau 2.
La diarrhée a entraîné l'arrêt de GLUCOPHAGE XR chez 0,6 % des patients. De plus, les effets indésirables suivants ont été signalés chez ≥ 1,0 % à ≤ 5,0 % des patients sous GLUCOPHAGE XR et ont été plus fréquemment signalés avec GLUCOPHAGE XR qu'avec le placebo : douleurs abdominales, constipation, distension abdominale, dyspepsie/brûlures d'estomac, flatulences, étourdissements, maux de tête, infection respiratoire, troubles du goût.
Expérience post-commercialisation
Les effets indésirables suivants ont été identifiés lors de l'utilisation post-approbation de la metformine. Étant donné que ces réactions sont signalées volontairement par une population de taille incertaine, il n'est pas toujours possible d'estimer de manière fiable leur fréquence ou d'établir une relation causale avec l'exposition au médicament.
Des lésions hépatiques cholestatiques, hépatocellulaires et hépatocellulaires mixtes ont été rapportées avec l'utilisation post-commercialisation de la metformine.
INTERACTIONS MÉDICAMENTEUSES
Le tableau 3 présente les interactions médicamenteuses cliniquement significatives avec GLUCOPHAGE/GLUCOPHAGE XR.
AVERTISSEMENTS
Inclus dans le cadre du "PRÉCAUTIONS" Section
PRÉCAUTIONS
Acidose lactique
Il y a eu des cas post-commercialisation d'acidose lactique associée à la metformine, y compris des cas mortels. Ces cas avaient un début subtil et étaient accompagnés de symptômes non spécifiques tels que des malaises, des myalgies, des douleurs abdominales, une détresse respiratoire ou une somnolence accrue ; cependant, une hypotension et des bradyarythmies résistantes sont survenues avec une acidose sévère. L'acidose lactique associée à la metformine était caractérisée par des concentrations sanguines élevées de lactate (> 5 mmol/L), une acidose à trou anionique (sans signe de cétonurie ou de cétonémie) et une augmentation du rapport lactate : pyruvate ; les concentrations plasmatiques de metformine étaient généralement > 5 mcg/mL. La metformine diminue l'absorption hépatique de lactate, ce qui augmente les taux sanguins de lactate, ce qui peut augmenter le risque d'acidose lactique, en particulier chez les patients à risque.
Si une acidose lactique associée à la metformine est suspectée, des mesures générales de soutien doivent être instituées rapidement en milieu hospitalier, ainsi que l'arrêt immédiat de GLUCOPHAGE/GLUCOPHAGE 500 mg XR. Chez les patients traités par GLUCOPHAGE/GLUCOPHAGE XR avec un diagnostic ou une forte suspicion d'acidose lactique, une hémodialyse rapide est recommandée pour corriger l'acidose et éliminer la metformine accumulée (le chlorhydrate de metformine est dialysable avec une clairance allant jusqu'à 170 mL/min dans de bonnes conditions hémodynamiques). L'hémodialyse a souvent entraîné l'inversion des symptômes et la guérison.
Éduquez les patients et leurs familles sur les symptômes de l'acidose lactique et, si ces symptômes surviennent, demandez-leur d'arrêter GLUCOPHAGE/GLUCOPHAGE 1000 mg XR et de signaler ces symptômes à leur fournisseur de soins de santé.
Pour chacun des facteurs de risque connus et possibles d'acidose lactique associée à la metformine, des recommandations visant à réduire le risque et à gérer l'acidose lactique associée à la metformine sont fournies ci-dessous :
- Insuffisance rénale - Les cas d'acidose lactique post-commercialisation associés à la metformine sont principalement survenus chez des patients présentant une insuffisance rénale importante.
Le risque d'accumulation de metformine et d'acidose lactique associée à la metformine augmente avec la sévérité de l'insuffisance rénale car la metformine est en grande partie excrétée par les reins. Les recommandations cliniques basées sur la fonction rénale du patient comprennent [voir DOSAGE ET ADMINISTRATION , PHARMACOLOGIE CLINIQUE ] :
- Avant d'initier GLUCOPHAGE/GLUCOPHAGE 850 mg XR, obtenir une estimation du débit de filtration glomérulaire (DFGe).
- GLUCOPHAGE/GLUCOPHAGE XR est contre-indiqué chez les patients dont le DFGe est inférieur à 30 mL/min/1,73 m2 [voir CONTRE-INDICATIONS ].
- L'initiation de GLUCOPHAGE/GLUCOPHAGE XR n'est pas recommandée chez les patients dont le DFGe est compris entre 30 et 45 mL/min/1,73 m2.
- Obtenir un eGFR au moins une fois par an chez tous les patients prenant GLUCOPHAGE/ GLUCOPHAGE 1000 mg XR. Chez les patients à risque de développer une insuffisance rénale (par exemple, les personnes âgées), la fonction rénale doit être évaluée plus fréquemment.
- Chez les patients prenant GLUCOPHAGE/GLUCOPHAGE 500 mg XR dont le DFGe est inférieur à 45 mL/min/1,73 m2, évaluer le bénéfice et le risque de poursuivre le traitement.
- Interactions médicamenteuses — L'utilisation concomitante de GLUCOPHAGE/GLUCOPHAGE XR avec des médicaments spécifiques peut augmenter le risque d'acidose lactique associée à la metformine : ceux qui altèrent la fonction rénale, entraînent des modifications hémodynamiques importantes, interfèrent avec l'équilibre acido-basique ou augmentent l'accumulation de metformine. Envisager une surveillance plus fréquente des patients.
- 65 ans ou plus — Le risque d'acidose lactique associée à la metformine augmente avec l'âge du patient, car les patients âgés sont plus susceptibles d'avoir une insuffisance hépatique, rénale ou cardiaque que les patients plus jeunes. Évaluer la fonction rénale plus fréquemment chez les patients âgés.
- Études radiologiques avec produit de contraste — L'administration intravasculaire de produits de contraste iodés chez les patients traités par la metformine a entraîné une diminution aiguë de la fonction rénale et la survenue d'une acidose lactique. Arrêter GLUCOPHAGE/GLUCOPHAGE XR au moment ou avant une procédure d'imagerie par contraste iodé chez les patients avec un DFGe compris entre 30 et 60 mL/min/1,73 m2 ; chez les patients ayant des antécédents d'insuffisance hépatique, d'alcoolisme ou d'insuffisance cardiaque ; ou chez les patients qui recevront un produit de contraste iodé intra-artériel. Réévaluer l'eGFR 48 heures après la procédure d'imagerie et redémarrer GLUCOPHAGE/GLUCOPHAGE XR si la fonction rénale est stable.
- Chirurgie et autres procédures - La rétention de nourriture et de liquides pendant les procédures chirurgicales ou autres peut augmenter le risque de déplétion volémique, d'hypotension et d'insuffisance rénale. GLUCOPHAGE/GLUCOPHAGE XR doit être temporairement interrompu pendant que les patients ont un apport alimentaire et hydrique restreint.
- États hypoxiques — Plusieurs des cas post-commercialisation d'acidose lactique associée à la metformine sont survenus dans le cadre d'une insuffisance cardiaque congestive aiguë (en particulier lorsqu'elle s'accompagnait d'hypoperfusion et d'hypoxémie). Le collapsus cardiovasculaire (choc), l'infarctus aigu du myocarde, la septicémie et d'autres conditions associées à l'hypoxémie ont été associés à l'acidose lactique et peuvent provoquer une azotémie prérénale. Lorsqu'un tel événement se produit, arrêtez GLUCOPHAGE/GLUCOPHAGE 1000mg XR.
- Consommation excessive d'alcool - L'alcool potentialise l'effet de la metformine sur le métabolisme du lactate. Les patients doivent être mis en garde contre une consommation excessive d'alcool pendant le traitement par GLUCOPHAGE/GLUCOPHAGE XR.
- Insuffisance hépatique - Les patients atteints d'insuffisance hépatique ont développé des cas d'acidose lactique associée à la metformine. Cela peut être dû à une altération de la clairance du lactate entraînant des taux sanguins de lactate plus élevés. Par conséquent, évitez d'utiliser GLUCOPHAGE/GLUCOPHAGE XR chez les patients présentant des signes cliniques ou de laboratoire de maladie hépatique.
Carence en vitamine B12
Dans les essais cliniques sur GLUCOPHAGE 1000 mg d'une durée de 29 semaines, une diminution à des niveaux inférieurs à la normale des taux sériques de vitamine B12 précédemment normaux a été observée chez environ 7 % des patients. Une telle diminution, peut-être due à une interférence avec l'absorption de B12 par le complexe B12-facteur intrinsèque, peut être associée à une anémie mais semble être rapidement réversible avec l'arrêt de GLUCOPHAGE ou de la supplémentation en vitamine B12. Certains individus (ceux dont l'apport ou l'absorption de vitamine B12 ou de calcium est insuffisant) semblent être prédisposés à développer des taux de vitamine B12 inférieurs à la normale. Mesurer les paramètres hématologiques sur une base annuelle et la vitamine B12 à des intervalles de 2 à 3 ans chez les patients sous GLUCOPHAGE/GLUCOPHAGE 500 mg XR et prendre en charge toute anomalie [voir EFFETS INDÉSIRABLES ].
Hypoglycémie avec utilisation concomitante d'insuline et d'insuline
Sécrétagogues
L'insuline et les sécrétagogues de l'insuline (p. ex., sulfonylurée) sont connus pour provoquer une hypoglycémie. GLUCOPHAGE/GLUCOPHAGE XR peut augmenter le risque d'hypoglycémie lorsqu'il est associé à l'insuline et/ou à un sécrétagogue de l'insuline. Par conséquent, une dose plus faible d'insuline ou de sécrétagogue d'insuline peut être nécessaire pour minimiser le risque d'hypoglycémie lorsqu'il est utilisé en association avec GLUCOPHAGE/GLUCOPHAGE XR [voir INTERACTIONS MÉDICAMENTEUSES ].
Résultats macrovasculaires
Il n'y a pas eu d'études cliniques établissant des preuves concluantes de réduction du risque macrovasculaire avec GLUCOPHAGE/GLUCOPHAGE 850 mg XR.
Informations sur les conseils aux patients
Conseillez au patient de lire l'étiquetage patient approuvé par la FDA ( INFORMATIONS PATIENTS ).
Acidose lactique
Expliquer les risques de l'acidose lactique, ses symptômes et les conditions qui prédisposent à son développement. Conseillez aux patients d'arrêter GLUCOPHAGE/GLUCOPHAGE XR immédiatement et d'informer rapidement leur fournisseur de soins de santé en cas d'hyperventilation inexpliquée, de myalgies, de malaise, de somnolence inhabituelle ou d'autres symptômes non spécifiques. Conseiller les patients contre la consommation excessive d'alcool et informer les patients de l'importance de tests réguliers de la fonction rénale pendant le traitement par GLUCOPHAGE/GLUCOPHAGE XR. Demandez aux patients d'informer leur médecin qu'ils prennent GLUCOPHAGE/GLUCOPHAGE 500 mg XR avant toute intervention chirurgicale ou radiologique, car un arrêt temporaire peut être nécessaire [voir AVERTISSEMENTS ET PRECAUTIONS ].
Hypoglycémie
Informer les patients qu'une hypoglycémie peut survenir lorsque GLUCOPHAGE/GLUCOPHAGE XR est co-administré avec des sulfonylurées orales et de l'insuline. Expliquer aux patients recevant un traitement concomitant les risques d'hypoglycémie, ses symptômes et son traitement, ainsi que les conditions qui prédisposent à son développement [voir AVERTISSEMENTS ET PRECAUTIONS ].
Carence en vitamine B12
Informer les patients de l'importance des paramètres hématologiques réguliers pendant le traitement par GLUCOPHAGE/GLUCOPHAGE XR [voir AVERTISSEMENTS ET PRECAUTIONS ].
Femmes en âge de procréer
Informez les femmes que le traitement par GLUCOPHAGE/GLUCOPHAGE XR peut entraîner une ovulation chez certaines femmes anovulatoires préménopausées, ce qui peut entraîner une grossesse non désirée [voir Utilisation dans des populations spécifiques ].
Informations sur l'administration de Glucophage XR
Informez les patients que GLUCOPHAGE 500 mg XR doit être avalé entier et non écrasé, coupé ou mâché, et que les ingrédients inactifs peuvent occasionnellement être éliminés dans les selles sous forme de masse molle pouvant ressembler au comprimé d'origine.
Toxicologie non clinique
Carcinogenèse, mutagenèse, altération de la fertilité
Des études de cancérogénicité à long terme ont été réalisées chez le rat (durée d'administration de 104 semaines) et la souris (durée d'administration de 91 semaines) à des doses allant jusqu'à 900 mg/kg/jour et 1 500 mg/kg/jour, respectivement. Ces doses sont à la fois environ 3 fois la dose quotidienne humaine maximale recommandée de 2550 mg sur la base de comparaisons de surface corporelle. Aucune preuve de cancérogénicité avec la metformine n'a été trouvée chez les souris mâles ou femelles. De même, aucun potentiel tumorigène n'a été observé avec la metformine chez les rats mâles. Il y avait, cependant, une incidence accrue de polypes utérins stromaux bénins chez les rats femelles traités avec 900 mg/kg/jour.
Il n'y avait aucune preuve d'un potentiel mutagène de la metformine dans les tests in vitro suivants : test d'Ames (S. typhimurium), test de mutation génique (cellules de lymphome de souris) ou test d'aberrations chromosomiques (lymphocytes humains). Les résultats du test in vivo du micronoyau chez la souris étaient également négatifs.
La fertilité des rats mâles ou femelles n'a pas été affectée par la metformine lorsqu'elle a été administrée à des doses aussi élevées que 600 mg/kg/jour, soit environ 2 fois la dose quotidienne maximale recommandée chez l'homme de 2550 mg sur la base de comparaisons de surface corporelle.
Utilisation dans des populations spécifiques
Grossesse
Résumé des risques
Les données limitées sur GLUCOPHAGE/GLUCOPHAGE XR chez les femmes enceintes ne sont pas suffisantes pour déterminer un risque associé au médicament de malformations congénitales majeures ou de fausse couche. Les études publiées sur l'utilisation de la metformine pendant la grossesse n'ont pas rapporté d'association claire avec la metformine et le risque d'anomalie congénitale majeure ou de fausse couche [voir Données ]. Il existe des risques pour la mère et le fœtus associés à un diabète sucré mal contrôlé pendant la grossesse [voir Considérations cliniques ].
Aucun effet indésirable sur le développement n'a été observé lorsque la metformine a été administrée à des rats et des lapins Sprague Dawley gravides pendant la période d'organogenèse à des doses allant jusqu'à 2 et 5 fois, respectivement, une dose clinique de 2550 mg, en fonction de la surface corporelle [voir Données ].
Le risque de fond estimé de malformations congénitales majeures est de 6 à 10 % chez les femmes atteintes de diabète sucré prégestationnel avec une HbA1C > 7 et a été signalé comme étant aussi élevé que 20 à 25 % chez les femmes avec une HbA1C > 10. Le risque de fond estimé de fausse couche pour la population indiquée est inconnu. Dans la population générale des États-Unis, le risque de fond estimé de malformations congénitales majeures et de fausse couche dans les grossesses cliniquement reconnues est de 2 à 4 % et de 15 à 20 %, respectivement.
Considérations cliniques
Risque maternel et/ou embryonnaire/fœtal associé à la maladie
Un diabète sucré mal contrôlé pendant la grossesse augmente le risque maternel d'acidocétose diabétique, de pré-éclampsie, d'avortements spontanés, d'accouchement prématuré, de mortinaissance et de complications à l'accouchement. Un diabète sucré mal contrôlé augmente le risque fœtal de malformations congénitales majeures, de mortinaissance et de morbidité liée à la macrosomie.
Données
Données humaines
Les données publiées provenant d'études post-commercialisation n'ont pas signalé d'association claire avec la metformine et des malformations congénitales majeures, des fausses couches ou des issues maternelles ou fœtales indésirables lorsque la metformine a été utilisée pendant la grossesse. Cependant, ces études ne peuvent pas établir avec certitude l'absence de tout risque associé à la metformine en raison de limites méthodologiques, notamment la petite taille de l'échantillon et des groupes de comparaison incohérents.
Données animales
Le chlorhydrate de metformine n'a pas eu d'effet néfaste sur les résultats du développement lorsqu'il a été administré à des rats et des lapins gravides à des doses allant jusqu'à 600 mg/kg/jour. Cela représente une exposition d'environ 2 et 5 fois une dose clinique de 2550 mg basée sur des comparaisons de surface corporelle pour les rats et les lapins, respectivement. La détermination des concentrations fœtales a démontré une barrière placentaire partielle à la metformine.
Lactation
Résumé des risques
Un nombre limité d'études publiées rapportent que la metformine est présente dans le lait maternel [voir Données ]. Cependant, il n'y a pas suffisamment d'informations pour déterminer les effets de la metformine sur le nourrisson allaité et aucune information disponible sur les effets de la metformine sur la production de lait. Par conséquent, les avantages de l'allaitement pour le développement et la santé doivent être pris en compte, ainsi que le besoin clinique de la mère de GLUCOPHAGE/GLUCOPHAGE 500 mg XR et tout effet indésirable potentiel sur l'enfant allaité de GLUCOPHAGE/GLUCOPHAGE 850 mg XR ou de l'affection maternelle sous-jacente.
Données
Des études cliniques publiées sur l'allaitement rapportent que la metformine est présente dans le lait maternel, ce qui a entraîné des doses chez le nourrisson d'environ 0,11 % à 1 % de la dose maternelle ajustée en fonction du poids et un rapport lait/plasma compris entre 0,13 et 1. Cependant, les études n'ont pas été conçues pour établir définitivement le risque d'utilisation de la metformine pendant l'allaitement en raison de la petite taille de l'échantillon et des données limitées sur les événements indésirables recueillies chez les nourrissons.
Femelles et mâles de potentiel reproducteur
Discuter du risque de grossesse non désirée chez les femmes préménopausées, car le traitement par GLUCOPHAGE/GLUCOPHAGE XR peut entraîner l'ovulation chez certaines femmes anovulatoires.
Utilisation pédiatrique
Glucophage
L'innocuité et l'efficacité de GLUCOPHAGE pour le traitement du diabète sucré de type 2 ont été établies chez les patients pédiatriques âgés de 10 à 16 ans. L'innocuité et l'efficacité de GLUCOPHAGE n'ont pas été établies chez les patients pédiatriques de moins de 10 ans.
L'utilisation de GLUCOPHAGE 850 mg chez les patients pédiatriques de 10 à 16 ans pour le traitement du diabète sucré de type 2 est étayée par des preuves issues d'études adéquates et bien contrôlées de GLUCOPHAGE chez les adultes avec des données supplémentaires provenant d'une étude clinique contrôlée chez des patients pédiatriques de 10 à 16 ans âgés atteints de diabète sucré de type 2, qui a démontré une réponse similaire dans le contrôle glycémique à celle observée chez les adultes [voir Etudes cliniques ]. Dans cette étude, les effets indésirables étaient similaires à ceux décrits chez les adultes. Une dose quotidienne maximale de 2000 mg de GLUCOPHAGE 1000 mg est recommandée. [Voir DOSAGE ET ADMINISTRATION .]
Glucophage 1000mg XR
L'innocuité et l'efficacité de GLUCOPHAGE XR chez les patients pédiatriques n'ont pas été établies.
Utilisation gériatrique
Les études cliniques contrôlées de GLUCOPHAGE/GLUCOPHAGE XR n'ont pas inclus un nombre suffisant de patients âgés pour déterminer s'ils répondent différemment des patients plus jeunes. En général, la sélection de la dose pour un patient âgé doit être prudente, en commençant généralement à l'extrémité inférieure de la plage posologique, reflétant la plus grande fréquence de diminution de la fonction hépatique, rénale ou cardiaque, et de maladie concomitante ou d'un autre traitement médicamenteux et le risque plus élevé d'acidose lactique. Évaluer la fonction rénale plus fréquemment chez les patients âgés [voir AVERTISSEMENTS ET PRECAUTIONS ].
Insuffisance rénale
La metformine est en grande partie excrétée par les reins et le risque d'accumulation de metformine et d'acidose lactique augmente avec le degré d'insuffisance rénale. GLUCOPHAGE/GLUCOPHAGE 850 mg XR est contre-indiqué en cas d'insuffisance rénale sévère, chez les patients dont le débit de filtration glomérulaire estimé (DFGe) est inférieur à 30 mL/min/1,73 m2 [voir DOSAGE ET ADMINISTRATION , CONTRE-INDICATIONS , AVERTISSEMENTS ET PRECAUTIONS , et PHARMACOLOGIE CLINIQUE ].
Insuffisance hépatique
L'utilisation de la metformine chez les patients atteints d'insuffisance hépatique a été associée à certains cas d'acidose lactique. GLUCOPHAGE/GLUCOPHAGE 500mg XR n'est pas recommandé chez les patients insuffisants hépatiques. [voir AVERTISSEMENTS ET PRECAUTIONS ].
SURDOSAGE
Un surdosage de chlorhydrate de metformine s'est produit, y compris l'ingestion de quantités supérieures à 50 grammes. Une hypoglycémie a été rapportée dans environ 10 % des cas, mais aucune association causale avec la metformine n'a été établie. Une acidose lactique a été rapportée dans environ 32 % des cas de surdosage de metformine [voir AVERTISSEMENTS ET PRECAUTIONS ]. La metformine est dialysable avec une clairance allant jusqu'à 170 mL/min dans de bonnes conditions hémodynamiques. Par conséquent, l'hémodialyse peut être utile pour éliminer le médicament accumulé chez les patients chez qui un surdosage en metformine est suspecté.
CONTRE-INDICATIONS
GLUCOPHAGE 1000 mg et GLUCOPHAGE 850 mg XR sont contre-indiqués chez les patients présentant :
- Insuffisance rénale sévère (DFGe inférieur à 30 mL/min/1,73 m2) [voir AVERTISSEMENTS ET PRECAUTIONS ].
- Hypersensibilité à la metformine.
- Acidose métabolique aiguë ou chronique, y compris acidocétose diabétique, avec ou sans coma.
PHARMACOLOGIE CLINIQUE
Mécanisme d'action
La metformine est un agent antihyperglycémiant qui améliore la tolérance au glucose chez les patients atteints de diabète sucré de type 2, abaissant à la fois la glycémie basale et postprandiale. La metformine diminue la production hépatique de glucose, diminue l'absorption intestinale du glucose et améliore la sensibilité à l'insuline en augmentant l'absorption et l'utilisation périphériques du glucose. Avec le traitement par la metformine, la sécrétion d'insuline reste inchangée tandis que les niveaux d'insuline à jeun et la réponse plasmatique à l'insuline pendant toute la journée peuvent diminuer.
Pharmacocinétique
Absorption
La biodisponibilité absolue d'un comprimé de GLUCOPHAGE 500 mg administré à jeun est d'environ 50 à 60 %. Des études utilisant des doses orales uniques de GLUCOPHAGE 500 à 1500 mg et 850 à 2550 mg, indiquent qu'il existe un manque de proportionnalité de la dose avec l'augmentation des doses, ce qui est dû à une diminution de l'absorption plutôt qu'à une altération de l'élimination. Aux doses cliniques et aux schémas posologiques habituels de GLUCOPHAGE, les concentrations plasmatiques à l'état d'équilibre de la metformine sont atteintes en 24 à 48 heures et sont généralement
Après une dose orale unique de GLUCOPHAGE 500 mg XR, la Cmax est atteinte avec une valeur médiane de 7 heures et un intervalle de 4 à 8 heures. Les concentrations plasmatiques maximales sont environ 20 % inférieures à celles de la même dose de GLUCOPHAGE 1 000 mg, cependant, l'étendue de l'absorption (mesurée par l'ASC) est comparable à celle de GLUCOPHAGE.
À l'état d'équilibre, l'ASC et la Cmax sont moins que proportionnelles à la dose pour GLUCOPHAGE XR dans la plage de 500 à 2 000 mg administrés une fois par jour. Les concentrations plasmatiques maximales sont d'environ 0,6, 1,1, 1,4 et 1,8 mcg/mL pour des doses de 500, 1000, 1500 et 2000 mg une fois par jour, respectivement. Le degré d'absorption de la metformine (mesuré par l'ASC) de GLUCOPHAGE 500 mg XR à une dose de 2 000 mg une fois par jour est similaire à la même dose quotidienne totale administrée sous forme de comprimés de GLUCOPHAGE 850 mg à 1 000 mg deux fois par jour. Après administration répétée de GLUCOPHAGE XR, la metformine ne s'est pas accumulée dans le plasma.
Effet de la nourriture :
La nourriture diminue le degré d'absorption et retarde légèrement l'absorption de la metformine, comme le montrent une concentration plasmatique maximale moyenne (Cmax) inférieure d'environ 40 %, une aire sous la courbe concentration plasmatique en fonction du temps (ASC) inférieure de 25 % et une diminution de 35 - allongement d'une minute du temps nécessaire pour atteindre le pic de concentration plasmatique (Tmax) après l'administration d'un seul comprimé de 850 mg de GLUCOPHAGE avec de la nourriture, par rapport au même dosage administré à jeun.
Bien que le degré d'absorption de la metformine (mesuré par l'ASC) du comprimé GLUCOPHAGE XR ait augmenté d'environ 50 % lorsqu'il était administré avec de la nourriture, la nourriture n'a eu aucun effet sur la Cmax et le Tmax de la metformine. Les repas riches et faibles en matières grasses ont eu le même effet sur la pharmacocinétique de GLUCOPHAGE XR.
Distribution
Le volume apparent de distribution (V/F) de la metformine après des doses orales uniques de GLUCOPHAGE 850 mg était en moyenne de 654 ± 358 L. La metformine est liée de manière négligeable aux protéines plasmatiques. La metformine se répartit dans les érythrocytes, probablement en fonction du temps.
Métabolisme
Des études à dose unique intraveineuse chez des sujets normaux démontrent que la metformine est excrétée sous forme inchangée dans les urines et ne subit pas de métabolisme hépatique (aucun métabolite n'a été identifié chez l'homme) ni d'excrétion biliaire.
Élimination
La clairance rénale (voir tableau 4) est environ 3,5 fois supérieure à la clairance de la créatinine, ce qui indique que la sécrétion tubulaire est la principale voie d'élimination de la metformine. Après administration orale, environ 90 % du médicament absorbé est éliminé par voie rénale dans les 24 premières heures, avec une demi-vie d'élimination plasmatique d'environ 6,2 heures. Dans le sang, la demi-vie d'élimination est d'environ 17,6 heures, suggérant que la masse érythrocytaire pourrait être un compartiment de distribution.
Populations spécifiques
Insuffisance rénale
Chez les patients dont la fonction rénale est diminuée, la demi-vie plasmatique et sanguine de la metformine est prolongée et la clairance rénale est diminuée (voir tableau 3) [voir DOSAGE ET ADMINISTRATION , CONTRE-INDICATIONS , AVERTISSEMENTS ET PRECAUTIONS et Utilisation dans des populations spécifiques ].
Insuffisance hépatique
Aucune étude pharmacocinétique de la metformine n'a été menée chez des patients atteints d'insuffisance hépatique [voir AVERTISSEMENTS ET PRECAUTIONS et Utilisation dans des populations spécifiques ].
Gériatrie
Des données limitées provenant d'études pharmacocinétiques contrôlées de GLUCOPHAGE 1000 mg chez des sujets âgés en bonne santé suggèrent que la clairance plasmatique totale de la metformine est diminuée, que la demi-vie est prolongée et que la Cmax est augmentée, par rapport aux sujets jeunes en bonne santé. Il semble que la modification de la pharmacocinétique de la metformine avec l'âge s'explique principalement par une modification de la fonction rénale (voir Tableau 4). [Voir AVERTISSEMENTS ET PRECAUTIONS et Utilisation dans des populations spécifiques ].
Pédiatrie
Après administration d'un seul comprimé oral de GLUCOPHAGE 500 mg avec de la nourriture, la moyenne géométrique de la Cmax et de l'ASC de la metformine différait de moins de 5 % entre les patients pédiatriques diabétiques de type 2 (12-16 ans) et les adultes en bonne santé de sexe et de poids appariés (20- 45 ans), tous avec une fonction rénale normale.
Le genre
Les paramètres pharmacocinétiques de la metformine ne différaient pas significativement entre les sujets normaux et les patients atteints de diabète sucré de type 2 lorsqu'ils étaient analysés selon le sexe (hommes = 19, femmes = 16).
Course
Aucune étude des paramètres pharmacocinétiques de la metformine en fonction de la race n'a été réalisée.
Interactions médicamenteuses
Évaluation in vivo des interactions médicamenteuses
Etudes cliniques
Glucophage
Études cliniques adultes
Un essai clinique américain multicentrique, en double aveugle, contrôlé par placebo, impliquant des patients obèses atteints de diabète sucré de type 2 dont l'hyperglycémie n'était pas suffisamment contrôlée par une prise en charge diététique seule (glycémie à jeun [FPG] de base d'environ 240 mg/dL) a été menée. Les patients ont été traités par GLUCOPHAGE (jusqu'à 2550 mg/jour) ou un placebo pendant 29 semaines. Les résultats sont présentés dans le tableau 7.
Le poids corporel initial moyen était de 201 livres et de 206 livres dans les bras GLUCOPHAGE 850 mg et placebo, respectivement. La variation moyenne du poids corporel entre le départ et la semaine 29 était de -1,4 lb et de -2,4 lb dans les bras GLUCOPHAGE 1000 mg et placebo, respectivement. Une étude de 29 semaines, en double aveugle, contrôlée par placebo, portant sur GLUCOPHAGE et le glyburide, seuls et en association , a été menée chez des patients obèses atteints de diabète sucré de type 2 qui n'avaient pas réussi à obtenir un contrôle glycémique adéquat alors qu'ils recevaient des doses maximales de glyburide (glycémie à jeun de base d'environ 250 mg/dL). Les patients randomisés dans le bras combiné ont commencé le traitement par GLUCOPHAGE 500 mg et glyburide 20 mg. A la fin de chaque semaine des 4 premières semaines de l'essai, ces patients ont vu leurs doses de GLUCOPHAGE 500 mg augmentées de 500 mg s'ils n'avaient pas atteint l'objectif de glycémie à jeun. Après la semaine 4, de tels ajustements posologiques ont été effectués mensuellement, bien qu'aucun patient n'ait été autorisé à dépasser 2500 mg de GLUCOPHAGE. Les patients du bras GLUCOPHAGE seul (metformine plus placebo) ont arrêté le glyburide et ont suivi le même schéma de titration. Les patients du bras glyburide ont continué la même dose de glyburide. A la fin de l'essai, environ 70% des patients du groupe association prenaient GLUCOPHAGE 2000 mg/glyburide 20 mg ou GLUCOPHAGE 2500 mg/glyburide 20 mg. Les résultats sont présentés dans le tableau 8.
Le poids corporel initial moyen était de 202 livres, 203 livres et 204 livres dans les groupes GLUCOPHAGE/glyburide, glyburide et GLUCOPHAGE 500 mg, respectivement. La variation moyenne du poids corporel entre le départ et la semaine 29 était de 0,9 lb, -0,7 lb et -8,4 lb dans les groupes GLUCOPHAGE/glyburide, glyburide et GLUCOPHAGE 850 mg, respectivement.
Études cliniques pédiatriques
Une étude en double aveugle contrôlée par placebo chez des patients pédiatriques âgés de 10 à 16 ans atteints de diabète de type 2 (GJ moyen 182,2 mg/dL), traitement par GLUCOPHAGE (jusqu'à 2000 mg/jour) pendant 16 semaines maximum (durée moyenne de traitement 11 semaines) a été réalisée. Les résultats sont présentés dans le tableau 9.
Le poids corporel initial moyen était de 205 livres et de 189 livres dans les bras GLUCOPHAGE 850 mg et placebo, respectivement. La variation moyenne du poids corporel entre le départ et la semaine 16 était de -3,3 lb et de -2,0 lb dans les bras GLUCOPHAGE 500 mg et placebo, respectivement.
Glucophage XR
Une étude de 24 semaines, en double aveugle, contrôlée par placebo portant sur GLUCOPHAGE 1000 mg XR, pris une fois par jour avec le repas du soir, a été menée chez des patients atteints de diabète sucré de type 2 qui n'avaient pas réussi à contrôler leur glycémie avec un régime alimentaire et de l'exercice. Les patients entrant dans l'étude avaient une HbA1c initiale moyenne de 8,0 % et une FPG initiale moyenne de 176 mg/dL. La dose de traitement a été augmentée à 1 500 mg une fois par jour si, à la semaine 12, l'HbA1c était ≥ 7,0 % mais
Une étude de 16 semaines, en double aveugle, contrôlée par placebo et dose-réponse de GLUCOPHAGE 500 mg XR, pris une fois par jour avec le repas du soir ou deux fois par jour avec les repas, a été menée chez des patients atteints de diabète sucré de type 2 qui n'avaient pas réussi à atteindre leur glycémie contrôler avec un régime et de l'exercice. Les résultats sont présentés dans le tableau 10.
Le poids corporel initial moyen était de 193 lb, 192 lb, 188 lb, 196 lb, 193 lb et 194 lb dans les bras GLUCOPHAGE XR 500 mg, 1000 mg, 1500 mg et 2000 mg une fois par jour, 1000 mg deux fois par jour et placebo, respectivement . La variation moyenne du poids corporel entre le départ et la semaine 16 était de -1,3 lb, -1,3 lb, -0,7 lb, -1,5 lb, -2,2 lb et -1,8 lb, respectivement.
Une étude randomisée en double aveugle de 24 semaines portant sur GLUCOPHAGE XR, pris une fois par jour avec le repas du soir, et GLUCOPHAGE 500 mg, pris deux fois par jour (avec le petit-déjeuner et le repas du soir), a été menée chez des patients atteints de diabète sucré de type 2 qui avaient été traité avec GLUCOPHAGE 500 mg deux fois par jour pendant au moins 8 semaines avant l'entrée à l'étude. Les résultats sont présentés dans le tableau 11.
Le poids corporel initial moyen était de 210 lb, 203 lb et 193 lb dans les bras GLUCOPHAGE 500 mg deux fois par jour et GLUCOPHAGE XR 1 000 mg et 1 500 mg une fois par jour, respectivement. La variation moyenne du poids corporel entre le départ et la semaine 24 était de 0,9 lb, 1,1 lb et 0,9 lb, respectivement.
INFORMATIONS PATIENTS
GLUCOPHAGE® [gloo-ko-fahzh] (chlorhydrate de metformine) Comprimés
et
GLUCOPHAGE® XR [gloo-ko-fahzh XR] (chlorhydrate de metformine) Comprimés à libération prolongée
Lisez les informations destinées aux patients fournies avec GLUCOPHAGE et GLUCOPHAGE 1000 mg XR avant de commencer à le prendre et chaque fois que vous recevez une recharge. Il peut y avoir de nouvelles informations. Cette notice ne remplace pas une discussion avec votre fournisseur de soins de santé au sujet de votre état de santé ou de votre traitement.
Quelles sont les informations les plus importantes que je devrais connaître sur GLUCOPHAGE 1000mg et GLUCOPHAGE 500mg XR ?
Des effets indésirables graves peuvent survenir chez les personnes prenant GLUCOPHAGE ou GLUCOPHAGE 1000 mg XR, notamment :
Acidose lactique. Le chlorhydrate de metformine, le médicament contenu dans GLUCOPHAGE 500 mg et GLUCOPHAGE XR, peut provoquer un effet indésirable rare mais grave appelé acidose lactique (une accumulation d'acide lactique dans le sang) qui peut entraîner la mort. L'acidose lactique est une urgence médicale et doit être traitée à l'hôpital.
Arrêtez de prendre GLUCOPHAGE ou GLUCOPHAGE 500 mg XR et appelez immédiatement votre fournisseur de soins de santé si vous présentez l'un des symptômes suivants d'acidose lactique :
- se sentir très faible et fatigué
- avez des douleurs musculaires inhabituelles (pas normales)
- avoir du mal à respirer
- avoir une somnolence inhabituelle ou dormir plus longtemps que d'habitude
- avez des problèmes gastriques ou intestinaux inexpliqués avec des nausées et des vomissements, ou de la diarrhée
- avoir froid, surtout dans les bras et les jambes
- se sentir étourdi ou étourdi
- avoir un rythme cardiaque lent ou irrégulier
Vous avez plus de chance de contracter une acidose lactique si vous :
- avoir des problèmes rénaux. Les personnes dont les reins ne fonctionnent pas correctement ne doivent pas prendre GLUCOPHAGE 850 mg OU GLUCOPHAGE XR.
- avoir des problèmes de foie.
- avez une insuffisance cardiaque congestive qui nécessite un traitement médicamenteux.
- boire beaucoup d'alcool (consommation excessive d'alcool très fréquente ou à court terme).
- se déshydrater (perdre une grande quantité de fluides corporels). Cela peut arriver si vous êtes malade avec de la fièvre, des vomissements ou de la diarrhée. La déshydratation peut également survenir lorsque vous transpirez beaucoup avec une activité ou un exercice et que vous ne buvez pas suffisamment de liquides.
- avoir certains tests radiographiques avec des colorants injectables ou des agents de contraste.
- Subir une opération chirurgicale.
- avez une crise cardiaque, une infection grave ou un accident vasculaire cérébral.
- êtes âgé de 80 ans ou plus et n'avez pas fait tester votre fonction rénale.
Que sont GLUCOPHAGE et GLUCOPHAGE 1000mg XR ?
- GLUCOPHAGE et GLUCOPHAGE XR sont des médicaments délivrés sur ordonnance qui contiennent du chlorhydrate de metformine. GLUCOPHAGE 500 mg et GLUCOPHAGE 1000 mg XR sont utilisés avec un régime alimentaire et de l'exercice pour aider à contrôler l'hyperglycémie (hyperglycémie) chez les adultes atteints de diabète de type 2.
- GLUCOPHAGE 850 mg et GLUCOPHAGE 500 mg XR ne sont pas destinés aux personnes atteintes de diabète de type 1.
- GLUCOPHAGE 850 mg et GLUCOPHAGE 500 mg XR ne sont pas destinés aux personnes atteintes d'acidocétose diabétique (augmentation des corps cétoniques dans le sang ou l'urine).
GLUCOPHAGE 850mg et GLUCOPHAGE 1000mg XR ont le même principe actif. Cependant, GLUCOPHAGE XR agit plus longtemps dans votre corps. Ces deux médicaments aident à contrôler votre glycémie de plusieurs façons. Il s'agit notamment d'aider votre corps à mieux répondre à l'insuline qu'il produit naturellement, de diminuer la quantité de sucre produite par votre foie et de diminuer la quantité de sucre absorbée par vos intestins. GLUCOPHAGE 1000 mg et GLUCOPHAGE 850 mg XR n'entraînent pas la production d'insuline par votre corps.
Qui ne devrait pas prendre GLUCOPHAGE ou GLUCOPHAGE 850mg XR ?
Certaines conditions augmentent votre risque d'avoir une acidose lactique ou causent d'autres problèmes si vous prenez l'un de ces médicaments. La plupart des conditions énumérées ci-dessous peuvent augmenter vos chances de contracter une acidose lactique.
Ne prenez jamais GLUCOPHAGE 1000 mg ou GLUCOPHAGE 500 mg XR si vous :
- avoir des problèmes rénaux
- êtes allergique au chlorhydrate de metformine contenu dans GLUCOPHAGE ou GLUCOPHAGE 850 mg XR ou à l'un des ingrédients contenus dans GLUCOPHAGE ou GLUCOPHAGE XR. Voir la fin de cette notice pour la liste complète des ingrédients de GLUCOPHAGE et GLUCOPHAGE XR.
- allez recevoir une injection de colorant ou d'agents de contraste pour une radiographie ou si vous allez subir une intervention chirurgicale et que vous ne pouvez pas manger ou boire beaucoup. Dans ces situations, GLUCOPHAGE 1000 mg ou GLUCOPHAGE XR devront être arrêtés pendant une courte période. Discutez avec votre professionnel de la santé du moment où vous devez arrêter GLUCOPHAGE 850 mg ou GLUCOPHAGE 850 mg XR et du moment où vous devez recommencer GLUCOPHAGE ou GLUCOPHAGE XR. Voir « Quelle est l'information la plus importante que je devrais connaître sur GLUCOPHAGE ou GLUCOPHAGE XR ? »
Que dois-je dire à mon fournisseur de soins de santé avant de prendre GLUCOPHAGE ou GLUCOPHAGE 1000 mg XR ?
Avant de prendre GLUCOPHAGE 500 mg ou GLUCOPHAGE XR, informez votre professionnel de la santé si vous :
- avoir un diabète de type 1. GLUCOPHAGE 850 mg ou GLUCOPHAGE 500 mg XR ne doivent pas être utilisés pour traiter les personnes atteintes de diabète de type 1.
- avez des antécédents ou un risque d'acidocétose diabétique (taux élevés de certains acides, appelés cétones, dans le sang ou l'urine). GLUCOPHAGE 1000 mg ou GLUCOPHAGE XR ne doivent pas être utilisés pour le traitement de l'acidocétose diabétique.
- avoir des problèmes rénaux.
- avoir des problèmes de foie.
- avez des problèmes cardiaques, y compris une insuffisance cardiaque congestive.
- sont âgés de plus de 80 ans. Si vous avez plus de 80 ans, vous ne devez pas prendre GLUCOPHAGE 1000 mg ou GLUCOPHAGE XR à moins que vos reins aient été contrôlés et qu'ils soient normaux.
- buvez de l'alcool très souvent ou buvez beaucoup d'alcool dans le cadre d'une consommation excessive d'alcool à court terme.
- prennent de l'insuline.
- avoir d'autres conditions médicales.
- êtes enceinte ou envisagez de devenir enceinte. On ne sait pas si GLUCOPHAGE ou GLUCOPHAGE 850mg XR nuira à votre bébé à naître. Si vous êtes enceinte, discutez avec votre fournisseur de soins de santé de la meilleure façon de contrôler votre glycémie pendant votre grossesse.
- allaitez ou envisagez d'allaiter. On ne sait pas si GLUCOPHAGE 850 mg ou GLUCOPHAGE XR passe dans votre lait maternel. Discutez avec votre professionnel de la santé de la meilleure façon de nourrir votre bébé pendant que vous prenez GLUCOPHAGE 500 mg ou GLUCOPHAGE 500 mg XR.
Informez votre professionnel de la santé de tous les médicaments que vous prenez, y compris les médicaments sur ordonnance et en vente libre, les vitamines et les suppléments à base de plantes. Connaissez les médicaments que vous prenez. Conservez-en une liste pour la montrer à votre fournisseur de soins de santé et à votre pharmacien lorsque vous recevez un nouveau médicament.
- GLUCOPHAGE ou GLUCOPHAGE XR peuvent affecter le mode d'action d'autres médicaments, et d'autres médicaments peuvent affecter le mode d'action de GLUCOPHAGE ou GLUCOPHAGE XR.
Peut-on utiliser GLUCOPHAGE ou GLUCOPHAGE 500mg XR chez l'enfant ?
Il a été démontré que GLUCOPHAGE 1000 mg abaisse efficacement la glycémie chez les enfants (âgés de 10 à 16 ans) atteints de diabète de type 2. GLUCOPHAGE 1000 mg n'a pas été étudié chez les enfants de moins de 10 ans. GLUCOPHAGE 500 mg n'a pas été étudié en association avec d'autres médicaments oraux de contrôle de la glycémie ou de l'insuline chez l'enfant. Si vous avez des questions sur l'utilisation de GLUCOPHAGE 1000 mg chez les enfants, parlez-en à votre médecin ou à un autre professionnel de la santé.
GLUCOPHAGE XR n'a pas été étudié chez les enfants.
Comment dois-je prendre GLUCOPHAGE ou GLUCOPHAGE XR ?
- Prenez GLUCOPHAGE 850 mg ou GLUCOPHAGE 850 mg XR exactement comme votre professionnel de la santé vous l'a indiqué.
- GLUCOPHAGE ou GLUCOPHAGE 850 mg XR doivent être pris avec les repas pour aider à atténuer les effets secondaires des maux d'estomac.
- Avalez GLUCOPHAGE ou GLUCOPHAGE 500mg XR entier. Ne pas écraser, couper ou mâcher GLUCOPHAGE 1000mg XR.
- Vous pouvez parfois passer une masse molle dans vos selles (selles) qui ressemble à GLUCOPHAGE 850mg ou GLUCOPHAGE XR comprimés. Ceci n'est pas nocif et n'affectera pas la façon dont GLUCOPHAGE 850 mg XR agit pour contrôler votre diabète.
- Lorsque votre corps est soumis à certains types de stress, comme la fièvre, un traumatisme (comme un accident de voiture), une infection ou une intervention chirurgicale, la quantité de médicaments contre le diabète dont vous avez besoin peut changer. Informez immédiatement votre fournisseur de soins de santé si vous avez l'un de ces problèmes.
- Votre fournisseur de soins de santé doit effectuer des tests sanguins pour vérifier le bon fonctionnement de vos reins avant et pendant votre traitement par GLUCOPHAGE 1000 mg ou GLUCOPHAGE 500 mg XR.
- Votre fournisseur de soins de santé vérifiera votre diabète par des tests sanguins réguliers, y compris votre taux de sucre dans le sang et votre taux d'hémoglobine A1C.
- Suivez les instructions de votre fournisseur de soins de santé pour traiter une glycémie trop basse (hypoglycémie). Parlez à votre fournisseur de soins de santé si l'hypoglycémie est un problème pour vous. Voir "Quels sont les effets secondaires possibles de GLUCOPHAGE ou GLUCOPHAGE XR?"
- Vérifiez votre glycémie selon les instructions de votre fournisseur de soins de santé.
- Suivez votre régime alimentaire prescrit et votre programme d'exercice tout en prenant GLUCOPHAGE 850 mg ou GLUCOPHAGE 850 mg XR.
- Si vous manquez une dose de GLUCOPHAGE 1000 mg ou GLUCOPHAGE 850 mg XR, prenez la dose suivante telle que prescrite, sauf indication contraire de votre professionnel de la santé. Ne prenez pas de dose supplémentaire le lendemain.
- Si vous avez pris trop de GLUCOPHAGE 500 mg ou GLUCOPHAGE 500 mg XR, appelez votre fournisseur de soins de santé, le centre antipoison local ou rendez-vous immédiatement aux urgences de l'hôpital le plus proche.
Que dois-je éviter pendant que je prends GLUCOPHAGE ou GLUCOPHAGE 1000mg XR ?
Ne buvez pas beaucoup de boissons alcoolisées pendant que vous prenez GLUCOPHAGE ou GLUCOPHAGE XR. Cela signifie que vous ne devez pas consommer trop d'alcool pendant de courtes périodes et que vous ne devez pas boire beaucoup d'alcool de façon régulière. L'alcool peut augmenter le risque d'acidose lactique.
Quels sont les effets secondaires de GLUCOPHAGE et GLUCOPHAGE XR ?
- Acidose lactique. La metformine, l'ingrédient actif de GLUCOPHAGE 1000 mg et GLUCOPHAGE 500 mg XR, peut provoquer une affection rare mais grave appelée acidose lactique (une accumulation d'acide dans le sang) pouvant entraîner la mort. L'acidose lactique est une urgence médicale et doit être traitée à l'hôpital.
Appelez immédiatement votre médecin si vous présentez l'un des symptômes suivants, qui pourraient être des signes d'acidose lactique :
- vous avez froid aux mains ou aux pieds
- vous vous sentez étourdi ou étourdi
- vous avez un rythme cardiaque lent ou irrégulier
- vous vous sentez très faible ou fatigué
- vous avez du mal à respirer
- vous vous sentez somnolent ou somnolent
- vous avez des douleurs à l'estomac, des nausées ou des vomissements
La plupart des personnes qui ont eu une acidose lactique avec la metformine ont d'autres choses qui, combinées à la metformine, ont conduit à l'acidose lactique. Informez votre médecin si vous présentez l'un des cas suivants, car vous avez un risque plus élevé de contracter une acidose lactique avec GLUCOPHAGE 850 mg ou GLUCOPHAGE 500 mg XR si vous :
- avez de graves problèmes rénaux ou vos reins sont affectés par certains tests aux rayons X qui utilisent un colorant injectable
- avoir des problèmes de foie
- boire de l'alcool très souvent, ou boire beaucoup d'alcool lors d'une consommation excessive d'alcool à court terme
- se déshydrater (perdre une grande quantité de fluides corporels). Cela peut arriver si vous êtes malade avec de la fièvre, des vomissements ou de la diarrhée. La déshydratation peut également survenir lorsque vous transpirez beaucoup avec une activité ou un exercice et que vous ne buvez pas suffisamment de liquides.
- Subir une opération chirurgicale
- avez une crise cardiaque, une infection grave ou un accident vasculaire cérébral
Les effets secondaires courants de GLUCOPHAGE 500 mg et GLUCOPHAGE 1000 mg XR comprennent la diarrhée, les nausées et les maux d'estomac. Ces effets secondaires disparaissent généralement après avoir pris le médicament pendant un certain temps. Prendre votre médicament avec les repas peut aider à réduire ces effets secondaires. Informez votre médecin si les effets secondaires vous dérangent beaucoup, durent plus de quelques semaines, réapparaissent après leur disparition ou commencent plus tard le traitement. Il se peut que vous ayez besoin d'une dose plus faible ou que vous deviez arrêter de prendre le médicament pendant une courte période ou pour de bon.
Environ 3 personnes sur 100 qui prennent GLUCOPHAGE ou GLUCOPHAGE 1000 mg XR ont un goût métallique désagréable lorsqu'elles commencent à prendre le médicament. Cela dure peu de temps.
GLUCOPHAGE 850 mg et GLUCOPHAGE 500 mg XR provoquent rarement par eux-mêmes une hypoglycémie (faible taux de sucre dans le sang). Cependant, une hypoglycémie peut survenir si vous ne mangez pas suffisamment, si vous buvez de l'alcool ou si vous prenez d'autres médicaments pour abaisser votre taux de sucre dans le sang.
Comment conserver GLUCOPHAGE 500 mg et GLUCOPHAGE XR ?
Conservez GLUCOPHAGE et GLUCOPHAGE 850 mg XR entre 68 °F et 77 °F (20 °C et 25 °C).
Gardez GLUCOPHAGE 850 mg et GLUCOPHAGE 500 mg XR et tous les médicaments hors de la portée des enfants.
Informations générales sur l'utilisation de GLUCOPHAGE 850mg et GLUCOPHAGE 850mg XR
Si vous avez des questions ou des problèmes, parlez-en à votre médecin ou à un autre fournisseur de soins de santé. Vous pouvez demander à votre médecin ou à votre pharmacien des informations sur GLUCOPHAGE 850mg et GLUCOPHAGE 500mg XR destinées aux professionnels de santé. Les médicaments sont parfois prescrits à des fins autres que celles énumérées dans une notice d'information destinée aux patients. Ne pas utiliser GLUCOPHAGE 1000 mg ou GLUCOPHAGE 1000 mg XR pour une affection pour laquelle il n'a pas été prescrit. Ne partagez pas vos médicaments avec d'autres personnes.
Quels sont les ingrédients de GLUCOPHAGE et GLUCOPHAGE 500mg XR ?
Principes actifs de GLUCOPHAGE : chlorhydrate de metformine.
Ingrédients inactifs de chaque comprimé de GLUCOPHAGE : povidone et stéarate de magnésium. De plus, l'enrobage des comprimés de 500 mg et 850 mg contient de l'hypromellose et l'enrobage du comprimé de 1000 mg contient de l'hypromellose et du polyéthylène glycol.
Principes actifs de GLUCOPHAGE 1000mg XR : chlorhydrate de metformine.
Ingrédients inactifs de chaque comprimé de GLUCOPHAGE 1000 mg XR 500 mg : carboxyméthylcellulose sodique, hypromellose, cellulose microcristalline et stéarate de magnésium.
Ingrédients inactifs de chaque comprimé de GLUCOPHAGE XR 750 mg : carboxyméthylcellulose sodique, hypromellose et stéarate de magnésium.
Qu'est-ce que le diabète de type 2 ?
Le diabète de type 2 est une condition dans laquelle votre corps ne produit pas suffisamment d'insuline et l'insuline que votre corps produit ne fonctionne pas aussi bien qu'elle le devrait. Votre corps peut aussi fabriquer trop de sucre. Lorsque cela se produit, le sucre (glucose) s'accumule dans le sang. Cela peut entraîner de graves problèmes médicaux.
L'objectif principal du traitement du diabète est d'abaisser votre glycémie à un niveau normal.
L'hyperglycémie peut être réduite par un régime alimentaire et de l'exercice, et par certains médicaments si nécessaire.
Discutez avec votre fournisseur de soins de santé de la façon de prévenir, de reconnaître et de prendre en charge l'hypoglycémie, l'hyperglycémie (hyperglycémie) et les problèmes que vous avez à cause de votre diabète.
