Indocin 25mg, 50mg, 75mg Indomethacin Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
Qu'est-ce qu'Indocin 50 mg et comment est-il utilisé ?
Indocin est un médicament d'ordonnance utilisé pour traiter les symptômes d'inflammation et de douleur associés à l'arthrose, à la polyarthrite rhumatoïde, à l'arthrite goutteuse ou à la spondylarthrite ankylosante. Indocin 25 mg peut être utilisé seul ou avec d'autres médicaments.
Indocin 50 mg appartient à une classe de médicaments appelés anti-inflammatoires non stéroïdiens (AINS).
On ne sait pas si Indocin 25 mg est sûr et efficace chez les enfants de moins de 2 ans pour le traitement des troubles rhumatoïdes inflammatoires.
Quels sont les effets secondaires possibles d'Indocin 50mg ?
L'indocine peut provoquer des effets secondaires graves, notamment :
- démangeaison de la peau,
- changements de vision,
- gonflement,
- prise de poids rapide,
- essoufflement,
- perte d'appétit,
- douleur dans le haut du ventre,
- nausée,
- vomissement,
- diarrhée,
- fatigue inhabituelle,
- démangeaison,
- symptômes pseudo-grippaux,
- urine foncée,
- jaunissement de la peau ou des yeux (jaunisse),
- selles sanglantes ou goudronneuses,
- crachats de sang ou de vomi ressemblant à du marc de café,
- peu ou pas de miction,
- gonflement des pieds ou des chevilles,
- peau pâle
- ,
- étourdissements, et
- mains et pieds froids
Consultez immédiatement un médecin si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires les plus courants d'Indocin comprennent:
- indigestion,
- nausée,
- maux de tête, et
- vertiges
Dites au médecin si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas.
Ce ne sont pas tous les effets secondaires possibles d'Indocin. Pour plus d'informations, consultez votre médecin ou votre pharmacien.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
ATTENTION
RISQUE D'ÉVÉNEMENTS CARDIO-VASCULAIRES ET GASTRO-INTESTINAUX GRAVES
Événements thrombotiques cardiovasculaires
- Les anti-inflammatoires non stéroïdiens (AINS) entraînent un risque accru d'événements thrombotiques cardiovasculaires graves, notamment d'infarctus du myocarde et d'accident vasculaire cérébral, qui peuvent être mortels. Ce risque peut survenir au début du traitement et peut augmenter avec la durée d'utilisation [voir AVERTISSEMENTS ET PRECAUTIONS ].
- INDOCIN 75 mg est contre-indiqué dans le cadre d'un pontage aortocoronarien (PAC) [voir CONTRE-INDICATIONS et AVERTISSEMENTS ET PRECAUTIONS ].
Saignement gastro-intestinal, ulcération et perforation
- Les AINS entraînent un risque accru d'effets indésirables gastro-intestinaux (GI) graves, notamment des saignements, des ulcérations et des perforations de l'estomac ou des intestins, qui peuvent être fatals. Ces événements peuvent survenir à tout moment pendant l'utilisation et sans symptômes d'avertissement. Les patients âgés et les patients ayant des antécédents d'ulcère peptique et/ou d'hémorragie gastro-intestinale sont plus à risque d'événements gastro-intestinaux graves [voir AVERTISSEMENTS ET PRECAUTIONS ].
LA DESCRIPTION
INDOCIN (indométhacine) suspension orale est un anti-inflammatoire non stéroïdien, disponible sous forme de suspension orale contenant 25 mg d'indométhacine par 5 ml, de l'alcool à 1 % et de l'acide sorbique à 0,1 % ajouté comme conservateur pour l'administration orale. Le nom chimique est l'acide -(4-chlorobenzoyl)-5-méthoxy-2-méthyl-1Hindole-3-acétique. Le poids moléculaire est de 357,8. Sa formule moléculaire est C19H16ClNO4 et sa structure chimique est la suivante.
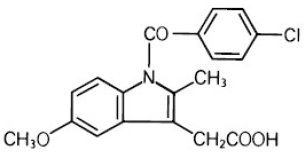
L'indométhacine est une poudre cristalline blanche à jaune. Il est pratiquement insoluble dans l'eau et peu soluble dans l'alcool. L'indométhacine a un pKa de 4,5 et est stable dans les milieux neutres ou légèrement acides et se décompose dans les alcalis forts. La suspension a un pH de 4,0 à 5,0.
Les ingrédients inactifs d'INDOCIN 75 mg comprennent : une émulsion AF antimousse, des arômes, de l'eau purifiée, de l'hydroxyde de sodium ou de l'acide chlorhydrique pour ajuster le pH, une solution de sorbitol et de la gomme adragante. La suspension orale INDOCIN, 25 mg par 5 ml, est une suspension blanc cassé au goût d'ananas et de noix de coco et de menthe.
LES INDICATIONS
INDOCIN 75mg Suppositoire est indiqué pour :
- Polyarthrite rhumatoïde modérée à sévère, y compris poussées aiguës de maladies chroniques
- Spondylarthrite ankylosante modérée à sévère
- Arthrose modérée à sévère
- Epaule douloureuse aiguë (bursite et/ou tendinite)
- Arthrite goutteuse aiguë
DOSAGE ET ADMINISTRATION
Instructions générales de dosage
Considérez attentivement les avantages et les risques potentiels d'INDOCIN et d'autres options de traitement avant de décider d'utiliser INDOCIN. Utilisez la dose efficace la plus faible pendant la durée la plus courte compatible avec les objectifs de traitement de chaque patient [voir AVERTISSEMENTS ET PRECAUTIONS ].
Après avoir observé la réponse au traitement initial par l'indométhacine, la dose et la fréquence doivent être ajustées en fonction des besoins individuels du patient.
Les effets indésirables semblent généralement corrélés à la dose d'indométhacine. Par conséquent, tous les efforts doivent être faits pour déterminer la dose efficace la plus faible pour chaque patient.
Suppositoires
Les suppositoires INDOCIN sont disponibles sous forme de suppositoires de 50 mg à usage rectal uniquement. Les suppositoires INDOCIN 25 mg ne sont pas destinés à une utilisation orale ou intravaginale.
Instructions de dosage des suppositoires
CETTE SECTION FAIT PRINCIPALEMENT RÉFÉRENCE À LA CAPSULE D'INDOMÉTHACINE, USP POSOLOGIE ORALE POUR DES CONSEILS D'UTILISATION DES SUPPOSITOIRES.
Les suppositoires INDOCIN 50 mg peuvent remplacer les gélules d'indométhacine, USP; cependant, il y aura des différences significatives entre les deux schémas posologiques dans les taux sanguins d'indométhacine [voir PHARMACOLOGIE CLINIQUE ].
Recommandations posologiques orales pour les stades actifs des éléments suivants :
Polyarthrite rhumatoïde modérée à sévère, y compris poussées aiguës de maladies chroniques ; Spondylarthrite ankylosante modérée à sévère ; Et arthrose modérée à sévère
Capsules d'indométhacine, USP 25 mg deux fois par jour. ou trois fois par jour. Si cela est bien toléré, augmenter la dose quotidienne de 25 mg ou de 50 mg, si la persistance des symptômes l'exige, à intervalles hebdomadaires jusqu'à l'obtention d'une réponse satisfaisante ou jusqu'à ce qu'une dose quotidienne totale de 150-200 mg soit atteinte. Des doses supérieures à cette quantité n'augmentent généralement pas l'efficacité du médicament.
Chez les patients qui ont des douleurs nocturnes persistantes et/ou des raideurs matinales, l'administration d'une grande partie, jusqu'à un maximum de 100 mg, de la dose quotidienne totale au coucher, soit par voie orale soit par des suppositoires rectaux, peut être utile pour procurer un soulagement. La dose quotidienne totale ne doit pas dépasser 200 mg. Dans les poussées aiguës de polyarthrite rhumatoïde chronique, il peut être nécessaire d'augmenter la posologie de 25 mg ou, si nécessaire, de 50 mg par jour.
Si des effets indésirables mineurs se développent lors de l'augmentation de la posologie, réduire rapidement la posologie jusqu'à une dose tolérée et surveiller étroitement le patient.
Si des effets indésirables graves surviennent, arrêtez le médicament. Une fois la phase aiguë de la maladie maîtrisée, une tentative de réduction de la dose quotidienne doit être répétée jusqu'à ce que le patient reçoive la plus petite dose efficace ou que le médicament soit arrêté.
Des instructions soigneuses et des observations de chaque patient sont essentielles pour prévenir des effets indésirables graves, irréversibles, voire mortels.
Étant donné que l'âge avancé semble augmenter le risque d'effets indésirables, INDOCIN doit être utilisé avec plus de prudence chez les personnes âgées. [voir Utilisation dans des populations spécifiques ]
Épaule douloureuse aiguë (bursite et/ou tendinite)
Capsules d'indométhacine, USP 75-150 mg par jour en 3 ou 4 doses fractionnées.
Le médicament doit être arrêté après que les signes et les symptômes de l'inflammation ont été contrôlés pendant plusieurs jours. Le cours habituel du traitement est de 7 à 14 jours.
Arthrite goutteuse aiguë
Capsules d'indométhacine, USP 50 mg trois fois par jour. Jusqu'à ce que la douleur soit tolérable. La dose doit ensuite être rapidement réduite jusqu'à l'arrêt complet du médicament. Un soulagement définitif de la douleur a été rapporté dans les 2 à 4 heures. La sensibilité et la chaleur disparaissent généralement en 24 à 36 heures et le gonflement disparaît progressivement en 3 à 5 jours.
COMMENT FOURNIE
Formes posologiques et points forts
Suppositoires INDOCIN 50mg
50 mg d'indométhacine. Blanc et opaque.
Stockage et manutention
Suppositoires INDOCIN® (suppositoires d'indométhacine USP), 50 mg chacun, sont des suppositoires rectaux blancs, opaques et fournis en boîtes de 30 ( CDN 69344-102-33).
Stockage
Conserver au réfrigérateur entre 2° et 8°C (36° et 46°F).
Fabriqué par : G&W Laboratories, Inc., South Plainfield, NJ 07080. Révisé : juillet 2019
EFFETS SECONDAIRES
Les effets indésirables suivants sont discutés plus en détail dans d'autres sections de l'étiquetage :
- Événements thrombotiques cardiovasculaires [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Saignement gastro-intestinal, ulcération et perforation [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Hépatotoxicité [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Hypertension [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Insuffisance cardiaque et œdème [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Toxicité rénale et hyperkaliémie [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Réactions anaphylactiques [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Réactions cutanées graves [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Toxicité hématologique [voir AVERTISSEMENTS ET PRECAUTIONS ]
Expérience des essais cliniques
Étant donné que les essais cliniques sont menés dans des conditions très variables, les taux d'effets indésirables observés dans les essais cliniques d'un médicament ne peuvent pas être directement comparés aux taux des essais cliniques d'un autre médicament et peuvent ne pas refléter les taux observés dans la pratique clinique.
Dans une étude gastroscopique chez 45 sujets sains, le nombre d'anomalies de la muqueuse gastrique était significativement plus élevé dans le groupe recevant des gélules d'indométhacine que dans le groupe prenant des suppositoires INDOCIN ou un placebo.
Dans une étude clinique comparative en double aveugle portant sur 175 patients atteints de polyarthrite rhumatoïde, cependant, l'incidence des effets indésirables gastro-intestinaux supérieurs avec les suppositoires INDOCIN ou les gélules d'indométhacine était comparable. L'incidence des effets indésirables gastro-intestinaux inférieurs était plus élevée dans le groupe des suppositoires.
Les réactions défavorables pour les capsules d'indomethacin énumérées dans la table suivante ont été arrangées dans deux groupes : (1) l'incidence plus grande que 1 %; et (2) incidence inférieure à 1 %. L'incidence pour le groupe (1) a été obtenue à partir de 33 essais cliniques contrôlés en double aveugle rapportés dans la littérature (1 092 patients). L'incidence pour le groupe (2) était basée sur des rapports d'essais cliniques, dans la littérature et sur des rapports volontaires depuis la commercialisation. La probabilité d'une relation causale existe entre l'indométhacine et ces effets indésirables, dont certains n'ont été rapportés que rarement.
Les effets indésirables rapportés avec les capsules d'indométhacine peuvent survenir lors de l'utilisation des suppositoires. De plus, une irritation rectale et un ténesme ont été rapportés chez des patients ayant reçu les suppositoires.
Relation causale inconnue
D'autres réactions ont été rapportées mais sont survenues dans des circonstances où une relation causale n'a pas pu être établie. Cependant, dans ces événements rarement signalés, la possibilité ne peut être exclue. Par conséquent, ces observations sont répertoriées pour servir d'information d'alerte aux médecins :
Cardiovasculaire: Thrombophlébite
Hématologique : Bien qu'il y ait eu plusieurs rapports de leucémie, les informations à l'appui sont faibles
Génito-urinaire : Fréquence urinaire
Une rare occurrence de fasciite nécrosante fulminante, en particulier en association avec le streptocoque hémolytique du groupe Aβ, a été décrite chez des personnes traitées par des anti-inflammatoires non stéroïdiens, dont l'indométhacine, parfois avec une issue fatale.
INTERACTIONS MÉDICAMENTEUSES
Voir le tableau 2 pour les interactions médicamenteuses cliniquement significatives avec l'indométhacine.
Effets sur les tests de laboratoire
INDOCIN réduit l'activité basale de la rénine plasmatique (ARP), ainsi que les élévations de l'ARP induites par l'administration de furosémide ou la déplétion saline ou volémique. Ces faits doivent être pris en compte lors de l'évaluation de l'activité de la rénine plasmatique chez les patients hypertendus. Des résultats faussement négatifs au test de suppression de la dexaméthasone (DST) chez des patients traités par l'indométhacine ont été rapportés. Ainsi, les résultats du DST doivent être interprétés avec prudence chez ces patients.
AVERTISSEMENTS
Inclus dans le cadre du "PRÉCAUTIONS" Section
PRÉCAUTIONS
Événements thrombotiques cardiovasculaires
Des essais cliniques portant sur plusieurs AINS sélectifs et non sélectifs de la COX-2 d'une durée pouvant aller jusqu'à trois ans ont montré un risque accru d'événements thrombotiques cardiovasculaires (CV) graves, notamment d'infarctus du myocarde (IM) et d'accident vasculaire cérébral, qui peuvent être mortels. Sur la base des données disponibles, il n'est pas clair que le risque d'événements thrombotiques CV soit similaire pour tous les AINS. L'augmentation relative des événements thrombotiques CV graves par rapport au niveau de référence conférée par l'utilisation d'AINS semble être similaire chez les personnes avec et sans maladie CV connue ou facteurs de risque de maladie CV. Cependant, les patients présentant une maladie CV ou des facteurs de risque connus présentaient une incidence absolue plus élevée d'événements thrombotiques CV graves en excès, en raison de leur taux de base plus élevé. Certaines études observationnelles ont montré que ce risque accru d'événements thrombotiques CV graves commençait dès les premières semaines de traitement. L'augmentation du risque thrombotique CV a été observée le plus systématiquement à des doses plus élevées.
Pour minimiser le risque potentiel d'événement CV indésirable chez les patients traités par AINS, utiliser la dose efficace la plus faible pendant la durée la plus courte possible. Les médecins et les patients doivent rester attentifs à l'apparition de tels événements, tout au long du traitement, même en l'absence de symptômes CV antérieurs. Les patients doivent être informés des symptômes des événements CV graves et des mesures à prendre s'ils surviennent.
Il n'existe aucune preuve cohérente que l'utilisation concomitante d'aspirine atténue le risque accru d'événements thrombotiques CV graves associés à l'utilisation d'AINS. L'utilisation concomitante d'aspirine et d'un AINS, tel que l'indométhacine, augmente le risque d'événements gastro-intestinaux (GI) graves [voir Saignement gastro-intestinal, ulcération et perforation ].
Chirurgie post pontage aortocoronarien (CABG)
Deux grands essais cliniques contrôlés portant sur un AINS sélectif de la COX-2 pour le traitement de la douleur au cours des 10 à 14 premiers jours suivant un pontage coronarien ont révélé une incidence accrue d'infarctus du myocarde et d'accident vasculaire cérébral. Les AINS sont contre-indiqués dans le cadre d'un PAC [voir CONTRE-INDICATIONS ].
Patients post-IM
Des études observationnelles menées dans le registre national danois ont démontré que les patients traités par AINS dans la période post-IM présentaient un risque accru de récidive d'infarctus, de décès d'origine CV et de mortalité toutes causes confondues dès la première semaine de traitement. Dans cette même cohorte, l'incidence des décès au cours de la première année suivant l'IM était de 20 pour 100 années-personnes chez les patients traités par AINS contre 12 pour 100 années-personnes chez les patients non exposés aux AINS. Bien que le taux absolu de décès ait quelque peu diminué après la première année après l'infarctus du myocarde, le risque relatif accru de décès chez les utilisateurs d'AINS a persisté pendant au moins les quatre années de suivi suivantes. Éviter l'utilisation d'INDOCIN 75 mg chez les patients ayant récemment subi un IM à moins que les bénéfices ne soient censés l'emporter sur le risque d'événements thrombotiques CV récurrents. Si INDOCIN est utilisé chez des patients avec un IM récent, surveiller les patients pour des signes d'ischémie cardiaque.
Saignement gastro-intestinal, ulcération et perforation
Les AINS, y compris l'indométhacine, provoquent des effets indésirables gastro-intestinaux (GI) graves, notamment une inflammation, des saignements, une ulcération et une perforation de l'œsophage, de l'estomac, de l'intestin grêle ou du gros intestin, qui peuvent être fatals. Ces événements indésirables graves peuvent survenir à tout moment, avec ou sans symptômes précurseurs, chez les patients traités par AINS. Seul un patient sur cinq qui développe un événement indésirable gastro-intestinal supérieur grave sous traitement par AINS est symptomatique. Des ulcères gastro-intestinaux supérieurs, des saignements macroscopiques ou des perforations causés par les AINS sont survenus chez environ 1 % des patients traités pendant 3 à 6 mois et chez environ 2 % à 4 % des patients traités pendant un an. Cependant, même un traitement à court terme par AINS n'est pas sans risque.
Facteurs de risque de saignement gastro-intestinal, d'ulcération et de perforation
Les patients ayant des antécédents d'ulcère peptique et/ou d'hémorragie gastro-intestinale qui utilisaient des AINS avaient un risque plus de 10 fois plus élevé de développer une hémorragie gastro-intestinale par rapport aux patients sans ces facteurs de risque. D'autres facteurs qui augmentent le risque d'hémorragie gastro-intestinale chez les patients traités avec des AINS comprennent une durée plus longue du traitement par AINS ; utilisation concomitante de corticostéroïdes oraux, d'aspirine, d'anticoagulants ou d'inhibiteurs sélectifs de la recapture de la sérotonine (ISRS) ; fumeur; Utilisation d'alcool; âge avancé; et un mauvais état de santé général. La plupart des rapports post-commercialisation d'événements gastro-intestinaux mortels sont survenus chez des patients âgés ou affaiblis. De plus, les patients atteints d'une maladie hépatique avancée et/ou d'une coagulopathie présentent un risque accru d'hémorragie gastro-intestinale.
Stratégies pour minimiser les risques gastro-intestinaux chez les patients traités par AINS
- Utilisez la dose efficace la plus faible pendant la durée la plus courte possible.
- Évitez l'administration de plus d'un AINS à la fois.
- Éviter l'utilisation chez les patients à risque plus élevé à moins que les bénéfices attendus ne l'emportent sur le risque accru de saignement. Pour ces patients, ainsi que ceux présentant des saignements gastro-intestinaux actifs, envisagez des thérapies alternatives autres que les AINS.
- Restez attentif aux signes et symptômes d'ulcération et de saignement gastro-intestinaux pendant le traitement par AINS.
- Si un événement indésirable GI grave est suspecté, initier rapidement une évaluation et un traitement, et interrompre INDOCIN jusqu'à ce qu'un événement indésirable GI grave soit exclu.
- Dans le cadre de l'utilisation concomitante d'aspirine à faible dose pour la prophylaxie cardiaque, surveiller de plus près les patients afin de déceler tout signe d'hémorragie gastro-intestinale [voir INTERACTIONS MÉDICAMENTEUSES ].
Hépatotoxicité
Des élévations de l'ALT ou de l'AST (trois fois ou plus la limite supérieure de la normale [LSN]) ont été signalées chez environ 1 % des patients traités par AINS dans les essais cliniques. De plus, des cas rares, parfois mortels, d'atteinte hépatique grave, y compris une hépatite fulminante, une nécrose hépatique et une insuffisance hépatique, ont été signalés.
Des élévations de l'ALT ou de l'AST (moins de trois fois la LSN) peuvent survenir chez jusqu'à 15 % des patients traités par des AINS, y compris l'indométhacine.
Informez les patients des signes avant-coureurs et des symptômes d'hépatotoxicité (p. ex., nausées, fatigue, léthargie, diarrhée, prurit, jaunisse, sensibilité de l'hypochondre droit et symptômes pseudo-grippaux). Si des signes cliniques et des symptômes compatibles avec une maladie du foie se développent, ou si des manifestations systémiques se produisent (par exemple, éosinophilie, éruption cutanée, etc.), arrêtez INDOCIN immédiatement et effectuez une évaluation clinique du patient.
Hypertension
Les AINS, y compris INDOCIN 50 mg, peuvent entraîner une nouvelle apparition d'hypertension ou une aggravation d'une hypertension préexistante, l'un ou l'autre pouvant contribuer à l'augmentation de l'incidence des événements CV. Les patients prenant des inhibiteurs de l'enzyme de conversion de l'angiotensine (ECA), des diurétiques thiazidiques ou des diurétiques de l'anse peuvent présenter une réponse altérée à ces traitements lorsqu'ils prennent des AINS [voir INTERACTIONS MÉDICAMENTEUSES ].
Surveiller la tension artérielle (TA) au début du traitement par AINS et tout au long du traitement.
Insuffisance cardiaque et œdème
La méta-analyse Coxib and traditional NSAID Trialists' Collaboration d'essais contrôlés randomisés a démontré une augmentation d'environ deux fois des hospitalisations pour insuffisance cardiaque chez les patients traités sélectivement par COX-2 et les patients traités par AINS non sélectifs par rapport aux patients traités par placebo. Dans une étude du registre national danois sur des patients souffrant d'insuffisance cardiaque, l'utilisation d'AINS a augmenté le risque d'infarctus du myocarde, d'hospitalisation pour insuffisance cardiaque et de décès.
De plus, une rétention hydrique et un œdème ont été observés chez certains patients traités par AINS. L'utilisation d'indométhacine peut atténuer les effets CV de plusieurs agents thérapeutiques utilisés pour traiter ces affections médicales (par exemple, les diurétiques, les inhibiteurs de l'ECA ou les antagonistes des récepteurs de l'angiotensine [ARA]) [voir INTERACTIONS MÉDICAMENTEUSES ].
Éviter l'utilisation d'INDOCIN 50 mg chez les patients souffrant d'insuffisance cardiaque sévère à moins que les bénéfices ne l'emportent sur le risque d'aggravation de l'insuffisance cardiaque. Si INDOCIN est utilisé chez des patients souffrant d'insuffisance cardiaque sévère, surveiller les patients pour des signes d'aggravation de l'insuffisance cardiaque.
Toxicité rénale et hyperkaliémie
Toxicité rénale
L'administration à long terme d'AINS a entraîné une nécrose papillaire rénale et d'autres lésions rénales.
Une toxicité rénale a également été observée chez des patients chez qui les prostaglandines rénales ont un rôle compensateur dans le maintien de la perfusion rénale. Chez ces patients, l'administration d'un AINS peut entraîner une réduction dose-dépendante de la formation des prostaglandines et, accessoirement, du débit sanguin rénal, ce qui peut précipiter une décompensation rénale manifeste. Les patients les plus à risque de cette réaction sont ceux qui présentent une fonction rénale altérée, une déshydratation, une hypovolémie, une insuffisance cardiaque, un dysfonctionnement hépatique, ceux qui prennent des diurétiques et des inhibiteurs de l'ECA ou des ARA, et les personnes âgées. L'arrêt du traitement par AINS est généralement suivi d'un retour à l'état antérieur au traitement.
Aucune information provenant d'études cliniques contrôlées n'est disponible concernant l'utilisation d'INDOCIN 75 mg chez les patients atteints d'insuffisance rénale avancée. Les effets rénaux d'INDOCIN peuvent accélérer la progression de la dysfonction rénale chez les patients atteints d'insuffisance rénale préexistante.
Corriger le statut volémique chez les patients déshydratés ou hypovolémiques avant de commencer INDOCIN. Surveiller la fonction rénale chez les patients atteints d'insuffisance rénale ou hépatique, d'insuffisance cardiaque, de déshydratation ou d'hypovolémie pendant l'utilisation d'INDOCIN [voir INTERACTIONS MÉDICAMENTEUSES ]. Éviter l'utilisation d'INDOCIN chez les patients atteints d'insuffisance rénale avancée à moins que l'on s'attende à ce que les avantages l'emportent sur le risque d'aggravation de la fonction rénale. Si INDOCIN 75 mg est utilisé chez des patients atteints d'insuffisance rénale avancée, surveiller les patients pour détecter tout signe d'aggravation de la fonction rénale.
Il a été rapporté que l'ajout du diurétique d'épargne potassique, le triamtérène, à un programme d'entretien d'indométhacine a entraîné une insuffisance rénale aiguë réversible chez deux des quatre volontaires sains. L'indométhacine et le triamtérène ne doivent pas être administrés ensemble.
Hyperkaliémie
Des augmentations de la concentration sérique de potassium, y compris une hyperkaliémie, ont été rapportées avec l'utilisation d'AINS, même chez certains patients sans insuffisance rénale. Chez les patients ayant une fonction rénale normale, ces effets ont été attribués à un état hyporéninémique-hypoaldostéronisme.
L'indométhacine et les diurétiques épargneurs de potassium peuvent être associés à une augmentation des taux sériques de potassium. Les effets potentiels de l'indométhacine et des diurétiques épargneurs de potassium sur les taux de potassium et la fonction rénale doivent être pris en compte lorsque ces agents sont administrés simultanément.
Réactions anaphylactiques
L'indométhacine a été associée à des réactions anaphylactiques chez les patients avec ou sans hypersensibilité connue à l'indométhacine et chez les patients souffrant d'asthme sensible à l'aspirine [voir CONTRE-INDICATIONS et Exacerbation de l'asthme lié à la sensibilité à l'aspirine ].
Cherchez de l'aide d'urgence si une réaction anaphylactique se produit.
Exacerbation de l'asthme lié à la sensibilité à l'aspirine
Une sous-population de patients asthmatiques peut avoir un asthme sensible à l'aspirine qui peut inclure une rhinosinusite chronique compliquée par des polypes nasaux ; bronchospasme sévère, potentiellement mortel ; et/ou intolérance à l'aspirine et aux autres AINS. Étant donné qu'une réactivité croisée entre l'aspirine et d'autres AINS a été rapportée chez ces patients sensibles à l'aspirine, INDOCIN est contre-indiqué chez les patients présentant cette forme de sensibilité à l'aspirine [voir CONTRE-INDICATIONS ]. Lorsqu'INDOCIN est utilisé chez des patients souffrant d'asthme préexistant (sans sensibilité connue à l'aspirine), surveiller les patients pour détecter tout changement dans les signes et les symptômes de l'asthme.
Réactions cutanées graves
Les AINS, y compris l'indométhacine, peuvent provoquer des effets indésirables cutanés graves tels que la dermatite exfoliative, le syndrome de Stevens-Johnson (SJS) et la nécrolyse épidermique toxique (TEN), qui peuvent être fatals. Ces événements graves peuvent survenir sans avertissement. Informer les patients des signes et symptômes des réactions cutanées graves et d'arrêter l'utilisation d'INDOCIN 25 mg dès la première apparition d'une éruption cutanée ou de tout autre signe d'hypersensibilité. INDOCIN est contre-indiqué chez les patients ayant déjà présenté des réactions cutanées graves aux AINS [voir CONTRE-INDICATIONS ].
Fermeture prématurée du canal artériel fœtal
L'indométhacine peut provoquer une fermeture prématurée du canal artériel fœtal. Éviter l'utilisation d'AINS, y compris INDOCIN, chez les femmes enceintes à partir de 30 semaines de gestation (troisième trimestre) [voir Utilisation dans des populations spécifiques ].
Toxicité hématologique
Une anémie est survenue chez des patients traités par AINS. Cela peut être dû à une perte de sang occulte ou importante, à une rétention d'eau ou à un effet incomplètement décrit sur l'érythropoïèse. Si un patient traité par INDOCIN 25 mg présente des signes ou des symptômes d'anémie, surveiller l'hémoglobine ou l'hématocrite.
Les AINS, y compris INDOCIN, peuvent augmenter le risque d'événements hémorragiques. Les affections comorbides, telles que les troubles de la coagulation ou l'utilisation concomitante de warfarine, d'autres anticoagulants, d'agents antiplaquettaires (p. ex., aspirine), d'inhibiteurs de la recapture de la sérotonine (ISRS) et d'inhibiteurs de la recapture de la sérotonine et de la noradrénaline (IRSN) peuvent augmenter ce risque. Surveiller ces patients pour des signes de saignement [voir INTERACTIONS MÉDICAMENTEUSES ].
Masquage de l'inflammation et de la fièvre
L'activité pharmacologique d'INDOCIN 75 mg dans la réduction de l'inflammation, et éventuellement de la fièvre, peut diminuer l'utilité des signes diagnostiques dans la détection des infections.
Surveillance en laboratoire
Étant donné que des saignements gastro-intestinaux graves, une hépatotoxicité et des lésions rénales peuvent survenir sans symptômes ou signes avant-coureurs, envisagez de surveiller périodiquement les patients sous traitement AINS à long terme avec un CBC et un profil chimique [voir Saignement gastro-intestinal, ulcération et perforation, hépatotoxicité, toxicité rénale et hyperkaliémie ].
Effets sur le système nerveux central
INDOCIN 75 mg peut aggraver la dépression ou d'autres troubles psychiatriques, l'épilepsie et le parkinsonisme, et doit être utilisé avec beaucoup de prudence chez les patients atteints de ces affections. Arrêtez INDOCIN 25 mg si des effets indésirables graves sur le SNC se développent.
INDOCIN peut causer de la somnolence; par conséquent, avertissez les patients de ne pas s'engager dans des activités nécessitant de la vigilance mentale et de la coordination motrice, telles que la conduite d'une voiture. L'indométhacine peut également causer des maux de tête. Les céphalées qui persistent malgré la réduction de la posologie nécessitent l'arrêt du traitement par INDOCIN.
Effets oculaires
Des dépôts cornéens et des troubles rétiniens, y compris ceux de la macula, ont été observés chez certains patients ayant reçu un traitement prolongé par INDOCIN. Soyez attentif à l'association possible entre les changements notés et INDOCIN. Il est conseillé d'arrêter le traitement si de tels changements sont observés. Une vision floue peut être un symptôme important et justifier un examen ophtalmologique approfondi. Étant donné que ces changements peuvent être asymptomatiques, un examen ophtalmologique à intervalles réguliers est souhaitable chez les patients recevant un traitement prolongé. INDOCIN n'est pas indiqué pour un traitement à long terme.
Informations sur les conseils aux patients
Conseillez au patient de lire l'étiquetage patient approuvé par la FDA ( Guide des médicaments ) qui accompagne chaque ordonnance délivrée. Informez les patients, les familles ou leurs soignants des informations suivantes avant de commencer le traitement par INDOCIN et périodiquement au cours du traitement en cours. Les suppositoires INDOCIN 75 mg sont à usage rectal uniquement. Conseillez aux patientes de ne pas utiliser les suppositoires INDOCIN 50 mg par voie orale ou intra-vaginale.
Événements thrombotiques cardiovasculaires
Conseillez aux patients d'être attentifs aux symptômes d'événements thrombotiques cardiovasculaires, y compris les douleurs thoraciques, l'essoufflement, la faiblesse ou les troubles de l'élocution, et de signaler immédiatement tout symptôme à leur fournisseur de soins de santé [voir AVERTISSEMENTS ET PRECAUTIONS ].
Saignement gastro-intestinal, ulcération et perforation
Conseillez aux patients de signaler les symptômes d'ulcérations et de saignements, y compris les douleurs épigastriques, la dyspepsie, le méléna et l'hématémèse à leur fournisseur de soins de santé. En cas d'utilisation concomitante d'aspirine à faible dose pour la prophylaxie cardiaque, informer les patients du risque accru et des signes et symptômes d'hémorragie gastro-intestinale [voir AVERTISSEMENTS ET PRECAUTIONS ].
Hépatotoxicité
Informer les patients des signes avant-coureurs et des symptômes d'hépatotoxicité (p. ex., nausées, fatigue, léthargie, prurit, diarrhée, jaunisse, sensibilité du quadrant supérieur droit et symptômes « pseudo-grippaux »). Si cela se produit, demandez aux patients d'arrêter INDOCIN et de consulter immédiatement un médecin [voir AVERTISSEMENTS ET PRECAUTIONS ].
Insuffisance cardiaque et œdème
Conseillez aux patients d'être attentifs aux symptômes d'insuffisance cardiaque congestive, y compris l'essoufflement, la prise de poids inexpliquée ou l'œdème, et de contacter leur fournisseur de soins de santé si de tels symptômes surviennent [voir AVERTISSEMENTS ET PRECAUTIONS ].
Réactions anaphylactiques
Informer les patients des signes d'une réaction anaphylactique (par exemple, difficulté à respirer, gonflement du visage ou de la gorge). Demandez aux patients de demander de l'aide d'urgence immédiate si ceux-ci se produisent [voir CONTRE-INDICATIONS et AVERTISSEMENTS ET PRECAUTIONS ].
Réactions cutanées graves
Conseillez aux patients d'arrêter INDOCIN immédiatement s'ils développent tout type d'éruption cutanée et de contacter leur fournisseur de soins de santé dès que possible [voir AVERTISSEMENTS ET PRECAUTIONS ].
Fertilité féminine
Informez les femmes en âge de procréer qui désirent une grossesse que les AINS, y compris INDOCIN 75 mg, peuvent être associés à un retard réversible de l'ovulation [voir Utilisation dans des populations spécifiques ].
Toxicité fœtale
Informer les femmes enceintes d'éviter l'utilisation d'INDOCIN 50 mg et d'autres AINS à partir de 30 semaines de gestation en raison du risque de fermeture prématurée du canal artériel fœtal [voir AVERTISSEMENTS ET PRECAUTIONS et Utilisation dans des populations spécifiques ].
Éviter l'utilisation concomitante d'AINS
Informez les patients que l'utilisation concomitante d'INDOCIN avec d'autres AINS ou salicylates (par exemple, diflunisal, salsalate) n'est pas recommandée en raison du risque accru de toxicité gastro-intestinale et de l'augmentation faible ou nulle de l'efficacité [voir AVERTISSEMENTS ET PRECAUTIONS et INTERACTIONS MÉDICAMENTEUSES ]. Alerter les patients que des AINS peuvent être présents dans des médicaments « en vente libre » pour le traitement du rhume, de la fièvre ou de l'insomnie.
Utilisation d'AINS et d'aspirine à faible dose
Informez les patients de ne pas utiliser d'aspirine à faible dose en même temps qu'INDOCIN jusqu'à ce qu'ils en parlent à leur fournisseur de soins de santé [voir INTERACTIONS MÉDICAMENTEUSES ].
Toxicologie non clinique
Carcinogenèse, mutagenèse, altération de la fertilité
Carcinogenèse
Dans une étude de toxicité orale chronique de 81 semaines chez le rat à des doses allant jusqu'à 1 mg/kg/jour (0,05 fois la MRHD sur une base en mg/m2), l'indométhacine n'a eu aucun effet tumorigène. L'indométhacine n'a produit aucun changement néoplasique ou hyperplasique lié au traitement dans les études cancérigènes chez le rat (période d'administration de 73 à 110 semaines) et la souris (période d'administration de 62 à 88 semaines) à des doses allant jusqu'à 1,5 mg/kg/jour (0,04 fois [souris ] et 0,07 fois [rats] la MRHD sur une base mg/m2, respectivement).
Mutagenèse
L'indométhacine n'a eu aucun effet mutagène dans les tests bactériens in vitro et une série de tests in vivo, y compris le test médié par l'hôte, les létaux récessifs liés au sexe chez la drosophile et le test du micronoyau chez la souris.
Altération de la fertilité
L'indométhacine à des doses allant jusqu'à 0,5 mg/kg/jour n'a eu aucun effet sur la fertilité chez la souris dans une étude de reproduction sur deux générations (0,01 fois la MRHD sur une base en mg/m2) ou une étude de reproduction sur deux portées chez le rat (0,02 fois la MRHD sur une base mg/m2).
Utilisation dans des populations spécifiques
Grossesse
Résumé des risques
L'utilisation d'AINS, dont INDOCIN 25 mg, au cours du troisième trimestre de la grossesse augmente le risque de fermeture prématurée du canal artériel fœtal. Évitez l'utilisation d'AINS, y compris INDOCIN, chez les femmes enceintes à partir de 30 semaines de gestation (troisième trimestre).
Il n'y a pas d'études adéquates et bien contrôlées d'INDOCIN chez les femmes enceintes. Les données d'études observationnelles concernant les risques embryofœtaux potentiels de l'utilisation d'AINS chez les femmes au cours du premier ou du deuxième trimestre de la grossesse ne sont pas concluantes. Dans la population générale des États-Unis, toutes les grossesses cliniquement reconnues, quelle que soit l'exposition aux médicaments, ont un taux de fond de 2 à 4 % pour les malformations majeures et de 15 à 20 % pour les pertes de grossesse. Dans les études de reproduction chez l'animal, une ossification fœtale retardée a été observée avec l'administration d'indométhacine à des souris et à des rats pendant l'organogenèse à des doses de 0,1 et 0,2 fois, respectivement, la dose humaine maximale recommandée (MRHD, 200 mg). Dans les études publiées chez les souris enceintes, l'indométhacine a produit une toxicité maternelle et la mort, une augmentation des résorptions fœtales et des malformations fœtales à 0,1 fois la MRHD. Lorsque les mères de rats et de souris ont reçu une dose au cours des trois derniers jours de gestation, l'indométhacine a produit une nécrose neuronale chez la progéniture à 0,1 et 0,05 fois la MRHD, respectivement [voir Données ]. Sur la base de données animales, il a été démontré que les prostaglandines jouent un rôle important dans la perméabilité vasculaire de l'endomètre, l'implantation de blastocystes et la décidualisation. Dans des études animales, l'administration d'inhibiteurs de la synthèse des prostaglandines tels que l'indométhacine a entraîné une augmentation des pertes avant et après l'implantation.
Considérations cliniques
Travail ou accouchement
Il n'y a pas d'études sur les effets d'INDOCIN 75 mg pendant le travail ou l'accouchement. Dans les études animales, les AINS, y compris l'indométhacine, inhibent la synthèse des prostaglandines, retardent la parturition et augmentent l'incidence de la mortinaissance.
Données
Données animales
Des études de reproduction ont été menées chez des souris et des rats à des doses de 0,5, 1,0, 2,0 et 4,0 mg/kg/jour. À l'exception de l'ossification fœtale retardée à 4 mg/kg/jour (0,1 fois [souris] et 0,2 fois [rats] la MRHD sur une base mg/m2, respectivement) considérée comme secondaire à la diminution du poids fœtal moyen, aucune augmentation des malformations fœtales n'a été observée. observée par rapport aux groupes témoins. D'autres études chez les souris rapportées dans la littérature utilisant des doses plus élevées (5 à 15 mg/kg/jour, 0,1 à 0,4 fois MRHD sur une base mg/m2) ont décrit la toxicité maternelle et la mort, l'augmentation des résorptions fœtales et les malformations fœtales. Des études comparables chez des rongeurs utilisant de fortes doses d'aspirine ont montré des effets maternels et fœtaux similaires.
Chez le rat et la souris, l'administration maternelle d'indométhacine à raison de 4,0 mg/kg/jour (0,2 fois et 0,1 fois la MRHD en mg/m2) au cours des 3 derniers jours de gestation a été associée à une incidence accrue de nécrose neuronale dans le diencéphale chez les fœtus nés vivants, cependant, aucune augmentation de la nécrose neuronale n'a été observée à 2,0 mg/kg/jour par rapport aux groupes témoins (0,1 fois et 0,05 fois la MRHD sur une base en mg/m2). L'administration de 0,5 ou 4,0 mg/kg/jour à la progéniture au cours des 3 premiers jours de vie n'a pas provoqué d'augmentation de la nécrose neuronale à l'une ou l'autre des doses.
Lactation
Résumé des risques
D'après les données cliniques publiées disponibles, l'indométhacine peut être présente dans le lait maternel. Les avantages de l'allaitement pour le développement et la santé doivent être pris en compte, ainsi que le besoin clinique de la mère pour INDOCIN 25 mg et tout effet indésirable potentiel sur le nourrisson allaité à cause d'INDOCIN 75 mg ou de l'affection maternelle sous-jacente.
Données
Dans une étude, les niveaux d'indométhacine dans le lait maternel étaient inférieurs à la sensibilité du test (
Femelles et mâles de potentiel reproducteur
Infertilité
Femelles
Sur la base du mécanisme d'action, l'utilisation d'AINS médiés par les prostaglandines, y compris INDOCIN, peut retarder ou prévenir la rupture des follicules ovariens, qui a été associée à une infertilité réversible chez certaines femmes. Des études animales publiées ont montré que l'administration d'inhibiteurs de la synthèse des prostaglandines a le potentiel de perturber la rupture folliculaire médiée par les prostaglandines nécessaire à l'ovulation. De petites études chez des femmes traitées avec des AINS ont également montré un retard réversible de l'ovulation. Envisager l'arrêt des AINS, y compris INDOCIN, chez les femmes qui ont des difficultés à concevoir ou qui font l'objet d'un examen d'infertilité.
Utilisation pédiatrique
L'innocuité et l'efficacité chez les patients pédiatriques de 14 ans et moins n'ont pas été établies.
INDOCIN 75 mg ne doit pas être prescrit aux patients pédiatriques de 14 ans et moins, sauf si la toxicité ou le manque d'efficacité associés à d'autres médicaments justifient le risque.
Dans l'expérience avec plus de 900 patients pédiatriques rapportés dans la littérature ou au fabricant qui ont été traités avec des capsules d'indométhacine, les effets secondaires chez les patients pédiatriques étaient comparables à ceux rapportés chez les adultes. L'expérience chez les patients pédiatriques s'est limitée à l'utilisation de capsules d'indométhacine.
Si une décision est prise d'utiliser l'indométhacine pour les patients pédiatriques de deux ans ou plus, ces patients doivent être étroitement surveillés et une évaluation périodique de la fonction hépatique est recommandée. Des cas d'hépatotoxicité ont été signalés chez des patients pédiatriques atteints de polyarthrite rhumatoïde juvénile, y compris des décès. Si un traitement par l'indométhacine est institué, une dose initiale suggérée est de 1 à 2 mg/kg/jour administrée en doses fractionnées. La dose quotidienne maximale ne doit pas dépasser 3 mg/kg/jour ou 150-200 mg/jour, selon la valeur la moins élevée. Des données limitées sont disponibles pour étayer l'utilisation d'une dose quotidienne maximale de 4 mg/kg/jour ou de 150 à 200 mg/jour, selon la valeur la moins élevée. À mesure que les symptômes disparaissent, la dose quotidienne totale doit être réduite au niveau le plus bas requis pour contrôler les symptômes, ou le médicament doit être arrêté.
Utilisation gériatrique
Les patients âgés, comparés aux patients plus jeunes, sont plus à risque d'effets indésirables cardiovasculaires, gastro-intestinaux et/ou rénaux graves associés aux AINS. Si le bénéfice attendu pour le patient âgé l'emporte sur ces risques potentiels, commencez le dosage à l'extrémité inférieure de la plage de dosage et surveillez les patients pour détecter tout effet indésirable [voir AVERTISSEMENTS ET PRECAUTIONS ].
L'indométhacine peut entraîner une confusion ou, rarement, une psychose [voir EFFETS INDÉSIRABLES ] ; les médecins doivent rester attentifs à la possibilité de tels effets indésirables chez les personnes âgées.
L'indométhacine et ses métabolites sont connus pour être en grande partie excrétés par les reins, et le risque de réactions indésirables à ce médicament peut être plus élevé chez les patients présentant une insuffisance rénale. Étant donné que les patients âgés sont plus susceptibles d'avoir une fonction rénale diminuée, soyez prudent dans cette population de patients, et il peut être utile de surveiller la fonction rénale [voir PHARMACOLOGIE CLINIQUE ].
SURDOSAGE
Les symptômes consécutifs à des surdosages aigus d'AINS se sont généralement limités à une léthargie, une somnolence, des nausées, des vomissements et des douleurs épigastriques, qui ont généralement été réversibles avec des soins de soutien. Des saignements gastro-intestinaux se sont produits. Une hypertension, une insuffisance rénale aiguë, une dépression respiratoire et un coma sont survenus, mais étaient rares [voir AVERTISSEMENTS ET PRECAUTIONS ].
Gérer les patients avec des soins symptomatiques et de soutien suite à un surdosage d'AINS. Il n'y a pas d'antidote spécifique. Envisager des vomissements et/ou du charbon activé (60 à 100 grammes chez l'adulte, 1 à 2 grammes par kg de poids corporel chez les patients pédiatriques) et/ou cathartique osmotique chez les patients symptomatiques observés dans les quatre heures suivant l'ingestion ou chez les patients présentant un surdosage important ( 5 à 10 fois la dose recommandée). La diurèse forcée, l'alcalinisation de l'urine, l'hémodialyse ou l'hémoperfusion peuvent ne pas être utiles en raison d'une forte liaison aux protéines.
Pour plus d'informations sur le traitement du surdosage, contactez un centre antipoison (1-800-222-1222).
CONTRE-INDICATIONS
INDOCIN 75 mg est contre-indiqué chez les patients suivants :
- Hypersensibilité connue (p. ex., réactions anaphylactiques et réactions cutanées graves) à l'indométhacine ou à l'un des composants du médicament [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Antécédents d'asthme, d'urticaire ou d'autres réactions de type allergique après la prise d'aspirine ou d'autres AINS. Des réactions anaphylactiques sévères, parfois fatales, aux AINS ont été rapportées chez ces patients [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Dans le cadre d'un pontage aortocoronarien (PAC) [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Chez les patients ayant des antécédents de proctite ou de saignement rectal récent
PHARMACOLOGIE CLINIQUE
Mécanisme d'action
L'indométhacine a des propriétés analgésiques, anti-inflammatoires et antipyrétiques.
Le mécanisme d'action d'INDOCIN, comme celui des autres AINS, n'est pas complètement élucidé mais implique l'inhibition de la cyclooxygénase (COX-1 et COX-2).
L'indométhacine est un puissant inhibiteur de la synthèse des prostaglandines in vitro. Les concentrations d'indométhacine atteintes pendant le traitement ont produit des effets in vivo. Les prostaglandines sensibilisent les nerfs afférents et potentialisent l'action de la bradykinine dans l'induction de la douleur chez les modèles animaux. Les prostaglandines sont des médiateurs de l'inflammation. L'indométhacine étant un inhibiteur de la synthèse des prostaglandines, son mode d'action peut être dû à une diminution des prostaglandines dans les tissus périphériques.
Pharmacocinétique
Absorption
Suite à des doses orales uniques de gélules d'indométhacine 25 mg ou 50 mg, l'indométhacine est facilement absorbée, atteignant des concentrations plasmatiques maximales d'environ 1 et 2 mcg/mL, respectivement, à environ 2 heures. Les gélules d'indométhacine administrées par voie orale sont pratiquement 100 % biodisponibles, 90 % de la dose étant absorbée dans les 4 heures. Avec un schéma thérapeutique typique de 25 ou 50 mg trois fois par jour, les concentrations plasmatiques à l'état d'équilibre de l'indométhacine sont en moyenne 1,4 fois celles après la première dose.
Le taux d'absorption est plus rapide à partir du suppositoire rectal qu'à partir des capsules d'indométhacine. Ordinairement, par conséquent, la quantité totale absorbée par le suppositoire devrait être au moins équivalente à la capsule. Dans des essais cliniques contrôlés, cependant, la quantité d'indométhacine absorbée s'est avérée légèrement inférieure (80 à 90 %) à celle absorbée par les gélules d'indométhacine. C'est probablement parce que certains sujets n'ont pas retenu le matériel du suppositoire pendant l'heure nécessaire pour assurer une absorption complète. Étant donné que le suppositoire se dissout assez rapidement plutôt que de fondre lentement, il est rarement récupéré sous une forme reconnaissable si le patient conserve le suppositoire pendant plus de quelques minutes.
Distribution
L'indométhacine est fortement liée aux protéines dans le plasma (environ 99 %) dans la plage attendue des concentrations plasmatiques thérapeutiques. L'indométhacine traverse la barrière hémato-encéphalique et le placenta et apparaît dans le lait maternel.
Élimination
Métabolisme
L'indométhacine existe dans le plasma sous forme de médicament parent et de ses métabolites desméthyl, desbenzoyl et desméthyldesbenzoyl, tous sous forme non conjuguée. Il se forme une formation appréciable de conjugués glucuronides de chaque métabolite et d'indométhacine.
Excrétion
L'indométhacine est éliminée par excrétion rénale, métabolisme et excrétion biliaire. L'indométhacine subit une circulation entérohépatique appréciable. Environ 60 % d'une dose orale sont récupérés dans l'urine sous forme de médicament et de métabolites (26 % sous forme d'indométhacine et de son glucuronide), et 33 % sont récupérés dans les fèces (1,5 % sous forme d'indométhacine). La demi-vie moyenne de l'indométhacine est estimée à environ 4,5 heures.
Populations spécifiques
Pédiatrique
La pharmacocinétique d'INDOCIN n'a pas été étudiée chez les patients pédiatriques.
Course
Les différences pharmacocinétiques dues à la race n'ont pas été identifiées.
Insuffisance hépatique
La pharmacocinétique d'INDOCIN 75 mg n'a pas été étudiée chez les patients insuffisants hépatiques.
Insuffisance rénale
La pharmacocinétique d'INDOCIN 75 mg n'a pas été étudiée chez les patients insuffisants rénaux [voir AVERTISSEMENTS ET PRECAUTIONS ].
Études sur les interactions médicamenteuses
Aspirine
Dans une étude chez des volontaires sains, il a été constaté que l'administration concomitante chronique de 3,6 g d'aspirine par jour diminue les taux sanguins d'indométhacine d'environ 20 % [voir INTERACTIONS MÉDICAMENTEUSES ].
Lorsque les AINS ont été administrés avec de l'aspirine, la liaison aux protéines des AINS a été réduite, bien que la clairance des AINS libres n'ait pas été modifiée. La signification clinique de cette interaction n'est pas connue. Voir le tableau 2 pour les interactions médicamenteuses cliniquement significatives des AINS avec l'aspirine [voir INTERACTIONS MÉDICAMENTEUSES ].
Diflunisal
Chez des volontaires sains recevant de l'indométhacine, l'administration de diflunisal a diminué la clairance rénale et augmenté significativement les taux plasmatiques d'indométhacine [voir INTERACTIONS MÉDICAMENTEUSES ].
Etudes cliniques
INDOCIN 25 mg s'est avéré être un agent anti-inflammatoire efficace, approprié pour une utilisation à long terme dans la polyarthrite rhumatoïde, la spondylarthrite ankylosante et l'arthrose.
INDOCIN procure un soulagement des symptômes ; il ne modifie pas l'évolution progressive de la maladie sous-jacente.
INDOCIN 75 mg supprime l'inflammation dans la polyarthrite rhumatoïde, comme en témoigne le soulagement de la douleur et la réduction de la fièvre, de l'enflure et de la sensibilité. L'amélioration chez les patients traités par INDOCIN pour la polyarthrite rhumatoïde a été démontrée par une réduction du gonflement des articulations, du nombre moyen d'articulations atteintes et de la raideur matinale ; par une mobilité accrue démontrée par une diminution du temps de marche ; et par une capacité fonctionnelle améliorée démontrée par une augmentation de la force de préhension. INDOCIN peut permettre de réduire la dose de stéroïdes chez les patients recevant des stéroïdes pour les formes les plus sévères de polyarthrite rhumatoïde. Dans de tels cas, la dose de stéroïdes doit être réduite lentement et les patients suivis de très près pour tout effet indésirable éventuel.
INFORMATIONS PATIENTS
Quelles sont les informations les plus importantes que je devrais connaître sur les médicaments appelés anti-inflammatoires non stéroïdiens (AINS) ?
Les AINS peuvent provoquer des effets secondaires graves, notamment :
- Risque accru de crise cardiaque ou d'accident vasculaire cérébral pouvant entraîner la mort. Ce risque peut survenir au début du traitement et peut augmenter :
- avec des doses croissantes d'AINS
- avec une utilisation plus longue des AINS
- Risque accru de saignement, d'ulcères et de déchirures (perforation) de l'œsophage (tube menant de la bouche à l'estomac), de l'estomac et des intestins :
Le risque de développer un ulcère ou des saignements augmente avec :
Les AINS ne doivent être utilisés que :
- à tout moment pendant l'utilisation
- sans symptômes précurseurs
- qui peut causer la mort
- antécédents d'ulcères de l'estomac ou de saignements de l'estomac ou de l'intestin avec l'utilisation d'AINS
- prendre des médicaments appelés « corticostéroïdes », « anticoagulants », « ISRS » ou « SNRI »
- augmentation des doses d'AINS
- âge avancé
- utilisation plus longue des AINS
- mauvaise santé
- fumeur
- maladie hépatique avancée
- buvant de l'alcool
- problèmes de saignement
- exactement comme prescrit
- à la dose la plus faible possible pour votre traitement
- pour le temps le plus court nécessaire
Que sont les AINS ?
Les AINS sont utilisés pour traiter la douleur et les rougeurs, l'enflure et la chaleur (inflammation) causées par des conditions médicales telles que différents types d'arthrite, les crampes menstruelles et d'autres types de douleur à court terme.
Qui ne devrait pas prendre d'AINS ?
Ne prenez pas d'AINS :
- si vous avez eu une crise d'asthme, de l'urticaire ou une autre réaction allergique à l'aspirine ou à tout autre AINS.
- juste avant ou après un pontage coronarien.
Avant de prendre des AINS, informez votre fournisseur de soins de santé de toutes vos conditions médicales, y compris si vous :
- avez des problèmes de foie ou de rein
- avoir une pression artérielle élevée
- avoir de l'asthme
- êtes enceinte ou envisagez de devenir enceinte. Parlez à votre fournisseur de soins de santé si vous envisagez de prendre des AINS pendant la grossesse.
Vous ne devez pas prendre d'AINS après 29 semaines de grossesse.
- allaitez ou envisagez d'allaiter.
Informez votre fournisseur de soins de santé de tous les médicaments que vous prenez, y compris les médicaments sur ordonnance ou en vente libre, les vitamines ou les suppléments à base de plantes. Les AINS et certains autres médicaments peuvent interagir entre eux et provoquer des effets secondaires graves. Ne commencez pas à prendre un nouveau médicament sans en parler d'abord à votre fournisseur de soins de santé.
Quels sont les effets secondaires possibles des AINS ?
Les AINS peuvent provoquer des effets secondaires graves, notamment :
Voir "Quelles sont les informations les plus importantes que je devrais connaître sur les médicaments appelés anti-inflammatoires non stéroïdiens (AINS) ?"
- hypertension artérielle nouvelle ou aggravée
- insuffisance cardiaque
- problèmes de foie, y compris insuffisance hépatique
- problèmes rénaux, y compris insuffisance rénale
- faible taux de globules rouges (anémie)
- réactions cutanées potentiellement mortelles
- réactions allergiques potentiellement mortelles
- Les autres effets secondaires des AINS comprennent : douleurs à l'estomac, constipation, diarrhée, gaz, brûlures d'estomac, nausées, vomissements et étourdissements.
Obtenez immédiatement de l'aide d'urgence si vous présentez l'un des symptômes suivants :
- essoufflement ou difficulté à respirer
- douleur thoracique
- faiblesse dans une partie ou un côté de votre corps
- troubles de l'élocution
- gonflement du visage ou de la gorge
Arrêtez de prendre votre AINS et appelez immédiatement votre fournisseur de soins de santé si vous présentez l'un des symptômes suivants :
- nausée
- plus fatigué ou plus faible que d'habitude
- diarrhée
- démangeaison
- votre peau ou vos yeux sont jaunes
- indigestion ou douleur à l'estomac
- symptômes pseudo-grippaux
- Vomir du sang
- il y a du sang dans vos selles ou elles sont noires et collantes comme du goudron
- prise de poids inhabituelle
- éruption cutanée ou cloques avec fièvre
- gonflement des bras, des jambes, des mains et des pieds
Si vous prenez trop de votre AINS, appelez votre fournisseur de soins de santé ou obtenez une aide médicale immédiatement.
Ce ne sont pas tous les effets secondaires possibles des AINS. Pour plus d'informations, renseignez-vous auprès de votre professionnel de la santé ou de votre pharmacien sur les AINS. Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
Autres informations sur les AINS
- L'aspirine est un AINS, mais il n'augmente pas le risque de crise cardiaque. L'aspirine peut provoquer des saignements dans le cerveau, l'estomac et les intestins. L'aspirine peut également provoquer des ulcères dans l'estomac et les intestins.
- Certains AINS sont vendus à des doses plus faibles sans ordonnance (en vente libre). Parlez à votre fournisseur de soins de santé avant d'utiliser des AINS en vente libre pendant plus de 10 jours.
Informations générales sur l'utilisation sûre et efficace des AINS
Les médicaments sont parfois prescrits à des fins autres que celles énumérées dans un guide des médicaments. N'utilisez pas d'AINS pour une condition pour laquelle il n'a pas été prescrit. Ne donnez pas d'AINS à d'autres personnes, même si elles présentent les mêmes symptômes que vous. Cela peut leur nuire.
Si vous souhaitez plus d'informations sur les AINS, parlez-en à votre fournisseur de soins de santé. Vous pouvez demander à votre pharmacien ou à votre professionnel de la santé des informations sur les AINS destinées aux professionnels de la santé.
Ce guide de médication a été approuvé par la Food and Drug Administration des États-Unis.
