Traitement contre le cholestérol: Lipitor 10mg, 20mg, 40mg Atorvastatin Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
Qu'est-ce que Lipitor 40 mg et comment est-il utilisé ?
Lipitor 10 mg est un médicament délivré sur ordonnance utilisé pour réduire les taux sanguins de « mauvais » cholestérol (lipoprotéines de basse densité ou LDL), pour augmenter les taux de « bon » cholestérol (lipoprotéines de haute densité ou HDL) et pour réduire les triglycérides et pour traiter les symptômes de l'hypercholestérolémie (hyperlipidémie) et réduire le risque d'accident vasculaire cérébral, de crise cardiaque ou d'autres complications cardiaques. Lipitor 40 mg peut être utilisé seul ou avec d'autres médicaments.
Lipitor 10 mg appartient à une classe de médicaments appelés agents hypolipidémiants, statines, inhibiteurs de l'HMG-CoA réductase.
On ne sait pas si Lipitor 10 mg est sûr et efficace chez les enfants de moins de 10 ans.
Quels sont les effets secondaires possibles de Lipitor ?
Lipitor 10 mg peut provoquer des effets indésirables graves, notamment :
- douleur ou brûlure lorsque vous urinez,
- douleur dans le haut du ventre,
- la faiblesse,
- se sentir fatigué,
- perte d'appétit,
- urine foncée,
- jaunissement de la peau ou des yeux (jaunisse),
- peu ou pas d'urine,
- gonflement des pieds ou des chevilles, et
- essoufflement
Consultez immédiatement un médecin si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires les plus courants de Lipitor comprennent :
- douleur articulaire,
- nez encombré,
- mal de gorge,
- diarrhée, et
- douleur dans les bras ou les jambes
Dites au médecin si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas.
Ce ne sont pas tous les effets secondaires possibles de Lipitor. Pour plus d'informations, consultez votre médecin ou votre pharmacien.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
LA DESCRIPTION
LIPITOR est un hypolipémiant de synthèse. L'atorvastatine est un inhibiteur de la 3-hydroxy-3-méthylglutaryl-coenzyme A (HMG-CoA) réductase. Cette enzyme catalyse la conversion de HMG-CoA en mévalonate, une étape précoce et limitante de la biosynthèse du cholestérol.
L'atorvastatine calcique est [R-(R*, R*)]-2-(4-fluorophényl)-β, δ-dihydroxy-5-(1-méthyléthyl)-3-phényl-4-[(phénylamino)carbonyl]- Acide 1Hpyrrole-1-heptanoïque, sel de calcium (2:1) trihydraté. La formule empirique de l'atorvastatine calcique est (C33H34FN2O5)2Ca•3H2O et son poids moléculaire est de 1209,42. Sa formule structurale est :
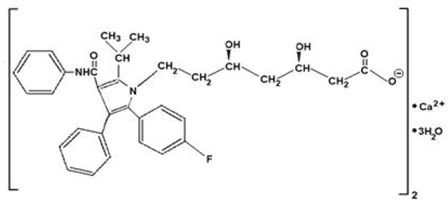
L'atorvastatine calcique est une poudre cristalline blanche à blanc cassé insoluble dans les solutions aqueuses de pH 4 et moins. L'atorvastatine calcique est très légèrement soluble dans l'eau distillée, le tampon phosphate pH 7,4 et l'acétonitrile; légèrement soluble dans l'éthanol; et librement soluble dans le méthanol.
Les comprimés LIPITOR pour administration orale contiennent 10, 20, 40 ou 80 mg d'atorvastatine et les ingrédients inactifs suivants : carbonate de calcium, USP; cire de candelilla,FCC; croscarmellose sodique, NF; hydroxypropylcellulose, NF; lactose monohydraté, NF; stéarate de magnésium, NF; cellulose microcristalline, NF; Opadry White YS-1-7040 (hypromellose, polyéthylène glycol, talc, dioxyde de titane); polysorbate 80, NF; émulsion de siméthicone.
LES INDICATIONS
La thérapie avec des agents altérant les lipides ne devrait être qu'un élément de l'intervention sur les facteurs de risque multiples chez les personnes présentant un risque significativement accru de maladie vasculaire athéroscléreuse due à l'hypercholestérolémie. Un traitement médicamenteux est recommandé en complément d'un régime alimentaire lorsque la réponse à un régime limité en graisses saturées et en cholestérol et à d'autres mesures non pharmacologiques seules a été inadéquate. Chez les patients atteints de coronaropathie ou présentant plusieurs facteurs de risque de coronaropathie, LIPITOR 20 mg peut être débuté en même temps qu'un régime alimentaire.
Prévention des maladies cardiovasculaires chez les adultes
Chez les patients adultes sans maladie coronarienne cliniquement évidente, mais présentant de multiples facteurs de risque de maladie coronarienne tels que l'âge, le tabagisme, l'hypertension, un faible taux de HDL-C ou des antécédents familiaux de maladie coronarienne précoce, LIPITOR 10 mg est indiqué pour :
- Réduire le risque d'infarctus du myocarde
- Réduire le risque d'AVC
- Réduire le risque de procédures de revascularisation et d'angine de poitrine
Chez les patients adultes atteints de diabète de type 2 et sans maladie coronarienne cliniquement évidente, mais présentant de multiples facteurs de risque de maladie coronarienne tels que la rétinopathie, l'albuminurie, le tabagisme ou l'hypertension, LIPITOR est indiqué pour :
- Réduire le risque d'infarctus du myocarde
- Réduire le risque d'AVC
Chez les patients adultes présentant une maladie coronarienne cliniquement évidente, LIPITOR 20 mg est indiqué pour :
- Réduire le risque d'infarctus du myocarde non mortel
- Réduire le risque d'AVC mortel et non mortel
- Réduire le risque de procédures de revascularisation
- Réduire le risque d'hospitalisation pour CHF
- Réduire le risque d'angine
Hyperlipidémie
LIPITOR 20mg est indiqué :
- En complément d'un régime alimentaire pour réduire les taux élevés de C total, de LDL-C, d'apo B et de TG et pour augmenter le HDL-C chez les patients adultes atteints d'hypercholestérolémie primaire (hétérozygote familiale et non familiale) et de dyslipidémie mixte (types IIa et IIb de Fredrickson) ;
- En complément d'un régime alimentaire pour le traitement de patients adultes présentant des taux sériques élevés de TG (Fredrickson Type IV);
- Pour le traitement des patients adultes atteints de dysbêtalipoprotéinémie primaire (Fredrickson Type III) qui ne répondent pas de manière adéquate au régime ;
- Pour réduire le C total et le LDL-C chez les patients atteints d'hypercholestérolémie familiale homozygote (HoFH) en complément d'autres traitements hypolipémiants (par exemple, aphérèse des LDL) ou si ces traitements ne sont pas disponibles ;
- En complément d'un régime alimentaire pour réduire les taux de C total, de LDL-C et d'apo B chez les patients pédiatriques, âgés de 10 à 17 ans, atteints d'hypercholestérolémie familiale hétérozygote (HeFH) si, après un essai adéquat de thérapie diététique, les résultats suivants sont cadeau:
- il y a des antécédents familiaux positifs de maladie cardiovasculaire prématurée ou
- deux ou plusieurs autres facteurs de risque de MCV sont présents chez le patient pédiatrique
Limites d'utilisation
LIPITOR 40 mg n'a pas été étudié dans des conditions où l'anomalie lipoprotéique majeure est l'élévation des chylomicrons (Fredrickson Types I et V).
DOSAGE ET ADMINISTRATION
Hyperlipidémie et dyslipidémie mixte
La dose initiale recommandée de LIPITOR 10 mg est de 10 ou 20 mg une fois par jour. Les patients qui ont besoin d'une réduction importante du LDL-C (plus de 45 %) peuvent commencer à 40 mg une fois par jour. La gamme posologique de LIPITOR est de 10 à 80 mg une fois par jour. LIPITOR 10 mg peut être administré en une seule prise à tout moment de la journée, avec ou sans nourriture. La dose initiale et les doses d'entretien de LIPITOR doivent être individualisées en fonction des caractéristiques du patient telles que l'objectif du traitement et la réponse. Après initiation et/ou titration de LIPITOR 10 mg, les taux de lipides doivent être analysés dans les 2 à 4 semaines et la posologie ajustée en conséquence.
Hypercholestérolémie familiale hétérozygote chez les patients pédiatriques (âgés de 10 à 17 ans)
La dose initiale recommandée de LIPITOR 10 mg est de 10 mg/jour ; la gamme de doses habituelles est de 10 à 20 mg par voie orale une fois par jour [voir Etudes cliniques ]. Les doses doivent être individualisées en fonction de l'objectif thérapeutique recommandé [voir INDICATIONS ET USAGE et PHARMACOLOGIE CLINIQUE ]. Les ajustements doivent être effectués à des intervalles de 4 semaines ou plus.
Hypercholestérolémie familiale homozygote
La posologie de LIPITOR 20 mg chez les patients atteints d'HFHo est de 10 à 80 mg par jour. LIPITOR 20 mg doit être utilisé en complément d'autres traitements hypolipidémiants (par exemple aphérèse des LDL) chez ces patients ou si ces traitements ne sont pas disponibles.
Thérapie hypolipémiante concomitante
LIPITOR 20 mg peut être utilisé avec des résines d'acides biliaires. L'association d'inhibiteurs de l'HMG-CoA réductase (statines) et de fibrates doit généralement être utilisée avec prudence [voir AVERTISSEMENTS ET PRECAUTIONS et INTERACTIONS MÉDICAMENTEUSES ].
Posologie chez les patients atteints d'insuffisance rénale
La maladie rénale n'affecte pas les concentrations plasmatiques ni la réduction du LDL-C de LIPITOR ; ainsi, l'adaptation de la posologie chez les patients atteints d'insuffisance rénale n'est pas nécessaire [voir AVERTISSEMENTS ET PRECAUTIONS et PHARMACOLOGIE CLINIQUE ].
Posologie chez les patients prenant de la cyclosporine, de la clarithromycine, de l'itraconazole, du letermovir ou certains inhibiteurs de la protéase
Chez les patients prenant de la cyclosporine ou l'inhibiteur de la protéase du VIH tipranavir plus ritonavir ou l'inhibiteur de la protéase du virus de l'hépatite C (VHC) glécaprévir plus pibrentasvir ou letermovir lorsqu'il est co-administré avec la cyclosporine, le traitement par LIPITOR 40 mg doit être évité. Chez les patients séropositifs prenant du lopinavir plus du ritonavir, utilisez la dose la plus faible nécessaire de LIPITOR. Chez les patients prenant de la clarithromycine, de l'itraconazole, de l'elbasvir plus du grazoprévir, ou chez les patients séropositifs prenant une association de saquinavir plus ritonavir, darunavir plus ritonavir, fosamprénavir, fosamprénavir plus ritonavir ou letermovir, le traitement avec LIPITOR doit être limité à 20 mg, et une évaluation clinique appropriée est nécessaire. recommandé de s'assurer que la dose la plus faible nécessaire de LIPITOR 20 mg est utilisée. Chez les patients prenant l'inhibiteur de la protéase du VIH, le traitement par nelfinavir avec LIPITOR 10 mg doit être limité à 40 mg [voir AVERTISSEMENTS ET PRECAUTIONS et INTERACTIONS MÉDICAMENTEUSES ].
COMMENT FOURNIE
Formes posologiques et points forts
Les comprimés LIPITOR sont blancs, elliptiques, pelliculés et sont disponibles en quatre dosages (voir tableau 1).
Stockage et manutention
Comprimés de 10 mg (10 mg d'atorvastatine) : codé « PD 155 » d'un côté et « 10 » de l'autre.
CDN 0071-0155-23 bouteilles de 90 CDN 0071-0155-40 10 x 10 plaquettes thermoformées
Comprimés de 20 mg (20 mg d'atorvastatine) : codé « PD 156 » d'un côté et « 20 » de l'autre.
CDN 0071-0156-23 bouteilles de 90 CDN 0071-0156-40 10 x 10 plaquettes thermoformées
Comprimés de 40 mg (40 mg d'atorvastatine) : codé « PD 157 » d'un côté et « 40 » de l'autre.
CDN 0071-0157-23 bouteilles de 90 CDN 0071-0157-40 10 x 10 plaquettes thermoformées
Comprimés de 80 mg (80 mg d'atorvastatine) : codé « PD 158 » d'un côté et « 80 » de l'autre.
CDN 0071-0158-23 bouteilles de 90 CDN 0071-0158-73 bouteilles de 500 CDN 0071-0158-92 8 x 8 plaquettes thermoformées
Stockage
Le magasin à la température de pièce contrôlée 20 – 25°C (68 – 77°F) [voit USP].
Distribué par : Parke-Davis, Division of Pfizer Inc., NY, NY 10017. Révisé : août 2021
EFFETS SECONDAIRES
Les effets indésirables graves suivants sont discutés plus en détail dans d'autres sections de l'étiquette :
- Myopathie et rhabdomyolyse [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Anomalies des enzymes hépatiques [voir AVERTISSEMENTS ET PRECAUTIONS ]
Expérience des essais cliniques
Étant donné que les essais cliniques sont menés dans des conditions très variables, les taux d'effets indésirables observés dans les essais cliniques d'un médicament ne peuvent pas être directement comparés aux taux des essais cliniques d'un autre médicament et peuvent ne pas refléter les taux observés dans la pratique.
Dans la base de données des essais cliniques contrôlés par placebo LIPITOR de 16 066 patients (8755 LIPITOR contre 7311 placebo ; tranche d'âge 10-93 ans, 39 % de femmes, 91 % de Caucasiens, 3 % de Noirs, 2 % d'Asiatiques, 4 % d'autres) avec une médiane durée de traitement de 53 semaines, 9,7 % des patients sous LIPITOR 10 mg et 9,5 % des patients sous placebo ont arrêté en raison d'effets indésirables quelle qu'en soit la cause. Les cinq effets indésirables les plus fréquents chez les patients traités par LIPITOR 20 mg ayant conduit à l'arrêt du traitement et survenus à une fréquence supérieure à celle du placebo ont été : myalgies (0,7 %), diarrhées (0,5 %), nausées (0,4 %), augmentation de l'alanine aminotransférase (0,4 %), et augmentation des enzymes hépatiques (0,4 %).
Les effets indésirables les plus fréquemment rapportés (incidence ≥ 2 % et supérieure au placebo) quelle qu'en soit la cause, chez les patients traités par LIPITOR dans les essais contrôlés par placebo (n = 8755) étaient : rhinopharyngite (8,3 %), arthralgie (6,9 %), diarrhée ( 6,8 %), des douleurs aux extrémités (6,0 %) et des infections des voies urinaires (5,7 %).
Le tableau 2 résume la fréquence des effets indésirables cliniques, quelle qu'en soit la cause, signalés chez ≥ 2 % et à un taux supérieur au placebo chez les patients traités par LIPITOR (n = 8 755), issus de dix-sept essais contrôlés par placebo.
Les autres effets indésirables signalés dans les études contrôlées par placebo comprennent :
Corps dans son ensemble : malaise, pyrexie; Système digestif: gêne abdominale, éructation, flatulence, hépatite, cholestase; Système musculo-squelettique: douleurs musculo-squelettiques, fatigue musculaire, douleurs cervicales, gonflement des articulations ; Système métabolique et nutritionnel : augmentation des transaminases, test de la fonction hépatique anormal, augmentation des phosphatases alcalines sanguines, augmentation de la créatine phosphokinase, hyperglycémie ; Système nerveux: cauchemar; Système respiratoire: épistaxis; Peau et phanères : urticaire; Sens particuliers : vision floue, acouphènes ; Système urogénital : globules blancs urine positive.
Essai anglo-scandinave sur les résultats cardiaques (ASCOT)
Dans ASCOT [voir Etudes cliniques impliquant 10 305 participants (tranche d'âge 40-80 ans, 19 % de femmes ; 94,6 % de Caucasiens, 2,6 % d'Africains, 1,5 % de Sud-Asiatiques, 1,3 % mixte/autre) traités par LIPITOR 10 mg par jour (n = 5 168) ou un placebo (n =5 137), le profil de sécurité et de tolérance du groupe traité par LIPITOR 10 mg a été comparable à celui du groupe traité par placebo pendant un suivi médian de 3,3 ans.
Étude collaborative sur le diabète de l'atorvastatine (CARDS)
Dans CARTES [voir Etudes cliniques ] portant sur 2 838 sujets (tranche d'âge 39-77 ans, 32 % de femmes ; 94,3 % de Caucasiens, 2,4 % de Sud-Asiatiques, 2,3 % d'Afro-Caraïbes, 1,0 % d'autres) atteints de diabète de type 2 et traités par LIPITOR 10 mg par jour (n = 1 428) ou placebo (n = 1 410), il n'y avait pas de différence dans la fréquence globale des effets indésirables ou des effets indésirables graves entre les groupes de traitement au cours d'un suivi médian de 3,9 ans. Aucun cas de rhabdomyolyse n'a été rapporté.
Étude sur le traitement de nouvelles cibles (TNT)
En TNT [voir Etudes cliniques impliquant 10 001 sujets (tranche d'âge 29-78 ans, 19 % de femmes ; 94,1 % de Caucasiens, 2,9 % de Noirs, 1,0 % d'Asiatiques, 2,0 % d'autres) atteints de coronaropathie cliniquement évidente traités par LIPITOR 10 mg par jour (n = 5 006) ou LIPITOR 80 mg par jour (n = 4995), il y a eu plus d'effets indésirables graves et d'abandons dus à des effets indésirables dans le groupe à forte dose d'atorvastatine (92, 1,8 % ; 497, 9,9 %, respectivement) par rapport au groupe à faible dose (69 , 1,4 % ; 404, 8,1 %, respectivement) au cours d'un suivi médian de 4,9 ans. Des élévations persistantes des transaminases (≥ 3 x LSN deux fois en 4 à 10 jours) sont survenues chez 62 (1,3 %) personnes sous atorvastatine 80 mg et chez neuf (0,2 %) personnes sous atorvastatine 10 mg. Les élévations de CK (≥ 10 x LSN) étaient faibles dans l'ensemble, mais étaient plus élevées dans le groupe de traitement à forte dose d'atorvastatine (13, 0,3 %) par rapport au groupe à faible dose d'atorvastatine (6, 0,1 %).
Diminution progressive des critères d'évaluation grâce à une étude de réduction lipidique agressive (IDEAL)
Dans IDEAL [voir Etudes cliniques impliquant 8 888 sujets (tranche d'âge 26-80 ans, 19 % de femmes ; 99,3 % de Caucasiens, 0,4 % d'Asiatiques, 0,3 % de Noirs, 0,04 % d'autres) traités par LIPITOR 80 mg/jour (n = 4 439) ou simvastatine 20-40 mg quotidiennement (n = 4449), il n'y avait pas de différence dans la fréquence globale des effets indésirables ou des effets indésirables graves entre les groupes de traitement au cours d'un suivi médian de 4,8 ans.
Prévention des accidents vasculaires cérébraux par réduction agressive des niveaux de cholestérol (SPARCL)
Dans SPARCL impliquant 4731 sujets (tranche d'âge 21-92 ans, 40 % de femmes ; 93,3 % de Caucasiens, 3,0 % de Noirs, 0,6 % d'Asiatiques, 3,1 % d'autres) sans maladie coronarienne cliniquement évidente mais avec un accident vasculaire cérébral ou un accident ischémique transitoire (AIT) dans la 6 mois précédents traités par LIPITOR 80 mg (n = 2365) ou un placebo (n = 2366) pendant un suivi médian de 4,9 ans, il y avait une incidence plus élevée d'élévations persistantes des transaminases hépatiques (≥ 3 x LSN deux fois en 4-10 jours) dans le groupe atorvastatine (0,9 %) par rapport au placebo (0,1 %). Les élévations de CK (> 10 x LSN) étaient rares, mais étaient plus élevées dans le groupe atorvastatine (0,1 %) par rapport au placebo (0,0 %). Le diabète a été rapporté comme effet indésirable chez 144 sujets (6,1 %) dans le groupe atorvastatine et 89 sujets (3,8 %) dans le groupe placebo [voir AVERTISSEMENTS ET PRECAUTIONS ].
Dans une analyse post-hoc, LIPITOR 80 mg a réduit l'incidence des AVC ischémiques (218/2365, 9,2 % vs 274/2366, 11,6 %) et augmenté l'incidence des AVC hémorragiques (55/2365, 2,3 % vs 33/ 2366, 1,4 %) par rapport au placebo. L'incidence des AVC hémorragiques mortels était similaire entre les groupes (17 LIPITOR 40 mg vs 18 placebo). L'incidence des AVC hémorragiques non mortels était significativement plus élevée dans le groupe atorvastatine (38 AVC hémorragiques non mortels) que dans le groupe placebo (16 AVC hémorragiques non mortels). Les sujets qui sont entrés dans l'étude avec un AVC hémorragique semblaient présenter un risque accru d'AVC hémorragique [7 (16 %) LIPITOR vs 2 (4 %) placebo].
Il n'y a pas eu de différence significative entre les groupes de traitement pour la mortalité toutes causes : 216 (9,1%) dans le groupe LIPITOR 80 mg/j vs 211 (8,9%) dans le groupe placebo. Les proportions de sujets ayant subi un décès cardiovasculaire étaient numériquement plus faibles dans le groupe LIPITOR 80 mg (3,3 %) que dans le groupe placebo (4,1 %). Les proportions de sujets ayant subi un décès non cardiovasculaire étaient numériquement plus importantes dans le groupe LIPITOR 80 mg (5,0 %) que dans le groupe placebo (4,0 %).
Effets indésirables des études cliniques de LIPITOR 20 mg chez les patients pédiatriques
Dans une étude contrôlée de 26 semaines chez des garçons et des filles postménarchiques atteints d'HFHe (âgés de 10 à 17 ans) (n = 140, 31 % de femmes ; 92 % de Caucasiens, 1,6 % de Noirs, 1,6 % d'Asiatiques, 4,8 % d'autres), l'innocuité et le profil de tolérance de LIPITOR 10 à 20 mg par jour, en complément d'un régime alimentaire pour réduire les taux de cholestérol total, de LDL-C et d'apo B, était généralement similaire à celui du placebo [voir Utilisation dans des populations particulières et Etudes cliniques ].
Expérience post-commercialisation
Les effets indésirables suivants ont été identifiés lors de l'utilisation post-approbation de LIPITOR. Étant donné que ces réactions sont signalées volontairement par une population de taille incertaine, il n'est pas toujours possible d'estimer de manière fiable leur fréquence ou d'établir une relation causale avec l'exposition au médicament.
Les effets indésirables associés au traitement par LIPITOR signalés depuis l'introduction sur le marché, qui ne sont pas énumérés ci-dessus, quelle que soit l'évaluation de la causalité, comprennent les suivants : anaphylaxie, œdème de Quincke, éruptions cutanées bulleuses (y compris érythème polymorphe, syndrome de Stevens-Johnson et nécrolyse épidermique toxique), rhabdomyolyse , myosite, fatigue, rupture de tendon, insuffisance hépatique mortelle et non mortelle, étourdissements, dépression, neuropathie périphérique, pancréatite et maladie pulmonaire interstitielle.
De rares cas de myopathie nécrosante à médiation immunitaire associés à l'utilisation de statines ont été signalés [voir AVERTISSEMENTS ET PRECAUTIONS ].
Il y a eu de rares rapports post-commercialisation de troubles cognitifs (par exemple, perte de mémoire, oubli, amnésie, troubles de la mémoire, confusion) associés à l'utilisation de statines. Ces problèmes cognitifs ont été signalés pour toutes les statines. Les rapports sont généralement non graves et réversibles à l'arrêt des statines, avec des délais variables d'apparition des symptômes (1 jour à plusieurs années) et de résolution des symptômes (médiane de 3 semaines).
INTERACTIONS MÉDICAMENTEUSES
Interactions médicamenteuses pouvant augmenter le risque de myopathie et de rhabdomyolyse avec LIPITOR
LIPITOR est un substrat du CYP3A4 et des transporteurs (p. ex. OATP1B1/1B3, P-gp ou BCRP). Les concentrations plasmatiques de LIPITOR peuvent être significativement augmentées lors de l'administration concomitante d'inhibiteurs du CYP3A4 et de transporteurs. Le tableau 3 comprend une liste de médicaments qui peuvent augmenter l'exposition à Lipitor et peuvent augmenter le risque de myopathie et de rhabdomyolyse lorsqu'ils sont utilisés de façon concomitante et des instructions pour les prévenir ou les gérer [voir AVERTISSEMENTS ET PRECAUTIONS et PHARMACOLOGIE CLINIQUE ].
Interactions médicamenteuses susceptibles de réduire l'exposition à LIPITOR
Le tableau 4 présente les interactions médicamenteuses susceptibles de diminuer l'exposition à LIPITOR 20 mg et les instructions pour les prévenir ou les gérer.
LIPITOR 20mg Effets sur d'autres médicaments
Le tableau 5 présente l'effet de LIPITOR sur d'autres médicaments et les instructions pour les prévenir ou les gérer.
AVERTISSEMENTS
Inclus dans le cadre du PRÉCAUTIONS section.
PRÉCAUTIONS
Myopathie et rhabdomyolyse
LIPITOR 10 mg peut provoquer une myopathie (douleur musculaire, sensibilité ou faiblesse avec une créatine kinase (CK) supérieure à dix fois la limite supérieure de la normale) et une rhabdomyolyse (avec ou sans insuffisance rénale aiguë secondaire à une myoglobinurie). De rares décès sont survenus à la suite d'une rhabdomyolyse avec l'utilisation de statines, y compris LIPITOR.
Facteurs de risque de myopathie
Les facteurs de risque de myopathie comprennent l'âge de 65 ans ou plus, une hypothyroïdie non contrôlée, une insuffisance rénale, l'utilisation concomitante de certains autres médicaments et une posologie plus élevée de LIPITOR [voir INTERACTIONS MÉDICAMENTEUSES ].
Étapes pour prévenir ou réduire le risque de myopathie et de rhabdomyolyse
L'exposition à LIPITOR peut être augmentée par des interactions médicamenteuses dues à l'inhibition de l'enzyme 3A4 du cytochrome P450 (CYP3A4) et/ou de transporteurs (p. -gp]), entraînant un risque accru de myopathie et de rhabdomyolyse. L'utilisation concomitante de cyclosporine, de gemfibrozil, de tipranavir plus ritonavir ou de glecaprevir plus pibrentasvir avec LIPITOR n'est pas recommandée. Des modifications posologiques de LIPITOR 40 mg sont recommandées pour les patients prenant certains antiviraux, antifongiques azolés ou antibiotiques macrolides [voir DOSAGE ET ADMINISTRATION ]. Des cas de myopathie/rhabdomyolyse ont été rapportés avec l'atorvastatine co-administrée avec des doses modificatrices des lipides (> 1 gramme/jour) de niacine, de fibrates, de colchicine et de lédipasvir plus sofosbuvir. Considérez si le bénéfice de l'utilisation de ces produits l'emporte sur le risque accru de myopathie et de rhabdomyolyse [voir INTERACTIONS MÉDICAMENTEUSES ].
La prise concomitante de grandes quantités, plus de 1,2 litre par jour, de jus de pamplemousse n'est pas recommandée chez les patients prenant LIPITOR [voir INTERACTIONS MÉDICAMENTEUSES ].
Arrêtez LIPITOR en cas d'élévation marquée des taux de CK ou si une myopathie est diagnostiquée ou suspectée. Les symptômes musculaires et les augmentations de CK peuvent disparaître si LIPITOR est arrêté. Arrêter temporairement LIPITOR 40 mg chez les patients présentant une affection aiguë ou grave à haut risque de développer une insuffisance rénale secondaire à une rhabdomyolyse (par exemple, septicémie ; choc ; hypovolémie sévère ; chirurgie majeure ; traumatisme ; troubles métaboliques, endocriniens ou électrolytiques sévères ; ou épilepsie non contrôlée) .
Informer les patients du risque de myopathie et de rhabdomyolyse lors de l'instauration ou de l'augmentation de la posologie de LIPITOR. Demandez aux patients de signaler rapidement toute douleur, sensibilité ou faiblesse musculaire inexpliquée, en particulier si elle est accompagnée de malaise ou de fièvre.
Myopathie nécrosante à médiation immunitaire
De rares cas de myopathie nécrosante à médiation immunitaire (IMNM), une myopathie auto-immune, associée à l'utilisation de statines ont été signalés. L'IMNM se caractérise par : une faiblesse musculaire proximale et une élévation de la créatine kinase sérique, qui persistent malgré l'arrêt du traitement par statine ; anticorps anti-HMG CoA réductase positif; biopsie musculaire montrant une myopathie nécrosante ; et amélioration avec des agents immunosuppresseurs. Des tests neuromusculaires et sérologiques supplémentaires peuvent être nécessaires. Un traitement avec des agents immunosuppresseurs peut être nécessaire. Envisagez attentivement le risque d'IMNM avant d'initier une autre statine. Si le traitement est initié avec une statine différente, surveiller les signes et symptômes de l'IMNM.
Dysfonctionnement du foie
Les statines, comme certaines autres thérapies hypolipidémiantes, ont été associées à des anomalies biochimiques de la fonction hépatique. Des élévations persistantes (> 3 fois la limite supérieure de la normale [LSN] survenant à 2 reprises ou plus) des transaminases sériques sont survenues chez 0,7 % des patients ayant reçu LIPITOR dans les essais cliniques. L'incidence de ces anomalies était de 0,2 %, 0,2 %, 0,6 % et 2,3 % pour 10, 20, 40 et 80 mg, respectivement.
Un patient dans les essais cliniques a développé un ictère. L'augmentation des tests de la fonction hépatique (LFT) chez d'autres patients n'a pas été associée à un ictère ou à d'autres signes ou symptômes cliniques. Lors de la réduction de la dose, de l'interruption ou de l'arrêt du traitement, les taux de transaminases sont revenus aux niveaux de prétraitement ou s'en sont approchés sans séquelles. Dix-huit des 30 patients présentant des élévations persistantes du LFT ont poursuivi le traitement avec une dose réduite de LIPITOR.
Il est recommandé d'effectuer des tests d'enzymes hépatiques avant d'initier le traitement par LIPITOR 40 mg et de les répéter selon les indications cliniques. De rares cas d'insuffisance hépatique mortelle et non mortelle ont été signalés après commercialisation chez des patients prenant des statines, y compris l'atorvastatine. Si une atteinte hépatique grave accompagnée de symptômes cliniques et/ou d'hyperbilirubinémie ou d'ictère survient pendant le traitement par LIPITOR 10 mg, interrompez rapidement le traitement. Si une étiologie alternative n'est pas trouvée, ne pas redémarrer LIPITOR.
LIPITOR 10 mg doit être utilisé avec prudence chez les patients qui consomment des quantités importantes d'alcool et/ou qui ont des antécédents de maladie du foie. Une maladie hépatique active ou des élévations persistantes inexpliquées des transaminases sont des contre-indications à l'utilisation de LIPITOR [voir CONTRE-INDICATIONS ].
Fonction endocrinienne
Des augmentations de l'HbA1c et de la glycémie à jeun ont été rapportées avec les inhibiteurs de l'HMG-CoA réductase, y compris LIPITOR.
Les statines interfèrent avec la synthèse du cholestérol et pourraient théoriquement atténuer la production de stéroïdes surrénaliens et/ou gonadiques. Des études cliniques ont montré que LIPITOR 20 mg ne réduit pas la concentration basale de cortisol plasmatique ni n'altère la réserve surrénalienne. Les effets des statines sur la fertilité masculine n'ont pas été étudiés chez un nombre suffisant de patients. Les effets, s'il y en a, sur l'axe hypophyso-gonadique chez les femmes préménopausées sont inconnus. La prudence s'impose si une statine est administrée en même temps que des médicaments susceptibles de diminuer les niveaux ou l'activité des hormones stéroïdes endogènes, tels que le kétoconazole, la spironolactone et la cimétidine.
Toxicité du SNC
Une hémorragie cérébrale a été observée chez une chienne traitée pendant 3 mois à 120 mg/kg/jour. Une hémorragie cérébrale et une vacuolisation du nerf optique ont été observées chez une autre chienne qui a été sacrifiée dans un état moribond après 11 semaines de doses croissantes jusqu'à 280 mg/kg/jour. La dose de 120 mg/kg a entraîné une exposition systémique d'environ 16 fois l'aire sous la courbe du plasma humain (ASC, 0 à 24 heures) sur la base de la dose humaine maximale de 80 mg/jour. Une seule convulsion tonique a été observée chez chacun des 2 chiens mâles (un traité à 10 mg/kg/jour et un à 120 mg/kg/jour) dans une étude de 2 ans. Aucune lésion du SNC n'a été observée chez la souris après un traitement chronique jusqu'à 2 ans à des doses allant jusqu'à 400 mg/kg/jour ou chez le rat à des doses allant jusqu'à 100 mg/kg/jour. Ces doses étaient de 6 à 11 fois (souris) et de 8 à 16 fois (rat) l'ASC humaine (0–24) sur la base de la dose humaine maximale recommandée de 80 mg/jour.
Des lésions vasculaires du SNC, caractérisées par des hémorragies périvasculaires, un œdème et une infiltration de cellules mononucléaires dans les espaces périvasculaires, ont été observées chez des chiens traités avec d'autres membres de cette classe. Un médicament chimiquement similaire de cette classe a produit une dégénérescence du nerf optique (dégénérescence wallérienne des fibres rétinogéniques) chez des chiens cliniquement normaux de manière dose-dépendante à une dose qui a produit des taux plasmatiques de médicament environ 30 fois plus élevés que le taux moyen de médicament chez les humains prenant le médicament le plus élevé. posologie recommandée.
Utilisation chez les patients ayant récemment subi un AVC ou un AIT
Dans une analyse post-hoc de l'étude SPARCL (Stroke Prevention by Aggressive Reduction in Cholesterol Levels) dans laquelle LIPITOR 80 mg versus placebo a été administré à 4 731 sujets sans coronaropathie ayant subi un accident vasculaire cérébral ou un AIT au cours des 6 mois précédents, une incidence plus élevée de un AVC hémorragique a été observé dans le groupe LIPITOR 80 mg par rapport au groupe placebo (55, 2,3 % atorvastatine vs 33, 1,4 % placebo ; HR : 1,68, IC 95 % : 1,09, 2,59 ; p = 0,0168). L'incidence des accidents vasculaires cérébraux hémorragiques mortels était similaire dans tous les groupes de traitement (17 contre 18 pour les groupes atorvastatine et placebo, respectivement). L'incidence des AVC hémorragiques non mortels était significativement plus élevée dans le groupe atorvastatine (38, 1,6 %) que dans le groupe placebo (16, 0,7 %).
Certaines caractéristiques initiales, y compris les AVC hémorragiques et lacunaires à l'entrée dans l'étude, ont été associées à une incidence plus élevée d'AVC hémorragiques dans le groupe atorvastatine [voir EFFETS INDÉSIRABLES ].
Informations sur les conseils aux patients
Conseillez au patient de lire l'étiquetage patient approuvé par la FDA ( INFORMATIONS PATIENTS ).
Les patients prenant LIPITOR 10 mg doivent être informés que le cholestérol est une maladie chronique et qu'ils doivent respecter leurs médicaments ainsi que le régime alimentaire recommandé par le programme national d'éducation sur le cholestérol (NCEP), un programme d'exercice régulier, le cas échéant, et des tests périodiques d'un panel de lipides à jeun pour déterminer l'atteinte des objectifs.
Les patients doivent être informés des substances qu'ils ne doivent pas prendre en concomitance avec l'atorvastatine [voir MISES EN GARDE ET PRÉCAUTIONS]. Il faut également conseiller aux patients d'informer les autres professionnels de santé prescrivant un nouveau médicament qu'ils prennent LIPITOR.
Douleur musculaire
Tous les patients débutant un traitement par LIPITOR doivent être informés du risque de myopathie et doivent signaler rapidement toute douleur, sensibilité ou faiblesse musculaire inexpliquée, en particulier si elles s'accompagnent de malaises ou de fièvre ou si ces signes ou symptômes musculaires persistent après l'arrêt de LIPITOR. Le risque que cela se produise est accru lors de la prise de certains types de médicaments ou de la consommation de plus grandes quantités (> 1 litre) de jus de pamplemousse. Ils devraient discuter de tous les médicaments, qu'ils soient sur ordonnance ou en vente libre, avec leur professionnel de la santé.
Des enzymes hépatiques
Il est recommandé d'effectuer des tests d'enzymes hépatiques avant l'initiation de LIPITOR 40 mg et si des signes ou symptômes d'atteinte hépatique apparaissent. Tous les patients traités par LIPITOR doivent être avisés de signaler rapidement tout symptôme pouvant indiquer une atteinte hépatique, notamment fatigue, anorexie, gêne abdominale supérieure droite, urine foncée ou jaunisse.
Toxicité embryofœtale
Conseiller aux femmes en âge de procréer du risque pour le fœtus, d'utiliser une contraception efficace pendant le traitement et d'informer leur professionnel de la santé d'une grossesse connue ou suspectée [voir CONTRE-INDICATIONS et Utilisation dans des populations spécifiques ].
Lactation
Déconseiller aux femmes d'allaiter pendant le traitement par LIPITOR [voir CONTRE-INDICATIONS et Utilisation dans des populations spécifiques ].
L'étiquetage de ce produit a peut-être été mis à jour. Pour les informations de prescription les plus récentes, veuillez visiter www.pfizer.com.
Toxicologie non clinique
Carcinogenèse, mutagenèse, altération de la fertilité
Dans une étude de cancérogénicité de 2 ans chez le rat à des doses de 10, 30 et 100 mg/kg/jour, 2 tumeurs rares ont été trouvées dans le muscle chez les femelles à forte dose : dans l'une, il y avait un rhabdomyosarcome et, dans une autre, il y avait un fibrosarcome. Cette dose représente une valeur plasmatique de l'ASC (0 à 24) d'environ 16 fois l'exposition plasmatique humaine moyenne au médicament après une dose orale de 80 mg.
Une étude de cancérogénicité de 2 ans chez des souris ayant reçu 100, 200 ou 400 mg/kg/jour a entraîné une augmentation significative des adénomes hépatiques chez les mâles à forte dose et des carcinomes du foie chez les femelles à forte dose. Ces résultats se sont produits à des valeurs plasmatiques d'ASC (0 à 24) d'environ 6 fois l'exposition plasmatique humaine moyenne au médicament après une dose orale de 80 mg.
In vitro, l'atorvastatine n'a pas été mutagène ou clastogène dans les tests suivants avec et sans activation métabolique : le test d'Ames avec Salmonella typhimurium et Escherichia coli, le test de mutation directe HGPRT dans des cellules pulmonaires de hamster chinois et le test d'aberration chromosomique dans des cellules pulmonaires de hamster chinois. . L'atorvastatine s'est avérée négative dans le test in vivo du micronoyau chez la souris.
Chez les rats femelles, l'atorvastatine à des doses allant jusqu'à 225 mg/kg (56 fois l'exposition humaine) n'a pas provoqué d'effets indésirables sur la fertilité. Des études chez des rats mâles réalisées à des doses allant jusqu'à 175 mg/kg (15 fois l'exposition humaine) n'ont produit aucune modification de la fertilité. Il y avait une aplasie et une aspermie dans l'épididyme de 2 des 10 rats traités avec 100 mg/kg/jour d'atorvastatine pendant 3 mois (16 fois l'ASC humaine à la dose de 80 mg); le poids des testicules était significativement inférieur à 30 et 100 mg/kg et le poids de l'épididyme était inférieur à 100 mg/kg. Des rats mâles ayant reçu 100 mg/kg/jour pendant 11 semaines avant l'accouplement ont présenté une diminution de la motilité des spermatozoïdes, une concentration de la tête des spermatides et une augmentation des spermatozoïdes anormaux. L'atorvastatine n'a provoqué aucun effet indésirable sur les paramètres du sperme ou sur l'histopathologie des organes reproducteurs chez des chiens ayant reçu des doses de 10, 40 ou 120 mg/kg pendant deux ans.
Utilisation dans des populations spécifiques
Grossesse
Résumé des risques
LIPITOR 10 mg est contre-indiqué chez la femme enceinte car la sécurité chez la femme enceinte n'a pas été établie et il n'y a aucun bénéfice apparent des médicaments hypolipidémiants pendant la grossesse. Étant donné que les inhibiteurs de l'HMG-CoA réductase diminuent la synthèse du cholestérol et éventuellement la synthèse d'autres substances biologiquement actives dérivées du cholestérol, LIPITOR peut être nocif pour le fœtus lorsqu'il est administré à une femme enceinte. LIPITOR 40 mg doit être arrêté dès qu'une grossesse est reconnue [voir CONTRE-INDICATIONS ]. Les données limitées publiées sur l'utilisation de l'atorvastatine sont insuffisantes pour déterminer un risque associé au médicament de malformations congénitales majeures ou de fausse couche. Dans les études de reproduction chez l'animal chez le rat et le lapin, il n'y a eu aucun signe de toxicité embryo-fœtale ou de malformations congénitales à des doses allant jusqu'à 30 et 20 fois, respectivement, l'exposition humaine à la dose humaine maximale recommandée (MRHD) de 80 mg, basée sur le corps. surface (mg/m ). Chez les rats ayant reçu de l'atorvastatine pendant la gestation et la lactation, une diminution de la croissance et du développement postnatals a été observée à des doses ≥ 6 fois la MRHD (voir Données ).
Le risque de fond estimé de malformations congénitales majeures et de fausse couche pour la population indiquée est inconnu. Dans la population générale des États-Unis, le risque de fond estimé de malformations congénitales majeures et de fausse couche dans les grossesses cliniquement reconnues est de 2 à 4 % et de 15 à 20 %, respectivement.
Données
Données humaines
Des données limitées publiées sur l'atorvastatine calcique provenant d'études observationnelles, de méta-analyses et de rapports de cas n'ont pas montré de risque accru de malformations congénitales majeures ou de fausse couche. De rares cas d'anomalies congénitales ont été signalés à la suite d'une exposition intra-utérine à d'autres inhibiteurs de l'HMGCoA réductase. Dans une revue d'environ 100 grossesses suivies de manière prospective chez des femmes exposées à la simvastatine ou à la lovastatine, l'incidence des anomalies congénitales, des avortements spontanés et des morts fœtales/mortinaissances n'a pas dépassé ce qui serait attendu dans la population générale. Le nombre de cas est suffisant pour exclure une augmentation ≥ 3 à 4 fois des anomalies congénitales par rapport à l'incidence de fond. Dans 89 % des grossesses suivies de manière prospective, le traitement médicamenteux a été initié avant la grossesse et a été interrompu à un moment donné du premier trimestre lorsque la grossesse a été identifiée.
Données animales
L'atorvastatine traverse le placenta du rat et atteint un niveau dans le foie fœtal équivalent à celui du plasma maternel. L'atorvastatine a été administrée à des rates et à des lapines gravides pendant l'organogenèse à des doses orales allant jusqu'à 300 mg/kg/jour et 100 mg/kg/jour, respectivement. L'atorvastatine n'a pas été tératogène chez le rat à des doses allant jusqu'à 300 mg/kg/jour ou chez le lapin à des doses allant jusqu'à 100 mg/kg/jour. Ces doses ont entraîné des multiples d'environ 30 fois (rat) ou 20 fois (lapin) l'exposition humaine à la MRHD basée sur la surface (mg/m ). Chez le rat, la dose toxique pour la mère de 300 mg/kg a entraîné une augmentation des pertes post-implantation et une diminution du poids corporel du fœtus. Aux doses maternellement toxiques de 50 et 100 mg/kg/jour chez le lapin, il y a eu augmentation des pertes post-implantation et à 100 mg/kg/jour, le poids corporel des fœtus a diminué.
Dans une étude chez des rates gravides ayant reçu 20, 100 ou 225 mg/kg/jour du 7e jour de gestation au 20e jour de lactation (sevrage), il y a eu une diminution de la survie à la naissance, au 4e jour postnatal, au sevrage et après le sevrage chez les ratons des mères ont reçu 225 mg/kg/jour, dose à laquelle une toxicité maternelle a été observée. Le poids corporel des ratons a diminué jusqu'au jour postnatal 21 à 100 mg/kg/jour et jusqu'au jour postnatal 91 à 225 mg/kg/jour. Le développement des petits a été retardé (performance du rotarod à 100 mg/kg/jour et sursaut acoustique à 225 mg/kg/jour ; détachement des pennes et ouverture des yeux à 225 mg/kg/jour). Ces doses correspondent à 6 fois (100 mg/kg) et 22 fois (225 mg/kg) l'exposition humaine à la MRHD, sur la base de l'ASC.
Lactation
Résumé des risques
L'utilisation de LIPITOR 40 mg est contre-indiquée pendant l'allaitement [voir CONTRE-INDICATIONS ]. Il n'y a pas d'informations disponibles sur les effets du médicament sur le nourrisson allaité ou sur les effets du médicament sur la production de lait. On ne sait pas si l'atorvastatine est présente dans le lait maternel, mais il a été démontré qu'un autre médicament de cette classe passe dans le lait maternel et que l'atorvastatine est présente dans le lait de rat. En raison du risque d'effets indésirables graves chez un nourrisson allaité, informez les femmes que l'allaitement n'est pas recommandé pendant le traitement par LIPITOR.
Femelles et mâles de potentiel reproducteur
La contraception
LIPITOR peut nuire au fœtus lorsqu'il est administré à une femme enceinte. Conseiller aux femmes en âge de procréer d'utiliser une contraception efficace pendant le traitement par LIPITOR [voir Utilisation dans des populations spécifiques ].
Utilisation pédiatrique
Hypercholestérolémie familiale hétérozygote (HeFH)
L'innocuité et l'efficacité de LIPITOR 20 mg ont été établies chez des patients pédiatriques, âgés de 10 à 17 ans, avec HeFH en complément d'un régime alimentaire pour réduire les taux de cholestérol total, de LDL-C et d'apo B lorsque, après un essai adéquat de régime thérapie, les éléments suivants sont présents :
- LDL-C ≥ 190 mg/dL, ou
- LDL-C ≥ 160 mg/dL et
- des antécédents familiaux positifs d'HF ou de MCV prématurée chez un parent au premier ou au deuxième degré, ou
- deux ou plusieurs autres facteurs de risque de MCV sont présents.
L'utilisation de LIPITOR 20mg pour cette indication est étayée par des preuves de [voir DOSAGE ET ADMINISTRATION , EFFETS INDÉSIRABLES , PHARMACOLOGIE CLINIQUE , et Etudes cliniques ] :
- Un essai clinique contrôlé par placebo d'une durée de 6 mois chez 187 garçons et filles post-ménarchiques, âgés de 10 à 17 ans. Les patients traités par LIPITOR 10 mg ou 20 mg par jour ont présenté un profil d'effets indésirables généralement similaire à celui des patients traités par placebo. Dans cette étude contrôlée limitée, il n'y avait aucun effet significatif sur la croissance ou la maturation sexuelle chez les garçons ou sur la durée du cycle menstruel chez les filles.
- Un essai ouvert non contrôlé de trois ans qui a inclus 163 patients pédiatriques âgés de 10 à 15 ans avec HeFH qui ont été titrés pour atteindre un LDL-C cible
Informer les filles post-ménarchiques des recommandations en matière de contraception, si cela est approprié pour la patiente [voir Utilisation dans des populations spécifiques ].
L'efficacité à long terme d'un traitement par LIPITOR initié dans l'enfance pour réduire la morbi-mortalité à l'âge adulte n'a pas été établie.
L'innocuité et l'efficacité de LIPITOR 10 mg n'ont pas été établies chez les patients pédiatriques de moins de 10 ans atteints d'HFHe.
Hypercholestérolémie familiale homozygote (HoFH)
L'efficacité clinique de LIPITOR 20 mg à des doses allant jusqu'à 80 mg/jour pendant 1 an a été évaluée dans une étude non contrôlée de patients atteints d'HFHo incluant 8 patients pédiatriques [voir Etudes cliniques ].
Utilisation gériatrique
Sur les 39 828 patients qui ont reçu LIPITOR 40 mg dans les études cliniques, 15 813 (40 %) étaient âgés de ≥ 65 ans et 2 800 (7 %) étaient âgés de ≥ 75 ans. Aucune différence globale d'innocuité ou d'efficacité n'a été observée entre ces sujets et les sujets plus jeunes, et d'autres expériences cliniques rapportées n'ont pas identifié de différences dans les réponses entre les patients âgés et les patients plus jeunes, mais une plus grande sensibilité de certains adultes plus âgés ne peut être exclue. L'âge avancé (≥ 65 ans) étant un facteur prédisposant à la myopathie, LIPITOR doit être prescrit avec prudence chez la personne âgée.
Insuffisance hépatique
Lipitor est contre-indiqué chez les patients atteints d'une maladie hépatique active pouvant inclure des élévations persistantes inexpliquées des taux de transaminases hépatiques [voir CONTRE-INDICATIONS et PHARMACOLOGIE CLINIQUE ].
SURDOSAGE
Il n'existe pas de traitement spécifique du surdosage de LIPITOR. En cas de surdosage, le patient doit être traité de manière symptomatique et des mesures de soutien doivent être mises en place si nécessaire. En raison de la forte liaison du médicament aux protéines plasmatiques, l'hémodialyse ne devrait pas augmenter de manière significative la clairance de LIPITOR 20 mg.
CONTRE-INDICATIONS
- Maladie hépatique active, pouvant inclure des élévations persistantes inexpliquées des taux de transaminases hépatiques
- Hypersensibilité à l'un des composants de ce médicament
- Grossesse [voir Utilisation dans des populations spécifiques].
- Allaitement [voir Utilisation dans des populations spécifiques].
PHARMACOLOGIE CLINIQUE
Mécanisme d'action
LIPITOR 20 mg est un inhibiteur sélectif et compétitif de l'HMG-CoA réductase, l'enzyme limitant la vitesse qui convertit la 3-hydroxy-3-méthylglutaryl-coenzyme A en mévalonate, un précurseur des stérols, dont le cholestérol. Dans les modèles animaux, LIPITOR 40 mg réduit les taux plasmatiques de cholestérol et de lipoprotéines en inhibant la HMG-CoA réductase et la synthèse du cholestérol dans le foie et en augmentant le nombre de récepteurs hépatiques des LDL à la surface des cellules pour améliorer l'absorption et le catabolisme des LDL ; LIPITOR réduit également la production de LDL et le nombre de particules de LDL.
Pharmacodynamie
LIPITOR, ainsi que certains de ses métabolites, sont pharmacologiquement actifs chez l'homme. Le foie est le principal site d'action et le site principal de la synthèse du cholestérol et de la clairance des LDL. La posologie du médicament, plutôt que la concentration systémique du médicament, est mieux corrélée à la réduction du LDL-C. L'individualisation de la posologie du médicament doit être basée sur la réponse thérapeutique [voir DOSAGE ET ADMINISTRATION ].
Pharmacocinétique
Absorption
LIPITOR est rapidement absorbé après administration orale ; les concentrations plasmatiques maximales sont atteintes en 1 à 2 heures. Le degré d'absorption augmente proportionnellement à la dose de LIPITOR. La biodisponibilité absolue de l'atorvastatine (médicament mère) est d'environ 14 % et la disponibilité systémique de l'activité inhibitrice de l'HMG-CoA réductase est d'environ 30 %. La faible disponibilité systémique est attribuée à la clairance présystémique dans la muqueuse gastro-intestinale et/ou au métabolisme de premier passage hépatique. Bien que la nourriture diminue le taux et l'étendue de l'absorption du médicament d'environ 25 % et 9 %, respectivement, comme évalué par la Cmax et l'ASC, la réduction du LDL-C est similaire, que LIPITOR 40 mg soit administré avec ou sans nourriture. Les concentrations plasmatiques de LIPITOR 20 mg sont plus faibles (environ 30 % pour la Cmax et l'ASC) après l'administration du médicament le soir par rapport au matin. Cependant, la réduction du LDL-C est la même quel que soit le moment de la journée d'administration du médicament [voir DOSAGE ET ADMINISTRATION ].
Distribution
Le volume de distribution moyen de LIPITOR 20 mg est d'environ 381 litres. LIPITOR 20 mg est lié à ≥ 98 % aux protéines plasmatiques. Un rapport sang/plasma d'environ 0,25 indique une mauvaise pénétration du médicament dans les globules rouges. D'après des observations chez le rat, LIPITOR 10 mg est susceptible d'être sécrété dans le lait maternel [voir CONTRE-INDICATIONS et Utilisation dans des populations spécifiques ].
Métabolisme
LIPITOR 20 mg est largement métabolisé en dérivés ortho- et parahydroxylés et en divers produits de bêta-oxydation. L'inhibition in vitro de l'HMG-CoA réductase par les métabolites ortho- et parahydroxylés est équivalente à celle de LIPITOR. Environ 70 % de l'activité inhibitrice circulante de la HMG-CoA réductase est attribuée aux métabolites actifs. Des études in vitro suggèrent l'importance du métabolisme de LIPITOR 40 mg par le cytochrome P450 3A4, en accord avec l'augmentation des concentrations plasmatiques de LIPITOR 20 mg chez l'homme suite à la co-administration avec l'érythromycine, un inhibiteur connu de cette isozyme [voir INTERACTIONS MÉDICAMENTEUSES ]. Chez les animaux, le métabolite ortho-hydroxy subit une glucuronidation supplémentaire.
Excrétion
LIPITOR 20 mg et ses métabolites sont éliminés principalement dans la bile après métabolisme hépatique et/ou extra-hépatique ; cependant, le médicament ne semble pas subir de recirculation entérohépatique. La demi-vie d'élimination plasmatique moyenne de LIPITOR chez l'homme est d'environ 14 heures, mais la demi-vie de l'activité inhibitrice de l'HMG-CoA réductase est de 20 à 30 heures en raison de la contribution des métabolites actifs. Moins de 2 % d'une dose de LIPITOR est retrouvée dans les urines après administration orale.
Populations spécifiques
Gériatrique
Les concentrations plasmatiques de LIPITOR sont plus élevées (environ 40 % pour la Cmax et 30 % pour l'ASC) chez les sujets âgés sains (âge ≥ 65 ans) que chez les jeunes adultes. Les données cliniques suggèrent un degré plus élevé de diminution du LDL à n'importe quelle dose de médicament dans la population de patients âgés par rapport aux adultes plus jeunes [voir Utilisation dans des populations spécifiques ].
Pédiatrique
La clairance orale apparente de l'atorvastatine chez les sujets pédiatriques semblait similaire à celle des adultes lorsqu'elle était mise à l'échelle allométriquement en fonction du poids corporel, car le poids corporel était la seule covariable significative dans le modèle pharmacocinétique de la population d'atorvastatine avec des données incluant des patients pédiatriques HeFH (âgés de 10 à 17 ans, n = 29) dans une étude ouverte de 8 semaines.
Le genre
Les concentrations plasmatiques de LIPITOR 40 mg chez la femme diffèrent de celles chez l'homme (environ 20 % plus élevées pour la Cmax et 10 % plus faibles pour l'ASC) ; cependant, il n'y a pas de différence cliniquement significative dans la réduction du LDL-C avec LIPITOR 10 mg entre les hommes et les femmes.
Insuffisance rénale
La maladie rénale n'a aucune influence sur les concentrations plasmatiques ou la réduction du LDL-C de LIPITOR ; ainsi, l'adaptation de la dose chez les patients atteints d'insuffisance rénale n'est pas nécessaire [voir DOSAGE ET ADMINISTRATION et AVERTISSEMENTS ET PRECAUTIONS ].
Hémodialyse
Bien qu'aucune étude n'ait été menée chez des patients atteints d'insuffisance rénale terminale, l'hémodialyse ne devrait pas améliorer de manière significative la clairance de LIPITOR 10 mg puisque le médicament est fortement lié aux protéines plasmatiques.
Insuffisance hépatique
Chez les patients atteints d'hépatopathie alcoolique chronique, les concentrations plasmatiques de LIPITOR sont nettement augmentées. La Cmax et l'ASC sont chacune 4 fois plus élevées chez les patients atteints de la maladie de Childs-Pugh A. La Cmax et l'ASC sont environ 16 fois et 11 fois plus élevées, respectivement, chez les patients atteints de la maladie de Childs-Pugh B [voir CONTRE-INDICATIONS ].
Études sur les interactions médicamenteuses
L'atorvastatine est un substrat des transporteurs hépatiques OATP1B1 et OATP1B3. Les métabolites de l'atorvastatine sont des substrats de l'OATP1B1. L'atorvastatine est également identifiée comme un substrat du transporteur d'efflux BCRP, qui peut limiter l'absorption intestinale et la clairance biliaire de l'atorvastatine.
TABLEAU 6 : Effet des médicaments co-administrés sur la pharmacocinétique de l'atorvastatine
TABLEAU 7 : Effet de l'atorvastatine sur la pharmacocinétique des médicaments co-administrés
LIPITOR n'a eu aucun effet cliniquement significatif sur le temps de prothrombine lorsqu'il a été administré à des patients recevant un traitement chronique à la warfarine.
Etudes cliniques
Prévention des maladies cardiovasculaires
Dans l'Anglo-Scandinavian Cardiac Outcomes Trial (ASCOT), l'effet de LIPITOR 10 mg sur les maladies coronariennes mortelles et non mortelles a été évalué chez 10 305 patients hypertendus âgés de 40 à 80 ans (moyenne de 63 ans), sans antécédent myocardique. infarctus du myocarde et avec des taux de TC ≤ 251 mg/dL (6,5 mmol/L). De plus, tous les patients présentaient au moins 3 des facteurs de risque cardiovasculaire suivants : sexe masculin (81,1 %), âge > 55 ans (84,5 %), tabagisme (33,2 %), diabète (24,3 %), antécédent de coronaropathie lors d'une première degré relatif (26 %), TC:HDL > 6 (14,3 %), maladie vasculaire périphérique (5,1 %), hypertrophie ventriculaire gauche (14,4 %), événement cérébrovasculaire antérieur (9,8 %), anomalie ECG spécifique (14,3 %), protéinurie /albuminurie (62,4 %). Dans cette étude en double aveugle contrôlée par placebo, les patients ont été traités par un traitement antihypertenseur (TA cible
L'effet de 10 mg/jour de LIPITOR sur les taux de lipides était similaire à celui observé lors d'essais cliniques antérieurs.
LIPITOR a significativement réduit le taux d'événements coronariens [maladie coronarienne mortelle (46 événements dans le groupe placebo contre 40 événements dans le groupe LIPITOR 40 mg) ou IDM non mortel (108 événements dans le groupe placebo contre 60 événements dans le groupe LIPITOR groupe 20 mg)] avec une réduction du risque relatif de 36 % [(basé sur des incidences de 1,9 % pour LIPITOR 40 mg contre 3,0 % pour le placebo), p = 0,0005 (voir Figure 1)]. La réduction du risque était constante quel que soit l'âge, le statut tabagique, l'obésité ou la présence d'un dysfonctionnement rénal. L'effet de LIPITOR a été observé quel que soit le taux initial de LDL. En raison du petit nombre d'événements, les résultats pour les femmes n'étaient pas concluants.
Figure 1 : Effet de LIPITOR 10 mg/jour sur l'incidence cumulée des infarctus du myocarde non mortels ou des décès par coronaropathie (dans ASCOT-LLA)
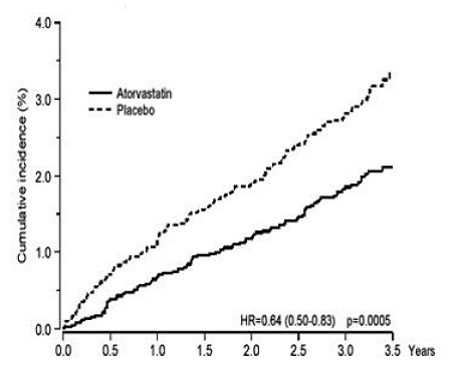
LIPITOR 40 mg a également réduit significativement le risque relatif de procédures de revascularisation de 42 % (incidences de 1,4 % pour LIPITOR 20 mg et 2,5 % pour le placebo). Bien que la réduction des AVC mortels et non mortels n'ait pas atteint un niveau de signification prédéfini (p = 0,01), une tendance favorable a été observée avec une réduction du risque relatif de 26 % (incidences de 1,7 % pour LIPITOR et 2,3 % pour le placebo) . Il n'y avait pas de différence significative entre les groupes de traitement pour les décès dus à des causes cardiovasculaires (p = 0,51) ou à des causes non cardiovasculaires (p = 0,17).
Dans l'étude CARDS (Collaborative Atorvastatin Diabetes Study), l'effet de LIPITOR sur les critères d'évaluation des maladies cardiovasculaires (MCV) a été évalué chez 2838 sujets (94 % de race blanche, 68 % d'hommes), âgés de 40 à 75 ans atteints de diabète de type 2 selon les critères de l'OMS, sans antécédent de maladie cardiovasculaire et avec LDL ≤ 160 mg/dL et TG ≤ 600 mg/dL. En plus du diabète, les sujets présentaient au moins un des facteurs de risque suivants : tabagisme actuel (23 %), hypertension (80 %), rétinopathie (30 %), ou microalbuminurie (9 %) ou macroalbuminurie (3 %). Aucun sujet sous hémodialyse n'a été inscrit à l'étude. Dans cet essai clinique multicentrique, contrôlé par placebo, en double aveugle, les sujets ont été répartis au hasard entre LIPITOR 10 mg par jour (1429) ou un placebo (1411) selon un rapport 1:1 et ont été suivis pendant une durée médiane de 3,9 ans. Le critère d'évaluation principal était la survenue de l'un des événements cardiovasculaires majeurs : infarctus du myocarde, décès par coronaropathie aiguë, angor instable, revascularisation coronarienne ou accident vasculaire cérébral. L'analyse principale était le délai avant la première occurrence du critère d'évaluation principal.
Les caractéristiques initiales des sujets étaient les suivantes : âge moyen de 62 ans, taux moyen d'HbA de 7,7 % ; médiane de LDL-C 120 mg/dL ; CT médiane 207 mg/dL ; TG médian 151 mg/dL ; HDL-C médian 52 mg/dL.
L'effet de LIPITOR 10 mg/jour sur les taux de lipides a été similaire à celui observé lors d'essais cliniques antérieurs.
LIPITOR a significativement réduit le taux d'événements cardiovasculaires majeurs (événements du critère d'évaluation principal) (83 événements dans le groupe LIPITOR contre 127 événements dans le groupe placebo) avec une réduction du risque relatif de 37 %, HR 0,63, IC à 95 % (0,48 ; 0,83) (p=0,001) (voir Figure 2). Un effet de LIPITOR a été observé quel que soit l'âge, le sexe ou les taux de lipides initiaux.
LIPITOR 20mg a significativement réduit le risque d'AVC de 48% (21 événements dans le groupe LIPITOR 10mg vs 39 événements dans le groupe placebo), HR 0,52, IC 95% (0,31, 0,89) (p=0,016) et a réduit le risque de IM de 42 % (38 événements dans le groupe LIPITOR vs 64 événements dans le groupe placebo), HR 0,58, IC 95,1 % (0,39, 0,86) (p = 0,007). Il n'y avait pas de différence significative entre les groupes de traitement pour l'angine de poitrine, les procédures de revascularisation et la mort coronarienne aiguë.
Il y a eu 61 décès dans le groupe LIPITOR contre 82 décès dans le groupe placebo (HR 0,73, p=0,059).
Figure 2 : Effet de LIPITOR à 10 mg/jour sur le délai d'apparition d'un événement cardiovasculaire majeur (infarctus du myocarde, décès par coronaropathie aiguë, angor instable, revascularisation coronarienne ou accident vasculaire cérébral) dans CARDS
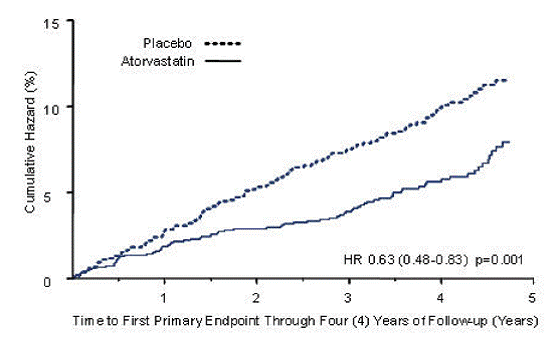
Dans l'étude Treating to New Targets Study (TNT), l'effet de LIPITOR 80 mg/jour vs LIPITOR 10 mg/jour sur la réduction des événements cardiovasculaires a été évalué chez 10 001 sujets (94 % blancs, 81 % hommes, 38 % ≥ 65 ans) avec une maladie coronarienne cliniquement évidente qui avait atteint un taux cible de LDL-C
Le traitement par LIPITOR 80 mg/jour a significativement réduit le taux d'EVCM (434 événements dans le groupe 80 mg/jour contre 548 événements dans le groupe 10 mg/jour) avec une réduction du risque relatif de 22 %, HR 0,78, IC 95 % (0,69, 0,89), p = 0,0002 (voir Figure 3 et Tableau 9). La réduction globale du risque était constante quel que soit l'âge (
Figure 3 : Effet de LIPITOR 80 mg/jour vs 10 mg/jour sur le délai d'apparition des événements cardiovasculaires majeurs (TNT)
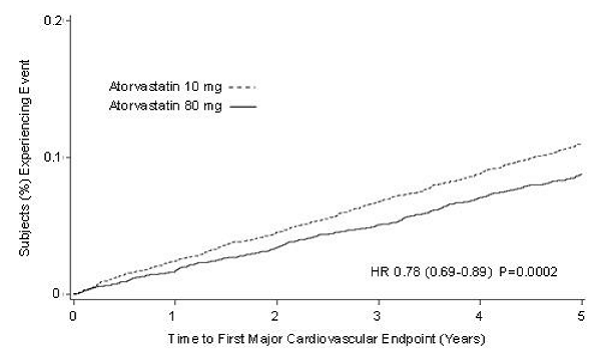
TABLEAU 8 : Aperçu des résultats d'efficacité dans le TNT
Parmi les événements qui constituaient le critère principal d'évaluation de l'efficacité, le traitement par LIPITOR 80 mg/jour a réduit de manière significative le taux d'IM non mortels non liés à l'intervention et d'AVC mortels et non mortels, mais pas de décès par coronaropathie ni d'arrêt cardiaque réanimé (Tableau 8). Parmi les critères d'évaluation secondaires prédéfinis, le traitement par LIPITOR 80 mg/jour a réduit significativement le taux de revascularisation coronarienne, d'angor et d'hospitalisation pour insuffisance cardiaque, mais pas de maladie vasculaire périphérique. La réduction du taux d'ICC avec hospitalisation n'a été observée que chez les 8 % de patients ayant des antécédents d'ICC.
Il n'y avait pas de différence significative entre les groupes de traitement pour la mortalité toutes causes confondues (Tableau 8). Les proportions de sujets ayant subi un décès d'origine cardiovasculaire, y compris les composantes du décès par coronaropathie et de l'accident vasculaire cérébral mortel, étaient numériquement plus faibles dans le groupe LIPITOR 80 mg que dans le groupe de traitement LIPITOR 10 mg. Les proportions de sujets ayant subi un décès non cardiovasculaire étaient numériquement plus importantes dans le groupe LIPITOR 80 mg que dans le groupe de traitement LIPITOR 10 mg.
Dans l'étude IDEAL (Incremental Decrease in Endpoints Through Aggressive Lipid Lowering Study), le traitement par LIPITOR 80 mg/jour a été comparé à un traitement par simvastatine 20–40 mg/jour chez 8 888 sujets jusqu'à 80 ans ayant des antécédents de maladie coronarienne pour évaluer si une réduction du risque CV peut être obtenue. Les patients étaient principalement des hommes (81 %), de race blanche (99 %) avec un âge moyen de 61,7 ans et un LDL-C moyen de 121,5 mg/dL lors de la randomisation ; 76 % étaient sous statine. Dans cet essai prospectif, randomisé, en ouvert et en aveugle (PROBE) sans période de rodage, les sujets ont été suivis pendant une durée médiane de 4,8 ans. Les taux moyens de cholestérol LDL-C, TC, TG, HDL et non HDL à la semaine 12 étaient de 78, 145, 115, 45 et 100 mg/dL pendant le traitement avec 80 mg de LIPITOR 40 mg et 105, 179, 142, 47 et 132 mg/dL pendant le traitement avec 20 à 40 mg de simvastatine.
Il n'y a pas eu de différence significative entre les groupes de traitement pour le critère de jugement principal, le taux de premier événement coronarien majeur (MC mortelle, IDM non mortel et arrêt cardiaque réanimé) : 411 (9,3 %) dans le groupe LIPITOR 80 mg/j vs 463 (10,4 %) dans le groupe simvastatine 20–40 mg/jour, HR 0,89, IC 95 % (0,78, 1,01), p = 0,07.
Il n'y avait pas de différences significatives entre les groupes de traitement pour la mortalité toutes causes : 366 (8,2 %) dans le groupe LIPITOR 80 mg/jour vs 374 (8,4 %) dans le groupe simvastatine 20–40 mg/jour. Les proportions de sujets ayant subi un décès CV ou non CV étaient similaires pour le groupe LIPITOR 80 mg et le groupe simvastatine 20–40 mg.
Hyperlipidémie et dyslipidémie mixte
LIPITOR réduit le C total, le LDL-C, le VLDL-C, l'apo B et les TG, et augmente le HDL-C chez les patients atteints d'hyperlipidémie (hétérozygote familiale et non familiale) et de dyslipidémie mixte (types IIa et IIb de Fredrickson). La réponse thérapeutique est observée dans les 2 semaines, et la réponse maximale est généralement obtenue dans les 4 semaines et maintenue pendant le traitement chronique.
LIPITOR est efficace dans une grande variété de populations de patients atteints d'hyperlipidémie, avec ou sans hypertriglycéridémie, chez les hommes et les femmes, et chez les personnes âgées.
Dans deux études dose-réponse multicentriques contrôlées par placebo chez des patients atteints d'hyperlipidémie, LIPITOR administré en une seule dose sur 6 semaines a réduit de manière significative le C total, le LDL-C, l'apo B et les TG. (Les résultats regroupés sont fournis dans le tableau 9.)
TABLEAU 9 : Réponse à la dose chez les patients atteints d'hyperlipidémie primaire (moyenne ajustée en % de changement par rapport au départ)*
Chez les patients atteints d'hyperlipoprotéinémie de Fredrickson de types IIa et IIb regroupés à partir de 24 essais contrôlés, les variations médianes (25e et 75e percentiles) du pourcentage de HDL-C par rapport à l'inclusion pour LIPITOR à 10, 20, 40 et 80 mg étaient de 6,4 (-1,4, 14), 8,7 (0, 17), 7,8 (0, 16) et 5,1 (-2,7, 15), respectivement. De plus, l'analyse des données regroupées a démontré des diminutions cohérentes et significatives du C total, du LDL-C, des TG, du C total/HDL-C et du LDLC/HDL-C.
Dans trois études multicentriques en double aveugle chez des patients atteints d'hyperlipidémie, LIPITOR a été comparé à d'autres statines. Après randomisation, les patients ont été traités pendant 16 semaines soit par LIPITOR 10 mg par jour, soit par une dose fixe de l'agent de comparaison (Tableau 10).
TABLEAU 10 : Changement moyen en pourcentage par rapport au départ au point final (essais en double aveugle, randomisés, contrôlés par un agent actif)
L'impact sur les résultats cliniques des différences d'effets de modification des lipides entre les traitements présentés dans le tableau 10 n'est pas connu. Le tableau 10 ne contient pas de données comparant les effets de LIPITOR à 10 mg et à des doses supérieures de lovastatine, de pravastatine et de simvastatine. Les médicaments comparés dans les études résumées dans le tableau ne sont pas nécessairement interchangeables.
Hypertriglycéridémie
La réponse à LIPITOR chez 64 patients atteints d'hypertriglycéridémie isolée (Fredrickson Type IV) traités dans plusieurs essais cliniques est présentée dans le tableau ci-dessous (Tableau 11). Pour les patients traités par LIPITOR, le taux initial médian (min, max) de TG était de 565 (267–1 502).
TABLEAU 11 : Patients combinés avec TG élevé isolé : pourcentage de changement médian (min, max) par rapport à la ligne de base
Dysbêtalipoprotéinémie
Les résultats d'une étude croisée en ouvert de 16 patients (génotypes : 14 apo E2/E2 et 2 apo E3/E2) atteints de dysbêtalipoprotéinémie (Fredrickson Type III) sont présentés dans le tableau ci-dessous (Tableau 12).
TABLEAU 12 : Étude croisée en ouvert de 16 patients atteints de dysbêtalipoprotéinémie (Fredrickson de type III)
Hypercholestérolémie familiale homozygote
Dans une étude sans groupe témoin simultané, 29 patients âgés de 6 à 37 ans atteints d'HFHo ont reçu des doses quotidiennes maximales de 20 à 80 mg de LIPITOR. La réduction moyenne du LDL-C dans cette étude était de 18 %. Vingt-cinq patients avec une réduction du LDL-C ont eu une réponse moyenne de 20 % (intervalle de 7 % à 53 %, médiane de 24 %) ; les 4 patients restants avaient des augmentations de 7% à 24% du LDL-C. Cinq des 29 patients avaient une fonction de récepteur LDL absente. Parmi ceux-ci, 2 patients avaient également un shunt porto-cave et n'avaient pas de réduction significative du LDL-C. Les 3 autres patients négatifs pour les récepteurs avaient une réduction moyenne du LDL-C de 22 %.
Hypercholestérolémie familiale hétérozygote chez les patients pédiatriques
Dans une étude en double aveugle contrôlée contre placebo suivie d'une phase en ouvert, 187 garçons et filles post-ménarchiques âgés de 10 à 17 ans (âge moyen 14,1 ans) atteints d'hypercholestérolémie familiale hétérozygote (HeFH) ou d'hypercholestérolémie sévère ont été randomisés pour LIPITOR (n = 140) ou placebo (n = 47) pendant 26 semaines, puis tous ont reçu LIPITOR 40 mg pendant 26 semaines. L'inclusion dans l'étude nécessitait 1) un niveau initial de LDL-C ≥ 190 mg/dL ou 2) un niveau initial de LDL-C ≥ 160 mg/dL et des antécédents familiaux positifs d'HF ou une maladie cardiovasculaire prématurée documentée au premier ou au deuxième degré relatif. La valeur initiale moyenne de LDL-C était de 218,6 mg/dL (intervalle : 138,5 à 385,0 mg/dL) dans le groupe LIPITOR par rapport à 230,0 mg/dL (intervalle : 160,0 à 324,5 mg/dL) dans le groupe placebo . La posologie de LIPITOR (une fois par jour) était de 10 mg pendant les 4 premières semaines et augmentée à 20 mg si le taux de LDL-C était > 130 mg/dL. Le nombre de patients traités par LIPITOR qui ont nécessité une augmentation de la dose à 20 mg après la semaine 4 pendant la phase en double aveugle était de 78 (55,7 %).
LIPITOR 10 mg a diminué de manière significative les taux plasmatiques de C total, de LDL-C, de triglycérides et d'apolipoprotéine B au cours de la phase en double aveugle de 26 semaines (voir Tableau 13).
TABLEAU 13 : Effets altérant les lipides de LIPITOR chez les adolescents garçons et filles atteints d'hypercholestérolémie familiale hétérozygote ou d'hypercholestérolémie sévère (changement moyen en pourcentage par rapport au départ au point final dans la population en intention de traiter)
La valeur moyenne de C-LDL obtenue était de 130,7 mg/dL (intervalle : 70,0 à 242,0 mg/dL) dans le groupe LIPITOR 10 mg, contre 228,5 mg/dL (intervalle : 152,0 à 385,0 mg/dL) dans le groupe placebo groupe pendant la phase en double aveugle de 26 semaines.
L'atorvastatine a également été étudiée dans le cadre d'un essai ouvert non contrôlé de trois ans qui comprenait 163 patients atteints d'HFHe âgés de 10 à 15 ans (82 garçons et 81 filles). Tous les patients avaient un diagnostic clinique d'HeFH confirmé par analyse génétique (s'il n'était pas déjà confirmé par les antécédents familiaux). Environ 98 % étaient de race blanche et moins de 1 % étaient noirs ou asiatiques. Le LDL-C moyen au départ était de 232 mg/dL. La dose initiale d'atorvastatine était de 10 mg une fois par jour et les doses ont été ajustées pour atteindre un objectif de
L'efficacité à long terme du traitement par LIPITOR 20 mg chez l'enfant pour réduire la morbi-mortalité à l'âge adulte n'a pas été établie.
INFORMATIONS PATIENTS
LIPITOR® comprimés d'atorvastatine calcique (LIP-ih-tore))
Lisez les informations destinées aux patients fournies avec LIPITOR 20 mg avant de commencer à le prendre et chaque fois que vous recevez une recharge. Il peut y avoir de nouvelles informations. Cette notice ne remplace pas une discussion avec votre médecin au sujet de votre état ou de votre traitement.
Si vous avez des questions sur LIPITOR, interrogez votre médecin ou votre pharmacien.
Qu'est-ce que LIPITOR ?
LIPITOR est un médicament délivré sur ordonnance qui abaisse le taux de cholestérol dans votre sang. Il abaisse le LDL-C («mauvais» cholestérol) et les triglycérides dans votre sang. Il peut également augmenter votre HDL-C (« bon » cholestérol). LIPITOR est destiné aux adultes et aux enfants de plus de 10 ans dont le cholestérol ne diminue pas suffisamment avec l'exercice et un régime pauvre en graisses seuls.
LIPITOR peut réduire le risque de crise cardiaque, d'accident vasculaire cérébral, de certains types de chirurgie cardiaque et de douleurs thoraciques chez les patients qui ont une maladie cardiaque ou des facteurs de risque de maladie cardiaque tels que :
- âge, tabagisme, hypertension artérielle, faible taux de HDL-C, maladie cardiaque dans la famille.
LIPITOR 20 mg peut réduire le risque de crise cardiaque ou d'accident vasculaire cérébral chez les patients diabétiques et présentant des facteurs de risque tels que :
- problèmes oculaires, problèmes rénaux, tabagisme ou hypertension artérielle.
LIPITOR 40mg commence à agir en 2 semaines environ.
Qu'est-ce que le cholestérol ?
Le cholestérol et les triglycérides sont des graisses fabriquées par votre corps. On les retrouve également dans les aliments. Vous avez besoin d'un peu de cholestérol pour être en bonne santé, mais trop n'est pas bon pour vous. Le cholestérol et les triglycérides peuvent obstruer vos vaisseaux sanguins. Il est particulièrement important de réduire votre taux de cholestérol si vous souffrez d'une maladie cardiaque, si vous fumez, si vous souffrez de diabète ou d'hypertension artérielle, si vous êtes âgé ou si une maladie cardiaque survient tôt dans votre famille.
Qui ne devrait pas prendre LIPITOR 40mg ?
Ne prenez jamais LIPITOR 10 mg si vous :
- êtes enceinte ou pensez que vous pourriez être enceinte, ou envisagez de devenir enceinte. LIPITOR peut nuire à votre bébé à naître. Si vous tombez enceinte, arrêtez de prendre LIPITOR 40 mg et appelez immédiatement votre médecin.
- allaitent. LIPITOR 20 mg peut passer dans votre lait maternel et être nocif pour votre bébé.
- avoir des problèmes de foie.
- êtes allergique à LIPITOR ou à l'un de ses ingrédients. L'ingrédient actif est l'atorvastatine. Voir la fin de cette notice pour la liste complète des ingrédients de LIPITOR.
La posologie de LIPITOR 20 mg n'a pas été établie chez les enfants de moins de 10 ans.
Avant de commencer LIPITOR
Informez votre médecin si vous :
- avez des douleurs musculaires ou une faiblesse
- boire plus de 2 verres d'alcool par jour
- avoir le diabète
- avoir un problème de thyroïde
- avoir des problèmes rénaux
Certains médicaments ne doivent pas être pris avec LIPITOR. Informez votre médecin de tous les médicaments que vous prenez, y compris les médicaments sur ordonnance et en vente libre, les vitamines et les suppléments à base de plantes. LIPITOR et certains autres médicaments peuvent interagir et provoquer des effets indésirables graves. Informez en particulier votre médecin si vous prenez des médicaments pour :
- votre système immunitaire
- cholestérol
- infections
- contrôle des naissances
- insuffisance cardiaque
- VIH ou SIDA
- virus de l'hépatite C
- anti-viraux
Connaissez tous les médicaments que vous prenez. Gardez-en une liste avec vous pour la montrer à votre médecin et à votre pharmacien.
Comment dois-je prendre LIPITOR 40mg ?
- Prenez LIPITOR 20 mg exactement comme prescrit par votre médecin. Ne modifiez pas votre dose et n'arrêtez pas LIPITOR sans en parler avec votre médecin. Votre médecin peut effectuer des tests sanguins pour vérifier votre taux de cholestérol pendant votre traitement par LIPITOR. Votre dose de LIPITOR peut être modifiée en fonction des résultats de ces tests sanguins.
- Prenez LIPITOR chaque jour à n'importe quel moment de la journée à peu près à la même heure chaque jour. LIPITOR 10 mg peut être pris avec ou sans nourriture. Ne cassez pas les comprimés LIPITOR avant de les prendre.
- Votre médecin doit vous initier à un régime pauvre en graisses avant de vous donner LIPITOR. Continuez à suivre ce régime faible en gras lorsque vous prenez LIPITOR.
- Si vous manquez une dose de LIPITOR, prenez-la dès que vous vous en souvenez. Ne prenez pas LIPITOR 10 mg si plus de 12 heures se sont écoulées depuis que vous avez oublié votre dernière dose. Attendez et prenez la dose suivante à l'heure habituelle. Ne prenez pas 2 doses de LIPITOR 10mg en même temps.
- Si vous avez pris trop de LIPITOR ou en cas de surdosage, appelez immédiatement votre médecin ou le centre antipoison. Ou rendez-vous aux urgences les plus proches.
Que dois-je éviter pendant que je prends LIPITOR 10 mg ?
- Parlez-en à votre médecin avant de commencer tout nouveau médicament. Cela comprend les médicaments sur ordonnance et en vente libre, les vitamines et les suppléments à base de plantes. LIPITOR et certains autres médicaments peuvent interagir et provoquer des effets indésirables graves.
- Ne tombez pas enceinte. Si vous tombez enceinte, arrêtez immédiatement de prendre LIPITOR et appelez votre médecin.
Quels sont les effets secondaires possibles de LIPITOR 10mg ?
LIPITOR peut provoquer des effets secondaires graves. Ces effets secondaires ne sont survenus qu'à un petit nombre de personnes. Votre médecin peut vous surveiller pour eux. Ces effets secondaires disparaissent généralement si votre dose est réduite ou si LIPITOR est arrêté. Ces effets secondaires graves comprennent :
- Problèmes musculaires. LIPITOR 40 mg peut provoquer de graves problèmes musculaires pouvant entraîner des problèmes rénaux, notamment une insuffisance rénale. Vous avez un risque accru de problèmes musculaires si vous prenez certains autres médicaments avec LIPITOR.
- Problèmes de foie. Votre médecin doit effectuer des tests sanguins pour vérifier votre foie avant que vous ne commenciez à prendre LIPITOR 20 mg et si vous présentez des symptômes de problèmes hépatiques pendant que vous prenez LIPITOR. Appelez immédiatement votre médecin si vous présentez les symptômes suivants de problèmes de foie :
- se sentir fatigué ou faible
- perte d'appétit
- douleur dans le haut du ventre
- urine de couleur ambre foncé
- jaunissement de votre peau ou du blanc de vos yeux
Appelez immédiatement votre médecin si vous avez :
- des problèmes musculaires comme une faiblesse, une sensibilité ou une douleur qui surviennent sans raison valable, surtout si vous avez également de la fièvre ou si vous vous sentez plus fatigué que d'habitude. Cela peut être un signe précoce d'un problème musculaire rare.
- des problèmes musculaires qui ne disparaissent pas même après que votre médecin vous a conseillé d'arrêter de prendre LIPITOR. Votre médecin peut faire d'autres tests pour diagnostiquer la cause de vos problèmes musculaires.
- réactions allergiques telles que gonflement du visage, des lèvres, de la langue et/ou de la gorge pouvant entraîner des difficultés à respirer ou à avaler pouvant nécessiter un traitement immédiat.
- nausée et vomissements.
- urine brune ou foncée.
- vous vous sentez plus fatigué que d'habitude
- votre peau et le blanc de vos yeux jaunissent.
- Douleur d'estomac.
- réactions cutanées allergiques.
Dans les études cliniques, les patients ont signalé les effets secondaires courants suivants lors de la prise de LIPITOR : diarrhée, maux d'estomac, douleurs musculaires et articulaires et altérations de certains tests sanguins de laboratoire.
Les effets indésirables supplémentaires suivants ont été rapportés avec LIPITOR :
fatigue, problèmes de tendons, perte de mémoire et confusion.
Parlez à votre médecin ou pharmacien si vous avez des effets indésirables qui vous dérangent ou qui ne disparaissent pas.
Ce ne sont pas tous les effets secondaires de LIPITOR. Demandez à votre médecin ou à votre pharmacien une liste complète.
Comment conserver LIPITOR
- Conservez LIPITOR à température ambiante, entre 68 et 77 °F (20 à 25 °C).
- Ne gardez pas de médicaments périmés ou dont vous n'avez plus besoin.
- Gardez LIPITOR et tous les médicaments hors de la portée des enfants. Assurez-vous que si vous jetez un médicament, il est hors de portée des enfants.
Informations générales sur LIPITOR
Des médicaments sont parfois prescrits pour des affections qui ne sont pas mentionnées dans les notices d'information destinées aux patients. Ne pas utiliser LIPITOR 10 mg pour une affection pour laquelle il n'a pas été prescrit. Ne donnez pas LIPITOR à d'autres personnes, même si elles ont le même problème que vous. Cela peut leur nuire.
Cette notice résume les informations les plus importantes sur LIPITOR. Si vous souhaitez plus d'informations, parlez-en à votre médecin. Vous pouvez demander à votre médecin ou à votre pharmacien des informations sur LIPITOR destinées aux professionnels de la santé. Ou vous pouvez vous rendre sur le site Web de LIPITOR à l'adresse www.lipitor.com.
Quels sont les ingrédients de LIPITOR ?
Ingrédient actif: atorvastatine calcique
Ingrédients inactifs: carbonate de calcium, USP; cire de candelilla, FCC; croscarmellose sodique, NF; hydroxypropylcellulose, NF; lactose monohydraté, NF; stéarate de magnésium, NF; cellulose microcristalline, NF; Opadry White YS-1-7040 (hypromellose, polyéthylèneglycol, talc, dioxyde de titane); polysorbate 80, NF; émulsion de siméthicone.
