Contrôle des naissances: Ovral 300mcg Norgestrel Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
LO/OVRAL®-28 (norgestrel et éthinylestradiol) Comprimés
Les patients doivent être informés que les contraceptifs oraux ne protègent pas contre la transmission du VIH (SIDA) et d'autres maladies sexuellement transmissibles (MST) telles que la chlamydia, l'herpès génital, les verrues génitales, la gonorrhée, l'hépatite B et la syphilis.
LA DESCRIPTION
Chaque comprimé LO/OVRAL de 300 mcg contient 0,3 mg de norgestrel (dl-13-beta-ethyl-17-alpha-ethinyl-17-beta-hydroxygon-4-en-3-one), un progestatif totalement synthétique, et 0,03 mg d'éthinylestradiol, (19-nor-17α-pregna-1,3,5(10)-trien-20-yne-3,17-diol). Les ingrédients inactifs présents sont la cellulose, le lactose, le stéarate de magnésium et la polacriline potassique.

LES INDICATIONS
Les contraceptifs oraux sont indiqués pour la prévention de la grossesse chez les femmes qui choisissent d'utiliser ce produit comme méthode de contraception.
Les contraceptifs oraux sont très efficaces. Le tableau I énumère les taux typiques de grossesses accidentelles chez les utilisatrices de contraceptifs oraux combinés et d'autres méthodes de contraception. L'efficacité de ces méthodes contraceptives, à l'exception de la stérilisation, du DIU et des implants, dépend de la fiabilité avec laquelle elles sont utilisées. L'utilisation correcte et cohérente des méthodes peut entraîner des taux d'échec inférieurs.
DOSAGE ET ADMINISTRATION
Pour obtenir une efficacité contraceptive maximale, Lo/Ovral 300mcg doit être pris exactement comme indiqué et à des intervalles ne dépassant pas 24 heures. La possibilité d'ovulation et de conception avant le début du traitement doit être envisagée.
La posologie de Lo/Ovral 300mcg est d'un comprimé par jour pendant 21 jours consécutifs par cycle menstruel selon le calendrier prescrit. Les comprimés sont ensuite arrêtés pendant 7 jours (trois semaines de prise, une semaine de repos).
Il est recommandé de prendre les comprimés Lo/Ovral 300mcg à la même heure chaque jour.
Au cours du premier cycle de médication, la patiente doit prendre un comprimé Lo/Ovral 300mcg par jour pendant vingt et un jours consécutifs, en commençant le premier jour (Jour 1 Début) de son cycle menstruel ou le dimanche suivant le début de ses règles ( Début du dimanche). (Le premier jour des menstruations est le premier jour.) Les comprimés sont ensuite interrompus pendant une semaine (7 jours). Les saignements de privation doivent généralement survenir dans les 3 jours suivant l'arrêt de Lo/Ovral et peuvent ne pas être terminés avant le début de la plaquette suivante. (Si Lo/Ovral 300mcg est pris pour la première fois après le premier jour d'un cycle menstruel ou après l'accouchement, la dépendance contraceptive ne doit pas être placée sur Lo/Ovral 300mcg avant les sept premiers jours consécutifs d'utilisation et une méthode d'accouchement complémentaire non hormonale le contrôle des naissances doit être utilisé pendant ces 7 jours. . La possibilité d'ovulation et de conception avant le début du traitement doit être envisagée.)
La patiente commence sa prochaine et toutes les cures suivantes de 21 jours de comprimés Lo/Ovral 300 mcg le même jour de la semaine qu'elle a commencé sa première cure, en suivant le même schéma : 21 jours de marche-7 jours de repos. Elle commence à prendre ses comprimés le 8e jour après le dernier comprimé de la plaquette précédente, qu'il y ait eu ou non des menstruations ou qu'elles soient toujours en cours. Si, au cours d'un cycle, la patiente commence à prendre les comprimés plus tard que le bon jour, elle doit se protéger contre la grossesse en utilisant une méthode contraceptive d'appoint non hormonale jusqu'à ce qu'elle ait pris un comprimé par jour pendant 7 jours consécutifs.
Lorsque la patiente passe d'un régime de 21 jours de comprimés, elle doit attendre 7 jours après son dernier comprimé avant de commencer Lo/Ovral. Elle aura probablement des saignements de privation au cours de cette semaine. Elle doit s'assurer qu'il ne s'écoule pas plus de 7 jours après son précédent régime de 21 jours. Lorsque la patiente passe d'un régime de comprimés de 28 jours, elle doit commencer sa première plaquette de Lo/Ovral 300 mcg le lendemain de son dernier comprimé. Elle ne devrait pas attendre des jours entre les packs. Le patient peut passer n'importe quel jour d'une pilule progestative et doit commencer Lo/Ovral le lendemain. En cas de changement d'un implant ou d'une injection, le patient doit commencer Lo/Ovral 300mcg le jour du retrait de l'implant ou le jour de la prochaine injection. Lors du passage d'une pilule, d'une injection ou d'un implant à progestatif seul, il faut conseiller à la patiente d'utiliser une méthode contraceptive d'appoint non hormonale pendant les 7 premiers jours de prise de comprimés.
En cas de spotting ou d'hémorragie intermenstruelle, le patient est invité à poursuivre le même régime. Ce type de saignement est généralement transitoire et sans importance ; cependant, si le saignement est persistant ou prolongé, il est conseillé à la patiente de consulter son professionnel de la santé. Bien qu'une grossesse soit peu probable si Lo/Ovral est pris conformément aux instructions, si l'hémorragie de privation ne se produit pas, la possibilité d'une grossesse doit être envisagée. Si la patiente n'a pas respecté le calendrier prescrit (oublié un ou plusieurs comprimés ou commencé à les prendre un jour plus tard qu'elle n'aurait dû), la probabilité de grossesse doit être envisagée au moment de la première période manquée et des mesures diagnostiques appropriées doivent être prises. . Si la patiente a adhéré au régime prescrit et manque deux règles consécutives, une grossesse doit être exclue. La contraception hormonale doit être interrompue si la grossesse est confirmée.
Pour obtenir des instructions supplémentaires pour les patients concernant les comprimés oubliés, consultez le QUE FAIRE SI VOUS MANQUEZ DES PILULES rubrique dans la ÉTIQUETAGE PATIENT DÉTAILLÉ dessous.
Chaque fois que la patiente oublie deux comprimés ou plus, elle doit également utiliser une autre méthode de contraception jusqu'à ce qu'elle ait pris un comprimé par jour pendant sept jours consécutifs. Si un saignement intermenstruel se produit suite à l'oubli de comprimés, il sera généralement transitoire et sans conséquence. La possibilité d'ovulation augmente avec chaque jour successif où les comprimés programmés sont manqués.
Lo/Ovral peut être instauré au plus tôt au 28e jour post-partum, chez la mère qui n'allaite pas ou après un avortement au cours du deuxième trimestre en raison du risque accru de thromboembolie (voir CONTRE-INDICATIONS, MISES EN GARDE, et PRECAUTIONS concernant la maladie thromboembolique ). Il doit être conseillé au patient d'utiliser une méthode d'appoint non hormonale pendant les 7 premiers jours de prise des comprimés. Cependant, si des rapports sexuels ont déjà eu lieu, une grossesse doit être exclue avant le début de l'utilisation d'un contraceptif oral combiné ou la patiente doit attendre ses premières règles. En cas d'avortement au cours du premier trimestre, si la patiente commence immédiatement Lo/Ovral 300mcg, aucune mesure contraceptive supplémentaire n'est nécessaire.
COMMENT FOURNIE
Les comprimés Lo/Ovral 300mcg (0,3 mg de norgestrel et 0,03 mg d'éthinylestradiol) sont disponibles en boîtes de 6 distributeurs PILPAK de 21 comprimés chacun comme suit :
NDC 0008-0078, comprimé blanc, rond marqué "WYETH" et "78".
Conserver à température ambiante contrôlée entre 20 °C et 25 °C (68 °F et 77 °F).
Références disponibles sur demande.
Wyeth Laboratories, A Wyeth-Ayerst Company, Philadelphie, PA 19101. Rev 07/03. Date de révision FDA : 06/03/2002
EFFETS SECONDAIRES
Un risque accru des effets indésirables graves suivants (voir AVERTISSEMENTS section pour plus d'informations) a été associée à l'utilisation de contraceptifs oraux :
Troubles thromboemboliques et thrombotiques et autres problèmes vasculaires (y compris thrombophlébite et thrombose veineuse avec ou sans embolie pulmonaire, thrombose mésentérique, thromboembolie artérielle, infarctus du myocarde, hémorragie cérébrale, thrombose cérébrale), carcinome des organes reproducteurs et des seins, néoplasie hépatique (y compris adénomes hépatiques ou tumeurs bénignes du foie), lésions oculaires (y compris thrombose vasculaire rétinienne), maladie de la vésicule biliaire, effets glucidiques et lipidiques, hypertension artérielle et céphalées, y compris migraine.
Les effets indésirables suivants ont été rapportés chez des patientes recevant des contraceptifs oraux et sont supposés être liés au médicament (classés par ordre alphabétique) :
Acné Aménorrhée Réactions anaphylactiques/anaphylactoïdes, y compris urticaire, œdème de Quincke et réactions graves accompagnées de symptômes respiratoires et circulatoires Saignements intermenstruels Modifications mammaires : sensibilité, douleur, hypertrophie, sécrétion Syndrome de Budd-Chiari Érosion et sécrétion cervicales, modification de l'ictère cholestatique Chorée, exacerbation de la colite Courbure de la cornée (pentification), modification de Diminution de la lactation en cas d'administration immédiatement après l'accouchement Étourdissements Œdème/rétention d'eau Érythème polymorphe Érythème noueux Symptômes gastro-intestinaux (tels que douleurs abdominales, crampes et ballonnements) Hirsutisme Intolérance aux lentilles de contact Libido, modifications de la Perte de cheveux Mélasma/chloasma pouvant persister Flux menstruel, modification de l'humeur Changements d'humeur, y compris dépression Nausées Nervosité Pancréatite Porphyrie, exacerbation de Rash (allergique) Taux de folate sérique, diminution de Spotting Lupus érythémateux disséminé, exacerbation de Infertilité temporaire après l'arrêt du traitement Vaginite, y compris g candidose Varices, aggravation des vomissements Poids ou appétit (augmentation ou diminution), modification de
Les effets indésirables suivants ont été rapportés chez les utilisatrices de contraceptifs oraux :
Cataractes Syndrome de type cystite Dysménorrhée Syndrome hémolytique et urémique Éruption hémorragique Névrite optique, pouvant entraîner une perte partielle ou totale de la vision Porphyrie Syndrome prémenstruel Fonction rénale, altération
INTERACTIONS MÉDICAMENTEUSES
Modifications de l'efficacité contraceptive associées à l'administration concomitante d'autres produits :
L'efficacité contraceptive peut être réduite lorsque les contraceptifs hormonaux sont co-administrés avec des antibiotiques, des anticonvulsivants et d'autres médicaments qui augmentent le métabolisme des stéroïdes contraceptifs. Cela pourrait entraîner une grossesse non désirée ou des saignements intermenstruels. Les exemples incluent la rifampine, la rifabutine, les barbituriques, la primidone, la phénylbutazone, la phénytoïne, la dexaméthasone, la carbamazépine, le felbamate, l'oxcarbazépine, le topiramate, la griséofulvine et le modafinil.
Plusieurs cas d'échec contraceptif et d'hémorragies intermenstruelles ont été rapportés dans la littérature avec l'administration concomitante d'antibiotiques tels que l'ampicilline et d'autres pénicillines, et les tétracyclines, probablement en raison d'une diminution de la recirculation entérohépatique des œstrogènes. Cependant, les études de pharmacologie clinique portant sur les interactions médicamenteuses entre les contraceptifs oraux combinés et ces antibiotiques ont rapporté des résultats incohérents. La recirculation entérohépatique des œstrogènes peut également être diminuée par des substances qui réduisent le temps de transit intestinal.
Plusieurs des inhibiteurs de la protéase anti-VIH ont été étudiés avec la co-administration de contraceptifs hormonaux combinés oraux ; des changements significatifs (augmentation et diminution) des taux plasmatiques d'œstrogène et de progestatif ont été notés dans certains cas. L'innocuité et l'efficacité des contraceptifs oraux peuvent être affectées par l'administration concomitante d'inhibiteurs de la protéase anti-VIH. Les professionnels de la santé doivent consulter l'étiquette de chaque inhibiteur de la protéase anti-VIH pour obtenir de plus amples renseignements sur les interactions médicamenteuses.
Les produits à base de plantes contenant du millepertuis (Hypericum perforatum) peuvent induire des enzymes hépatiques (cytochrome P 450) et un transporteur de glycoprotéine p et peuvent réduire l'efficacité des stéroïdes contraceptifs. Cela peut également entraîner des saignements intermenstruels.
Lors de l'utilisation concomitante de produits contenant de l'éthinylestradiol et de substances susceptibles d'entraîner une diminution des concentrations plasmatiques d'hormones stéroïdes, il est recommandé d'utiliser une méthode contraceptive d'appoint non hormonale en plus de la prise régulière de Lo/Ovral. Si l'utilisation d'une substance entraînant une diminution des concentrations plasmatiques d'éthinylestradiol est nécessaire pendant une période prolongée, les contraceptifs oraux combinés ne doivent pas être considérés comme le contraceptif principal.
Après l'arrêt des substances susceptibles d'entraîner une diminution des concentrations plasmatiques d'éthinylestradiol, l'utilisation d'une méthode contraceptive d'appoint non hormonale est recommandée pendant 7 jours. L'utilisation prolongée d'une méthode d'appoint est recommandée après l'arrêt des substances qui ont entraîné l'induction d'enzymes microsomales hépatiques, entraînant une diminution des concentrations d'éthinylestradiol. Il peut s'écouler plusieurs semaines avant que l'induction enzymatique ne disparaisse complètement, en fonction de la posologie, de la durée d'utilisation et du taux d'élimination de la substance inductrice.
Augmentation des concentrations plasmatiques associées aux médicaments co-administrés
L'administration concomitante d'atorvastatine et de certains contraceptifs oraux contenant de l'éthinylestradiol augmente les valeurs de l'ASC de l'éthinylestradiol d'environ 20 %. Le mécanisme de cette interaction est inconnu. L'acide ascorbique et l'acétaminophène augmentent la biodisponibilité de l'éthinylestradiol puisque ces médicaments agissent comme des inhibiteurs compétitifs de la sulfatation de l'éthinylestradiol dans la paroi gastro-intestinale, une voie d'élimination connue de l'éthinylestradiol. Les inhibiteurs du CYP 3A4 tels que l'indinavir, l'itraconazole, le kétoconazole, le fluconazole et la troléandomycine peuvent augmenter les taux d'hormones plasmatiques. La troléandomycine peut également augmenter le risque de cholestase intrahépatique lors de la co-administration avec des contraceptifs oraux combinés.
Modifications des concentrations plasmatiques des médicaments coadministrés :
Les contraceptifs hormonaux combinés contenant certains œstrogènes synthétiques (p. ex., l'éthinylœstradiol) peuvent inhiber le métabolisme d'autres composés. Des concentrations plasmatiques accrues de cyclosporine, de prednisolone et d'autres corticostéroïdes, et de théophylline ont été rapportées lors de l'administration concomitante de contraceptifs oraux. Une diminution des concentrations plasmatiques d'acétaminophène et une augmentation de la clairance du témazépam, de l'acide salicylique, de la morphine et de l'acide clofibrique, dues à l'induction de la conjugaison (en particulier de la glucuronidation), ont été observées lorsque ces médicaments étaient administrés avec des contraceptifs oraux.
Les informations de prescription des médicaments concomitants doivent être consultées pour identifier les interactions potentielles.
Interactions avec les tests de laboratoire
Certains tests de la fonction endocrinienne et hépatique et certains composants sanguins peuvent être affectés par les contraceptifs oraux :
AVERTISSEMENTS
Le tabagisme augmente le risque d'effets secondaires cardiovasculaires graves liés à l'utilisation de contraceptifs oraux. Ce risque augmente avec l'âge et l'importance du tabagisme (dans les études épidémiologiques, 15 cigarettes ou plus par jour étaient associées à un risque significativement accru) et est assez marqué chez les femmes de plus de 35 ans. Les femmes qui utilisent des contraceptifs oraux doivent être fortement déconseillées de fumer.
L'utilisation de contraceptifs oraux est associée à des risques accrus de plusieurs affections graves, y compris les événements thrombotiques et thromboemboliques veineux et artériels (tels que l'infarctus du myocarde, la thromboembolie et l'accident vasculaire cérébral), la néoplasie hépatique, la maladie de la vésicule biliaire et l'hypertension, bien que le risque de morbidité grave ou la mortalité est très faible chez les femmes en bonne santé sans facteurs de risque sous-jacents. Le risque de morbidité et de mortalité augmente significativement en présence d'autres facteurs de risque sous-jacents tels que certaines thrombophilies héréditaires ou acquises, l'hypertension, les hyperlipidémies, l'obésité, le diabète, la chirurgie ou les traumatismes à risque accru de thrombose.
Les praticiens prescrivant des contraceptifs oraux doivent connaître les informations suivantes relatives à ces risques.
Les informations contenues dans cette notice sont basées principalement sur des études menées chez des patientes qui utilisaient des contraceptifs oraux contenant des doses d'œstrogènes et de progestatifs plus élevées que celles couramment utilisées aujourd'hui. L'effet de l'utilisation à long terme des contraceptifs oraux avec des doses plus faibles d'œstrogènes et de progestatifs reste à déterminer.
Tout au long de cet étiquetage, les études épidémiologiques rapportées sont de deux types : les études rétrospectives ou cas-témoins et les études prospectives ou de cohorte. Les études cas-témoins fournissent une mesure du risque relatif de maladie, à savoir un rapport entre l'incidence d'une maladie chez les utilisatrices de contraceptifs oraux et celle chez les non-utilisatrices. Le risque relatif ne renseigne pas sur la survenue clinique réelle d'une maladie. Les études de cohorte fournissent une mesure du risque attribuable, c'est-à-dire la différence d'incidence de la maladie entre les utilisatrices de contraceptifs oraux et les non-utilisatrices. Le risque attribuable fournit des informations sur l'occurrence réelle d'une maladie dans la population. Pour plus d'informations, le lecteur est renvoyé à un texte sur les méthodes épidémiologiques.
Troubles thromboemboliques et autres problèmes vasculaires
Infarctus du myocarde
Un risque accru d'infarctus du myocarde a été attribué à l'utilisation de contraceptifs oraux. Ce risque concerne principalement les fumeurs ou les femmes présentant d'autres facteurs de risque sous-jacents de maladie coronarienne tels que l'hypertension, l'hypercholestérolémie, l'obésité morbide et le diabète. Le risque relatif de crise cardiaque pour les utilisatrices actuelles de contraceptifs oraux a été estimé entre deux et six. Le risque est très faible en dessous de 30 ans.
Il a été démontré que le tabagisme en association avec l'utilisation de contraceptifs oraux contribue considérablement à l'incidence des infarctus du myocarde chez les femmes dans la trentaine ou plus, le tabagisme représentant la majorité des cas excédentaires. Il a été démontré que les taux de mortalité associés aux maladies circulatoires augmentent considérablement chez les fumeuses de plus de 35 ans et les non-fumeuses de plus de 40 ans (tableau II) chez les femmes qui utilisent des contraceptifs oraux.
TAUX DE MORTALITÉ PAR MALADIE CIRCULATOIRE POUR 100 000 ANNÉES-FEMMES SELON L'ÂGE, LE STATUT DE FUMEUR ET L'UTILISATION DE CONTRACEPTIFS ORAUX 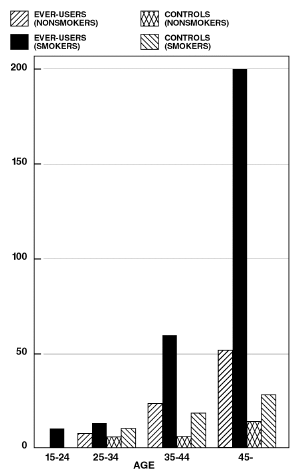
TABLEAU II. (Adapté de PM Layde et V. Beral, Lancet, 1:541-546, 1981.)
Les contraceptifs oraux peuvent aggraver les effets de facteurs de risque bien connus, tels que l'hypertension, le diabète, les hyperlipidémies, l'âge et l'obésité. En particulier, certains progestatifs sont connus pour diminuer le cholestérol HDL et provoquer une intolérance au glucose, tandis que les œstrogènes peuvent créer un état d'hyperinsulinisme. Il a été démontré que les contraceptifs oraux augmentent la tension artérielle chez les utilisatrices (voir AVERTISSEMENTS ). Des effets similaires sur les facteurs de risque ont été associés à un risque accru de maladie cardiaque. Les contraceptifs oraux doivent être utilisés avec prudence chez les femmes présentant des facteurs de risque de maladies cardiovasculaires.
Thrombose veineuse et thromboembolie
Un risque accru de maladie thromboembolique et thrombotique veineuse associé à l'utilisation de contraceptifs oraux est bien établi. Des études cas-témoins ont montré que le risque relatif des utilisatrices par rapport aux non-utilisatrices était de 3 pour le premier épisode de thrombose veineuse superficielle, de 4 à 11 pour la thrombose veineuse profonde ou l'embolie pulmonaire et de 1,5 à 6 pour les femmes présentant des conditions prédisposant à la maladie thromboembolique veineuse. . Des études de cohorte ont montré que le risque relatif était un peu plus faible, environ 3 pour les nouveaux cas et environ 4,5 pour les nouveaux cas nécessitant une hospitalisation. L'incidence approximative de thrombose veineuse profonde et d'embolie pulmonaire chez les utilisatrices de contraceptifs oraux combinés à faible dose (
Une augmentation de deux à quatre fois du risque relatif de complications thromboemboliques postopératoires a été rapportée avec l'utilisation de contraceptifs oraux. Le risque relatif de thrombose veineuse chez les femmes qui ont des conditions prédisposantes est le double de celui des femmes sans ces conditions médicales. Si possible, les contraceptifs oraux doivent être interrompus au moins quatre semaines avant et pendant deux semaines après une chirurgie élective d'un type associé à une augmentation du risque thromboembolique et pendant et après une immobilisation prolongée. Étant donné que la période post-partum immédiate est également associée à un risque accru de thromboembolie, les contraceptifs oraux doivent être commencés au plus tôt quatre semaines après l'accouchement chez les femmes qui choisissent de ne pas allaiter ou une interruption de grossesse au milieu du trimestre.
Maladies cérébrovasculaires
Il a été démontré que les contraceptifs oraux augmentent à la fois les risques relatifs et attribuables d'événements cérébrovasculaires (accidents vasculaires cérébraux thrombotiques et hémorragiques), bien que, en général, le risque soit le plus élevé chez les femmes hypertendues plus âgées (> 35 ans) qui fument également. L'hypertension s'est avérée être un facteur de risque pour les utilisateurs et les non-utilisateurs, pour les deux types d'AVC, tandis que le tabagisme interagissait pour augmenter le risque d'AVC hémorragique.
Dans une vaste étude, il a été démontré que le risque relatif d'accident vasculaire cérébral thrombotique variait de 3 pour les utilisateurs normotendus à 14 pour les utilisateurs souffrant d'hypertension sévère. Le risque relatif d'AVC hémorragique serait de 1,2 pour les non-fumeuses qui utilisaient des contraceptifs oraux, de 2,6 pour les fumeuses qui n'utilisaient pas de contraceptifs oraux, de 7,6 pour les fumeuses qui utilisaient des contraceptifs oraux, de 1,8 pour les utilisatrices normotendues et de 25,7 pour les utilisatrices souffrant d'hypertension sévère. Le risque attribuable est également plus élevé chez les femmes âgées. Les contraceptifs oraux augmentent également le risque d'accident vasculaire cérébral chez les femmes présentant d'autres facteurs de risque sous-jacents tels que certaines thrombophilies héréditaires ou acquises, les hyperlipidémies et l'obésité.
Femmes souffrant de migraine (en particulier migraine/maux de tête avec symptômes neurologiques focaux, voir CONTRE-INDICATIONS ) qui prennent des contraceptifs oraux combinés peuvent présenter un risque accru d'accident vasculaire cérébral.
Risque lié à la dose de maladie vasculaire des contraceptifs oraux
Une association positive a été observée entre la quantité d'oestrogène et de progestatif dans les contraceptifs oraux et le risque de maladie vasculaire. Une diminution des lipoprotéines de haute densité (HDL) sériques a été rapportée avec de nombreux agents progestatifs. Une diminution des lipoprotéines sériques de haute densité a été associée à une incidence accrue de cardiopathie ischémique. Étant donné que les œstrogènes augmentent le cholestérol HDL, l'effet net d'un contraceptif oral dépend de l'équilibre atteint entre les doses d'œstrogène et de progestatif et de la nature et de la quantité absolue de progestatif utilisé dans le contraceptif. La quantité des deux hormones doit être prise en compte dans le choix d'un contraceptif oral.
Minimiser l'exposition aux œstrogènes et aux progestatifs est conforme aux bons principes thérapeutiques. Pour toute combinaison oestrogène/progestatif particulière, le schéma posologique prescrit doit être celui qui contient le moins d'oestrogène et de progestatif compatible avec un faible taux d'échec et les besoins de chaque patient. Les nouveaux accepteurs d'agents contraceptifs oraux doivent commencer par des préparations contenant la plus faible teneur en œstrogènes jugée appropriée pour chaque patiente.
Persistance du risque de maladie vasculaire
Deux études ont montré la persistance du risque de maladie vasculaire pour les utilisatrices de contraceptifs oraux. Dans une étude aux États-Unis, le risque de développer un infarctus du myocarde après l'arrêt des contraceptifs oraux persiste pendant au moins 9 ans pour les femmes de 40 à 49 ans qui ont utilisé des contraceptifs oraux pendant cinq ans ou plus, mais ce risque accru n'a pas été démontré dans d'autres les groupes d'âge. Dans une autre étude en Grande-Bretagne, le risque de développer une maladie cérébrovasculaire a persisté pendant au moins 6 ans après l'arrêt des contraceptifs oraux, bien que l'excès de risque ait été très faible. Cependant, les deux études ont été réalisées avec des formulations de contraceptifs oraux contenant 50 mcg ou plus d'œstrogène.
Estimations de la mortalité due à l'utilisation de contraceptifs
Une étude a recueilli des données provenant de diverses sources qui ont estimé le taux de mortalité associé à différentes méthodes de contraception à différents âges (tableau III). Ces estimations incluent le risque combiné de décès associé aux méthodes contraceptives plus le risque attribuable à la grossesse en cas d'échec de la méthode. Chaque méthode de contraception a ses avantages et ses risques spécifiques. L'étude a conclu qu'à l'exception des utilisatrices de contraceptifs oraux de 35 ans et plus qui fument et de 40 ans et plus qui ne fument pas, la mortalité associée à toutes les méthodes de contraception est inférieure à celle associée à l'accouchement. L'observation d'une augmentation possible du risque de mortalité avec l'âge chez les utilisatrices de contraceptifs oraux est basée sur des données recueillies dans les années 1970, mais non rapportées avant 1983. Cependant, la pratique clinique actuelle implique l'utilisation de formulations à faible dose d'œstrogènes combinées à une restriction prudente de l'utilisation de contraceptifs oraux chez les femmes qui ne présentent pas les différents facteurs de risque listés dans cet étiquetage.
En raison de ces changements dans la pratique et, également, en raison de certaines nouvelles données limitées qui suggèrent que le risque de maladie cardiovasculaire associé à l'utilisation de contraceptifs oraux pourrait maintenant être inférieur à celui observé précédemment, le comité consultatif sur la fertilité et la santé maternelle a été chargé d'examiner le sujet en 1989. Le comité a conclu que bien que les risques de maladies cardiovasculaires puissent être accrus avec l'utilisation de contraceptifs oraux après l'âge de 40 ans chez les femmes non fumeuses en bonne santé (même avec les nouvelles formulations à faible dose), les risques potentiels pour la santé associés à la grossesse sont plus élevés chez les femmes. les femmes âgées et avec les procédures chirurgicales et médicales alternatives qui peuvent être nécessaires si ces femmes n'ont pas accès à des moyens de contraception efficaces et acceptables.
Par conséquent, le Comité a recommandé que les avantages de l'utilisation de contraceptifs oraux par les femmes non fumeuses en bonne santé de plus de 40 ans puissent l'emporter sur les risques éventuels. Bien sûr, les femmes âgées, comme toutes les femmes qui prennent des contraceptifs oraux, doivent prendre la formulation à la dose la plus faible possible qui soit efficace.
TABLEAU III-NOMBRE ANNUEL DE DÉCÈS LIÉS À LA NAISSANCE OU À LA MÉTHODE ASSOCIÉS AU CONTRÔLE DE LA FÉCONDITÉ POUR 100 000 FEMMES NON STÉRILES, PAR MÉTHODE DE CONTRÔLE DE LA FÉCONDITÉ ET SELON L'ÂGE
Carcinome des organes reproducteurs et des seins
De nombreuses études épidémiologiques ont examiné l'association entre l'utilisation de contraceptifs oraux et l'incidence du cancer du sein et du col de l'utérus.
Le risque de recevoir un diagnostic de cancer du sein peut être légèrement accru chez les utilisatrices actuelles et récentes de COC. Cependant, cet excès de risque semble diminuer avec le temps après l'arrêt du COC et 10 ans après l'arrêt, le risque accru disparaît. Certaines études rapportent un risque accru avec la durée d'utilisation tandis que d'autres études ne le font pas et aucune relation cohérente n'a été trouvée avec la dose ou le type de stéroïde. Certaines études ont signalé une légère augmentation du risque chez les femmes qui utilisent les COC pour la première fois à un plus jeune âge. La plupart des études montrent un schéma de risque similaire avec l'utilisation de COC, quels que soient les antécédents de reproduction de la femme ou ses antécédents familiaux de cancer du sein.
Les cancers du sein diagnostiqués chez les utilisatrices actuelles ou antérieures de CO ont tendance à être moins avancés sur le plan clinique que chez les non-utilisatrices.
Les femmes atteintes d'un cancer du sein connu ou suspecté ou ayant des antécédents personnels de cancer du sein ne doivent pas utiliser de contraceptifs oraux car le cancer du sein est généralement une tumeur sensible aux hormones.
Certaines études suggèrent que l'utilisation de contraceptifs oraux a été associée à une augmentation du risque de néoplasie cervicale intraépithéliale ou de cancer invasif du col de l'utérus dans certaines populations de femmes. Cependant, il continue d'y avoir une controverse sur la mesure dans laquelle ces résultats peuvent être dus à des différences de comportement sexuel et à d'autres facteurs.
Malgré de nombreuses études sur la relation entre l'utilisation combinée de contraceptifs oraux et les cancers du sein et du col de l'utérus, une relation de cause à effet n'a pas été établie.
Néoplasie hépatique
Les adénomes hépatiques bénins sont associés à l'utilisation de contraceptifs oraux, bien que l'incidence des tumeurs bénignes soit rare aux États-Unis. Des calculs indirects ont estimé que le risque attribuable était de l'ordre de 3,3 cas/100 000 pour les utilisateurs, un risque qui augmente après quatre ans ou plus d'utilisation. La rupture d'adénomes hépatiques rares et bénins peut entraîner la mort par hémorragie intra-abdominale.
Des études britanniques ont montré un risque accru de développer un carcinome hépatocellulaire chez les utilisatrices de contraceptifs oraux à long terme (> 8 ans).
Cependant, ces cancers sont extrêmement rares aux États-Unis, et le risque attribuable (l'incidence excessive) de cancers du foie chez les utilisatrices de contraceptifs oraux approche moins d'un par million d'utilisatrices.
Lésions oculaires
Il y a eu des rapports de cas cliniques de thrombose rétinienne associée à l'utilisation de contraceptifs oraux pouvant entraîner une perte partielle ou complète de la vision. Les contraceptifs oraux doivent être arrêtés en cas de perte de vision partielle ou complète inexpliquée ; apparition d'exophtalmie ou de diplopie ; œdème papillaire; ou des lésions vasculaires rétiniennes. Des mesures diagnostiques et thérapeutiques appropriées doivent être prises immédiatement.
Utilisation de contraceptifs oraux avant ou pendant la grossesse précoce
Des études épidémiologiques approfondies n'ont révélé aucun risque accru de malformations congénitales chez les nourrissons nés de femmes ayant utilisé des contraceptifs oraux avant la grossesse. Les études ne suggèrent pas non plus d'effet tératogène, notamment en ce qui concerne les anomalies cardiaques et les défauts de réduction des membres, en cas de prise par inadvertance en début de grossesse (voir Rubrique CONTRE-INDICATIONS ).
L'administration de contraceptifs oraux pour induire une hémorragie de privation ne doit pas être utilisée comme test de grossesse. Les contraceptifs oraux ne doivent pas être utilisés pendant la grossesse pour traiter la menace d'avortement ou l'avortement habituel.
Il est recommandé que pour tout patient qui a manqué deux règles consécutives, une grossesse soit exclue avant de continuer à utiliser un contraceptif oral. Si la patiente n'a pas respecté le calendrier prescrit, la possibilité d'une grossesse doit être envisagée au moment de la première période manquée. L'utilisation de contraceptifs oraux doit être interrompue si la grossesse est confirmée.
Maladie de la vésicule biliaire
Les contraceptifs oraux combinés peuvent aggraver une maladie de la vésicule biliaire existante et accélérer le développement de cette maladie chez des femmes auparavant asymptomatiques. Des études antérieures ont rapporté une augmentation du risque relatif à vie de chirurgie de la vésicule biliaire chez les utilisatrices de contraceptifs oraux et d'œstrogènes. Cependant, des études plus récentes ont montré que le risque relatif de développer une maladie de la vésicule biliaire chez les utilisatrices de contraceptifs oraux peut être minime. Les découvertes récentes de risque minimal peuvent être liées à l'utilisation de formulations contraceptives orales contenant des doses hormonales plus faibles d'œstrogènes et de progestatifs.
Effets métaboliques des glucides et des lipides
Il a été démontré que les contraceptifs oraux provoquent une intolérance au glucose chez un pourcentage important d'utilisateurs. Les contraceptifs oraux contenant plus de 75 mcg d'œstrogènes provoquent un hyperinsulinisme, tandis que des doses plus faibles d'œstrogènes provoquent moins d'intolérance au glucose. Les progestatifs augmentent la sécrétion d'insuline et créent une résistance à l'insuline, cet effet variant selon les différents agents progestatifs. Cependant, chez la femme non diabétique, les contraceptifs oraux semblent n'avoir aucun effet sur la glycémie à jeun. En raison de ces effets démontrés, les femmes prédiabétiques et diabétiques doivent être étroitement surveillées pendant la prise de contraceptifs oraux.
Une petite proportion de femmes auront une hypertriglycéridémie persistante pendant qu'elles prennent la pilule. Comme discuté précédemment (voir AVERTISSEMENTS, et PRÉCAUTIONS ), des modifications des taux sériques de triglycérides et de lipoprotéines ont été signalées chez des utilisatrices de contraceptifs oraux.
Tension artérielle élevée
Les femmes souffrant d'hypertension non contrôlée ne doivent pas commencer la contraception hormonale. Une augmentation de la pression artérielle a été signalée chez les femmes prenant des contraceptifs oraux, et cette augmentation est plus probable chez les utilisatrices de contraceptifs oraux plus âgées et en cas d'utilisation continue. Les données du Royal College of General Practitioners et des essais randomisés ultérieurs ont montré que l'incidence de l'hypertension augmente avec l'augmentation des quantités de progestatifs.
Les femmes ayant des antécédents d'hypertension ou de maladies liées à l'hypertension, ou de maladie rénale, doivent être encouragées à utiliser une autre méthode de contraception. Si les femmes souffrant d'hypertension choisissent d'utiliser des contraceptifs oraux, elles doivent être étroitement surveillées et, en cas d'élévation significative de la pression artérielle, les contraceptifs oraux doivent être arrêtés (voir Rubrique CONTRE-INDICATIONS ). Pour la plupart des femmes, une tension artérielle élevée reviendra à la normale après l'arrêt des contraceptifs oraux, et il n'y a pas de différence dans la survenue d'hypertension entre les utilisatrices et les non-utilisatrices.
Mal de tête
L'apparition ou l'exacerbation d'une migraine ou le développement d'une céphalée avec un nouveau schéma récurrent, persistant ou sévère nécessite l'arrêt des contraceptifs oraux et l'évaluation de la cause. (Voir AVERTISSEMENTS et CONTRE-INDICATIONS. )
Irrégularités de saignement
Des saignements intermenstruels et des spottings sont parfois rencontrés chez les patientes sous contraceptifs oraux, en particulier au cours des trois premiers mois d'utilisation. Le type et la dose de progestatif peuvent être importants. Si le saignement persiste ou se reproduit, des causes non hormonales doivent être envisagées et des mesures diagnostiques adéquates doivent être prises pour exclure une tumeur maligne ou une grossesse en cas de saignement intermenstruel, comme dans le cas de tout saignement vaginal anormal. Si la pathologie a été exclue, le temps ou un changement vers une autre formulation peut résoudre le problème. Chez certaines femmes, les saignements de privation peuvent ne pas se produire pendant l'intervalle « sans comprimé » ou « sans comprimé actif ». Si le COC n'a pas été pris conformément aux instructions avant la première hémorragie de privation manquée, ou si deux hémorragies de privation consécutives sont manquées, la prise de comprimés doit être interrompue et une méthode de contraception non hormonale doit être utilisée jusqu'à ce que la possibilité d'une grossesse soit exclue.
Certaines femmes peuvent rencontrer une aménorrhée ou une oligoménorrhée post-pilule (éventuellement avec anovulation), en particulier lorsqu'une telle condition était préexistante.
Grossesse extra-utérine
Des grossesses extra-utérines et intra-utérines peuvent survenir en cas d'échec de la contraception.
PRÉCAUTIONS
Général
Les patients doivent être informés que les contraceptifs oraux ne protègent pas contre la transmission du VIH (SIDA) et d'autres maladies sexuellement transmissibles (MST) telles que la chlamydia, l'herpès génital, les verrues génitales, la gonorrhée, l'hépatite B et la syphilis.
Examen physique et suivi
Un historique médical personnel et familial périodique et un examen physique complet sont appropriés pour toutes les femmes, y compris les femmes utilisant des contraceptifs oraux. L'examen physique, cependant, peut être reporté jusqu'après le début des contraceptifs oraux si demandé par la femme et jugé approprié par le clinicien. L'examen physique doit inclure une référence particulière à la pression artérielle, aux seins, à l'abdomen et aux organes pelviens, y compris la cytologie cervicale, et les tests de laboratoire pertinents. En cas de saignements vaginaux anormaux non diagnostiqués, persistants ou récurrents, des mesures diagnostiques appropriées doivent être prises pour exclure une malignité. Les femmes ayant de forts antécédents familiaux de cancer du sein ou qui présentent des nodules mammaires doivent faire l'objet d'une surveillance particulière.
Troubles lipidiques
Les femmes qui sont traitées pour des hyperlipidémies doivent être suivies de près si elles choisissent d'utiliser des contraceptifs oraux. Certains progestatifs peuvent élever les taux de LDL et rendre plus difficile le contrôle des hyperlipidémies. (Voir AVERTISSEMENTS )
Chez les patients présentant des anomalies du métabolisme des lipoprotéines, les préparations contenant des œstrogènes peuvent être associées à des élévations rares mais significatives des triglycérides plasmatiques pouvant entraîner une pancréatite.
La fonction hépatique
Si la jaunisse se développe chez une femme recevant des contraceptifs hormonaux, le médicament doit être interrompu. Les hormones stéroïdes peuvent être mal métabolisées chez les patients présentant une fonction hépatique altérée.
Rétention d'eau
Les contraceptifs oraux peuvent provoquer un certain degré de rétention d'eau. Ils doivent être prescrits avec prudence, et uniquement avec une surveillance étroite, chez les patients présentant des affections susceptibles d'être aggravées par une rétention hydrique.
Troubles émotionnels
Les patients qui deviennent significativement déprimés pendant qu'ils prennent des contraceptifs oraux doivent arrêter le médicament et utiliser une autre méthode de contraception afin de déterminer si le symptôme est lié au médicament. Les femmes ayant des antécédents de dépression doivent être étroitement surveillées et le médicament doit être interrompu en cas de dépression importante.
Lentilles de contact
Les porteurs de lentilles de contact qui développent des changements visuels ou des changements dans la tolérance des lentilles doivent être évalués par un ophtalmologiste.
Gastro-intestinal
La diarrhée et/ou les vomissements peuvent réduire l'absorption hormonale entraînant une diminution des concentrations sériques.
Carcinogenèse
Voir Rubrique AVERTISSEMENTS.
Grossesse
Catégorie de grossesse X. Voir CONTRE-INDICATIONS et Rubriques AVERTISSEMENTS.
Mères allaitantes
De petites quantités de stéroïdes contraceptifs oraux et/ou de métabolites ont été identifiées dans le lait des mères allaitantes, et quelques effets indésirables sur l'enfant ont été signalés, notamment la jaunisse et l'hypertrophie mammaire. De plus, les contraceptifs oraux combinés administrés pendant la période post-partum peuvent interférer avec la lactation en diminuant la quantité et la qualité du lait maternel. Si possible, il faut conseiller à la mère qui allaite de ne pas utiliser de contraceptifs oraux combinés mais d'utiliser d'autres formes de contraception jusqu'à ce qu'elle ait complètement sevré son enfant.
Fertilité après l'arrêt
Les utilisatrices de contraceptifs oraux combinés peuvent éprouver un certain retard dans la grossesse après l'arrêt des COC, en particulier les femmes qui avaient des cycles menstruels irréguliers avant l'utilisation. La conception peut être retardée en moyenne de 1 à 2 mois chez les femmes arrêtant les COC par rapport aux femmes arrêtant les méthodes contraceptives non hormonales.
Il faut conseiller aux femmes qui ne souhaitent pas tomber enceintes après l'arrêt des COC d'utiliser une autre méthode de contraception.
Utilisation pédiatrique
L'innocuité et l'efficacité des comprimés de Lo/Ovral ont été établies chez les femmes en âge de procréer. L'innocuité et l'efficacité devraient être les mêmes pour les adolescents postpubères de moins de 16 ans et pour les utilisateurs de 16 ans et plus. L'utilisation de ce produit avant la ménarche n'est pas indiquée.
Utilisation gériatrique
Ce produit n'a pas été étudié chez les femmes de plus de 65 ans et n'est pas indiqué dans cette population.
Informations pour le patient
Voir Étiquetage des patients .
SURDOSAGE
Les symptômes de surdosage de contraceptifs oraux chez les adultes et les enfants peuvent inclure des nausées, des vomissements et de la somnolence/fatigue; une hémorragie de privation peut survenir chez les femmes. Il n'y a pas d'antidote spécifique et un traitement supplémentaire du surdosage, si nécessaire, est dirigé vers les symptômes.
Avantages pour la santé non contraceptifs
Les avantages pour la santé non contraceptifs suivants liés à l'utilisation de contraceptifs oraux sont étayés par des études épidémiologiques qui ont largement utilisé des formulations de contraceptifs oraux contenant des doses supérieures à 0,035 mg d'éthinylestradiol ou 0,05 mg de mestranol.
Effets sur les règles :
Augmentation de la régularité du cycle menstruel Diminution des pertes sanguines et diminution de l'incidence de l'anémie ferriprive Diminution de l'incidence de la dysménorrhée
Effets liés à l'inhibition de l'ovulation :
Diminution de l'incidence des kystes ovariens fonctionnels Diminution de l'incidence des grossesses extra-utérines
Effets d'une utilisation à long terme :
Diminution de l'incidence des fibroadénomes et des maladies fibrokystiques du sein Diminution de l'incidence des maladies inflammatoires pelviennes aiguës Diminution de l'incidence du cancer de l'endomètre Diminution de l'incidence du cancer de l'ovaire
CONTRE-INDICATIONS
Les contraceptifs oraux combinés ne doivent pas être utilisés chez les femmes présentant l'une des conditions suivantes :
Thrombophlébite ou troubles thromboemboliques Antécédents de thrombophlébite veineuse profonde ou de troubles thromboemboliques Maladie cérébro-vasculaire ou coronarienne (actuelle ou antérieure) Valvulopathies thrombogènes Troubles du rythme thrombogène Chirurgie majeure avec immobilisation prolongée Diabète avec atteinte vasculaire Céphalées avec symptômes neurologiques focaux Hypertension non contrôlée Connue ou carcinome du sein suspecté ou antécédents personnels de cancer du sein Carcinome de l'endomètre ou autre néoplasie dépendante des œstrogènes connue ou suspectée Hémorragie génitale anormale non diagnostiquée Ictère cholestatique de la grossesse ou ictère avec prise antérieure de pilule Adénomes ou carcinomes hépatiques, ou maladie car la fonction hépatique n'est pas revenue à la normale Grossesse connue ou suspectée Hypersensibilité à l'un des composants de Lo/Ovral
PHARMACOLOGIE CLINIQUE
Mode d'action
Les contraceptifs oraux combinés agissent par suppression des gonadotrophines. Bien que le principal mécanisme de cette action soit l'inhibition de l'ovulation, d'autres altérations comprennent des modifications de la glaire cervicale (qui augmentent la difficulté d'entrée des spermatozoïdes dans l'utérus) et de l'endomètre (qui réduisent la probabilité d'implantation).
INFORMATIONS PATIENTS
Ce produit (comme tous les contraceptifs oraux) est destiné à prévenir la grossesse. Les contraceptifs oraux ne protègent pas contre la transmission du VIH (SIDA) et d'autres maladies sexuellement transmissibles (MST) telles que la chlamydia, l'herpès génital, les verrues génitales, la gonorrhée, l'hépatite B et la syphilis.
Les contraceptifs oraux, également connus sous le nom de « pilules contraceptives » ou « la pilule », sont pris pour prévenir la grossesse et, lorsqu'ils sont pris correctement, ont un taux d'échec d'environ 1 % par an lorsqu'ils sont pris sans oublier de pilule. Le taux d'échec moyen est d'environ 5 % par an si l'on inclut les femmes qui oublient de prendre la pilule. Pour la plupart des femmes, les contraceptifs oraux sont également exempts d'effets secondaires graves ou désagréables. Cependant, oublier de prendre des pilules augmente considérablement les chances de grossesse.
Pour la majorité des femmes, les contraceptifs oraux peuvent être pris en toute sécurité. Mais certaines femmes courent un risque élevé de développer certaines maladies graves pouvant mettre leur vie en danger ou entraîner une invalidité temporaire ou permanente ou la mort. Les risques associés à la prise de contraceptifs oraux augmentent considérablement si vous :
- fumée
- avez une pression artérielle élevée, du diabète, un taux de cholestérol élevé ou une tendance à former des caillots sanguins, ou êtes obèse
- avez ou avez eu des troubles de la coagulation, une crise cardiaque, un accident vasculaire cérébral, une angine de poitrine, un cancer du sein ou des organes sexuels, une jaunisse, des tumeurs hépatiques malignes ou bénignes ou une intervention chirurgicale majeure avec immobilisation prolongée
- avez des maux de tête avec des symptômes neurologiques
Vous ne devez pas prendre la pilule si vous pensez être enceinte ou si vous avez des saignements vaginaux inexpliqués.
Le tabagisme augmente le risque d'effets indésirables graves sur le cœur et les vaisseaux sanguins liés à l'utilisation de contraceptifs oraux. Ce risque augmente avec l'âge et la quantité de tabac (15 cigarettes ou plus par jour ont été associées à un risque significativement accru) et est assez marqué chez les femmes de plus de 35 ans. Les femmes qui utilisent des contraceptifs oraux ne doivent pas fumer.
La plupart des effets secondaires de la pilule ne sont pas graves. Les effets les plus courants sont les nausées, les vomissements, les saignements entre les menstruations, la prise de poids, la sensibilité des seins et la difficulté à porter des lentilles de contact. Ces effets secondaires, en particulier les nausées et les vomissements, peuvent s'atténuer au cours des trois premiers mois d'utilisation.
Les effets secondaires graves de la pilule surviennent très rarement, surtout si vous êtes en bonne santé et que vous ne fumez pas. Cependant, vous devez savoir que les conditions médicales suivantes ont été associées ou aggravées par la pilule :
Les symptômes associés à ces effets secondaires graves sont décrits dans la notice détaillée qui vous est remise avec votre réserve de pilules. Avertissez votre professionnel de la santé si vous remarquez des troubles physiques inhabituels pendant que vous prenez la pilule. De plus, des médicaments comme la rifampicine, ainsi que certains anticonvulsivants et certains antibiotiques, des préparations à base de plantes contenant du millepertuis (Hypericum perforatum) et des médicaments contre le VIH/sida peuvent diminuer l'efficacité de la contraception orale.
Diverses études donnent des rapports contradictoires sur la relation entre le cancer du sein et l'utilisation de contraceptifs oraux.
L'utilisation de contraceptifs oraux peut augmenter légèrement vos chances de recevoir un diagnostic de cancer du sein, en particulier si vous avez commencé à utiliser des contraceptifs hormonaux à un plus jeune âge.
Après avoir cessé d'utiliser des contraceptifs hormonaux, les chances d'avoir un diagnostic de cancer du sein commencent à diminuer et disparaissent 10 ans après l'arrêt de la pilule. On ne sait pas si ce risque légèrement accru de diagnostic de cancer du sein est causé par la pilule. Il se peut que les femmes prenant la pilule aient été examinées plus souvent, de sorte que le cancer du sein était plus susceptible d'être détecté.
Vous devriez vous faire examiner régulièrement les seins par un professionnel de la santé et examiner vos propres seins une fois par mois. Dites à votre professionnel de la santé si vous avez des antécédents familiaux de cancer du sein ou si vous avez eu des nodules mammaires ou une mammographie anormale. Les femmes qui ont actuellement ou ont eu un cancer du sein ne doivent pas utiliser de contraceptifs oraux car le cancer du sein est généralement une tumeur hormono-sensible.
Certaines études ont trouvé une augmentation de l'incidence du cancer du col de l'utérus chez les femmes qui utilisent des contraceptifs oraux. Cependant, ce résultat peut être lié à des facteurs autres que l'utilisation de contraceptifs oraux. Il n'y a pas suffisamment de preuves pour exclure la possibilité que la pilule puisse causer de tels cancers.
La prise de la pilule combinée offre d'importants avantages non contraceptifs pour la santé. Ceux-ci incluent des menstruations moins douloureuses, moins de pertes de sang menstruelles et d'anémie, moins d'infections pelviennes et moins de cancers de l'ovaire et de la muqueuse de l'utérus.
Assurez-vous de discuter de toute condition médicale que vous pourriez avoir avec votre professionnel de la santé. Votre professionnel de la santé examinera vos antécédents médicaux et familiaux avant de vous prescrire des contraceptifs oraux et vous examinera. L'examen physique peut être reporté à un autre moment si vous en faites la demande et que le professionnel de la santé juge opportun de le reporter. Vous devez être réexaminée au moins une fois par an pendant que vous prenez des contraceptifs oraux. La notice d'information détaillée du patient vous donne des informations supplémentaires que vous devriez lire et discuter avec votre professionnel de la santé.
Ce produit (comme tous les contraceptifs oraux) est destiné à prévenir la grossesse. Il ne protège pas contre la transmission du VIH (SIDA) et d'autres maladies sexuellement transmissibles telles que la chlamydia, l'herpès génital, les verrues génitales, la gonorrhée, l'hépatite B et la syphilis.
ÉTIQUETAGE PATIENT DÉTAILLÉ
Ce produit (comme tous les contraceptifs oraux) est destiné à prévenir la grossesse. Les contraceptifs oraux ne protègent pas contre la transmission du VIH (SIDA) et d'autres maladies sexuellement transmissibles (MST) telles que la chlamydia, l'herpès génital, les verrues génitales, la gonorrhée, l'hépatite B et la syphilis.
INTRODUCTION
Toute femme qui envisage d'utiliser des contraceptifs oraux (la « pilule contraceptive » ou « la pilule ») doit comprendre les avantages et les risques de l'utilisation de cette forme de contraception. Cette notice vous fournira une grande partie des informations dont vous aurez besoin pour prendre cette décision et vous aidera également à déterminer si vous êtes à risque de développer l'un des effets secondaires graves de la pilule. Il vous indiquera comment prendre correctement la pilule afin qu'elle soit la plus efficace possible. Cependant, cette notice ne remplace pas une discussion approfondie entre vous et votre professionnel de la santé. Vous devez discuter des informations fournies dans cette notice avec lui, à la fois lorsque vous commencez à prendre la pilule et lors de vos visites de suivi. Vous devez également suivre les conseils de votre professionnel de la santé concernant les contrôles réguliers pendant que vous prenez la pilule.
EFFICACITÉ DES CONTRACEPTIFS ORAUX
Les contraceptifs oraux ou « pilules contraceptives » ou « la pilule » sont utilisés pour prévenir la grossesse et sont plus efficaces que la plupart des autres méthodes de contraception non chirurgicales. Lorsqu'elles sont prises correctement sans oublier de pilule, le risque de tomber enceinte est d'environ 1 % par an. Les taux d'échec moyens sont d'environ 5 % par an si l'on inclut les femmes qui oublient de prendre la pilule. La chance de devenir enceinte augmente avec chaque pilule oubliée pendant le cycle menstruel.
En comparaison, les taux d'échec moyens des autres méthodes de contraception au cours de la première année d'utilisation sont les suivants :
QUI NE DEVRAIT PAS PRENDRE DE CONTRACEPTIFS ORAUX
Le tabagisme augmente le risque d'effets indésirables graves sur le cœur et les vaisseaux sanguins liés à l'utilisation de contraceptifs oraux. Ce risque augmente avec l'âge et la quantité de tabac (15 cigarettes ou plus par jour ont été associées à un risque significativement accru) et est assez marqué chez les femmes de plus de 35 ans. Les femmes qui utilisent des contraceptifs oraux ne doivent pas fumer.
Certaines femmes ne devraient pas prendre la pilule. Vous ne devez pas prendre la pilule si vous avez l'une des conditions suivantes :
- Antécédents de crise cardiaque ou d'accident vasculaire cérébral
- Antécédents de caillots sanguins dans les jambes (thrombophlébite), les poumons (embolie pulmonaire) ou les yeux
- Antécédents de caillots sanguins dans les veines profondes de vos jambes
- Cancer du sein connu ou suspecté ou cancer de la muqueuse de l'utérus, du col de l'utérus ou du vagin ou certains cancers sensibles aux hormones
- Tumeur du foie (bénigne ou cancéreuse)
- Douleur thoracique (angine de poitrine)
- Saignements vaginaux inexpliqués (jusqu'à ce qu'un diagnostic soit établi par votre professionnel de la santé)
- Jaunissement du blanc des yeux ou de la peau (jaunisse) pendant la grossesse ou lors de l'utilisation précédente de la pilule
- Grossesse connue ou suspectée
- Troubles des valves cardiaques ou du rythme cardiaque pouvant être associés à la formation de caillots sanguins
- Diabète affectant votre circulation
- Maux de tête avec symptômes neurologiques
- Hypertension artérielle non contrôlée
- Maladie hépatique active avec tests anormaux de la fonction hépatique
- Allergie ou hypersensibilité à l'un des composants de Lo/Ovral
- Un besoin de chirurgie avec alitement prolongé
Dites à votre professionnel de la santé si vous avez l'une de ces conditions. Votre professionnel de la santé peut vous recommander une autre méthode de contraception.
AUTRES CONSIDÉRATIONS AVANT DE PRENDRE DES CONTRACEPTIFS ORAUX
Dites à votre professionnel de la santé si vous ou un membre de votre famille avez déjà eu :
- Nodules mammaires, maladie fibrokystique du sein, radiographie mammaire anormale ou mammographie
- Diabète
- Taux élevé de cholestérol ou de triglycérides
- Hypertension artérielle
- Une tendance à former des caillots sanguins
- Migraine ou autres maux de tête ou épilepsie
- La dépression
- Maladie de la vésicule biliaire, du foie, du cœur ou des reins
- Antécédents de menstruations rares ou irrégulières
Les femmes atteintes de l'une de ces conditions doivent être souvent contrôlées par leur professionnel de la santé si elles choisissent d'utiliser des contraceptifs oraux. Assurez-vous également d'informer votre professionnel de la santé si vous fumez ou prenez des médicaments.
RISQUES LIÉS À LA PRISE DE CONTRACEPTIFS ORAUX
1. Risque de développer des caillots sanguins
Les caillots sanguins et l'obstruction des vaisseaux sanguins sont les effets secondaires les plus graves de la prise de contraceptifs oraux et peuvent entraîner la mort ou une invalidité grave. En particulier, un caillot dans les jambes peut provoquer une thrombophlébite et un caillot qui se déplace vers les poumons peut provoquer un blocage soudain du vaisseau transportant le sang vers les poumons. Rarement, des caillots se forment dans les vaisseaux sanguins de l'œil et peuvent provoquer la cécité, une vision double ou une vision altérée.
Les utilisateurs de COC ont un risque plus élevé de développer des caillots sanguins que les non-utilisateurs. Ce risque est le plus élevé au cours de la première année d'utilisation des COC.
Si vous prenez des contraceptifs oraux et avez besoin d'une intervention chirurgicale non urgente, si vous devez rester au lit pour une maladie ou une blessure prolongée, ou si vous avez récemment accouché, vous risquez de développer des caillots sanguins. Vous devriez consulter votre professionnel de la santé au sujet de l'arrêt des contraceptifs oraux trois à quatre semaines avant la chirurgie et de ne pas prendre de contraceptifs oraux pendant deux semaines après la chirurgie ou pendant le repos au lit. Vous ne devez pas non plus prendre de contraceptifs oraux peu de temps après l'accouchement d'un bébé ou une interruption de grossesse au milieu du trimestre. Il est conseillé d'attendre au moins quatre semaines après l'accouchement si vous n'allaitez pas. Si vous allaitez, vous devez attendre d'avoir sevré votre enfant avant d'utiliser la pilule. (Voir aussi la section sur l'allaitement au sein PRÉCAUTIONS GÉNÉRALES. )
2. Crises cardiaques et accidents vasculaires cérébraux
Les contraceptifs oraux peuvent augmenter la tendance à développer des accidents vasculaires cérébraux (arrêt ou rupture des vaisseaux sanguins dans le cerveau) et l'angine de poitrine et les crises cardiaques (blocage des vaisseaux sanguins dans le cœur). Chacune de ces conditions peut entraîner la mort ou une invalidité grave.
Fumer augmente considérablement la possibilité de souffrir de crises cardiaques et d'accidents vasculaires cérébraux. De plus, le tabagisme et l'utilisation de contraceptifs oraux augmentent considérablement les risques de développer et de mourir d'une maladie cardiaque.

Les femmes souffrant de migraine (en particulier de migraine/maux de tête avec symptômes neurologiques) qui prennent des contraceptifs oraux peuvent également être plus à risque d'accident vasculaire cérébral.
3. Maladie de la vésicule biliaire
Les utilisatrices de contraceptifs oraux ont probablement un risque plus élevé que les non-utilisatrices d'avoir une maladie de la vésicule biliaire. Ce risque peut être lié aux pilules contenant de fortes doses d'œstrogènes. Les contraceptifs oraux peuvent aggraver une maladie de la vésicule biliaire existante ou accélérer le développement d'une maladie de la vésicule biliaire chez les femmes auparavant asymptomatiques.
4. Tumeurs du foie
Dans de rares cas, les contraceptifs oraux peuvent provoquer des tumeurs hépatiques bénignes mais dangereuses. Ces tumeurs bénignes du foie peuvent se rompre et provoquer une hémorragie interne mortelle. De plus, une association possible mais non définitive a été trouvée avec la pilule et les cancers du foie dans deux études dans lesquelles quelques femmes ayant développé ces cancers très rares se sont avérées avoir utilisé des contraceptifs oraux pendant de longues périodes. Cependant, les cancers du foie sont extrêmement rares. Le risque de développer un cancer du foie en utilisant la pilule est donc encore plus rare.
5. Cancer des organes reproducteurs et des seins
Diverses études donnent des rapports contradictoires sur la relation entre le cancer du sein et l'utilisation de contraceptifs oraux.
L'utilisation de contraceptifs oraux peut augmenter légèrement vos chances de recevoir un diagnostic de cancer du sein, en particulier si vous avez commencé à utiliser des contraceptifs hormonaux à un plus jeune âge.
Après avoir cessé d'utiliser des contraceptifs hormonaux, les chances d'avoir un diagnostic de cancer du sein commencent à diminuer et disparaissent 10 ans après l'arrêt de la pilule. On ne sait pas si ce risque légèrement accru de diagnostic de cancer du sein est causé par la pilule. Il se peut que les femmes prenant la pilule aient été examinées plus souvent, de sorte que le cancer du sein était plus susceptible d'être détecté.
Vous devriez vous faire examiner régulièrement les seins par un professionnel de la santé et examiner vos propres seins une fois par mois. Dites à votre professionnel de la santé si vous avez des antécédents familiaux de cancer du sein ou si vous avez eu des nodules mammaires ou une mammographie anormale. Les femmes qui ont actuellement ou ont eu un cancer du sein ne doivent pas utiliser de contraceptifs oraux car le cancer du sein est généralement une tumeur hormono-sensible.
Certaines études ont trouvé une augmentation de l'incidence du cancer du col de l'utérus chez les femmes qui utilisent des contraceptifs oraux. Cependant, ce résultat peut être lié à des facteurs autres que l'utilisation de contraceptifs oraux. Il n'y a pas suffisamment de preuves pour exclure la possibilité que la pilule puisse causer de tels cancers.
6. Métabolisme lipidique et inflammation du pancréas
Chez les patientes présentant des taux de lipides anormaux, des augmentations significatives des triglycérides plasmatiques ont été signalées au cours de l'œstrogénothérapie. Cela a conduit à une inflammation du pancréas dans certains cas.
RISQUE ESTIMÉ DE DÉCÈS D'UNE MÉTHODE DE CONTRÔLE DES NAISSANCES OU D'UNE GROSSESSE
Toutes les méthodes de contraception et de grossesse sont associées à un risque de développer certaines maladies pouvant entraîner une invalidité ou la mort. Une estimation du nombre de décès associés aux différentes méthodes de contraception et de grossesse a été calculée et est présentée dans le tableau suivant.
NOMBRE ANNUEL DE DÉCÈS LIÉS À LA NAISSANCE OU À LA MÉTHODE ASSOCIÉS AU CONTRÔLE DE LA FERTILITÉ POUR 100 000 FEMMES NON STÉRILES, PAR MÉTHODE DE CONTRÔLE DE LA FERTILITÉ ET SELON L'ÂGE
Dans le tableau ci-dessus, le risque de décès lié à toute méthode de contraception est inférieur au risque d'accouchement, sauf pour les utilisatrices de contraceptifs oraux de plus de 35 ans qui fument et les utilisatrices de pilules de plus de 40 ans même si elles ne fument pas. . On peut voir dans le tableau que pour les femmes âgées de 15 à 39 ans, le risque de décès était le plus élevé avec la grossesse (7 à 26 décès pour 100 000 femmes, selon l'âge). Parmi les utilisatrices de pilules non fumeuses, le risque de décès était toujours inférieur à celui associé à la grossesse pour tous les groupes d'âge, à l'exception des femmes de plus de 40 ans, où le risque passe à 32 décès pour 100 000 femmes, contre 28 décès associés. avec une grossesse à cet âge. Cependant, pour les utilisatrices de pilules qui fument et qui ont plus de 35 ans, le nombre estimé de décès dépasse ceux des autres méthodes de contraception. Si une femme a plus de 40 ans et fume, son risque estimé de décès est quatre fois plus élevé (117/100 000 femmes) que le risque estimé associé à une grossesse (28/100 000 femmes) dans ce groupe d'âge.
La suggestion selon laquelle les femmes de plus de 40 ans qui ne fument pas ne devraient pas prendre de contraceptifs oraux est basée sur des informations provenant d'anciennes pilules à forte dose. Un comité consultatif de la FDA a discuté de cette question en 1989 et a recommandé que les avantages de l'utilisation de contraceptifs oraux par des femmes en bonne santé et non fumeuses de plus de 40 ans puissent l'emporter sur les risques possibles. Les femmes âgées, comme toutes les femmes qui prennent des contraceptifs oraux, doivent prendre un contraceptif oral contenant le moins d'œstrogène et de progestatif compatible avec les besoins individuels de la patiente.
SIGNAUX D'AVERTISSEMENT
Si l'un de ces effets indésirables survient pendant que vous prenez des contraceptifs oraux, appelez immédiatement votre professionnel de la santé :
- Douleur thoracique aiguë, toux de sang ou essoufflement soudain (indiquant un possible caillot dans les poumons)
- Douleur au mollet (indiquant un possible caillot dans la jambe)
- Douleur thoracique écrasante ou lourdeur dans la poitrine (indiquant une possible crise cardiaque)
- Maux de tête ou vomissements intenses et soudains, étourdissements ou évanouissements, troubles de la vision ou de la parole, faiblesse ou engourdissement dans un bras ou une jambe (indiquant un possible accident vasculaire cérébral)
- Perte soudaine partielle ou complète de la vision (indiquant un possible caillot dans l'œil)
- Masses mammaires (indiquant un cancer du sein possible ou une maladie fibrokystique du sein ; demandez à votre professionnel de la santé de vous montrer comment examiner vos seins)
- Douleur ou sensibilité intense dans la région de l'estomac (indiquant une tumeur du foie éventuellement rompue)
- Difficulté à dormir, faiblesse, manque d'énergie, fatigue ou changement d'humeur (indiquant peut-être une dépression grave)
- Jaunisse ou jaunissement de la peau ou des globes oculaires, accompagné fréquemment de fièvre, de fatigue, de perte d'appétit, d'urines de couleur foncée ou de selles de couleur claire (indiquant de possibles problèmes de foie)
EFFETS SECONDAIRES DES CONTRACEPTIFS ORAUX
1. Saignements vaginaux irréguliers
Des saignements vaginaux irréguliers ou des saignotements peuvent survenir pendant que vous prenez les pilules. Les saignements irréguliers peuvent varier d'une légère coloration entre les menstruations à des saignements intermenstruels qui ressemblent beaucoup à des règles régulières. Les saignements irréguliers surviennent le plus souvent au cours des premiers mois d'utilisation de la contraception orale, mais peuvent également survenir après que vous ayez pris la pilule pendant un certain temps. Ces saignements peuvent être temporaires et n'indiquent généralement pas de problèmes graves. Il est important de continuer à prendre vos pilules à temps. Si le saignement survient au cours de plusieurs cycles ou dure plus de quelques jours, parlez-en à votre professionnel de la santé.
2. Lentilles de contact
Si vous portez des lentilles cornéennes et remarquez un changement dans votre vision ou une incapacité à porter vos lentilles, communiquez avec votre professionnel de la santé.
3. Rétention d'eau
Les contraceptifs oraux peuvent provoquer un œdème (rétention d'eau) avec gonflement des doigts ou des chevilles et peuvent augmenter votre tension artérielle. Si vous souffrez de rétention d'eau, contactez votre professionnel de la santé.
4. Mélasma
Un assombrissement ponctuel de la peau est possible, en particulier du visage.
5. Autres effets secondaires
D'autres effets secondaires peuvent inclure des nausées, une sensibilité des seins, un changement d'appétit, des maux de tête, de la nervosité, de la dépression, des étourdissements, une perte de cheveux, des éruptions cutanées, des infections vaginales, une inflammation du pancréas et des réactions allergiques.
Si l'un de ces effets secondaires vous dérange, appelez votre professionnel de la santé.
PRÉCAUTIONS GÉNÉRALES
1. Périodes manquées et utilisation de contraceptifs oraux avant ou pendant le début de la grossesse
Il peut y avoir des moments où vous ne pouvez pas avoir vos règles régulièrement après avoir terminé de prendre un cycle de pilules. Si vous avez pris vos pilules régulièrement et que vous manquez une période menstruelle, continuez à prendre vos pilules pour le cycle suivant, mais assurez-vous d'en informer votre professionnel de la santé. Si vous n'avez pas pris les pilules quotidiennement comme indiqué et que vous avez manqué une période menstruelle, ou si vous avez manqué deux périodes menstruelles consécutives, vous pouvez être enceinte. Consultez immédiatement votre professionnel de la santé pour déterminer si vous êtes enceinte. Arrêtez de prendre des contraceptifs oraux si la grossesse est confirmée.
Il n'existe aucune preuve concluante que l'utilisation de contraceptifs oraux soit associée à une augmentation des malformations congénitales lorsqu'elle est prise par inadvertance au début de la grossesse. Auparavant, quelques études avaient rapporté que les contraceptifs oraux pouvaient être associés à des malformations congénitales, mais ces résultats n'ont pas été confirmés dans des études plus récentes. Néanmoins, les contraceptifs oraux ne doivent pas être utilisés pendant la grossesse. Vous devriez vérifier auprès de votre professionnel de la santé les risques pour votre enfant à naître de tout médicament pris pendant la grossesse.
2. Pendant l'allaitement
Si vous allaitez, consultez votre professionnel de la santé avant de commencer les contraceptifs oraux. Une partie du médicament sera transmise à l'enfant dans le lait. Quelques effets indésirables sur l'enfant ont été rapportés, notamment un jaunissement de la peau (jaunisse) et une hypertrophie mammaire. De plus, les contraceptifs oraux peuvent diminuer la quantité et la qualité de votre lait. Si possible, n'utilisez pas de contraceptifs oraux pendant l'allaitement. Vous devez utiliser une autre méthode de contraception car l'allaitement n'offre qu'une protection partielle contre une grossesse, et cette protection partielle diminue de manière significative à mesure que vous allaitez pendant de plus longues périodes. Vous ne devriez envisager de commencer les contraceptifs oraux qu'après avoir complètement sevré votre enfant.
3. Tests de laboratoire
Si vous devez passer des tests de laboratoire, informez votre professionnel de la santé que vous prenez des contraceptifs oraux. Certains tests sanguins peuvent être affectés par les pilules contraceptives.
4. Interactions médicamenteuses
Certains médicaments peuvent interagir avec les pilules contraceptives pour les rendre moins efficaces dans la prévention de la grossesse ou provoquer une augmentation des saignements intermenstruels. Ces médicaments comprennent la rifampicine, des médicaments utilisés pour l'épilepsie tels que les barbituriques (par exemple, le phénobarbital) et la phénytoïne (DilantinR est une marque de ce médicament), la primidone (MysolineR), le topiramate (TopamaxR), la carbamazépine (Tegretol est une marque de ce médicament) , la phénylbutazone (Butazolidin® est une marque de ce médicament), certains médicaments utilisés pour le VIH ou le SIDA tels que le ritonavir (Norvir®), le modafinil (Provigil®), éventuellement certains antibiotiques (tels que l'ampicilline et d'autres pénicillines, et les tétracyclines) et les produits à base de plantes contenant Millepertuis (Hypericum perforatum). Vous devrez peut-être également utiliser une méthode de contraception non hormonale (telle que des préservatifs et/ou un spermicide) au cours de tout cycle au cours duquel vous prenez des médicaments susceptibles de réduire l'efficacité des contraceptifs oraux.
Vous pouvez être plus à risque d'un type spécifique de dysfonctionnement hépatique si vous prenez de la troléandomycine et des contraceptifs oraux en même temps.
Assurez-vous d'informer votre professionnel de la santé si vous prenez ou commencez à prendre d'autres médicaments, y compris des produits en vente libre ou des produits à base de plantes, pendant que vous prenez des contraceptifs oraux.
5. Maladies sexuellement transmissibles
Ce produit (comme tous les contraceptifs oraux) est destiné à prévenir la grossesse. Il ne protège pas contre la transmission du VIH (SIDA) et d'autres maladies sexuellement transmissibles telles que la chlamydia, l'herpès génital, les verrues génitales, la gonorrhée, l'hépatite B et la syphilis.
COMMENT PRENDRE LA PILULE
POINTS IMPORTANTS À RETENIR
AVANT DE COMMENCER À PRENDRE VOS PILULES :
1. ASSUREZ-VOUS DE LIRE CES DIRECTIVES :
Avant de commencer à prendre vos pilules.
Et chaque fois que vous ne savez pas quoi faire.
2. LA BONNE FAÇON DE PRENDRE LE COMPRIMÉ EST DE PRENDRE UN COMPRIMÉ CHAQUE JOUR À LA MÊME HEURE.
Si vous oubliez de prendre des pilules, vous pourriez tomber enceinte. Cela inclut le démarrage tardif du pack. Plus vous oubliez de pilules, plus vous avez de chances de tomber enceinte.
3. DE NOMBREUSES FEMMES ONT DES SPOTTINGS OU DES SAIGNEMENTS LÉGERS, OU PEUVENT SE SENTIR MAL À L'ESTOMAC PENDANT LES 1 À 3 PREMIÈRES PLAQUES DE PILULES.
Si vous avez mal au ventre, n'arrêtez pas de prendre la pilule. Le problème va généralement partir. Si cela ne disparaît pas, consultez votre professionnel de la santé.
4. LES PILULES MANQUÉES PEUVENT ÉGALEMENT PROVOQUER DES SPOTTINGS OU DES SAIGNEMENTS LÉGERS, même lorsque vous inventez ces pilules oubliées.
Les jours où vous prenez 2 pilules pour rattraper les pilules oubliées, vous pourriez aussi avoir un peu mal au ventre.
5. SI VOUS AVEZ DES VOMISSEMENTS (dans les 4 heures suivant la prise de votre pilule), vous devez suivre les instructions de QUE FAIRE SI VOUS MANQUEZ DES PILULES. SI VOUS AVEZ LA DIARRHÉE, ou SI VOUS PRENEZ DES MÉDICAMENTS, y compris des antibiotiques, vos pilules peuvent ne pas fonctionner aussi bien. Utilisez une méthode non hormonale d'appoint (telle que des préservatifs et/ou un spermicide) jusqu'à ce que vous consultiez votre professionnel de la santé.
6. SI VOUS AVEZ DE LA DIFFICULTÉ À VOUS RAPPELER DE PRENDRE LA PILULE, parlez à votre professionnel de la santé de la façon de faciliter la prise de la pilule ou de l'utilisation d'une autre méthode de contraception.
7. SI VOUS AVEZ DES QUESTIONS OU N'ÊTES PAS SÛR DES INFORMATIONS CONTENUES DANS CETTE NOTICE, appelez votre professionnel de la santé.
LO/OVRAL® ET LO/OVRAL®-28 (comprimés de norgestrel et d'éthinylestradiol)
AVANT DE COMMENCER À PRENDRE VOS PILULES
1. DÉCIDEZ À QUELLE HEURE DE LA JOURNÉE VOUS VOULEZ PRENDRE VOTRE COMPRIMÉ.
Il est important de le prendre à peu près à la même heure chaque jour.
2. REGARDEZ VOTRE PLAQUETTE DE PILULES POUR VOIR SI ELLE CONTIENT 21 OU 28 PILULES :
La plaquette de 21 pilules contient 21 pilules blanches "actives" (avec des hormones) à prendre pendant 3 semaines, suivies d'une semaine sans pilule.
La plaquette de 28 pilules contient 21 pilules blanches "actives" (avec hormones) à prendre pendant 3 semaines, suivies d'une semaine de rappel de pilules roses (sans hormones).
3. TROUVEZ AUSSI :
1) où sur la plaquette pour commencer à prendre des pilules, et
2) dans quel ordre prendre les pilules (suivez les flèches).
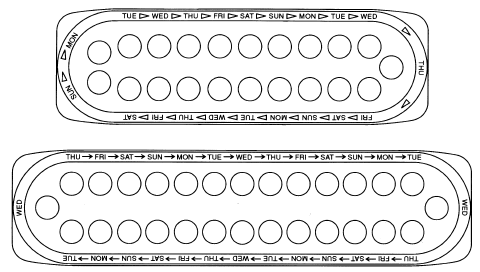
4. ASSUREZ-VOUS D'AVOIR PRÊT À TOUT MOMENT :
UN AUTRE TYPE DE CONTRÔLE DES NAISSANCES (tels que des préservatifs et/ou un spermicide) à utiliser en cas d'oubli de pilules.
UN PACK DE PILULES SUPPLÉMENTAIRE ET COMPLET.
QUAND COMMENCER LA PREMIÈRE PLAQUETTE DE PILULES
Pour la plaquette de pilules de 21 jours, vous avez le choix entre deux jours pour commencer à prendre votre première plaquette de pilules. (Voir JOUR 1 DEBUT ou DIMANCHE START directions ci-dessous. ) Décidez avec votre professionnel de la santé quelle est la meilleure journée pour vous. La plaquette de pilules de 28 jours ne convient qu'à un DÉBUT DU DIMANCHE. Pour chaque plaquette de pilules, choisissez une heure de la journée dont vous vous souviendrez facilement.
DÉBUT DU JOUR 1 :
Ces instructions concernent uniquement la plaquette de 21 jours. La plaquette de pilules de 28 jours ne contient pas de JOUR 1 DEBUT régime posologique.
1. Prenez la première pilule blanche "active" de la première plaquette pendant les 24 premières heures de vos règles.
2. Vous n'aurez pas besoin d'utiliser une méthode contraceptive non hormonale d'appoint, puisque vous commencez la pilule au début de vos règles.
DÉBUT DU DIMANCHE :
Ces instructions concernent soit la plaquette de 21 jours, soit la plaquette de 28 jours.
1. Prenez la première pilule blanche "active" de la première plaquette le dimanche suivant le début de vos règles, même si vous saignez toujours. Si vos règles commencent le dimanche, commencez la plaquette le jour même.
2. Utilisez une méthode de contraception non hormonale (telle que des préservatifs et/ou un spermicide) comme méthode d'appoint si vous avez des rapports sexuels à tout moment à partir du dimanche où vous commencez votre première plaquette jusqu'au dimanche suivant (7 jours).
QUE FAIRE PENDANT LE MOIS
1. PRENEZ UN COMPRIMÉ À LA MÊME HEURE CHAQUE JOUR JUSQU'À CE QUE LA PLAQUETTE SOIT VIDE.
Ne sautez pas de pilules même si vous avez des saignotements ou des saignements entre les menstruations ou si vous avez mal à l'estomac (nausées).
Ne sautez pas de pilules même si vous n'avez pas de relations sexuelles très fréquentes.
2. LORSQUE VOUS TERMINEZ UNE PLAQUETTE OU CHANGEZ DE MARQUE DE PILULES :
21 comprimés : attendez 7 jours avant de commencer la plaquette suivante. Vous aurez probablement vos règles au cours de cette semaine. Assurez-vous qu'il ne s'écoule pas plus de 7 jours entre les packs de 21 jours.
28 pilules : Commencez la plaquette suivante le lendemain de votre dernière pilule « de rappel ». N'attendez pas de jours entre les packs.
QUE FAIRE SI VOUS MANQUEZ DES PILULES
La pilule peut ne pas être aussi efficace si vous oubliez des pilules « actives » blanches, et en particulier si vous oubliez les premières ou les dernières pilules « actives » blanches d'une plaquette.
Si vous Mlle 1 pilule "active" blanche :
1. Prenez-le dès que vous vous en souvenez. Prenez le prochain comprimé à l'heure habituelle. Cela signifie que vous pouvez prendre 2 comprimés en 1 jour.
2. Vous POUVEZ DEVENIR ENCEINTE si vous avez des relations sexuelles dans les 7 jours suivant l'oubli de pilules. Vous DEVEZ utiliser une méthode de contraception non hormonale (telle que des préservatifs et/ou un spermicide) comme solution de secours pendant ces 7 jours.
Si vous Mlle 2 pilules "actives" blanches d'affilée SEMAINE 1 OU SEMAINE 2 de votre pack :
1. Prenez 2 comprimés le jour dont vous vous souvenez et 2 comprimés le jour suivant.
2. Prenez ensuite 1 comprimé par jour jusqu'à ce que vous ayez terminé la plaquette.
3. Vous POUVEZ DEVENIR ENCEINTE si vous avez des rapports sexuels dans les 7 jours suivant l'oubli de pilules. Vous DEVEZ utiliser une méthode de contraception non hormonale (telle que des préservatifs et/ou un spermicide) comme solution de secours pendant ces 7 jours.
Si vous Mlle 2 pilules "actives" blanches d'affilée LA 3ème SEMAINE :
La Entrée du jour 1 les instructions concernent uniquement la plaquette de pilules de 21 jours. La plaquette de pilules de 28 jours ne convient pas au schéma posologique DAY 1 START. La Entrée du dimanche les instructions sont pour la plaquette de pilules de 21 jours ou de 28 jours.
1. Si vous êtes un débutant du jour 1 :
JETEZ le reste de la plaquette de pilules et commencez une nouvelle plaquette le jour même.
Si vous êtes un débutant du dimanche :
Continuez à prendre 1 comprimé par jour jusqu'à dimanche.
Le dimanche, JETEZ le reste de la plaquette et commencez une nouvelle plaquette de pilules le même jour.
2. Vous n'aurez peut-être pas vos règles ce mois-ci, mais c'est normal. Cependant, si vous manquez vos règles 2 mois de suite, appelez votre professionnel de la santé car vous pourriez être enceinte.
3. Vous POUVEZ DEVENIR ENCEINTE si vous avez des rapports sexuels dans les 7 jours suivant l'oubli de pilules. Vous DEVEZ utiliser une méthode de contraception non hormonale (telle que des préservatifs et/ou un spermicide) comme solution de secours pendant ces 7 jours.
Si vous MANQUEZ 3 pilules "actives" blanches OU PLUS d'affilée (pendant les 3 premières semaines) :
La Entrée du jour 1 les instructions concernent uniquement la plaquette de pilules de 21 jours. La plaquette de pilules de 28 jours ne contient pas de JOUR 1 DEBUT régime posologique. La Entrée du dimanche les instructions sont pour la plaquette de pilules de 21 jours ou de 28 jours.
1 Si vous êtes un débutant du jour 1 :
JETEZ le reste de la plaquette de pilules et commencez une nouvelle plaquette le jour même.
Si vous êtes un débutant du dimanche :
Continuez à prendre 1 comprimé par jour jusqu'à dimanche.
Le dimanche, JETEZ le reste de la plaquette et commencez une nouvelle plaquette de pilules le même jour.
2. Vous n'aurez peut-être pas vos règles ce mois-ci, mais c'est normal. Cependant, si vous manquez vos règles 2 mois de suite, appelez votre professionnel de la santé car vous pourriez être enceinte.
3. Vous POUVEZ DEVENIR ENCEINTE si vous avez des rapports sexuels dans les 7 jours suivant l'oubli de pilules. Vous DEVEZ utiliser une méthode de contraception non hormonale (telle que des préservatifs et/ou un spermicide) comme solution de secours pendant ces 7 jours.
UN RAPPEL POUR CEUX SUR LES PACKS DE 28 JOURS
Si vous oubliez l'une des 7 pilules roses "de rappel" au cours de la semaine 4 :
JETEZ les pilules que vous avez oubliées.
Continuez à prendre 1 comprimé par jour jusqu'à ce que la plaquette soit vide.
Vous n'avez pas besoin d'une méthode contraceptive non hormonale de secours si vous commencez votre prochaine plaquette à temps.
ENFIN, SI VOUS N'ÊTES TOUJOURS PAS SÛR DE QUE FAIRE DES PILULES QUE VOUS AVEZ MANQUÉES
Utilisez une MÉTHODE DE CONTRÔLE DES NAISSANCES NON HORMONALE D'APPOINT chaque fois que vous avez des rapports sexuels.
CONTINUEZ À PRENDRE UN COMPRIMÉ CHAQUE JOUR jusqu'à ce que vous puissiez joindre votre professionnel de la santé.
GROSSESSE PAR ERREUR DE PILULE
L'incidence de l'échec de la pilule entraînant une grossesse est d'environ 1 % si elle est prise tous les jours conformément aux instructions, mais le taux d'échec moyen est d'environ 5 %, y compris les femmes qui ne prennent pas toujours la pilule exactement comme indiqué sans en oublier aucune. Si vous tombez enceinte, le risque pour le fœtus est minime, mais vous devez arrêter de prendre vos pilules et discuter de la grossesse avec votre professionnel de la santé.
GROSSESSE APRÈS ARRÊT DE LA PILULE
Il peut y avoir un certain retard avant de devenir enceinte après avoir cessé d'utiliser des contraceptifs oraux, surtout si vous aviez des cycles menstruels irréguliers avant d'utiliser des contraceptifs oraux. Il peut être conseillé de reporter la conception jusqu'à ce que vous commenciez à avoir des règles régulières une fois que vous avez arrêté de prendre la pilule et que vous désirez une grossesse.
Il ne semble pas y avoir d'augmentation des malformations congénitales chez les nouveau-nés lorsque la grossesse survient peu après l'arrêt de la pilule.
Si vous ne désirez pas de grossesse, vous devez utiliser une autre méthode de contraception immédiatement après avoir arrêté la pilule contraceptive orale.
SURDOSAGE
Un surdosage peut provoquer des nausées, des vomissements et de la fatigue/somnolence. L'hémorragie de privation peut
surviennent chez les femelles. En cas de surdosage, contactez votre professionnel de la santé ou votre pharmacien.
LES AUTRES INFORMATIONS
Votre professionnel de la santé examinera vos antécédents médicaux et familiaux avant de vous prescrire des contraceptifs oraux et vous examinera. L'examen physique peut être reporté à un autre moment si vous en faites la demande et que le professionnel de la santé juge opportun de le reporter. Vous devriez être réexaminé au moins une fois par an. Assurez-vous d'informer votre professionnel de la santé s'il existe des antécédents familiaux de l'une des conditions énumérées précédemment dans cette notice. Assurez-vous de respecter tous les rendez-vous avec votre professionnel de la santé, car c'est le moment de déterminer s'il y a des signes précoces d'effets secondaires liés à l'utilisation de contraceptifs oraux.
N'utilisez pas le médicament pour une condition autre que celle pour laquelle il a été prescrit. Ce médicament vous a été spécifiquement prescrit ; ne le donnez pas à d'autres personnes qui pourraient vouloir des pilules contraceptives.
AVANTAGES POUR LA SANTÉ DES CONTRACEPTIFS ORAUX
En plus de prévenir la grossesse, l'utilisation de contraceptifs oraux peut offrir certains avantages.
Elles sont:
- Les cycles menstruels peuvent devenir plus réguliers.
- Le flux sanguin pendant les menstruations peut être plus léger et moins de fer peut être perdu. Par conséquent, l'anémie due à une carence en fer est moins susceptible de se produire.
- La douleur ou d'autres symptômes pendant la menstruation peuvent être moins fréquents.
- Les kystes ovariens peuvent survenir moins fréquemment.
- Une grossesse extra-utérine (tubaire) peut survenir moins fréquemment.
- Des kystes ou des masses non cancéreuses dans le sein peuvent survenir moins fréquemment.
- La maladie inflammatoire pelvienne aiguë peut survenir moins fréquemment.
- L'utilisation de contraceptifs oraux peut offrir une certaine protection contre le développement de deux formes de cancer : le cancer des ovaires et le cancer de la muqueuse de l'utérus.
Si vous voulez plus d'informations sur les pilules contraceptives, demandez à votre professionnel de la santé ou à votre pharmacien. Ils ont une brochure plus technique appelée l'étiquetage professionnel que vous voudrez peut-être lire.
