Ventolin Inhaler 100mcg Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
Qu'est-ce que la ventoline et comment est-elle utilisée ?
Ventolin HFA est un médicament d'ordonnance utilisé pour traiter les symptômes de l'asthme aigu ou sévère, ou induit par l'exercice (broncospasme). Ventolin HFA peut être utilisé seul ou avec d'autres médicaments.
Ventolin HFA appartient à une classe de médicaments appelés bêta2 agonistes.
On ne sait pas si Ventolin HFA est sûr et efficace chez les enfants de moins de 4 ans.
Quels sont les effets secondaires possibles de la ventoline ?
La ventoline peut provoquer des effets secondaires graves, notamment :
- respiration sifflante,
- étouffement,
- problèmes de respiration,
- douleur thoracique,
- rythme cardiaque rapide,
- des battements de cœur battants,
- flottant dans ta poitrine,
- Maux de tête sévères,
- battant dans votre cou ou vos oreilles,
- douleur ou brûlure lorsque vous urinez,
- augmentation de la soif,
- augmentation de la miction,
- bouche sèche,
- odeur d'haleine fruitée,
- crampes dans les jambes,
- constipation
- battements cardiaques irréguliers,
- engourdissement ou fourmillement,
- faiblesse musculaire et
- sensation de boiterie
Consultez immédiatement un médecin si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires les plus courants de la ventoline comprennent :
- douleur thoracique,
- battements de cœur rapides ou battants,
- vertiges,
- se sentir tremblant,
- nervosité,
- mal de tête,
- mal au dos,
- courbatures,
- maux d'estomac,
- mal de gorge,
- douleur aux sinus et
- nez qui coule ou bouché
Dites au médecin si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas.
Ce ne sont pas tous les effets secondaires possibles de Ventoline. Pour plus d'informations, consultez votre médecin ou votre pharmacien.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
LA DESCRIPTION
Le composant actif de VENTOLIN HFA est le sulfate d'albutérol, USP, la forme racémique de l'albutérol et un bronchodilatateur bêta-adrénergique relativement sélectif. Le sulfate d'albutérol a le nom chimique α1 - [(tert-butylamino)méthyl]-4-hydroxy-m-xylène-α, α'-sulfate de diol (2:1)(sel) et la structure chimique suivante :
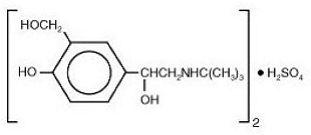
Le sulfate d'albutérol est une poudre cristalline blanche d'un poids moléculaire de 576,7 et la formule empirique est (C13H21NO3)2•H2SO4. Il est soluble dans l'eau et légèrement soluble dans l'éthanol.
Le nom recommandé par l'Organisation mondiale de la santé pour l'albutérol base est le salbutamol.
VENTOLIN HFA est un inhalateur en plastique bleu muni d'un strapcap bleu contenant une bombe aérosol-doseur sous pression munie d'un compteur. Chaque cartouche contient une suspension microcristalline de sulfate d'albutérol dans le propulseur HFA-134a (1,1,1,2-tétrafluoroéthane). Il ne contient aucun autre excipient.
Après amorçage, chaque actionnement de l'inhalateur délivre 120 mcg de sulfate d'albutérol, USP dans 75 mg de suspension de la valve et 108 mcg de sulfate d'albutérol, USP de l'embout buccal (équivalent à 90 mcg de base d'albutérol de l'embout buccal).
Amorcer VENTOLIN HFA avant la première utilisation, lorsque l'inhalateur n'a pas été utilisé pendant plus de 2 semaines ou lorsque l'inhalateur est tombé. Pour amorcer VENTOLIN HFA, libérez 4 pulvérisations dans l'air loin du visage, en agitant bien avant chaque pulvérisation.
LES INDICATIONS
Bronchospasme
VENTOLIN® HFA en aérosol pour inhalation est indiqué pour le traitement ou la prévention du bronchospasme chez les patients âgés de 4 ans et plus atteints d'une maladie obstructive réversible des voies respiratoires.
Bronchospasme induit par l'exercice
VENTOLIN HFA est indiqué pour la prévention du bronchospasme induit par l'exercice chez les patients âgés de 4 ans et plus.
DOSAGE ET ADMINISTRATION
Bronchospasme
Pour le traitement des épisodes aigus de bronchospasme ou la prévention des symptômes associés au bronchospasme, la posologie usuelle chez l'adulte et l'enfant est de 2 inhalations répétées toutes les 4 à 6 heures ; chez certains patients, 1 inhalation toutes les 4 heures peut suffire. Une administration plus fréquente ou un plus grand nombre d'inhalations n'est pas recommandée.
Bronchospasme induit par l'exercice
Pour la prévention du bronchospasme induit par l'exercice, la posologie habituelle pour les adultes et les enfants âgés de 4 ans et plus est de 2 inhalations 15 à 30 minutes avant l'exercice.
Informations administratives
VENTOLIN HFA doit être administré uniquement par inhalation orale.
Amorçage
L'amorçage de VENTOLIN HFA est essentiel pour garantir une teneur appropriée en albutérol à chaque actionnement. Amorcer VENTOLIN HFA avant la première utilisation, lorsque l'inhalateur n'a pas été utilisé pendant plus de 2 semaines ou lorsque l'inhalateur est tombé. Pour amorcer VENTOLIN HFA, libérez 4 pulvérisations dans l'air loin du visage, en agitant bien avant chaque pulvérisation.
Nettoyage
Pour garantir un dosage correct et éviter le blocage de l'orifice de l'actionneur, lavez l'actionneur à l'eau tiède et laissez-le sécher complètement à l'air libre au moins une fois par semaine.
COMMENT FOURNIE
Formes posologiques et points forts
Aérosol pour inhalation. Inhalateur en plastique bleu avec un strapcap bleu contenant une bombe aérosol-doseur pressurisée contenant 60 ou 200 inhalations-doseurs et munie d'un compteur. Chaque actionnement délivre 108 mcg de sulfate d'albutérol (90 mcg de base d'albutérol) à partir de l'embout buccal.
Stockage et manutention
VENTOLIN HFA Aérosol pour inhalation est fourni dans les boîtes de 1 suivantes sous forme de bidon en aluminium sous pression équipé d'un compteur et fourni avec un actionneur en plastique bleu avec un strapcap bleu :
CDN 0173-0682-20 Bidon de 18 g contenant 200 actionnements CDN 0173-0682-21 Boîte de 8 g contenant 60 pressions CDN 0173-0682-24 Cartouche institutionnelle de 8 g contenant 60 activations
Chaque inhalateur est scellé dans une pochette en aluminium anti-humidité avec un déshydratant qui doit être jeté lorsque la pochette est ouverte. Chaque inhalateur est emballé avec une notice d'information destinée aux patients.
L'actionneur bleu fourni avec VENTOLIN HFA ne doit pas être utilisé avec d'autres cartouches de produit, et les actionneurs d'autres produits ne doivent pas être utilisés avec une cartouche de VENTOLIN HFA.
VENTOLIN HFA a un compteur attaché à la cartouche. Le compteur commence à 204 ou 64 et compte à rebours chaque fois qu'un spray est libéré. La quantité correcte de médicament à chaque actionnement ne peut pas être assurée après que le compteur indique 000, même si la cartouche n'est pas complètement vide et continuera à fonctionner. L'inhalateur doit être jeté lorsque le compteur indique 000 ou 12 mois après avoir été retiré de la pochette en aluminium anti-humidité, selon la première éventualité.
Tenir hors de portée des enfants. Éviter de vaporiser dans les yeux.
Contenu sous pression : ne pas percer. Ne pas utiliser ou entreposer près d'une source de chaleur ou d'une flamme nue. L'exposition à des températures supérieures à 120°F peut provoquer un éclatement. Ne jetez jamais la cartouche dans le feu ou l'incinérateur.
Conserver à température ambiante entre 68 °F et 77 °F (20 °C et 25 °C) ; excursions autorisées de 59°F à 86°F (15°C à 30°C) [Voir Température ambiante contrôlée USP ]. Rangez l'inhalateur avec l'embout buccal vers le bas. Pour de meilleurs résultats, l'inhalateur doit être à température ambiante avant utilisation. BIEN AGITER AVANT CHAQUE PULVÉRISATION.
GlaxoSmithKline, Research Triangle Park, NC 27709. Révisé : décembre 2014
EFFETS SECONDAIRES
L'utilisation de VENTOLIN HFA peut être associée à ce qui suit :
- Bronchospasme paradoxal [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Effets cardiovasculaires [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Réactions d'hypersensibilité immédiates [voir AVERTISSEMENTS ET PRECAUTIONS ]
- Hypokaliémie [voir AVERTISSEMENTS ET PRECAUTIONS ]
Expérience des essais cliniques
Étant donné que les essais cliniques sont menés dans des conditions très variables, les taux d'effets indésirables observés dans les essais cliniques d'un médicament ne peuvent pas être directement comparés aux taux des essais cliniques d'un autre médicament et peuvent ne pas refléter les taux observés dans la pratique.
Les données sur l'innocuité décrites ci-dessous reflètent l'exposition à VENTOLIN HFA chez 248 sujets traités par VENTOLIN HFA dans 3 essais cliniques contrôlés par placebo d'une durée de 2 à 12 semaines. Les données provenant d'adultes et d'adolescents sont basées sur 2 essais cliniques au cours desquels 202 sujets asthmatiques âgés de 12 ans et plus ont été traités par VENTOLIN HFA 2 inhalations 4 fois par jour pendant 12 semaines. La population adulte/adolescente était de 92 femmes, 110 hommes et 163 blancs, 19 noirs, 18 hispaniques, 2 autres. Les données provenant de sujets pédiatriques sont basées sur 1 essai clinique dans lequel 46 sujets asthmatiques âgés de 4 à 11 ans ont été traités par VENTOLIN HFA 2 inhalations 4 fois par jour pendant 2 semaines. La population était de 21 femmes, 25 hommes et 25 blancs, 17 noirs, 3 hispaniques, 1 autre.
Sujets adultes et adolescents âgés de 12 ans et plus : Les deux essais randomisés à double insu de 12 semaines menés auprès de 610 sujets adultes et adolescents asthmatiques comparant VENTOLIN HFA, un inhalateur d'albutérol propulsé par CFC 11/12 et un inhalateur placebo HFA-134a. Dans l'ensemble, l'incidence et la nature des effets indésirables signalés pour VENTOLIN HFA et un inhalateur d'albutérol propulsé par CFC 11/12 étaient comparables. Le tableau 1 énumère l'incidence de tous les effets indésirables (qu'ils soient considérés par l'investigateur comme étant liés ou non au médicament) de ces essais qui se sont produits à un taux de 3 % ou plus dans le groupe traité par VENTOLIN HFA et plus fréquemment dans le groupe traité avec VENTOLIN HFA que dans le groupe inhalateur placebo HFA-134a.
Les effets indésirables signalés par moins de 3 % des sujets adultes et adolescents recevant VENTOLIN HFA et par une plus grande proportion de sujets recevant VENTOLIN HFA que ceux recevant l'inhalateur placebo HFA-134a et pouvant être liés à VENTOLIN HFA comprennent la diarrhée, la laryngite, œdème oropharyngé, toux, troubles pulmonaires, tachycardie et extrasystoles. Des palpitations et des étourdissements ont également été observés avec VENTOLIN HFA.
Sujets pédiatriques âgés de 4 à 11 ans : Les résultats de l'essai clinique de 2 semaines chez des sujets pédiatriques asthmatiques âgés de 4 à 11 ans ont montré que cette population pédiatrique présentait un profil d'effets indésirables similaire à celui des populations adultes et adolescentes.
Trois essais ont été menés pour évaluer l'innocuité et l'efficacité de VENTOLIN HFA chez des sujets âgés de 0 à 4 ans. Les résultats de ces essais n'ont pas établi l'efficacité de VENTOLIN HFA dans ce groupe d'âge [voir Utilisation dans des populations spécifiques ]. L'efficacité de VENTOLIN HFA n'ayant pas été démontrée chez les enfants âgés de 0 à 48 mois, l'innocuité de VENTOLIN HFA dans ce groupe d'âge ne peut être établie. Cependant, le profil de sécurité observé dans la population pédiatrique de moins de 4 ans était comparable à celui observé chez les sujets pédiatriques plus âgés et chez les adultes et les adolescents. Lorsque les taux d'incidence des effets indésirables étaient plus élevés chez les sujets de moins de 4 ans par rapport aux sujets plus âgés, les taux d'incidence les plus élevés ont été notés dans tous les bras de traitement, y compris le placebo. Ces effets indésirables comprenaient une infection des voies respiratoires supérieures, une rhinopharyngite, une pyrexie et une tachycardie.
Expérience post-commercialisation
En plus des réactions défavorables annoncées des essais cliniques, les réactions défavorables suivantes ont été identifiées pendant l'utilisation de postapprobation de sulfate albuterol. Étant donné que ces réactions sont signalées volontairement par une population de taille incertaine, il n'est pas toujours possible d'estimer de manière fiable leur fréquence ou d'établir une relation causale avec l'exposition au médicament. Ces événements ont été choisis pour inclusion en raison de leur gravité, de leur fréquence de déclaration ou de leur lien de causalité avec l'albutérol ou d'une combinaison de ces facteurs.
Des cas de bronchospasme paradoxal, d'enrouement, d'arythmie (y compris fibrillation auriculaire, tachycardie supraventriculaire) et de réactions d'hypersensibilité (y compris urticaire, œdème de Quincke, éruption cutanée) ont été signalés après l'utilisation de VENTOLIN HFA.
En outre, l'albutérol, comme d'autres agents sympathomimétiques, peut provoquer des effets indésirables tels qu'hypokaliémie, hypertension, vasodilatation périphérique, angine de poitrine, tremblements, stimulation du système nerveux central, hyperactivité, insomnie, maux de tête, crampes musculaires, assèchement ou irritation de l'oropharynx et troubles métaboliques. acidose.
INTERACTIONS MÉDICAMENTEUSES
Les autres bronchodilatateurs sympathomimétiques en aérosol à courte durée d'action ne doivent pas être utilisés en concomitance avec l'albutérol. Si des médicaments adrénergiques supplémentaires doivent être administrés par n'importe quelle voie, ils doivent être utilisés avec prudence pour éviter des effets cardiovasculaires délétères.
Agents bloquants des récepteurs bêta-adrénergiques
Non seulement les bêta-bloquants bloquent l'effet pulmonaire des bêta-agonistes, tels que VENTOLIN HFA, mais ils peuvent également provoquer un bronchospasme sévère chez les patients asthmatiques. Par conséquent, les patients asthmatiques ne doivent normalement pas être traités par des bêta-bloquants. Cependant, dans certaines circonstances, il peut ne pas y avoir d'alternative acceptable à l'utilisation d'agents bloquants bêta-adrénergiques pour ces patients ; les bêta-bloquants cardiosélectifs peuvent être envisagés, même s'ils doivent être administrés avec prudence.
Diurétiques non épargneurs de potassium
Les modifications de l'ECG et/ou l'hypokaliémie pouvant résulter de l'administration de diurétiques non épargneurs de potassium (tels que les diurétiques de l'anse ou thiazidiques) peuvent être fortement aggravées par les bêta-agonistes, en particulier lorsque la dose recommandée de bêta-agoniste est dépassée. Bien que la signification clinique de ces effets ne soit pas connue, la prudence s'impose lors de l'administration concomitante de VENTOLIN HFA avec des diurétiques non épargneurs de potassium.
Digoxine
Des diminutions moyennes de 16 % à 22 % des taux sériques de digoxine ont été démontrées après l'administration intraveineuse et orale d'une dose unique d'albutérol, respectivement, à des volontaires sains qui avaient reçu de la digoxine pendant 10 jours. La pertinence clinique de ces résultats pour les patients atteints de maladie obstructive des voies respiratoires qui reçoivent de l'albutérol et de la digoxine inhalés de manière chronique n'est pas claire. Néanmoins, il serait prudent d'évaluer soigneusement les taux sériques de digoxine chez les patients qui reçoivent actuellement de la digoxine et de l'albutérol.
Inhibiteurs de la monoamine oxydase et antidépresseurs tricycliques
VENTOLIN HFA doit être administré avec une extrême prudence aux patients traités par des inhibiteurs de la monoamine oxydase ou des antidépresseurs tricycliques, ou dans les 2 semaines suivant l'arrêt de ces agents, car l'action de l'albutérol sur le système vasculaire peut être potentialisée.
AVERTISSEMENTS
Inclus dans le cadre du PRÉCAUTIONS section.
PRÉCAUTIONS
Bronchospasme paradoxal
VENTOLIN HFA peut produire un bronchospasme paradoxal, qui peut mettre la vie en danger. Si un bronchospasme paradoxal survient après l'administration de VENTOLIN HFA, il faut l'arrêter immédiatement et instaurer un autre traitement. Il convient de reconnaître que le bronchospasme paradoxal, lorsqu'il est associé à des formulations inhalées, survient fréquemment lors de la première utilisation d'une nouvelle cartouche.
Détérioration de l'asthme
L'asthme peut s'aggraver de manière aiguë sur une période de quelques heures ou de façon chronique sur plusieurs jours ou plus. Si le patient a besoin de plus de doses de VENTOLIN HFA que d'habitude, cela peut être un marqueur de déstabilisation de l'asthme et nécessite une réévaluation du patient et du schéma thérapeutique, en accordant une attention particulière à la nécessité éventuelle d'un traitement anti-inflammatoire, par exemple des corticostéroïdes.
Utilisation d'agents anti-inflammatoires
L'utilisation de bronchodilatateurs agonistes bêta-adrénergiques seuls peut ne pas être suffisante pour contrôler l'asthme chez de nombreux patients. Il convient d'envisager rapidement l'ajout d'agents anti-inflammatoires, par exemple des corticostéroïdes, au schéma thérapeutique.
Effets cardiovasculaires
VENTOLIN HFA, comme tous les autres agonistes bêta2-adrénergiques, peut produire des effets cardiovasculaires cliniquement significatifs chez certains patients, tels que des modifications du pouls ou de la tension artérielle. Si de tels effets surviennent, il peut être nécessaire d'arrêter VENTOLIN HFA. De plus, il a été rapporté que les bêta-agonistes produisaient des modifications de l'électrocardiogramme (ECG), telles qu'un aplatissement de l'onde T, un allongement de l'intervalle QTc et une dépression du segment ST. La pertinence clinique de ces résultats est inconnue. Par conséquent, VENTOLIN HFA, comme toutes les autres amines sympathomimétiques, doit être utilisé avec prudence chez les patients présentant des troubles cardiovasculaires sous-jacents, en particulier une insuffisance coronarienne, des arythmies cardiaques et une hypertension.
Ne pas dépasser la dose recommandée
Des décès ont été signalés en association avec une utilisation excessive de médicaments sympathomimétiques inhalés chez des patients asthmatiques. La cause exacte du décès est inconnue, mais un arrêt cardiaque suite au développement inattendu d'une crise d'asthme aiguë sévère et d'une hypoxie subséquente est suspecté.
Réactions d'hypersensibilité immédiates
Des réactions d'hypersensibilité immédiates (p. ex., urticaire, œdème de Quincke, éruption cutanée, bronchospasme, hypotension), y compris l'anaphylaxie, peuvent survenir après l'administration de VENTOLIN HFA [voir CONTRE-INDICATIONS ].
Conditions coexistantes
VENTOLIN HFA, comme les autres amines sympathomimétiques, doit être utilisé avec prudence chez les patients souffrant de troubles convulsifs, d'hyperthyroïdie ou de diabète sucré et chez les patients qui répondent de manière inhabituelle aux amines sympathomimétiques. De fortes doses d'albutérol par voie intraveineuse ont été rapportées pour aggraver le diabète sucré préexistant et l'acidocétose.
Hypokaliémie
Les médicaments agonistes bêta-adrénergiques peuvent produire une hypokaliémie importante chez certains patients, éventuellement par shunt intracellulaire, ce qui a le potentiel de produire des effets cardiovasculaires indésirables [voir PHARMACOLOGIE CLINIQUE ]. La diminution du potassium sérique est généralement transitoire et ne nécessite pas de supplémentation.
Informations sur les conseils aux patients
Conseillez au patient de lire l'étiquetage patient approuvé par la FDA ( RENSEIGNEMENTS POUR LE PATIENT et mode d'emploi ).
Fréquence d'utilisation
Informer les patients que l'action de VENTOLIN HFA doit durer jusqu'à 4 à 6 heures. N'utilisez pas VENTOLIN HFA plus fréquemment que recommandé. Aviser les patients de ne pas augmenter la dose ou la fréquence des doses de VENTOLIN HFA sans consulter le médecin. Demandez aux patients de consulter immédiatement un médecin si le traitement par VENTOLIN HFA devient moins efficace pour le soulagement des symptômes, si les symptômes s'aggravent et/ou s'ils doivent utiliser le produit plus fréquemment que d'habitude.
Amorçage
Demandez aux patients d'amorcer VENTOLIN HFA avant la première utilisation, lorsque l'inhalateur n'a pas été utilisé pendant plus de 2 semaines ou lorsque l'inhalateur est tombé. Pour amorcer VENTOLIN HFA, libérez 4 pulvérisations dans l'air loin du visage, en agitant bien avant chaque pulvérisation.
Nettoyage
Pour garantir un dosage correct et éviter le blocage de l'orifice de l'actionneur, demandez aux patients de laver l'actionneur à l'eau tiède et de le laisser sécher complètement à l'air libre au moins une fois par semaine. Informez les patients que des instructions de nettoyage détaillées sont incluses dans la notice d'information destinée aux patients.
Bronchospasme paradoxal
Informer les patients que VENTOLIN HFA peut produire un bronchospasme paradoxal. Demandez-leur d'arrêter VENTOLIN HFA en cas de bronchospasme paradoxal.
Consommation concomitante de drogues
Avisez les patients que pendant qu'ils utilisent VENTOLIN HFA, les autres médicaments inhalés et les médicaments contre l'asthme doivent être pris uniquement selon les directives du médecin.
Effets indésirables courants
Les effets indésirables courants du traitement par l'albutérol inhalé comprennent des palpitations, des douleurs thoraciques, une fréquence cardiaque rapide, des tremblements et de la nervosité.
Grossesse
Conseillez aux patientes enceintes ou qui allaitent de contacter leur médecin au sujet de l'utilisation de VENTOLIN HFA.
VENTOLIN est une marque déposée du groupe de sociétés GSK. Les autres marques répertoriées sont des marques déposées de leurs propriétaires respectifs et ne sont pas des marques déposées du groupe de sociétés GSK. Les fabricants de ces marques ne sont pas affiliés et ne cautionnent pas le groupe de sociétés GSK ou ses produits.
Toxicologie non clinique
Carcinogenèse, mutagenèse, altération de la fertilité
Dans une étude de 2 ans chez des rats Sprague-Dawley, le sulfate d'albutérol a provoqué une augmentation liée à la dose de l'incidence des léiomyomes bénins du mésovarium à des doses alimentaires de 2,0 mg/kg et plus (environ 14 et 6 fois la MRHDID pour les adultes et enfants, respectivement, sur une base mg/m). Dans une autre étude, cet effet a été bloqué par la co-administration de propranolol, un antagoniste bêta-adrénergique non sélectif. Dans une étude de 18 mois chez des souris CD-1, le sulfate d'albutérol n'a montré aucun signe de tumorigénicité à des doses alimentaires allant jusqu'à 500 mg/kg (environ 1 700 et 800 fois le MRHDID pour les adultes et les enfants, respectivement, sur une base mg/m² ). Dans une étude de 22 mois chez des hamsters dorés, le sulfate d'albutérol n'a montré aucune preuve de tumorigénicité à des doses alimentaires allant jusqu'à 50 mg/kg (environ 225 et 110 fois la MRHDID pour les adultes et les enfants, respectivement, sur une base mg/m²).
Le sulfate d'albutérol n'était pas mutagène dans le test d'Ames ou dans un test de mutation chez la levure. Le sulfate d'albutérol n'était pas clastogène dans un test de lymphocytes périphériques humains ou dans un test de micronoyau de souris de souche AH1.
Les études de reproduction dans les rats n'ont démontré aucune évidence de fertilité diminuée aux doses orales de sulfate albuterol jusqu'à 50 mgs/kg (environ 340 fois le MRHDID pour les adultes sur une base mg/m2).
Utilisation dans des populations spécifiques
Grossesse
Effets tératogènes
Catégorie de grossesse C. Il n'y a pas d'essais adéquats et bien contrôlés avec VENTOLIN HFA ou le sulfate d'albutérol chez les femmes enceintes. Au cours de l'expérience de commercialisation mondiale, diverses anomalies congénitales, y compris des fentes palatines et des malformations des membres, ont été signalées chez la progéniture de patients traités par l'albutérol. Certaines mères prenaient plusieurs médicaments pendant leur grossesse. Aucun modèle cohérent de défauts ne peut être discerné et une relation entre l'utilisation d'albutérol et les anomalies congénitales n'a pas été établie. Des études de reproduction animale chez la souris et le lapin ont révélé des signes de tératogénicité. VENTOLIN HFA ne doit être utilisé pendant la grossesse que si le bénéfice potentiel justifie le risque potentiel pour le fœtus. Les femmes doivent être avisées de communiquer avec leur médecin si elles tombent enceintes pendant qu'elles prennent VENTOLIN HFA.
Dans une étude sur la reproduction chez la souris, le sulfate d'albutérol administré par voie sous-cutanée a entraîné la formation d'une fente palatine chez 5 fœtus sur 111 (4,5 %) à des expositions inférieures à la dose maximale recommandée par inhalation humaine quotidienne (MRHDID) pour les adultes sur une base en mg/m² et chez 10 sur 108 fœtus. (9,3 %) fœtus à environ 8 fois le MRHDID. Des effets similaires n'ont pas été observés à environ un onzième du MRHDID. Une fente palatine est également survenue chez 22 des 72 fœtus (30,5 %) de femelles traitées par voie sous-cutanée avec de l'isoprotérénol (témoin positif).
Dans une étude de reproduction chez le lapin, le sulfate d'albutérol administré par voie orale a produit un cranioschisis chez 7 des 19 fœtus (37 %) à environ 680 fois le MRHDID.
Dans une autre étude chez le lapin, une formulation de sulfate d'albutérol/HFA-134a administrée par inhalation a produit un élargissement de la partie frontale des fontanelles fœtales à environ un tiers du MRHDID.
Effets non tératogènes
Une étude dans laquelle des rats enceintes ont reçu une dose de sulfate d'albutérol radiomarqué a démontré que le matériel lié au médicament est transféré de la circulation maternelle au fœtus.
Travail et accouchement
Il n'y a pas d'essais humains bien contrôlés qui ont étudié les effets de VENTOLIN HFA sur le travail prématuré ou à terme. En raison du potentiel d'interférence des bêta-agonistes avec la contractilité utérine, l'utilisation de VENTOLIN HFA pendant le travail doit être limitée aux patientes pour lesquelles les avantages l'emportent clairement sur les risques.
Mères allaitantes
Les concentrations plasmatiques de sulfate d'albutérol et de HFA-134a après inhalation de doses thérapeutiques sont très faibles chez l'humain, mais on ne sait pas si les composants de VENTOLIN HFA sont excrétés dans le lait maternel. En raison du potentiel de tumorigénicité démontré pour l'albutérol dans les études animales et du manque d'expérience avec l'utilisation de VENTOLIN HFA par les mères qui allaitent, une décision doit être prise d'interrompre l'allaitement ou d'arrêter le médicament, en tenant compte de l'importance du médicament pour la mère. La prudence s'impose lorsque VENTOLIN HFA est administré à une femme qui allaite.
Utilisation pédiatrique
L'innocuité et l'efficacité de VENTOLIN HFA chez les enfants âgés de 4 ans et plus ont été établies sur la base de deux essais cliniques de 12 semaines chez des sujets asthmatiques âgés de 12 ans et plus et d'un essai clinique de 2 semaines chez des sujets asthmatiques âgés de 4 à 11 ans. [voir EFFETS INDÉSIRABLES , Etudes cliniques ]. L'innocuité et l'efficacité de VENTOLIN HFA chez les enfants de moins de 4 ans n'ont pas été établies. Trois essais ont été menés pour évaluer l'innocuité et l'efficacité de VENTOLIN HFA chez des sujets de moins de 4 ans et les résultats sont décrits ci-dessous.
Deux essais randomisés, en double aveugle et contrôlés par placebo d'une durée de 4 semaines ont été menés chez 163 sujets pédiatriques âgés de la naissance à 48 mois présentant des symptômes de bronchospasme associés à une maladie obstructive des voies respiratoires (présentant les symptômes suivants : respiration sifflante, toux, dyspnée ou oppression thoracique) . VENTOLIN HFA ou le placebo HFA ont été administrés avec une chambre de maintien à valve AeroChamber Plus® ou une chambre de maintien à valve Optichamber® avec masque 3 fois par jour. Dans un essai, VENTOLIN HFA à 90 mcg (n = 26), VENTOLIN HFA à 180 mcg (n = 25) et un placebo HFA (n = 26) ont été administrés à des enfants âgés de 24 à 48 mois. Dans le deuxième essai, VENTOLIN HFA à 90 mcg (n = 29), VENTOLIN HFA à 180 mcg (n = 29) et un placebo HFA (n = 28) ont été administrés à des enfants âgés entre la naissance et 24 mois. Au cours de la période de traitement de 4 semaines, il n'y a eu aucune différence de traitement dans les scores des symptômes de l'asthme entre les groupes recevant VENTOLIN HFA à 90 mcg, VENTOLIN HFA à 180 mcg et un placebo dans les deux essais.
Dans un troisième essai, VENTOLIN HFA a été évalué chez 87 sujets pédiatriques de moins de 24 mois pour le traitement de la respiration sifflante aiguë. VENTOLIN HFA a été livré avec une chambre de retenue à valve AeroChamber Plus dans cet essai. Il n'y avait aucune différence significative dans les scores des symptômes de l'asthme et le changement moyen par rapport au départ dans un score des symptômes de l'asthme entre VENTOLIN HFA 180 mcg et VENTOLIN HFA 360 mcg.
Des études de caractérisation de dose in vitro ont été réalisées pour évaluer l'administration de VENTOLIN HFA via des chambres de retenue avec des masques attachés. Les études ont été menées avec 2 chambres de détention différentes avec masques (petite et moyenne taille). Les données de l'étude in vitro lors de la simulation de la respiration du patient suggèrent que la dose de VENTOLIN HFA présentée pour inhalation via une chambre de retenue à valve avec masque sera comparable à la dose administrée chez les adultes sans chambre d'inhalation ni masque par kilogramme de poids corporel (tableau 2). Cependant, les essais cliniques chez les enfants de moins de 4 ans décrits ci-dessus suggèrent soit que la dose optimale de VENTOLIN HFA n'a pas été définie dans ce groupe d'âge, soit que VENTOLIN HFA n'est pas efficace dans ce groupe d'âge. L'innocuité et l'efficacité de VENTOLIN HFA administré avec ou sans dispositif d'espacement chez les enfants de moins de 4 ans n'ont pas été démontrées.
Utilisation gériatrique
Les essais cliniques de VENTOLIN HFA n'ont pas inclus un nombre suffisant de sujets âgés de 65 ans et plus pour déterminer si les sujets plus âgés réagissent différemment des sujets plus jeunes. L'autre expérience clinique annoncée n'a pas identifié de différences dans les réponses entre les patients assez âgés et plus jeunes. En général, la sélection de la dose pour un patient âgé doit être prudente, en commençant généralement à l'extrémité inférieure de la plage posologique, reflétant la plus grande fréquence de diminution de la fonction hépatique, rénale ou cardiaque et de maladie concomitante ou d'un autre traitement médicamenteux.
SURDOSAGE
Les signes et symptômes attendus en cas de surdosage d'albutérol sont ceux d'une stimulation bêta-adrénergique excessive et/ou de l'apparition ou de l'exagération de l'un des signes et symptômes de stimulation bêta-adrénergique (par exemple, convulsions, angine de poitrine, hypertension ou hypotension, tachycardie avec des fréquences à 200 battements/min, arythmies, nervosité, céphalées, tremblements, crampes musculaires, bouche sèche, palpitations, nausées, étourdissements, fatigue, malaise, insomnie, hyperglycémie, hypokaliémie, acidose métabolique).
Comme avec tous les médicaments sympathomimétiques inhalés, un arrêt cardiaque et même la mort peuvent être associés à une surdose de VENTOLIN HFA en aérosol pour inhalation.
Le traitement consiste en l'arrêt de VENTOLIN HFA ainsi qu'un traitement symptomatique approprié. L'utilisation judicieuse d'un bêta-bloquant cardiosélectif peut être envisagée, sachant qu'une telle médication peut provoquer un bronchospasme. Les preuves sont insuffisantes pour déterminer si la dialyse est bénéfique en cas de surdosage de VENTOLIN HFA.
CONTRE-INDICATIONS
VENTOLIN HFA est contre-indiqué chez les patients ayant des antécédents d'hypersensibilité à l'un des ingrédients [voir AVERTISSEMENTS ET PRECAUTIONS , LA DESCRIPTION ].
PHARMACOLOGIE CLINIQUE
Mécanisme d'action
Des études in vitro et des études pharmacologiques in vivo ont démontré que l'albutérol a un effet préférentiel sur les récepteurs bêta2-adrénergiques par rapport à l'isoprotérénol. Bien que les récepteurs bêta2-adrénergiques soient les récepteurs adrénergiques prédominants dans le muscle lisse bronchique et que les récepteurs bêta1-adrénergiques soient les récepteurs prédominants dans le cœur, il existe également des récepteurs bêta2-adrénergiques dans le cœur humain, représentant 10 % à 50 % du total des récepteurs bêta-adrénergiques. La fonction précise de ces récepteurs n'a pas été établie, mais leur présence soulève la possibilité que même les bêta2-agonistes sélectifs puissent avoir des effets cardiaques.
L'activation des récepteurs bêta2-adrénergiques sur le muscle lisse des voies respiratoires entraîne l'activation de l'adényl cyclase et une augmentation de la concentration intracellulaire de 3',5'-adénosine monophosphate cyclique (AMP cyclique). Cette augmentation de l'AMP cyclique conduit à l'activation de la protéine kinase A, qui inhibe la phosphorylation de la myosine et abaisse les concentrations de calcium ionique intracellulaire, entraînant une relaxation. L'albutérol détend les muscles lisses de toutes les voies respiratoires, de la trachée aux bronchioles terminales. L'albutérol agit comme un antagoniste fonctionnel pour détendre les voies respiratoires quel que soit le spasmogène impliqué, protégeant ainsi contre tous les défis bronchoconstricteurs. Des concentrations accrues d'AMP cyclique sont également associées à l'inhibition de la libération de médiateurs par les mastocytes dans les voies respiratoires.
Il a été démontré dans la plupart des essais cliniques contrôlés que l'albutérol a plus d'effet sur les voies respiratoires, sous la forme d'une relaxation des muscles lisses bronchiques, que l'isoprotérénol à des doses comparables tout en produisant moins d'effets cardiovasculaires. Des études cliniques contrôlées et d'autres expériences cliniques ont montré que l'albutérol inhalé, comme d'autres médicaments agonistes bêta-adrénergiques, peut produire un effet cardiovasculaire significatif chez certains patients, tel que mesuré par le pouls, la pression artérielle, les symptômes et/ou les modifications électrocardiographiques [voir AVERTISSEMENTS ET PRECAUTIONS ].
Pharmacocinétique
Les taux systémiques d'albutérol sont faibles après inhalation des doses recommandées. Un essai mené chez 12 sujets masculins et féminins en bonne santé utilisant une dose plus élevée (1 080 mcg d'albutérol base) a montré que des concentrations plasmatiques maximales moyennes d'environ 3 ng/mL se produisaient après l'administration lorsque l'albutérol était administré à l'aide du propulseur HFA-134a. Le délai moyen d'atteinte des concentrations maximales (Tmax) a été retardé après l'administration de VENTOLIN HFA (Tmax = 0,42 heure) par rapport à l'inhalateur d'albutérol propulsé par CFC (Tmax = 0,17 heure). La demi-vie plasmatique terminale apparente de l'albutérol est d'environ 4,6 heures. Aucun autre essai pharmacocinétique sur VENTOLIN HFA n'a été mené chez des nouveau-nés, des enfants ou des sujets âgés.
Toxicologie animale et/ou pharmacologie
Préclinique
Des études intraveineuses chez des rats avec du sulfate d'albutérol ont démontré que l'albutérol traverse la barrière hémato-encéphalique et atteint des concentrations cérébrales s'élevant à environ 5,0 % des concentrations plasmatiques. Dans les structures en dehors de la barrière hémato-encéphalique (glandes pinéale et pituitaire), les concentrations d'albutérol se sont avérées 100 fois supérieures à celles du cerveau entier.
Des études chez des animaux de laboratoire (porcs miniatures, rongeurs et chiens) ont démontré la survenue d'arythmies cardiaques et de mort subite (avec des signes histologiques de nécrose myocardique) lorsque des bêta-agonistes et des méthylxanthines sont administrés simultanément. La pertinence clinique de ces résultats est inconnue.
Propulseur HFA-134a
Chez les animaux et les humains, le propulseur HFA-134a s'est avéré être rapidement absorbé et rapidement éliminé, avec une demi-vie d'élimination de 3 à 27 minutes chez les animaux et de 5 à 7 minutes chez les humains. Le temps jusqu'à la concentration plasmatique maximale (Tmax) et le temps de séjour moyen sont tous deux extrêmement courts, entraînant une apparition transitoire de HFA-134a dans le sang sans signe d'accumulation.
Le propulseur HFA-134a est dépourvu d'activité pharmacologique, sauf à des doses très élevées chez les animaux (c'est-à-dire 380 à 1 300 fois l'exposition humaine maximale basée sur des comparaisons de l'aire sous la concentration plasmatique par rapport aux valeurs de la courbe temporelle [AUC]), produisant principalement de l'ataxie, des tremblements , dyspnée ou salivation. Ces événements sont similaires aux effets produits par les CFC structurellement apparentés, qui ont été largement utilisés dans les inhalateurs-doseurs.
Etudes cliniques
Bronchospasme associé à l'asthme
Sujets adultes et adolescents âgés de 12 ans et plus
L'efficacité de VENTOLIN HFA a été évaluée dans deux essais randomisés, à double insu et contrôlés par placebo de 12 semaines chez des sujets âgés de 12 ans et plus souffrant d'asthme léger à modéré. Ces essais ont inclus un total de 610 sujets (323 hommes, 287 femmes). Dans chaque essai, les sujets ont reçu 2 inhalations de VENTOLIN HFA, d'albutérol propulsé aux CFC 11/12 ou de placebo HFA-134a 4 fois par jour pendant 12 semaines. Les sujets prenant l'inhalateur placebo HFA-134a ont également pris VENTOLIN HFA pour le soulagement des symptômes de l'asthme au besoin. Certains sujets qui ont participé à ces essais cliniques utilisaient une corticothérapie inhalée concomitante. L'efficacité a été évaluée par le volume expiratoire maximal en 1 seconde (VEMS). Dans chacun de ces essais, 2 inhalations de VENTOLIN HFA ont produit une amélioration significativement plus importante du VEMS par rapport à la valeur avant le traitement que le placebo. Les résultats des 2 essais cliniques sont décrits ci-dessous.
Dans un essai randomisé à double insu de 12 semaines, VENTOLIN HFA (101 sujets) a été comparé à l'albutérol propulsé par CFC 11/12 (99 sujets) et à un inhalateur placebo HFA-134a (97 sujets) chez des sujets adolescents et adultes âgés 12 à 76 ans souffrant d'asthme léger à modéré. Les mesures en série du VEMS [indiquées ci-dessous sous forme de variation en pourcentage par rapport à la valeur initiale du jour du test au jour 1 (n = 297) et à la semaine 12 (n = 249)] ont démontré que 2 inhalations de VENTOLIN HFA produisaient une amélioration significativement plus importante du VEMS par rapport à la valeur de prétraitement que placebo.
VEMS en pourcentage de changement par rapport à la prédose dans un grand essai clinique de 12 semaines Jour 1 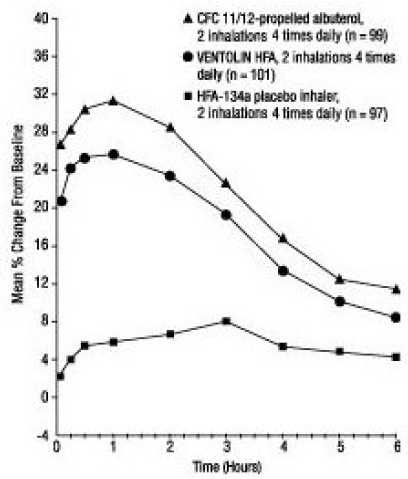
Semaine 12 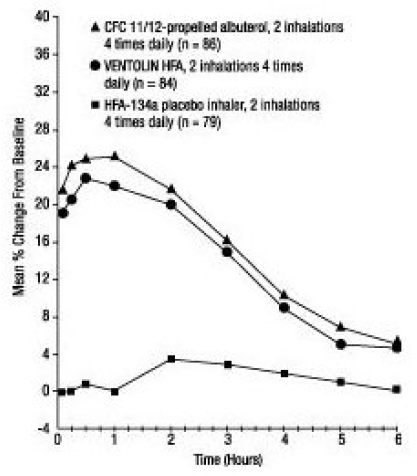
Dans la population de répondeurs (augmentation supérieure ou égale à 15 % du VEMS dans les 30 minutes suivant l'administration) traitée par VENTOLIN HFA, le délai moyen d'apparition d'une augmentation de 15 % du VEMS par rapport à la valeur de prétraitement était de 5,4 minutes, et le délai moyen l'effet maximal était de 56 minutes. La durée moyenne de l'effet mesurée par une augmentation de 15 % du VEMS par rapport à la valeur de prétraitement était d'environ 4 heures. Chez certains sujets, la durée de l'effet était aussi longue que 6 heures.
Le deuxième essai randomisé à double insu de 12 semaines a été mené pour évaluer l'efficacité et l'innocuité du passage de l'albutérol propulsé par CFC 11/12 à VENTOLIN HFA. Au cours de la phase de rodage de 3 semaines de l'essai, tous les sujets ont reçu de l'albutérol propulsé par CFC 11/12. Au cours de la phase de traitement en double aveugle, VENTOLIN HFA (91 sujets) a été comparé à l'albutérol propulsé aux CFC 11/12 (100 sujets) et à un inhalateur placebo HFA-134a (95 sujets) chez des sujets adultes et adolescents souffrant d'asthme léger à modéré. Des mesures en série du VEMS ont démontré que 2 inhalations de VENTOLIN HFA produisaient une amélioration significativement plus importante de la fonction pulmonaire que le placebo. Le passage de l'inhalateur d'albutérol propulsé par CFC 11/12 à VENTOLIN HFA n'a révélé aucun changement cliniquement significatif du profil d'efficacité.
Dans les 2 essais chez l'adulte, les résultats d'efficacité de VENTOLIN HFA étaient significativement supérieurs à ceux du placebo et étaient cliniquement comparables à ceux obtenus avec l'albutérol propulsé par CFC 11/12, bien que de petites différences numériques dans la réponse moyenne du VEMS et d'autres mesures aient été observées. Les médecins doivent reconnaître que les réponses individuelles aux agonistes bêta-adrénergiques administrés via différents propulseurs peuvent varier et que des réponses équivalentes chez les patients individuels ne doivent pas être supposées.
Sujets pédiatriques âgés de 4 à 11 ans
L'efficacité de VENTOLIN HFA a été évaluée dans un essai randomisé, à double insu et contrôlé par placebo d'une durée de 2 semaines chez 135 sujets pédiatriques âgés de 4 à 11 ans souffrant d'asthme léger à modéré. Dans cet essai, les sujets ont reçu VENTOLIN HFA, de l'albutérol propulsé par CFC 11/12 ou un placebo HFA-134a. Des mesures de la fonction pulmonaire en série ont démontré que 2 inhalations de VENTOLIN HFA produisaient une amélioration significativement plus importante de la fonction pulmonaire que le placebo et qu'il n'y avait pas de différences significatives entre les groupes traités par VENTOLIN HFA et l'albutérol propulsé par CFC 11/12. Dans la population de répondeurs traités par VENTOLIN HFA, le délai moyen d'apparition d'une augmentation de 15 % du débit expiratoire maximal (DEP) par rapport à la valeur de prétraitement était de 7,8 minutes, et le délai moyen d'effet maximal était d'environ 90 minutes. La durée moyenne de l'effet mesurée par une augmentation de 15 % du PEFR par rapport à la valeur de prétraitement était supérieure à 3 heures. Chez certains sujets, la durée de l'effet était aussi longue que 6 heures.
Bronchospasme induit par l'exercice
Un essai clinique contrôlé chez des sujets adultes asthmatiques (N = 24) a démontré que 2 inhalations de VENTOLIN HFA prises environ 30 minutes avant l'exercice prévenaient de manière significative le bronchospasme induit par l'exercice (mesuré par le pourcentage maximal de chute du VEMS après l'exercice) par rapport à un HFA-134a inhalateur placebo. De plus, VENTOLIN HFA s'est avéré cliniquement comparable à un inhalateur d'albutérol propulsé par CFC 11/12 pour cette indication.
INFORMATIONS PATIENTS
VENTOLIN® [vent' o-lin] HFA (sulfate d'albutérol) Aérosol pour inhalation
Lisez les renseignements destinés aux patients qui accompagnent l'aérosol pour inhalation VENTOLIN HFA avant de commencer à l'utiliser et chaque fois que vous recevez une recharge. Il peut y avoir de nouvelles informations. Ces informations patient ne remplacent pas la discussion avec votre fournisseur de soins de santé au sujet de votre état de santé ou de votre traitement.
Qu'est-ce que VENTOLIN HFA?
VENTOLIN HFA est un médicament inhalé sur ordonnance utilisé chez les personnes âgées de 4 ans et plus pour :
- traiter ou prévenir le bronchospasme chez les personnes atteintes d'une maladie obstructive réversible des voies respiratoires
- prévenir le bronchospasme induit par l'exercice
On ne sait pas si VENTOLIN HFA est sûr et efficace chez les enfants de moins de 4 ans.
Qui ne devrait pas utiliser VENTOLIN HFA?
Ne pas utiliser VENTOLIN HFA si vous êtes allergique au sulfate d'albutérol ou à l'un des ingrédients de VENTOLIN HFA. Voir « Quels sont les ingrédients de VENTOLIN HFA ? » ci-dessous pour une liste complète des ingrédients.
Que dois-je dire à mon fournisseur de soins de santé avant d'utiliser VENTOLIN HFA?
Informez votre fournisseur de soins de santé de tous vos problèmes de santé, y compris si vous :
- avoir des problèmes cardiaques.
- avoir une pression artérielle élevée.
- avoir des convulsions.
- avoir des problèmes de thyroïde.
- avoir le diabète.
- avez un faible taux de potassium dans le sang.
- êtes allergique à l'un des ingrédients de VENTOLIN HFA ou à tout autre médicament. Voir « Quels sont les ingrédients de VENTOLIN HFA ? » ci-dessous pour une liste complète des ingrédients.
- avoir d'autres conditions médicales.
- êtes enceinte ou planifiez une grossesse. On ne sait pas si VENTOLIN HFA peut nuire à votre bébé à naître.
- allaitent. On ne sait pas si le médicament contenu dans VENTOLIN HFA passe dans votre lait et s'il peut nuire à votre bébé.
Informez votre professionnel de la santé de tous les médicaments que vous prenez, y compris les médicaments sur ordonnance et en vente libre, les vitamines et les suppléments à base de plantes. VENTOLIN HFA et certains autres médicaments peuvent interagir entre eux. Cela peut provoquer des effets secondaires graves.
Informez particulièrement votre fournisseur de soins de santé si vous prenez :
- autres médicaments inhalés ou médicaments contre l'asthme
- médicaments bêta-bloquants
- diurétiques
- digoxine
- inhibiteurs de la monoamine oxydase
- antidépresseurs tricycliques
Demandez à votre fournisseur de soins de santé ou à votre pharmacien une liste de ces médicaments si vous n'êtes pas sûr.
Connaissez les médicaments que vous prenez. Conservez-en une liste pour la montrer à votre fournisseur de soins de santé et à votre pharmacien lorsque vous recevez un nouveau médicament.
Comment dois-je utiliser VENTOLIN HFA ?
Lisez les instructions étape par étape pour l'utilisation de VENTOLIN HFA à la fin de ces renseignements destinés aux patients.
- Ne pas utilisez VENTOLIN HFA à moins que votre fournisseur de soins de santé ne vous ait appris à utiliser l'inhalateur et que vous compreniez comment l'utiliser correctement.
- Les enfants doivent utiliser VENTOLIN HFA avec l'aide d'un adulte, conformément aux instructions du fournisseur de soins de santé de l'enfant.
- Utilisez VENTOLIN HFA exactement comme votre professionnel de la santé vous l'a indiqué. N'utilisez pas VENTOLIN HFA plus souvent que prescrit.
- Ne pas augmentez votre dose ou prenez des doses supplémentaires de VENTOLIN HFA sans en parler d'abord à votre fournisseur de soins de santé.
- Chaque dose de VENTOLIN HFA devrait durer jusqu'à 4 heures à 6 heures.
- Consultez immédiatement un médecin si VENTOLIN HFA ne soulage plus vos symptômes.
- Consultez immédiatement un médecin si vos symptômes s'aggravent ou si vous devez utiliser votre inhalateur plus souvent.
- Pendant que vous utilisez VENTOLIN HFA, utilisez d'autres médicaments inhalés et des médicaments contre l'asthme uniquement selon les directives de votre fournisseur de soins de santé.
- Appelez votre fournisseur de soins de santé si vos symptômes d'asthme comme une respiration sifflante et des difficultés respiratoires s'aggravent en quelques heures ou quelques jours. Votre fournisseur de soins de santé devra peut-être vous prescrire un autre médicament pour traiter vos symptômes.
Quels sont les effets secondaires possibles avec VENTOLIN HFA ?
VENTOLIN HFA peut provoquer des effets secondaires graves, notamment :
- aggravation des difficultés respiratoires, toux et respiration sifflante (bronchospasme paradoxal). Si cela se produit, arrêtez d'utiliser VENTOLIN HFA et appelez votre fournisseur de soins de santé ou obtenez de l'aide d'urgence immédiatement. Le bronchospasme paradoxal est plus susceptible de se produire lors de votre première utilisation d'une nouvelle cartouche de médicament.
- problèmes cardiaques, y compris une fréquence cardiaque plus rapide et une pression artérielle élevée
- décès possible chez les personnes asthmatiques qui utilisent trop de VENTOLIN HFA
- réactions allergiques graves. Appelez votre fournisseur de soins de santé ou obtenez des soins médicaux d'urgence si vous présentez l'un des symptômes suivants d'une réaction allergique grave :
- éruption
- urticaire
- gonflement du visage, de la bouche et de la langue
- problèmes de respiration
- changements dans les taux sanguins de laboratoire (sucre, potassium)
Les effets secondaires courants de VENTOLIN HFA comprennent :
- mal de gorge
- infection des voies respiratoires supérieures, y compris infection virale
- toux
- douleur musculaire
- votre cœur a l'impression de battre ou de s'emballer (palpitations)
- douleur thoracique
- rythme cardiaque rapide
- tremblement
- nervosité
- vertiges
Informez votre fournisseur de soins de santé de tout effet secondaire qui vous dérange ou qui ne disparaît pas.
Ce ne sont pas tous les effets secondaires de VENTOLIN HFA. Demandez à votre fournisseur de soins de santé ou à votre pharmacien pour plus d'informations.
Appelez votre médecin pour obtenir des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
Comment dois-je conserver VENTOLIN HFA?
- Conservez VENTOLIN HFA à température ambiante entre 68 °F et 77 °F (20 °C et 25 °C) avec l'embout buccal vers le bas.
- Le contenu de votre VENTOLIN HFA est sous pression : Ne pas percer. Ne pas utiliser ou entreposer près d'une source de chaleur ou d'une flamme nue. Des températures supérieures à 120 °F peuvent faire éclater la cartouche.
- Ne pas jeter au feu ou dans un incinérateur.
- Conservez VENTOLIN HFA dans le sachet en aluminium non ouvert et ouvrez-le uniquement lorsque vous êtes prêt à l'emploi.
- Gardez VENTOLIN HFA et tous les médicaments hors de la portée des enfants.
Informations générales sur l'utilisation sûre et efficace de VENTOLIN HFA
Des médicaments sont parfois prescrits à des fins non mentionnées dans une notice d'information destinée aux patients. N'utilisez pas VENTOLIN HFA pour une affection pour laquelle il n'a pas été prescrit. Ne donnez pas votre VENTOLIN HFA à d'autres personnes, même si elles ont la même condition que vous. Cela peut leur nuire.
Cette notice d'information destinée aux patients résume les informations les plus importantes sur VENTOLIN HFA. Si vous souhaitez plus d'informations, parlez-en à votre fournisseur de soins de santé ou à votre pharmacien. Vous pouvez demander à votre fournisseur de soins de santé ou à votre pharmacien des renseignements sur VENTOLIN HFA rédigés à l'intention des professionnels de la santé.
Pour plus d'informations sur VENTOLIN HFA, appelez le 1-888-825-5249 ou visitez notre site Web à www.ventolin.com.
Quels sont les ingrédients de VENTOLIN HFA ?
Ingrédient actif: sulfate d'albutérol
Ingrédient inactif : propulseur HFA-134a
Mode d'emploi
Pour inhalation orale uniquement
Votre inhalateur VENTOLIN HFA
- La boîte métallique contient le médicament. Voir Figure A.
Figure A 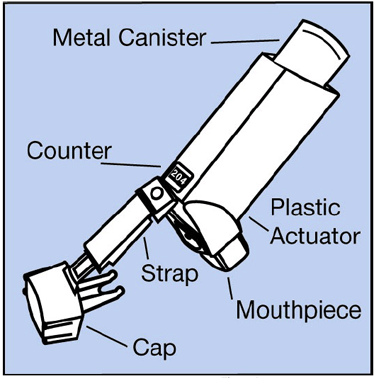
- La cartouche a un compteur pour indiquer le nombre de pulvérisations de médicament qu'il vous reste. Le numéro s'affiche à travers une fenêtre à l'arrière de l'actionneur. Voir la figure B.
Figure B 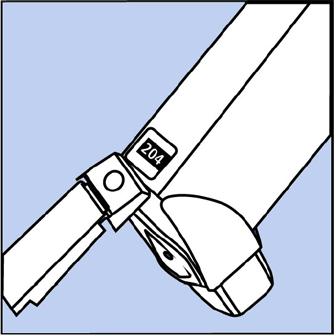
- Le compteur commence soit à 204 ou 064 selon la taille de l'inhalateur dont vous disposez. Le nombre décomptera de 1 chaque fois que vous pulvérisez l'inhalateur. Le compteur arrêtera de compter à 000.
- N'essayez pas de changer les chiffres ou de retirer le compteur de la cartouche métallique. Le compteur ne peut pas être réinitialisé et il est fixé en permanence à la cartouche.
- L'actionneur en plastique bleu pulvérise le médicament de la cartouche. L'actionneur a un capuchon de protection qui recouvre l'embout buccal. Voir Figure A . Gardez le capuchon de protection sur l'embout buccal lorsque la cartouche n'est pas utilisée. La sangle maintient le capuchon attaché à l'actionneur.
- Ne pas utiliser l'actionneur avec une cartouche de médicament de tout autre inhalateur.
- Ne pas utiliser une cartouche VENTOLIN HFA avec un actionneur de tout autre inhalateur.
Avant d'utiliser votre inhalateur VENTOLIN HFA
- Sortez VENTOLIN HFA du sachet en aluminium juste avant de l'utiliser pour la première fois. Jetez en toute sécurité la pochette et le sachet de séchage qui se trouve à l'intérieur de la pochette.
- L'inhalateur doit être à température ambiante avant de l'utiliser.
- Si votre enfant doit utiliser VENTOLIN HFA, surveillez-le de près pour vous assurer qu'il utilise l'inhalateur correctement. Votre fournisseur de soins de santé vous montrera comment votre enfant doit utiliser VENTOLIN HFA.
Amorçage de votre inhalateur VENTOLIN HFA
- Avant d'utiliser VENTOLIN HFA pour la première fois, vous devez amorcer l'inhalateur afin d'obtenir la bonne quantité de médicament lorsque vous l'utilisez.
- Pour amorcer l'inhalateur, retirez le capuchon de l'embout buccal et secouez bien l'inhalateur. Vaporisez ensuite l'inhalateur 1 fois dans l'air loin de votre visage. Voir Figure C. Éviter de vaporiser dans les yeux.
Figure C 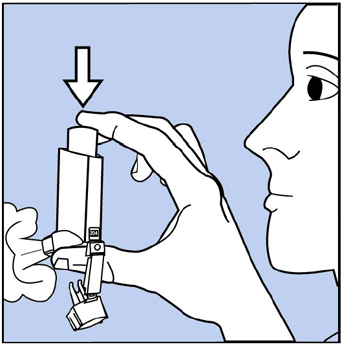
- Secouez et vaporisez l'inhalateur comme ceci 3 fois de plus pour terminer l'amorçage. Le compteur devrait maintenant indiquer 200 ou 60 , selon la taille de l'inhalateur dont vous disposez. Voir la figure D.
Figure D 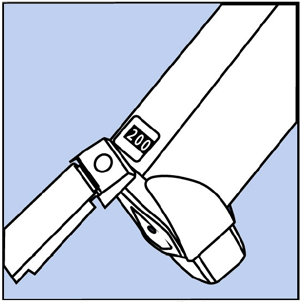
- Vous devez réamorcer votre inhalateur si vous ne l'avez pas utilisé depuis plus de 14 jours ou si vous le laissez tomber. Retirez le capuchon de l'embout buccal, secouez et vaporisez l'inhalateur 4 fois dans l'air loin de votre visage.
Comment utiliser votre inhalateur VENTOLIN HFA
Suivez ces étapes chaque fois que vous utilisez VENTOLIN HFA.
Étape 1. Assurez-vous que la cartouche s'insère fermement dans l'actionneur. Le compteur doit apparaître à travers la fenêtre de l'actionneur.
Bien agiter l'inhalateur avant chaque pulvérisation.
Retirez le capuchon de l'embout buccal de l'actionneur. Regardez à l'intérieur de l'embout buccal à la recherche d'objets étrangers et retirez tous ceux que vous voyez.
Étape 2. Tenez l'inhalateur avec l'embout buccal vers le bas. Voir Figure E .
Figure E 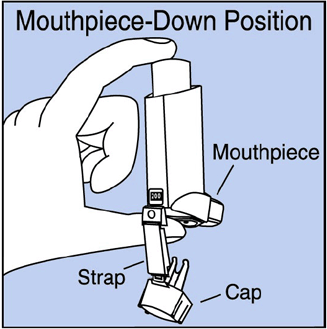
Étape 3. Expirez par la bouche et expulsez autant d'air que possible de vos poumons. Mettez l'embout buccal dans votre bouche et refermez vos lèvres autour. Voir Figure F .
Figure F 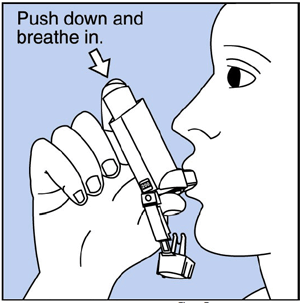
Étape 4. Poussez le haut de la cartouche vers le bas pendant que vous inspirez profondément et lentement par la bouche. Voir Figure F .
Étape 5. Une fois le spray sorti, retirez votre doigt de la cartouche. Après avoir inspiré à fond, retirez l'inhalateur de votre bouche et fermez la bouche.
Étape 6.Retenez votre respiration pendant environ 10 secondes ou aussi longtemps que vous le souhaitez. Expirez doucement aussi longtemps que vous le pouvez.
Si votre fournisseur de soins de santé vous a dit de nous donner plus de prières, attendez 1 minute et secouez à nouveau l'inhalateur. Répétez les étapes 2 à 6.
Étape 7. Remettez le capuchon sur l'embout buccal après chaque utilisation de l'inhalateur. Assurez-vous qu'il s'enclenche fermement en place.
Nettoyage de votre inhalateur VENTOLIN HFA
Nettoyez votre inhalateur au moins 1 fois par semaine. Vous ne verrez peut-être aucune accumulation de médicament sur l'inhalateur, mais il est important de le garder propre afin que l'accumulation de médicament ne bloque pas le spray. Voir la figure G.
Chiffre G 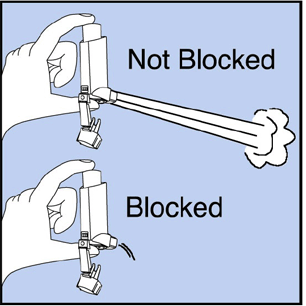
Étape 8. Retirez la cartouche de l'actionneur et retirez le capuchon de l'embout buccal. La sangle sur le capuchon restera attachée à l'actionneur.
Étape 9. Tenez l'actionneur sous le robinet et faites-y couler de l'eau chaude pendant environ 30 secondes. Voir Figure H.
Chiffre H 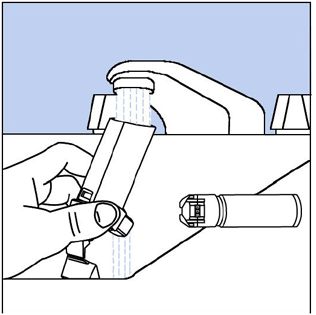
Étape 10. Retournez l'actionneur et faites couler de l'eau chaude dans l'embout buccal pendant environ 30 secondes. Voir Je figure .
Je figure 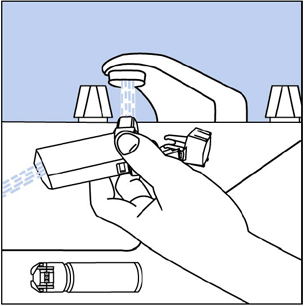
Étape 11. Secouez autant d'eau que possible de l'actionneur. Regardez dans l'embout buccal pour vous assurer que toute accumulation de médicament a été complètement éliminée. S'il y a une accumulation, répétez les étapes 9 et 10.
Étape 12. Laissez l'actionneur sécher à l'air pendant la nuit. Voir figure J.
Figure J 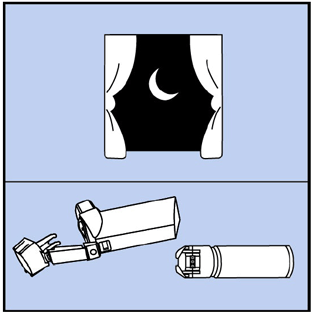
Étape 13. Lorsque l'actionneur est sec, placez le capuchon de protection sur l'embout buccal, puis placez la cartouche dans l'actionneur et assurez-vous qu'il est bien ajusté. Bien agiter l'inhalateur, retirer le capuchon et vaporiser l'inhalateur une fois dans l'air loin de votre visage. (Le compteur comptera à rebours de 1 chiffre.) Remettez le capuchon sur l'embout buccal.
Si vous devez utiliser votre inhalateur avant que l'actionneur ne soit complètement sec :
- Secouez autant d'eau que possible sur l'actionneur.
- Mettez le capuchon sur l'embout buccal, puis placez la cartouche dans l'actionneur et assurez-vous qu'elle est bien ajustée.
- Bien agiter l'inhalateur et vaporiser 1 fois dans l'air loin de votre visage.
- Prenez votre dose de VENTOLIN HFA comme prescrit.
- Suivez les étapes de nettoyage 8 à 13 ci-dessus.
Remplacement de votre inhalateur VENTOLIN HFA :
- Lorsque le compteur affiche 020, vous devez renouveler votre ordonnance ou demander à votre fournisseur de soins de santé si vous avez besoin d'une autre ordonnance pour VENTOLIN HFA.
- Jeter l'inhalateur quand le compteur lit 0 ou 12 mois après avoir ouvert le sachet en aluminium, selon la première éventualité. Vous ne devez pas continuer à utiliser l'inhalateur lorsque le compteur indique 000 car vous ne recevrez pas la bonne quantité de médicament.
- Ne pas utiliser l'inhalateur après la date de péremption indiquée sur l'emballage.
Pour une utilisation correcte de votre inhalateur VENTOLIN HFA, rappelez-vous :
- La cartouche doit toujours être bien ajustée dans l'actionneur.
- Inspirez profondément et lentement pour vous assurer que vous avez bien absorbé tous les médicaments.
- Retenez votre souffle pendant environ 10 secondes après avoir inhalé le médicament. Puis expirez complètement.
- Gardez toujours le capuchon de protection sur l'embout buccal lorsque votre inhalateur n'est pas utilisé.
- Rangez toujours votre inhalateur avec l'embout buccal pointant vers le bas.
- Nettoyez votre inhalateur au moins 1 fois par semaine.
Si vous avez des questions sur VENTOLIN HFA ou sur l'utilisation de votre inhalateur, appelez GlaxoSmithKline (GSK) au 1-888-825-5249 ou visitez www.ventolin.com.
Ces informations pour les patients et ces instructions d'utilisation ont été approuvées par la Food and Drug Administration des États-Unis.
