Traitement de l'asthme: Combivent 50/20mcg Levosalbutamol Utilisations, effets secondaires et dosage. Prix en Pharmacie. Medicaments generiques sans ordonnance.
Combivent® (bromure d'ipratropium et sulfate d'albutérol) Aérosol pour inhalation
Aérosol bronchodilatateur pour inhalation orale uniquement
LA DESCRIPTION
L'aérosol pour inhalation COMBIVENT est une combinaison de bromure d'ipratropium (sous forme de monohydrate) et de sulfate d'albutérol.
Le bromure d'ipratropium est un bronchodilatateur anticholinergique chimiquement décrit comme 8-azoniabicyclo[3.2.1] octane, 3-(3-hydroxy-1-oxo-2-phénylpropoxy)-8-méthyl8-(1-méthyléthyl)-, bromure monohydraté, ( 3-endo, 8-syn)- : un composé d'ammonium quaternaire synthétique apparenté chimiquement à l'atropine. Le bromure d'ipratropium est une substance cristalline blanche à blanc cassé, librement soluble dans l'eau et le méthanol, peu soluble dans l'éthanol et insoluble dans les solvants lipophiles tels que l'éther, le chloroforme et les fluorocarbures.
La formule structurale est :
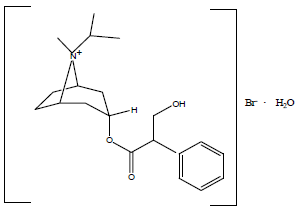 C20H30BrNO3•H2O bromure d'ipratropium Mol. Poids 430.4
C20H30BrNO3•H2O bromure d'ipratropium Mol. Poids 430.4
Le sulfate d'albutérol, chimiquement connu sous le nom de (1,3-benzènediméthanol, α'-[[(1,1diméthyléthyl) amino] méthyl]-4-hydroxy, sulfate (2:1)(sel), (±)- est un agent relativement sélectif bronchodilatateur bêta2-adrénergique. L'albutérol est le nom générique officiel aux États-Unis. Le nom recommandé par l'Organisation mondiale de la santé pour le médicament est le salbutamol. Le sulfate d'albutérol est une poudre cristalline blanche à blanc cassé, librement soluble dans l'eau et légèrement soluble dans l'alcool, chloroforme et éther. La formule structurale est la suivante :
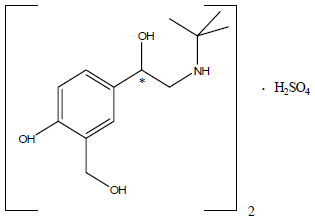 (C13H21NO3)2•H2SO4 sulfate d'albutérol Mol. Poids 576.7
(C13H21NO3)2•H2SO4 sulfate d'albutérol Mol. Poids 576.7
L'aérosol pour inhalation Combivent® (bromure d'ipratropium et sulfate d'albutérol) contient une suspension microcristalline de bromure d'ipratropium et de sulfate d'albutérol dans un aérosol doseur sous pression pour administration par inhalation orale. L'unité d'inhalation 200 a un poids net de 14,7 grammes. Chaque actionnement mesure 21 mcg de bromure d'ipratropium et 120 mcg de sulfate d'albutérol à partir de la valve et délivre 18 mcg de bromure d'ipratropium et 103 mcg de sulfate d'albutérol (équivalent à 90 mcg de base d'albutérol) à partir de l'embout buccal. Les excipients sont le dichlorodifluorométhane, le dichlorotétrafluoroéthane et le trichloromonofluorométhane comme propulseurs et la lécithine de soja.
LES INDICATIONS
L'aérosol pour inhalation COMBIVENT est indiqué chez les patients atteints de maladie pulmonaire obstructive chronique (MPOC) qui utilisent un bronchodilatateur en aérosol régulier et qui continuent de présenter des signes de bronchospasme et qui ont besoin d'un deuxième bronchodilatateur.
DOSAGE ET ADMINISTRATION
La dose d'aérosol pour inhalation COMBIVENT® est de deux inhalations quatre fois par jour. Les patients peuvent prendre des inhalations supplémentaires au besoin; cependant, le nombre total d'inhalations ne doit pas dépasser 12 en 24 heures. L'innocuité et l'efficacité de doses supplémentaires de COMBIVENT en aérosol pour inhalation au-delà de 12 bouffées/24 heures n'ont pas été étudiées. De plus, l'innocuité et l'efficacité de doses supplémentaires d'ipratropium ou d'albutérol en plus des doses recommandées de Combivent® (bromure d'ipratropium et sulfate d'albutérol) en aérosol pour inhalation n'ont pas été étudiées. Il est recommandé de "tester" trois fois avant la première utilisation et dans les cas où l'aérosol n'a pas été utilisé pendant plus de 24 heures. Éviter de vaporiser dans les yeux.
COMMENT FOURNIE
Aérosol pour inhalation COMBIVENT est fourni sous forme d'aérosol-doseur avec un embout buccal blanc doté d'un manchon transparent et incolore et d'un capuchon de protection orange. La cartouche d'aérosol pour inhalation COMBIVENT 20 mcg doit être utilisée uniquement avec l'embout buccal pour aérosol pour inhalation COMBIVENT 20 mcg et non avec d'autres embouts buccaux. Cet embout buccal ne doit pas être utilisé avec d'autres médicaments en aérosol. Chaque actionnement mesure 21 mcg de bromure d'ipratropium et 120 mcg de sulfate d'albutérol à partir de la valve et délivre 18 mcg de bromure d'ipratropium et 103 mcg de sulfate d'albutérol (équivalent à 90 mcg de base d'albutérol) à partir de l'embout buccal.
Chaque cartouche de 14,7 grammes fournit suffisamment de médicament pour 200 activations ( CDN 0597-001314).
Avertissement: La cartouche doit être jetée une fois que le nombre d'actionnements indiqué a été utilisé. La quantité correcte de médicament à chaque actionnement ne peut plus être assurée après ce point, même si la cartouche n'est pas complètement vide.
Conserver à 25 °C (77 °F); excursions autorisées jusqu'à 15°-30°C (59°-86°F) [voir Température ambiante contrôlée USP ]. Pour de meilleurs résultats, conservez la cartouche à température ambiante avant utilisation. Évitez l'excès d'humidité. Agiter vigoureusement le bidon pendant au moins 10 secondes avant utilisation.
Adressez vos demandes médicales à : http://us.boehringer-ingelheim.com, (800) 542-6257 ou (800) 459-9906 TTY.
Noter: La déclaration en retrait ci-dessous est requise par la Clean Air Act du gouvernement fédéral pour tous les produits contenant ou fabriqués avec des chlorofluorocarbures (CFC) :
Avertissement: Contient du trichloromonofluorométhane (CFC-11), du dichlorodifluorométhane (CFC-12) et du dichlorotétrafluoroéthane (CFC-114), des substances qui nuisent à la santé publique et à l'environnement en détruisant l'ozone dans la haute atmosphère.
Un avis similaire à celui ci-dessus Avertissement été placé dans l'information pour le patient de ce produit en vertu des règlements de l'Environmental Protection Agency (EPA). L'avertissement du patient stipule que le patient doit consulter son médecin s'il a des questions sur les alternatives.
Contenu sous pression: Ne pas percer. Ne pas utiliser ou entreposer près d'une source de chaleur ou d'une flamme nue. L'exposition à des températures supérieures à 120°F peut provoquer un éclatement. Ne jetez jamais l'inhalateur dans un feu ou un incinérateur.
Distribué par : Boehringer Ingelheim Pharmaceuticals, Inc. Ridgefield, CT 06877 États-Unis. Bromure d'ipratropium sous licence de : Boehringer Ingelheim International GmbH. Révisé : août 2012
EFFETS SECONDAIRES
Les informations sur les effets indésirables concernant l'aérosol pour inhalation Combivent® (bromure d'ipratropium et sulfate d'albutérol) sont tirées de deux essais cliniques contrôlés de 12 semaines (N = 358 pour l'aérosol pour inhalation COMBIVENT) comme indiqué dans le tableau 1.
Les autres effets indésirables signalés chez moins de deux pour cent des patients du groupe de traitement par aérosol pour inhalation COMBIVENT comprennent l'œdème, la fatigue, l'hypertension, les étourdissements, la nervosité, la paresthésie, les tremblements, la dysphonie, l'insomnie, la diarrhée, la bouche sèche, la dyspepsie, les vomissements, l'arythmie, palpitations, tachycardie, arthralgie, angine de poitrine, augmentation des expectorations, altération du goût et infection/dysurie des voies urinaires.
Des réactions de type allergique telles que des réactions cutanées, y compris des éruptions cutanées, du prurit et de l'urticaire (y compris de l'urticaire géante), des œdèmes de Quincke, y compris ceux de la langue, des lèvres et du visage, des laryngospasmes et des réactions anaphylactiques ont été signalées avec Combivent® (bromure d'ipratropium et sulfate d'albutérol). Inhalation Aérosol , avec réexamen positif dans certains cas. Beaucoup de ces patients avaient des antécédents d'allergies à d'autres médicaments et/ou aliments, y compris le soja (voir CONTRE-INDICATIONS ).
Expérience post-commercialisation
Dans un essai contrôlé par placebo d'une durée de 5 ans, des hospitalisations pour tachycardie supraventriculaire et/ou fibrillation auriculaire sont survenues avec un taux d'incidence de 0,5 % chez les patients atteints de MPOC recevant Atrovent® (bromure d'ipratropium) en aérosol pour inhalation CFC.
Les effets indésirables supplémentaires identifiés dans la littérature publiée et/ou la surveillance post-commercialisation de l'utilisation de produits contenant du bromure d'ipratropium (seul ou en association avec l'albutérol) incluent : hypersensibilité, œdème pharyngé, œdème buccal, rétention urinaire, mydriase, bronchospasme ( y compris bronchospasme paradoxal), précipitations ou aggravation d'un glaucome à angle fermé, glaucome, augmentation de la pression intraoculaire, douleur oculaire aiguë, vision en halo, vision floue, trouble de l'accommodation, irritation oculaire, œdème cornéen, hyperhémie conjonctivale, congestion nasale, assèchement des sécrétions , ulcères des muqueuses, stomatite, irritation due aux aérosols, irritation de la gorge, sécheresse de la gorge, respiration sifflante, exacerbation des symptômes de la MPOC, enrouement, palpitations, brûlures d'estomac, somnolence, stimulation du SNC, difficulté de coordination, bouffées vasomotrices, alopécie, hypotension, œdème, détresse gastro-intestinale (diarrhée, nausées, vomissements), troubles de la motilité gastro-intestinale, constipation, hypokaliémie, troubles mentaux, hyperhidrose, spasmes musculaires, faiblesse musculaire, myalgie, asthénie, ischémie myocardique, diminution de la pression artérielle diastolique et augmentation de la pression artérielle systolique.
Une acidose métabolique a été rapportée avec l'utilisation de produits contenant de l'albutérol.
INTERACTIONS MÉDICAMENTEUSES
L'aérosol pour inhalation COMBIVENT a été utilisé en concomitance avec d'autres médicaments, notamment des bronchodilatateurs sympathomimétiques, des méthylxanthines et des stéroïdes oraux et inhalés, couramment utilisés dans le traitement de la maladie pulmonaire obstructive chronique. À l'exception de l'albutérol, il n'y a pas d'études formelles évaluant pleinement les effets d'interaction de l'aérosol pour inhalation COMBIVENT et de ces médicaments en ce qui concerne l'innocuité et l'efficacité.
Agents anticholinergiques
Il existe un potentiel d'interaction additive avec les médicaments anticholinergiques utilisés en concomitance. Par conséquent, évitez la co-administration de COMBIVENT 50 mg en aérosol pour inhalation avec d'autres médicaments contenant des anticholinergiques.
Agents bêta-adrénergiques
La prudence est recommandée lors de la co-administration de COMBIVENT en aérosol pour inhalation et d'autres agents sympathomimétiques en raison du risque accru d'effets cardiovasculaires indésirables.
Agents bloquants des récepteurs bêta et l'albutérol inhibent l'effet l'un de l'autre. Les agents bloquants des récepteurs bêta doivent être utilisés avec prudence chez les patients dont les voies respiratoires sont hyperréactives.
Diurétiques
Les modifications de l'ECG et/ou l'hypokaliémie qui peuvent résulter de l'administration de diurétiques non épargneurs de potassium (tels que les diurétiques de l'anse ou thiazidiques) peuvent être fortement aggravées par les bêta-agonistes, en particulier lorsque la dose recommandée de bêta-agoniste est dépassée. Bien que la signification clinique de ces effets ne soit pas connue, la prudence est recommandée lors de la co-administration de médicaments contenant des bêta-agonistes, tels que COMBIVENT en aérosol pour inhalation, avec des diurétiques non épargneurs de potassium. Envisagez de surveiller les niveaux de potassium.
Inhibiteurs de la monoamine oxydase ou antidépresseurs tricycliques
L'aérosol pour inhalation COMBIVENT doit être administré avec une extrême prudence aux patients traités par des inhibiteurs de la monoamine oxydase ou des antidépresseurs tricycliques ou dans les deux semaines suivant l'arrêt de ces agents, car l'action de l'albutérol sur le système cardiovasculaire peut être potentialisée. Envisager un traitement alternatif chez les patients prenant des MAO ou des antidépresseurs tricycliques.
AVERTISSEMENTS
PRÉCAUTIONS
Général
Informations pour les patients
Les patients doivent être avertis d'éviter de vaporiser l'aérosol dans leurs yeux et être informés que cela peut entraîner une précipitation ou une aggravation d'un glaucome à angle fermé, une mydriase, une augmentation de la pression intraoculaire, une douleur ou un inconfort oculaire aigu, une vision floue temporaire, des halos visuels ou des images associées à des yeux rouges dus à une congestion conjonctivale et cornéenne. Les patients doivent également être informés qu'en cas d'apparition d'une combinaison de ces symptômes, ils doivent consulter leur médecin immédiatement.
L'action de COMBIVENT 20 mcg en aérosol pour inhalation doit durer 4 à 5 heures ou plus. L'aérosol pour inhalation COMBIVENT ne doit pas être utilisé plus fréquemment que recommandé. N'augmentez pas la dose ou la fréquence de l'aérosol pour inhalation COMBIVENT sans consulter votre médecin. Si vous constatez que le traitement par COMBIVENT 20 mcg en aérosol pour inhalation devient moins efficace pour le soulagement des symptômes, que vos symptômes s'aggravent et/ou que vous devez utiliser le produit plus fréquemment que d'habitude, vous devez consulter immédiatement un médecin. Pendant que vous prenez l'aérosol pour inhalation COMBIVENT, les autres médicaments inhalés ne doivent être pris que selon les directives de votre médecin. Si vous êtes enceinte ou allaitez, contactez votre médecin au sujet de l'utilisation de l'aérosol pour inhalation COMBIVENT. L'utilisation appropriée de Combivent® (bromure d'ipratropium et sulfate d'albutérol) en aérosol pour inhalation comprend une compréhension de la manière dont il doit être administré (voir Instructions d'utilisation pour le patient ).
Étant donné que des étourdissements, des troubles de l'accommodation, une mydriase et une vision floue peuvent survenir lors de l'utilisation de COMBIVENT 20 mcg, les patients doivent être avertis de ne pas s'engager dans des activités nécessitant l'équilibre et l'acuité visuelle telles que la conduite d'une voiture ou l'utilisation d'appareils ou de machines.
Carcinogenèse, mutagenèse, altération de la fertilité
Bromure d'ipratropium
Des études de cancérogénicité orale de deux ans chez le rat et la souris n'ont révélé aucune activité cancérogène à des doses allant jusqu'à 6 mg/kg. Cette dose correspond chez le rat et la souris à environ 230 et 110 fois la dose quotidienne maximale recommandée par inhalation de bromure d'ipratropium chez l'adulte, respectivement, sur une base en mg/m². Les résultats de diverses études de mutagénicité (test d'Ames, test de létalité dominante chez la souris, test du micronoyau chez la souris et aberration chromosomique de la moelle osseuse chez les hamsters chinois) se sont révélés négatifs.
La fertilité de rats mâles ou femelles à des doses orales allant jusqu'à 50 mg/kg (environ 1900 fois la dose d'inhalation quotidienne maximale recommandée chez l'adulte sur une base en mg/m²) n'a pas été affectée par l'administration de bromure d'ipratropium. À une dose orale de 500 mg/kg (environ 19 000 fois la dose quotidienne maximale recommandée par inhalation chez l'adulte sur une base en mg/m²), le bromure d'ipratropium a entraîné une diminution du taux de conception.
Albutérol
Comme d'autres agents de sa classe, l'albutérol a provoqué une augmentation significative, liée à la dose, de l'incidence des léiomyomes bénins du mésovarium dans une étude de 2 ans chez le rat à des doses alimentaires de 2, 10 et 50 mg/kg (environ 15, 65 et 330 fois la dose quotidienne maximale recommandée par inhalation chez l'adulte sur une base en mg/m²). Dans une autre étude, cet effet a été bloqué par la co-administration de propranolol. La pertinence de ces résultats pour l'homme n'est pas connue. Une étude de 18 mois chez la souris à des doses alimentaires allant jusqu'à 500 mg/kg (environ 1600 fois la dose quotidienne maximale recommandée par inhalation chez l'adulte sur une base en mg/m²) et une étude de 99 semaines chez le hamster à des doses orales allant jusqu'à 50 mg /kg (environ 220 fois la dose quotidienne maximale recommandée par inhalation chez l'adulte sur une base en mg/m²) n'a révélé aucun signe de tumorigénicité. Les études avec l'albutérol n'ont révélé aucune preuve de mutagenèse.
Les études de reproduction chez les rats avec du sulfate d'albutérol n'ont révélé aucun signe d'altération de la fertilité.
Grossesse
Aérosol pour inhalation COMBIVENT
Effets tératogènes : Catégorie de grossesse C
Il n'y a pas d'études adéquates et bien contrôlées de Combivent® (bromure d'ipratropium et sulfate d'albutérol) en aérosol pour inhalation, bromure d'ipratropium ou sulfate d'albutérol, chez les femmes enceintes. Aucune étude de reproduction animale n'a été menée avec l'aérosol pour inhalation COMBIVENT. Cependant, le sulfate d'albutérol s'est avéré tératogène chez la souris et le lapin. L'aérosol pour inhalation COMBIVENT ne doit être utilisé pendant la grossesse que si le bénéfice potentiel justifie le risque potentiel pour le fœtus.
Bromure d'ipratropium
Effets tératogènes
Des études de reproduction par voie orale ont été réalisées à des doses de 10 mg/kg chez la souris, 1000 mg/kg chez le rat et 125 mg/kg chez le lapin. Ces doses correspondent dans chaque espèce, respectivement, à environ 190, 38 000 et 9 400 fois la dose quotidienne maximale recommandée par inhalation chez l'adulte sur une base en mg/m². Des études de reproduction par inhalation ont été menées chez des rats et des lapins à des doses de 1,5 et 1,8 mg/kg (environ 55 et 140 fois la dose quotidienne maximale recommandée par inhalation chez l'adulte sur une base en mg/m²). Ces études n'ont démontré aucune preuve d'effets tératogènes résultant du bromure d'ipratropium. À des doses orales de 90 mg/kg et plus chez le rat (environ 3 400 fois la dose quotidienne maximale recommandée par inhalation chez l'adulte sur une base en mg/m²), une embryotoxicité a été observée sous la forme d'une résorption accrue. Cet effet n'est pas considéré comme pertinent pour l'utilisation humaine en raison des fortes doses auxquelles il a été observé et de la différence de voie d'administration.
Albutérol
Effets tératogènes
L'albutérol s'est avéré tératogène chez la souris et le lapin. Une étude de reproduction chez des souris CD-1 ayant reçu de l'albutérol par voie sous-cutanée (0,025, 0,25 et 2,5 mg/kg) a montré la formation d'une fente palatine chez 5 des 111 fœtus (4,5 %) à 0,25 mg/kg (équivalent à la dose quotidienne maximale recommandée par inhalation chez adultes sur une base mg/m²) et chez 10 fœtus sur 108 (9,3 %) à 2,5 mg/kg (environ 8 fois la dose quotidienne maximale recommandée par inhalation chez les adultes sur une base mg/m²). Aucune n'a été observée à 0,025 mg/kg (moins que la dose quotidienne maximale recommandée par inhalation chez l'adulte). Une fente palatine est également survenue chez 22 des 72 fœtus (30,5 %) traités avec 2,5 mg/kg d'isoprotérénol (témoin positif). Une étude de reproduction avec de l'albutérol par voie orale chez des lapins Stride Dutch a révélé un cranioschisis chez 7 des 19 (37 %) fœtus à 50 mg/kg (environ 660 fois la dose quotidienne maximale recommandée par inhalation chez l'adulte sur une base en mg/m²).
Travail et accouchement
En raison du potentiel d'interférence des bêta-agonistes avec la contractilité utérine, l'utilisation de l'aérosol pour inhalation Combivent® (bromure d'ipratropium et sulfate d'albutérol) pour le traitement de la BPCO pendant le travail doit être limitée aux patientes pour lesquelles les avantages l'emportent clairement sur les risques.
Mères allaitantes
On ne sait pas si les composants de l'aérosol pour inhalation COMBIVENT sont excrétés dans le lait maternel.
Bromure d'ipratropium
Étant donné que les cations quaternaires insolubles dans les lipides passent dans le lait maternel, la prudence s'impose lorsque l'aérosol pour inhalation COMBIVENT est administré à une mère qui allaite.
Albutérol
En raison du potentiel de tumorigénicité démontré pour l'albutérol dans les études animales, une décision doit être prise d'interrompre l'allaitement ou d'arrêter le médicament, en tenant compte de l'importance du médicament pour la mère.
Utilisation pédiatrique
La sécurité et l'efficacité dans la population pédiatrique n'ont pas été établies.
SURDOSAGE
On s'attend à ce que les effets du surdosage soient principalement liés au sulfate d'albutérol. Un surdosage aigu de bromure d'ipratropium par inhalation est peu probable car le bromure d'ipratropium n'est pas bien absorbé par voie systémique après administration par aérosol ou par voie orale. Les doses létales médianes orales de bromure d'ipratropium étaient supérieures à 1 001 mg/kg chez la souris (environ 19 000 fois la dose d'inhalation quotidienne maximale recommandée chez l'adulte sur une base en mg/m²) ; 1 663 mg/kg chez le rat (environ 62 000 fois la dose quotidienne maximale recommandée par inhalation chez l'adulte sur une base en mg/m²) ; et 400 mg/kg chez le chien (environ 50 000 fois la dose quotidienne maximale recommandée par inhalation chez l'adulte, sur une base en mg/m²). Alors que la dose létale médiane orale de sulfate d'albutérol chez la souris et le rat était supérieure à 2 000 mg/kg (environ 6 600 et 13 000 fois la dose quotidienne maximale recommandée par inhalation, respectivement, chez l'adulte sur une base en mg/m²), la dose létale médiane par inhalation n'a pu être déterminé. Les manifestations de surdosage avec l'albutérol peuvent inclure des douleurs angineuses, une hypertension, une hypokaliémie, une tachycardie avec des taux allant jusqu'à 200 battements par minute, une acidose métabolique et une exagération des effets pharmacologiques énumérés dans EFFETS INDÉSIRABLES. Comme avec tous les aérosols sympathomimétiques, un arrêt cardiaque et même la mort peuvent être associés à un abus. La dialyse n'est pas un traitement approprié pour un surdosage d'albutérol sous forme d'aérosol pour inhalation ; l'utilisation judicieuse d'un bêta-bloquant cardiovasculaire, tel que le tartrate de métoprolol, peut être indiquée.
CONTRE-INDICATIONS
L'aérosol pour inhalation COMBIVENT est contre-indiqué chez les patients ayant des antécédents d'hypersensibilité à la lécithine de soja ou à des produits alimentaires apparentés tels que le soja et l'arachide. L'aérosol pour inhalation COMBIVENT est également contre-indiqué chez les patients hypersensibles à tout autre composant du produit médicamenteux ou à l'atropine ou à ses dérivés.
PHARMACOLOGIE CLINIQUE
COMBIVENT 50 mg en aérosol pour inhalation est une combinaison du bronchodilatateur anticholinergique, le bromure d'ipratropium, et du bronchodilatateur bêta2-adrénergique, le sulfate d'albutérol.
Mécanisme d'action
Bromure d'ipratropium
Le bromure d'ipratropium est un agent anticholinergique (parasympatholytique) qui, d'après des études animales, semble inhiber les réflexes à médiation vagale en s'opposant à l'action de l'acétylcholine, l'agent transmetteur libéré au niveau des jonctions neuromusculaires dans les poumons. Les anticholinergiques empêchent les augmentations de la concentration intracellulaire de Ca++ qui sont causées par l'interaction de l'acétylcholine avec les récepteurs muscariniques sur le muscle lisse bronchique.
Sulfate d'albutérol
Des études in vitro et des études de pharmacologie in vivo ont démontré que l'albutérol a un effet préférentiel sur les récepteurs bêta2-adrénergiques par rapport à l'isoprotérénol. Bien qu'il soit reconnu que les récepteurs bêta2-adrénergiques sont les récepteurs prédominants sur le muscle lisse bronchique, des données récentes indiquent qu'il existe une population de récepteurs bêta2 dans le cœur humain qui comprend entre 10 % et 50 % des récepteurs cardiaques bêta-adrénergiques. La fonction précise de ces récepteurs n'est cependant pas encore établie (voir AVERTISSEMENTS ).
L'activation des récepteurs bêta2-adrénergiques sur le muscle lisse des voies respiratoires entraîne l'activation de l'adénylyl cyclase et une augmentation de la concentration intracellulaire de 3',5'-adénosine monophosphate cyclique (AMP cyclique). Cette augmentation de l'AMP cyclique conduit à l'activation de la protéine kinase A, qui inhibe la phosphorylation de la myosine et abaisse les concentrations de calcium ionique intracellulaire, entraînant une relaxation. L'albutérol détend les muscles lisses de toutes les voies respiratoires, de la trachée aux bronchioles terminales. L'albutérol agit comme un antagoniste fonctionnel pour détendre les voies respiratoires quel que soit le spasmogène impliqué, protégeant ainsi contre tous les défis bronchoconstricteurs. Des concentrations accrues d'AMP cyclique sont également associées à l'inhibition de la libération de médiateurs par les mastocytes dans les voies respiratoires.
Il a été démontré dans la plupart des essais cliniques que l'albutérol a plus d'effet de relaxation des muscles lisses bronchiques que l'isoprotérénol à des doses comparables tout en produisant moins d'effets cardiovasculaires. Cependant, tous les médicaments bêta-adrénergiques, y compris le sulfate d'albutérol, peuvent produire un effet cardiovasculaire significatif chez certains patients (voir PRÉCAUTIONS ).
COMBIVENT 20mcg Aérosol pour inhalation
L'aérosol pour inhalation Combivent® (bromure d'ipratropium et sulfate d'albutérol) devrait maximiser la réponse au traitement chez les patients atteints de maladie pulmonaire obstructive chronique (MPOC) en réduisant le bronchospasme par deux mécanismes distincts, anticholinergique (parasympatholytique) et sympathomimétique. L'administration simultanée d'un anticholinergique (bromure d'ipratropium) et d'un bêta2-sympathomimétique (sulfate d'albutérol) est conçue pour bénéficier au patient en produisant un effet bronchodilatateur plus important que lorsque l'un ou l'autre médicament est utilisé seul à la posologie recommandée.
Pharmacocinétique
Bromure d'ipratropium
Une grande partie de la dose administrée est avalée, comme le montrent les études sur l'excrétion fécale. Le bromure d'ipratropium est une amine quaternaire. Il n'est pas facilement absorbé dans la circulation systémique, que ce soit à partir de la surface des poumons ou du tractus gastro-intestinal, comme le confirment les études de concentration sanguine et d'excrétion rénale. Les taux plasmatiques de bromure d'ipratropium étaient inférieurs à la limite de sensibilité du dosage de 100 pg/mL.
La demi-vie d'élimination est d'environ 2 heures après inhalation ou administration intraveineuse. Le bromure d'ipratropium est très peu lié (0 à 9 % in vitro) à l'albumine plasmatique et à la glycoprotéine α1-acide. Il est partiellement métabolisé en produits d'hydrolyse d'esters inactifs. Après administration intraveineuse, environ la moitié de la dose est excrétée sous forme inchangée dans l'urine. Des études autoradiographiques chez le rat ont montré que le bromure d'ipratropium ne traverse pas la barrière hémato-encéphalique.
Sulfate d'albutérol
L'albutérol agit plus longtemps que l'isoprotérénol chez la plupart des patients car il n'est pas un substrat pour les processus d'absorption cellulaire des catécholamines ni pour le métabolisme par la catéchol-O-méthyl transférase. Au lieu de cela, le médicament est métabolisé par conjugaison en albutérol 4'-O-sulfate.
Dans une étude pharmacocinétique chez 12 hommes volontaires sains de deux inhalations de sulfate d'albutérol, dose de 103 mcg/inhalation par l'embout buccal, des concentrations plasmatiques maximales d'albutérol allant de 419 à 802 pg/mL (moyenne 599 ± 122 pg/mL) ont été obtenues en trois heures post-administration. Suite à cette administration d'une dose unique, 30,8 ± 10,2 % de la dose estimée dans l'embout buccal ont été excrétés sous forme inchangée dans les urines de 24 heures. Étant donné que le sulfate d'albutérol est rapidement et complètement absorbé, cette étude n'a pas pu faire la distinction entre l'absorption pulmonaire et gastro-intestinale.
La pharmacocinétique intraveineuse de l'albutérol a été étudiée dans un groupe comparable de 16 volontaires sains de sexe masculin ; la demi-vie terminale moyenne après une perfusion de 30 minutes de 1,5 mg était de 3,9 heures avec une clairance moyenne de 439 mL/min/1,73 m².
Des études intraveineuses d'albutérol chez des rats ont démontré que l'albutérol traversait la barrière hémato-encéphalique et atteignait des concentrations cérébrales s'élevant à environ 5 % des concentrations plasmatiques. Dans les structures en dehors de la barrière hémato-encéphalique (glandes pinéale et pituitaire), le médicament a atteint des concentrations plus de 100 fois supérieures à celles du cerveau entier.
Des études chez des rats gravides avec de l'albutérol tritié ont démontré qu'environ 10 % du médicament maternel en circulation étaient transférés au fœtus. La disposition dans les poumons fœtaux était comparable à celle des poumons maternels, mais la disposition du foie fœtal était de 1 % des niveaux du foie maternel.
Des études sur des animaux de laboratoire (porcs nains, rongeurs et chiens) ont démontré la survenue d'arythmies cardiaques et de mort subite (avec signes histologiques de nécrose myocardique) lorsque des bêta-agonistes et des méthylxanthines étaient administrés simultanément. La signification de ces résultats lorsqu'ils sont appliqués aux humains est inconnue.
COMBIVENT 50mg Aérosol pour Inhalation
Dans une étude pharmacocinétique croisée chez 12 volontaires sains de sexe masculin comparant le schéma d'absorption et d'excrétion de deux inhalations de Combivent® (bromure d'ipratropium et sulfate d'albutérol) en aérosol pour inhalation aux deux composants actifs individuellement, la co-administration de bromure d'ipratropium et de sulfate d'albutérol à partir d'un seul cartouche n'a pas modifié de manière significative l'absorption systémique de l'un ou l'autre des composants.
Les niveaux de bromure d'ipratropium sont restés inférieurs aux limites détectables (
Populations particulières
La pharmacocinétique de Combivent® (bromure d'ipratropium et sulfate d'albutérol) en aérosol pour inhalation ou de bromure d'ipratropium n'a pas été étudiée chez les patients insuffisants hépatiques ou rénaux ou chez les personnes âgées (voir PRÉCAUTIONS ).
Interactions médicament-médicament
Aucune étude pharmacocinétique spécifique n'a été menée pour évaluer les interactions médicamenteuses potentielles.
Pharmacodynamie
Bromure d'ipratropium
La bronchodilatation consécutive à l'inhalation de bromure d'ipratropium est principalement un effet local, spécifique au site, et non systémique.
Des études cliniques contrôlées ont démontré que le bromure d'ipratropium ne modifie ni la clairance mucociliaire ni le volume ou la viscosité des sécrétions respiratoires. Dans les études sans contrôle positif, le bromure d'ipratropium n'a pas modifié la taille de la pupille, l'accommodation ou l'acuité visuelle (voir EFFETS INDÉSIRABLES ).
Les études de ventilation/perfusion n'ont montré aucun effet cliniquement significatif sur les échanges gazeux pulmonaires ou la tension artérielle en oxygène. Aux doses recommandées, le bromure d'ipratropium ne produit pas de modifications cliniquement significatives du pouls ou de la tension artérielle.
Essais cliniques
Dans deux essais cliniques randomisés, en double aveugle et contrôlés par comparateur actif de 12 semaines, 1067 patients atteints de maladie pulmonaire obstructive chronique (MPOC) ont été évalués pour l'efficacité bronchodilatatrice de COMBIVENT 20 mcg en aérosol pour inhalation (358 patients) par rapport à ses composants, le bromure d'ipratropium (362 patients) et sulfate d'albutérol (347 patients).
Les mesures en série du VEMS (présentées ci-dessous sous la forme d'un pourcentage de variation par rapport à la ligne de base du jour du test) ont démontré que l'aérosol pour inhalation COMBIVENT produisait une amélioration significativement plus importante de la fonction pulmonaire que le bromure d'ipratropium ou le sulfate d'albutérol lorsqu'ils étaient administrés séparément. Le délai médian d'apparition d'une augmentation de 15 % du VEMS était de 15 minutes et le délai médian jusqu'au pic du VEMS était d'une heure pour l'aérosol pour inhalation COMBIVENT 20 mcg et ses composants. La durée médiane de l'effet telle que mesurée par le FEV1 était de 4 à 5 heures pour l'aérosol pour inhalation COMBIVENT comparativement à 4 heures pour le bromure d'ipratropium et à 3 heures pour le sulfate d'albutérol.
Variation en pourcentage du VEMS moyen ajusté par rapport à la ligne de base du jour du test - Analyse des points finaux de l'ensemble de données évaluables 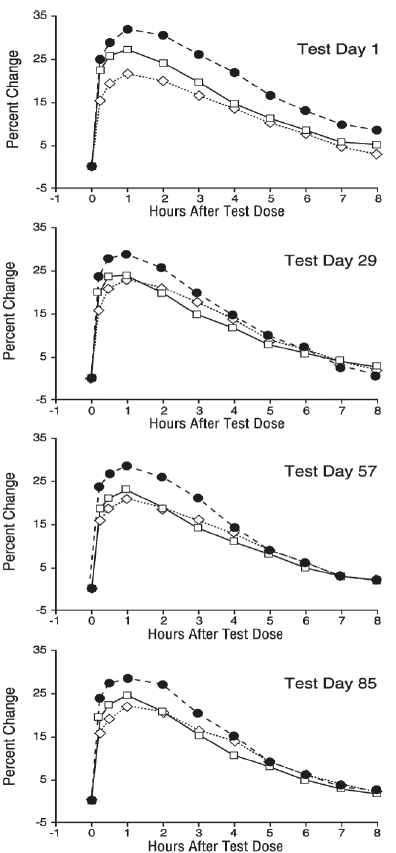
Ces études ont démontré que chaque composant de l'aérosol pour inhalation Combivent® (bromure d'ipratropium et sulfate d'albutérol) contribuait à l'amélioration de la fonction pulmonaire produite par l'association, en particulier pendant les 4 à 5 premières heures suivant l'administration, et que l'aérosol pour inhalation COMBIVENT était significativement plus efficace que le bromure d'ipratropium ou le sulfate d'albutérol administrés seuls.
Dans les 2 études contrôlées de 12 semaines, COMBIVENT 50 mg en aérosol pour inhalation n'a produit aucun changement dans les paramètres d'efficacité secondaires, y compris les scores de symptômes, les évaluations globales du médecin et le PEFR du matin, qui ont tous été surveillés tout au long de la période d'étude.
INFORMATIONS PATIENTS
Instructions d'utilisation pour le patient
Combivent® (bromure d'ipratropium et sulfate d'albutérol) Aérosol pour inhalation
Lisez attentivement les instructions complètes avant d'utiliser
Utilisez COMBIVENT 50 mg en aérosol pour inhalation exactement comme prescrit par votre médecin. Ne modifiez pas votre dose ou la fréquence d'utilisation de COMBIVENT 20 mcg en aérosol pour inhalation sans en parler avec votre médecin. Parlez à votre médecin si vous avez des questions sur votre état de santé ou votre traitement.
Informez votre médecin de tous les médicaments que vous prenez. COMBIVENT 50 mg en aérosol pour inhalation et certains autres médicaments peuvent interagir entre eux. N'utilisez pas d'autres médicaments inhalés avec COMBIVENT 20 mcg en aérosol pour inhalation à moins que votre médecin ne vous l'ait prescrit.
1. Insérez la cartouche métallique dans l'extrémité transparente de l'embout buccal (voir Figure 1). Assurez-vous que la cartouche est complètement et fermement insérée dans l'embout buccal. La cartouche d'aérosol pour inhalation COMBIVENT doit être utilisée uniquement avec l'embout buccal pour aérosol pour inhalation COMBIVENT. Cet embout buccal ne doit pas être utilisé avec d'autres médicaments inhalés.
Figure 1 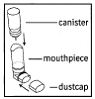
2. Retirez le capuchon anti-poussière orange. Si le capuchon n'est pas sur l'embout buccal, assurez-vous qu'il n'y a rien dans l'embout buccal avant utilisation. Pour de meilleurs résultats, la cartouche doit être à température ambiante avant utilisation.
3. Secouez et testez le spray. Effectuez cette étape avant la première utilisation et chaque fois que l'aérosol n'a pas été utilisé pendant plus de 24 heures ; sinon, passez directement à l'étape 4.
Après avoir secoué vigoureusement la cartouche pendant au moins 10 secondes (voir l'étape 4 pour les instructions sur le secouage), "test-spray" dans l'air 3 fois. Éviter de vaporiser dans les yeux.
4. Agiter vigoureusement la cartouche pendant au moins 10 secondes. Tenez la cartouche comme illustré à la figure 2.
IMPORTANT : Une agitation vigoureuse pendant au moins 10 secondes avant chaque pulvérisation est très importante pour une bonne performance du produit.
Pour de meilleurs résultats, effectuez les étapes 5 et 6 dans les 30 secondes suivant l'agitation de la cartouche.
Figure 2 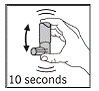
5. Expirez (expirez) profondément par la bouche. En tenant la cartouche à la verticale comme illustré à la figure 3, entre votre pouce et vos doigts, placez l'embout buccal dans votre bouche et fermez vos lèvres. Gardez les yeux fermés afin qu'aucun médicament ne soit pulvérisé dans vos yeux. L'aérosol pour inhalation de Combivent® (bromure d'ipratropium et sulfate d'albutérol) peut provoquer une vision floue, un glaucome à angle fermé ou une aggravation de cette affection ou des douleurs oculaires si le médicament est pulvérisé dans vos yeux.
figure 3 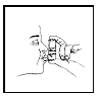
6. Inspirez (inhalez) lentement par la bouche et en même temps vaporisez le produit dans votre bouche.
Pour pulvériser le produit, appuyez fermement une fois sur la cartouche contre l'embout buccal comme indiqué sur la figure 4. Continuez à inspirer profondément.
Figure 4 
7. Retenez votre respiration pendant 10 secondes, retirez l'embout buccal de votre bouche et expirez lentement, comme illustré à la figure 5.
Figure 5 
8. Attendez environ 2 minutes, secouez à nouveau vigoureusement l'inhalateur pendant au moins 10 secondes (comme décrit à l'étape 4) et répétez les étapes 5 à 7.
9. Replacez le capuchon anti-poussière orange après utilisation.
10. Gardez l'embout buccal propre. Laver à l'eau chaude. Si du savon est utilisé, rincer abondamment à l'eau claire. Bien sécher avant utilisation. Une fois sec, replacez le capuchon sur l'embout buccal lorsque vous n'utilisez pas le médicament.
11. Gardez une trace du nombre de pulvérisations utilisées et jetez après 200 pulvérisations. Même si la cartouche n'est pas vide, vous ne pouvez pas être sûr de la quantité de médicament dans chaque pulvérisation après 200 pulvérisations.
12. Si la dose prescrite ne vous soulage pas ou si vos symptômes respiratoires s'aggravent, consultez immédiatement un médecin.
Noter: La déclaration en retrait ci-dessous est requise par la Clean Air Act du gouvernement fédéral pour tous les produits contenant ou fabriqués avec des chlorofluorocarbures (CFC) :
Ce produit contient du trichloromonofluorométhane (CFC-11), du dichlorodifluorométhane (CFC-12) et du dichlorotétrafluoroéthane (CFC-114), des substances qui nuisent à l'environnement en détruisant l'ozone dans la haute atmosphère.
Le contenu de l'aérosol pour inhalation Combivent® (bromure d'ipratropium et sulfate d'albutérol) est sous pression. Ne percez pas le bidon. Ne pas utiliser ou entreposer près d'une source de chaleur ou d'une flamme nue. L'exposition à des températures supérieures à 120°F peut provoquer un éclatement. Ne jetez jamais le récipient dans un feu ou un incinérateur.
Gardez l'aérosol pour inhalation COMBIVENT hors de la portée des enfants.
Éviter de vaporiser dans les yeux.
Adressez vos demandes médicales à : http://us.boehringer-ingelheim.com, (800) 542-6257 ou (800) 459-9906 TTY.
Conserver à 25 °C (77 °F); excursions autorisées jusqu'à 15°-30°C (59°-86°F) [voir Température ambiante contrôlée USP ]. Pour de meilleurs résultats, conservez la cartouche à température ambiante avant utilisation. Évitez l'excès d'humidité.
